El Desierto Chihuahuense es considerado como la región árida con mayor diversidad florística en el norte de México (Balleza & Villaseñor 2011). Rzedowski (1978) lo describió como un centro valioso para la comprensión de la flora mexicana, debido a los diversos factores que lo conforman, considerando que en las plantas que lo habitan se han registrado modificaciones anatómicas como suculencia, cubiertas protectoras con diversos tricomas o ceras y estomas hundidos, así como reducción foliar y cambios estacionales en la inclinación de la hoja, entre otras; que se han interpretado como soluciones evolutivas (Rzedowski 1968, Whittaker 1975, Nobel 1977, Gibson 2012). En las áreas desérticas se registran floras taxonómicamente diversas, que podría indicar que cada una se derivó de antepasados diferentes. Las características mencionadas anteriormente podrían considerarse convergencias evolutivas por adaptación a ambientes similares (Terrazas 1999, Fichtler & Worbes 2012, Gibson 2012, Oskolski & Akinlabi 2023). Por ello, el estudio de la madera en zonas desérticas permite comprender como las especies responden a las presiones hidráulicas negativas y altas temperaturas (Webber 1936, Carlquist 1975, Olson & Rosell 2013).
Algunos autores han asociado caracteres anatómicos de la madera como respuesta a la aridez; por ejemplo, anillos de crecimiento marcados, vasos agrupados con diámetros reducidos, elementos de vaso con engrosamientos helicoidales, presencia de traqueidas vasculares (Carlquist & Hoekman 1985), fibras medianas (900 a 1,600 µm) y radios bajos (Abundiz et al. 2004). Baas & Carlquist (1985) compararon la anatomía de la madera de la flora del sur de California e Israel y encontraron ligeras similitudes en los diámetros de vaso e incidencia de traqueidas, que atribuyeron a las diferencias en la composición florística de cada sitio. La comparación de los rasgos de la anatomía de la madera de ambientes áridos en México con una flora diversa podría revelar convergencias a este ambiente.
El estudio de la anatomía de la madera de las especies en la Sierra de Juárez ubicada en el Desierto Chihuahuense (México), permitirá comprender la diversidad estructural y cómo dichos caracteres confieren a las especies la capacidad de prosperar en estos ambientes extremos a partir del uso eficiente de los recursos disponibles. Se espera que estas especies presenten todos o algunos de caracteres de la madera antes mencionados que han sido asociados con ambientes áridos. Por lo que el objetivo de este estudio fue describir la anatomía de la madera de 32 especies leñosas del matorral xerófilo de la Sierra de Juárez y comparar los rasgos anatómicos de la madera con los presentes en otros dos sitios con un tipo de vegetación similar.
Materiales y métodos
La Sierra de Juárez se localiza al poniente del municipio de Ciudad Juárez, Chihuahua (31° 42' 8.73 " N, 106 ° 30 '19.48 "O) en el Desierto Chihuahuense (Figura 1). La altitud oscila de 1,000 a 1,900 m snm y cuenta con una extensión de 12,930 hectáreas. El clima de la región es árido-cálido (BWh, Köppen) con una precipitación media anual de 250 mm concentrados en los meses de julio a septiembre y un ligero aporte de nieve (< 40 mm) en invierno; con temperaturas extremas que oscilan entre los -10 y los 46 °C (IMIP 2010).
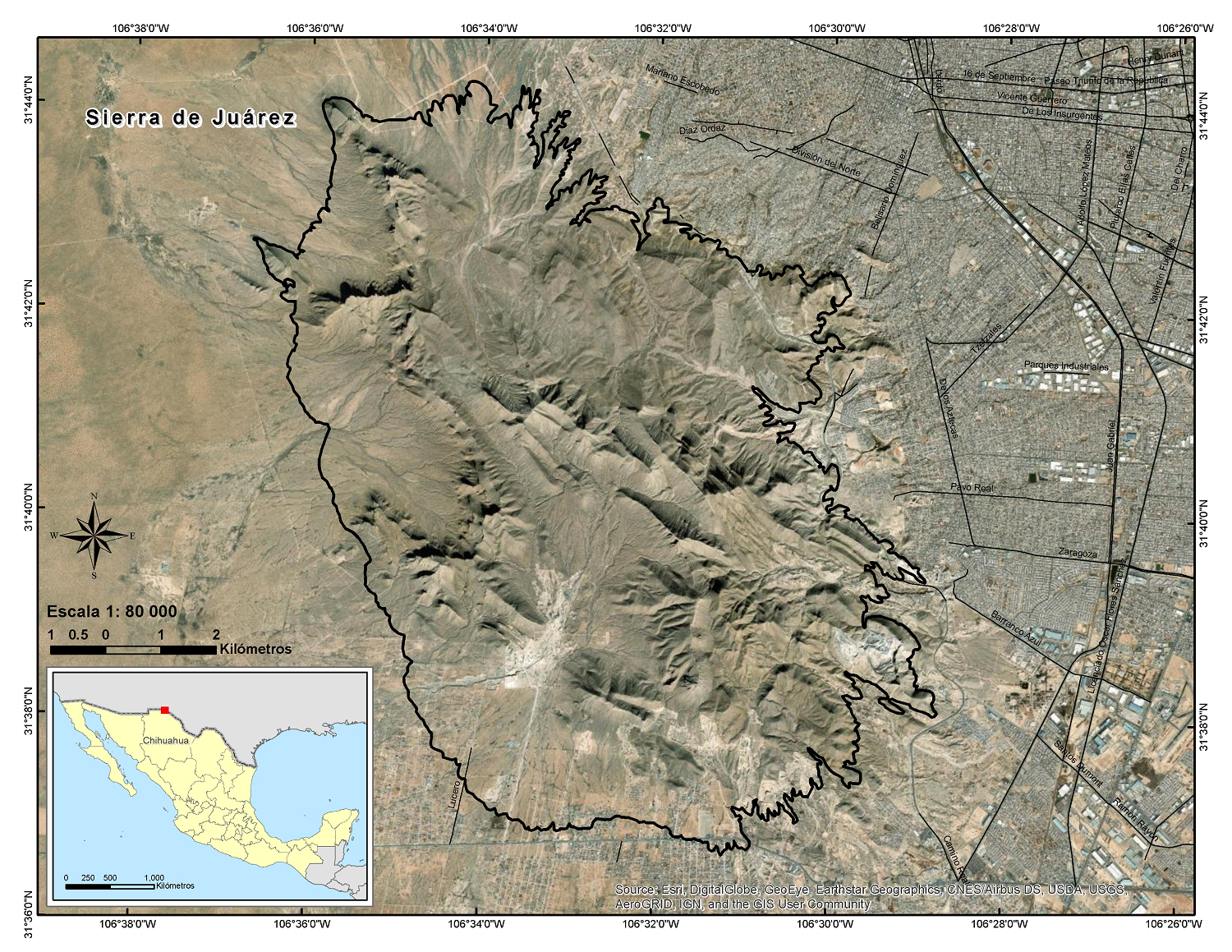
Figura 1 Mapa de la Sierra de Juárez. Carta topográfica 250,000 (INEGI 2023). Marco geoestadístico, INEGI 2021. Mapa elaborado en la Unidad de Cartografía Digital, ICB-UACJ.
Se seleccionaron únicamente especies leñosas en etapa reproductiva, de las cuales 30 fueron arbustos y dos sufrútices, Castilleja lanata A.Gray y Physaria purpurea (A.Gray) O'Kane & Al-Shehbaz (Tabla 1); ubicadas entre los 1,300 hasta los 1,700 m snm. Se registró la altura del individuo y la fenología de la hoja de acuerdo con Cavender-Bares et al. (2004) como caducifolia, siempre verde, semicaducifolia, se agregó la categoría de efímera. Se tomaron muestras de tres individuos por especie con una sierra manual. Para cada individuo se obtuvo un trozo de madera de 3 a 5 cm incluyendo la corteza, a una distancia de 5 a 8 cm del suelo para arbustos y para los sufrútices por arriba del cuello de la raíz. Todas las muestras se fijaron en formalina-ácido acético glacial-alcohol etílico (Ruzin 1999) de 24 a 72 hr y se ablandaron en glicerina-alcohol etílico-agua (1:1:1) hasta su procesamiento. Se obtuvieron secciones de 20 μm con un micrótomo de deslizamiento American Optical (Model 860) en los planos transversal, tangencial y radial. La mitad de los cortes se aclararon con hipoclorito de sodio comercial al 50 %. Todos los cortes se sometieron a una deshidratación gradual de alcoholes (50-100 %), se realizó tinción safranina/verde rápido y montaron con resina sintética. Los disociados se obtuvieron con solución de Jeffrey (Johansen 1940) a partir de astillas de madera que se removieron cercanas a cambium vascular. No se realizaron pruebas histoquímicas, los depósitos orgánicos se asignaron de acuerdo con literatura previa para cada grupo taxonómico y por su color. Para los depósitos inorgánicos, cristales de oxalato de calcio, se asignaron sus formas al revisar con luz polarizada (IAWA Committee 1989). Las descripciones se basaron en las propuestas de la Asociación Internacional de Anatomistas de la Madera (IAWA Committee 1989, 2004) y de Carlquist (1989) para Ephedraceae. Se cuantificaron por individuo por especie 25 mediciones o conteos para los caracteres de vasos (frecuencia, diámetro de madera temprana y tardía, grosor de pared de madera temprana y tardía, longitud del elemento), traqueidas, fibras (diámetro, grosor de pared, longitud) y radios (alto y ancho). Las mediciones se realizaron utilizando el software gratuito libre ImageJ v 1.45s, (Rasband 2012). Además, se determinó el índice de vulnerabilidad (iv = diámetro de vaso/frecuencia de vasos) y de mesomorfía (im = iv × longitud de elemento de vaso) propuestos por Carlquist (1977) y se asignó el grosor de la fibra (2 grosor de pared/diámetro total × 100) de acuerdo Ramírez-Martínez et al. (2017). Para cada especie se calculó la media y desviación estándar. Se realizó un análisis de conglomerado basado en el coeficiente de distancia Euclidiana, una técnica multivariante, para evaluar que caracteres cuantitativos indican similitud entre las especies que permiten la formación de grupos. Los análisis se llevaron a cabo en R Core Team (2024).
Tabla 1 Se listan las especies recolectadas en la Sierra de Juárez, Chihuahua en orden alfabético por familia. Las especies descritas por primera vez se indican con + y las sufrútices con *. Se presentan el acrónimo (Acr), la fenología de la hoja (Feho) [ca = caducifolias, e = efímeras, sc = semicaducifolia, sv = siempre verde] y la altura promedio de los tres individuos colectados.
| Especie | Acr | Feho | Altura cm | Especie | Acr | Feho | Altura cm |
|---|---|---|---|---|---|---|---|
| Cupressaceae | Fagaceae | ||||||
| Juniperus osteosperma (Torr.) | Juos | sv | 380 | Quercus pungens Liebm. | Qupu+ | ca | 127 |
| Ephedraceae | Fouquieriaceae | ||||||
| Ephedra aspera Engelm. ex S.Watson | Epas | e | 55 | Fouquieria splendens Engelm. | Fosp | ca | 227 |
| Ephedra trifurca Torr. ex S.Watson | Eptr | e | 65 | Hydrangeaceae | |||
| Anacardiaceae | Fendlera rupicola Engelm. & A.Gray | Feru | sv | 115 | |||
| Rhus aromatica Aiton | Rhar | ca | 130 | Koeberliniaceae | |||
| Rhus microphylla Engelm. | Rhmi | ca | 103 | Koeberlinia spinosa Zucc. | Kosp | e | 42 |
| Rhus virens Lindh. ex A. Gray | Rhvi | sv | 147 | Krameriaceae | |||
| Asteraceae | Krameria erecta Willd. | Krer | ca | 30 | |||
| Ageratina wrightii (A.Gray) R.M.King & H.Rob. | Agwr+ | sc | 40 | Lamiaceae | |||
| Flourensia cernua DC. | Flce+ | sc | 90 | Salvia pinguifolia (Fernald) Wooton & Standl. | Sapi+ | sv | 40 |
| Parthenium incanum Kunth | Pain | sv | 42 | Malvaceae | |||
| Sidneya tenuifolia (A.Gray) E.E.Schill. & Panero | Site+ | sv | 50 | Ayenia microphylla A.Gray | Aymi+ | ca | 38 |
| Bignoniaceae | Orobanchaceae | ||||||
| Chilopsis linearis (Cav.) Sweet | Chli | ca | 180 | Castilleja lanata A.Gray | Cala+* | sv | 25 |
| Boraginaceae | Rosaceae | ||||||
| Tiquilia greggii (Torr. & A.Gray) A.T.Richardson | Tigr+ | ca | 40 | Cercocarpus breviflorus A.Gray | Cebr+ | sc | 85 |
| Brassicaceae | Fallugia paradoxa (D.Don ex Tilloch & Taylor) Endl. ex Torr. | Fapa | sc | 83 | |||
| Physaria purpurea (A. Gray) O'Kane & Al-Shehbaz | Phpu+* | sv | 21 | Rutaceae | |||
| Cactaceae | Ptelea trifoliata L. | Pttr | ca | 88 | |||
| Cylindropuntia leptocaulis (DC.) F.M.Knuth | Cyle+ | e | 34 | Solanaceae | |||
| Crossosomataceae | Lycium berlandieri Dunal | Lybe+ | ca | 72 | |||
| Glossopetalon spinescens A.Gray | Glsp | sv | 37 | Verbenaceae | |||
| Fabaceae | Aloysia wrightii A.Heller | Alwr+ | ca | 58 | |||
| Mimosa zygophylla Benth. | Mizy+ | ca | 76 | Zygophyllaceae | |||
| Neltuma glandulosa (Torr.) Britton & Rose | Negl | ca | 150 | Larrea tridentata (DC.) Coville | Latr | sv | 70 |
| Vachellia constricta (Benth.) Seigler & Ebinger | Vaco+ | ca | 117 |
Adicionalmente, se compararon los resultados cualitativos de este trabajo con los de Abundiz et al. (2004) para un matorral xerófilo en Tehuacán, Puebla y los de Carlquist & Hoekman (1985) para el matorral de California, USA. También se llevó a cabo una comparación de los rasgos encontrados en las maderas de la Sierra de Juárez con lo registrado en la literatura para las especies, el género y la familia.
Resultados
A partir del análisis de la madera de las 32 especies estudiadas (Tabla 1) se presenta una síntesis de las características de la madera. En el material suplementario se dan las descripciones para cada especie (Material suplementario 1) y en la Tabla 1 se indica las 15 que se describen por primera vez (+). En el material suplementario Tablas S1-S6 (Material suplementario 2) se presentan de manera sintética los caracteres cuantitativos y cualitativos por especie y en las Figuras 2-5 se muestran características de la madera.
De las especies estudiadas incluyendo a Juniperus (Figura 2A), el 81 % presentó anillos de crecimiento marcados y en el 19 % fueron incospicuos. En Eudicotiledóneas y Ephedraceae predominó la porosidad anular (81 % spp., Figura 2B, F, H-K, N-Q), seguido por semi-anular (16 %, Figura 2G, L, M) y difusa solo en Castilleja lanata A.Gray (Figura 2R). Los anillos de crecimiento se reconocieron por diferencias en el diámetro de los vasos de la madera temprana y tardía o bien por las fibras de diámetro radial reducido; además por parénquima marginal en Rhus aromatica Aiton, Chilopsis linearis (Cav.) Sweet y Larrea tridentata (DC.) Coville.

Figura 2 Característica de la madera, en sección transversal, mostrando anillos de crecimiento, tipo de porosidad y arreglo de los vasos. A. Juniperus osteosperma. B. Ephedra trifurca. C. Rhus aromatica. D. Sidneya tenuifolia. E. Chilopsis linearis. F. Tiquilia greggi. G. Physaria purpurea. H. Cylindropuntia leptocaulis. I. Glossopetalon spinescens. J. Neltuma glandulosa. K. Quercus pungens. L. Fouquieria splendens. M. Fendlera rupicola. N. Koeberlinia spinosa. O. Krameria erecta. P. Salvia pinguifolia. Q. Ayenia microphylla. R. Castilleja lanata. S. Fallugia paradoxa. T. Ptelea trifoliata. U. Lycium berlandieri. V. Aloysia wrightii. W. Larrea tridentata. La barra es 300 μm en A-W.
En el 52 % de las especies los vasos se presentaron agrupados, mientras que en el 48 % solitarios (Material suplementario 2, Tabla S1). Solo en cinco especies los vasos tuvieron un arreglo distintivo; radial en Rhus microphylla Engelm., Fouquieria splendens Engelm. y Castilleja lanata y dendrítico en Rhus aromatica y Lycium berlandieri Dunal (Figura 2U). El 34 % de las especies presentaron depósitos en el lumen de los vasos como gomo-resinas en Rhus virens Lindh. ex A.Gray, Neltuma glandulosa (Torr.) Britton & Rose, Fendlera rupicola Engelm. & A.Gray (Figura 5F), Ayenia microphylla A.Gray y Ageratina wrightii A.Heller (Figura 5B), depósitos oscuros en Juniperus ostesoperma (Torr.) Little (Figura 5A), Flourencia cernua DC. y Parthenium incanum Kunth y tílides en Aloysia wrightii, Chilopsis linearis y Quercus pungens Liebm. (Figura 5E) (Material suplementario 2, Tabla S1).

Figura 3 Característica de la madera, en sección tangencial, mostrando los radios. A. Juniperus osteosperma. B. Ephedra trifurca. C. Rhus aromatica. D. Sidneya tenuifolia. E. Chilopsis linearis. F. Tiquilia greggi. G. Physaria purpurea. H. Cylindropuntia leptocaulis. I. Glossopetalon spinescens. J. Neltuma glandulosa. K. Quercus pungens. L. Fouquieria splendens. M. Fendlera rupicola. N. Koeberlinia spinosa. O. Krameria erecta. P. Salvia pinguifolia. Q. Ayenia microphylla. R. Castilleja lanata. S. Fallugia paradoxa. T. Ptelea trifoliata. U. Lycium berlandieri. V. Aloysia wrightii. W. Larrea tridentata. La barra es 300 μm en B, D, H, L-N, P; 100 μm en A, C, E, F, I-K, O, Q-W; 50 μm en G.

Figura 4 Detalles de las placas de perforación (pp), punteaduras intervasculares (pi) y punteaduras radio-vaso (pr-v) de la madera de algunas especies de la Sierra de Juárez. A. Sidneya teniufolia., pp simple (flecha , CTa). B. Fendlera rupicola, pp escalariforme (flecha) y fibrotraqueidas, CTa. C. Ephedra aspera, pp foraminada de 1 a 2 series (flecha , CTa). D. Chilopsis linearis, pi alternas (recuadro), CTa. E. Fallugia paradoxa, pi opuestas (recuadro), CTa. F. Physaria purpurea, pi pseudoescalariforme (recuadro), CTa. G. Rhus aromatica, pr-v semirebordeadas (recuadro), CR. H. Salvia pinguifolia, pr-v rebordeadas (recuadro), CR. I. Glossopetalon spinecens, pr-v simples (recuadro), CR. Barra es 20 μm en A-I. CTa = sección tangencial, CR = sección radial.
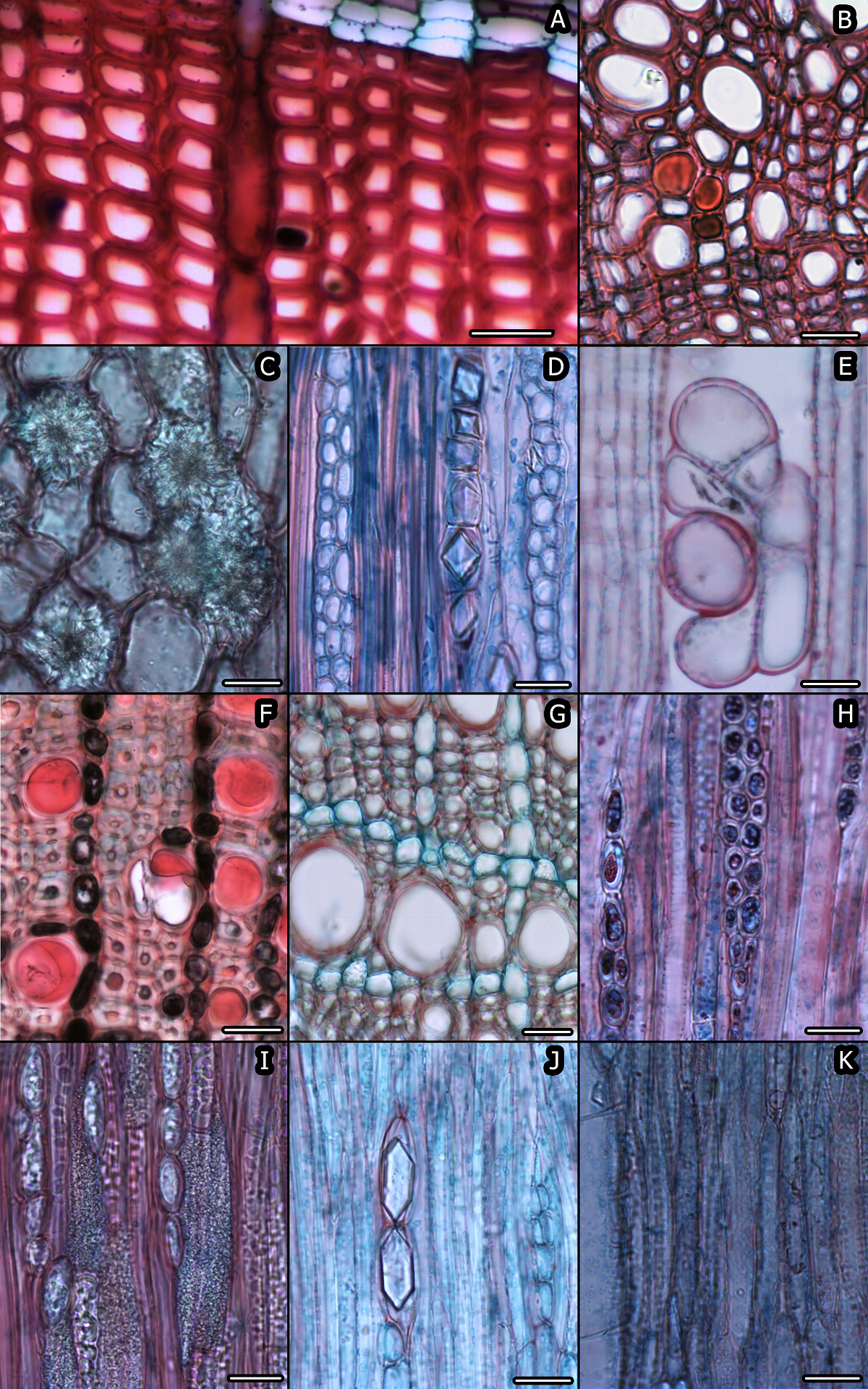
Figura 5 Depósitos orgánicos e inorgánicos de la madera de algunas especies de la Sierra de Juárez. A. Juniperus osteosperma, depósitos rojo-oscuro, CT. B. Ageratina wrightii, gomo-resinas, CT. C. Cylindropuntia leptocaulis, drusas, CTa. D. Neltuma glandulosa, cristal tipo “cámara”, CTa. E. Quercus pungens, tílide, CR. F. Fendlera rupicola, depósitos gomo-resinas. CT. G. Krameria erecta, parénquima no lignificado, CT. H. Cercocarpus breviflorus, depósitos oscuros, CTa. I. Lycium berlandieri, areniscas, CTa. J. Larrea tridentata, cristal prismático elongado, CTa. K. Larrea tridentata, parénquima estratificado, CTa. Barra es 20 μm en A-K. CT = sección transversal, CTa = sección tangencial, CR = sección radial.
La mayor frecuencia de vasos la tuvo Physaria purpurea (A.Gray) O'Kane & Al-Shehbaz (317 vasos/mm²) y la menor Neltuma glandulosa (70 vasos/mm²). El diámetro tangencial de los vasos de la madera temprana fluctuó de 68 μm en Quercus pungens hasta 13 μm en Glossopetalon spinecens A.Gray, con pared de 6 μm en Sidneya tenuifolia (A.Gray) E.E.Schill. & Panero a 1.5 μm en Koeberlinia spinosa Zucc. Para los vasos de la madera tardía el diámetro tangencial más amplio fue de Chilopsis linearis (40 μm) y el más angosto de Glossopetalon spinecens (8 μm), con pared de 5 μm en Sidneya tenuifolia a 1 μm en Koeberlinia spinosa. La longitud de los elementos de vaso varió en la media de 486 μm en Ephedra aspera Engelm. ex S.Watson a 63 μm en Physaria purpurea (Material suplementario 2, Tabla S2), con placas de perforación simple excepto en Ephedraceae con placa de tipo foraminada de 1 a 2 series y en Flendera rupicola escalariforme (Figura 4A-C); las punteaduras intervasculares generalmente fueron alternas (Figura 4D), opuestas en Aloysia wrightii, Fallugia paradoxa (D.Don ex Tilloch & Taylor) Endl. ex Torr (Figura 4E), Glossopetalon spinecens y Neltuma glandulosa, alternas a opuestas en Lycium berlandieri y Larrea tridentata y pseudoescalariformes en Physaria purpurea (Figura 4F); las punteaduras radio-vaso fueron simples en el 32 % de las especies, areoladas en el 46 % y en el 22 % semiareoladas (Figura 4G-I). El 58 % de las especies presentaron traqueidas vasculares o vasicéntricas (Material suplementario 2, Tabla S3). Se observaron engrosamientos helicoidales tanto en elementos de vaso como traqueidas vasculares y vasicéntricas en el 23 % de las especies. Solo en Rhus virens, Flourensia cernua, Parthenium incanum y Sidneya tenuifolia se observaron depósitos en traqueidas (Material suplementario 2, Tabla S3). El índice de vulnerabilidad fue menor a 1 en todas las especies analizadas, con una madera segura por redundancia de vasos, mientras que el índice de mesomorfia fue menor a 200 y se clasifican como especies xeromorfas.
Las fibras únicamente se presentaron en las Eudicotiledóneas y las dos especies de Ephedra; fueron predominantemente libriformes, seguidas de fibrotraqueidas. En Physaria purpurea las fibras libriformes se presentaron como parches en la matriz de parénquima y varias especies tuvieron gelatinosas (Material suplementario 2, Tabla S3). El 63 % de las especies presentó paredes gruesas y el resto muy gruesas (Material suplementario 2, Tabla S4). La longitud de fibras promedio fue de 770 μm en Vachellia constricta (Benth.) Seigler & Ebinger hasta 184 μm en Aloysia wrightii (Material suplementario 2, Tabla S4).
El parénquima axial fue variable en términos de abundancia y posición. Por ejemplo, en Juniperus solo hubo parénquima difuso; ausente en Cylindropuntia leptocaulis (DC.) F.M.Knuth o bien formó más del 90 % de la madera en Physaria purpurea. El paratraqueal escaso y vasicéntrico predominó (69 %) seguido del apotraqueal difuso y en agregados (Tabla S5); únicamente Krameria erecta Willd. presentó parénquima no lignificado (Figura 5G) y Larrea tridentata estratificado (Figura 5K). El 59 % de las especies presentaron depósitos inorgánicos como cristales (prismas, areniscas) y depósitos orgánicos obscuros y granos de almidón (Material suplementario 2, Tabla S5).
Los radios comúnmente fueron heterocelulares (84 %) y el resto homocelulares (Material suplementario 2, Tabla S6). Los radios exclusivamente uniseriados se registraron en Juniperus (Figura 3A), multiseriados como en Cylindropuntia leptocaulis (Figura 3H) o dimorfos como en Quercus pungens (Figura 3K). Los radios > 1,500 μm de alto estuvieron en Fallugia paradoxa y Cylindropuntia leptocaulis y hasta 48 μm de alto en Juniperus. La anchura de los radios varió de 8 μm en Tiquilia greggi (Torr. & A.Gray) A.T.Richardson hasta 175 μm en Cylindropuntia leptocaulis (Material suplementario 2, Tabla S6). El 72 % de las especies presentaron depósitos inorgánicos en los radios (Material suplementario 2, Tabla S5) y fueron cristales prismáticos en las especies de Rhus, Ayenia microphylla, Koeberlinia spinosa, Larrea tridentata (Figura 5J) y Quercus pungens; prismáticos tipo “cámara” en fabáceas (Figura 5D); drusas en Cylindropuntia leptocaulis (Figura 5C); areniscas en Lycium berlandieri (Figura 5I) y esferulitos Krameria erecta; además de depósitos oscuros en rosáceas (Figura 5H) y Sidneya tenuifolia.
Agrupación de especies. En el análisis de conglomerado, con base en los caracteres cuantitativos de la madera de las 32 especies analizadas, se recuperaron dos grupos (Figura 6). En el primero, con siete taxones, se encuentran las especies que presentaron la altura de radios mayor de 800 μm. El segundo grupo deja fuera a Juniperus por su anatomía única en el matorral. Este segundo grupo se subdivide en dos, excluyendo a Fouquieria splendens ya que el alto de sus radios fue mayor a 700 μm y menor a 800 μm y Physaria purpurea que presentó radios uniseriados exclusivamente con células erectas; el primer subgrupo tuvo una altura de radios intermedia, de 450 a 650 μm y el segundo subgrupo una altura de radios menor, de 150 a 300 μm. Con excepción de las dos especies de Ephedra, las otras especies que pertenecen a la misma familia como Anacardiaceae, Asteraceae, Fabaceae y Rosaceae no se agruparon.
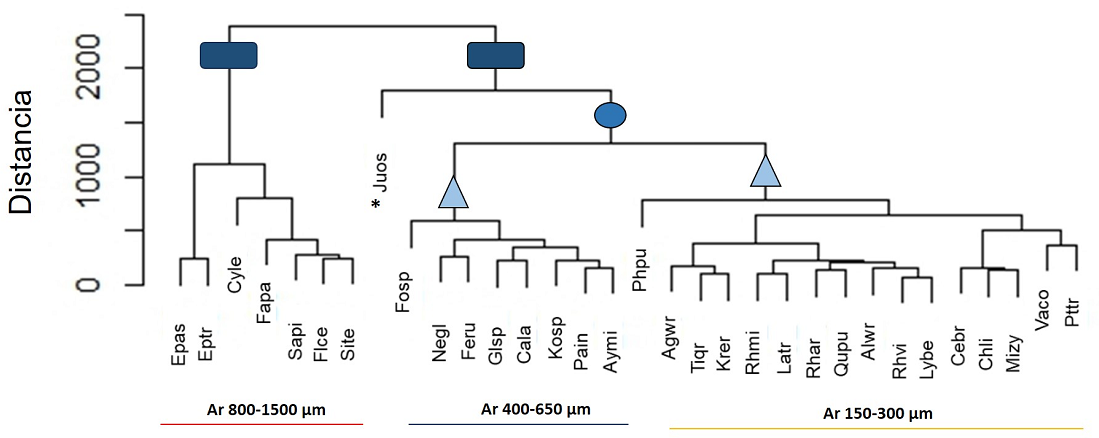
Figura 6 Agrupación de las 32 especies con base en sus caracteres cuantitativos de la madera. Las especies se dividen en dos grupos (rectángulos), el mayor (circulo) excluye a Juniperus osteosperma (Juos) y forma dos subgrupos (triángulos) que excluyen cada uno a su vez a Fouquieria splendens (Fosp) y Physaria purpurea (Phpu). Ar = Altura de radios, * = única especie que no presenta vasos. Los acrónimos de las especies se encuentran en la Tabla 1.
Discusión
Todas las especies mostraron las características típicas de la familia a la cual pertenecen (Metcalfe & Chalk 1950, Henrickson 1972, Gibson 1977, Michener 1983, Zhang 1992, Carlquist 1989, 2000, 2005, Pace et al. 2022), que se discuten más adelante. A pesar de la diversidad taxonómica analizada, las especies comparten en este matorral y con otros dos matorrales, anillos de crecimiento marcados, porosidad anular, fibras de paredes gruesas a muy gruesas y radios heterocelulares, mientras que la altura de los radios resulto ser el carácter cuantitativo más relevante para la agrupación de especies en la Sierra de Juárez. No hay caracteres cuantitativos que separen a las especies de la misma familia como grupos definidos.
Comparaciones de la madera por grupo taxonómico. Juniperus osteosperma (Cupressaceae) compartió la transición abrupta entre madera temprana y tardía, radios homocelulares exclusivamente uniseriados y campos de cruce tipo crupresoide con otras especies de Juniperus y específicamente el parénquima axial abundante con J. cedrus Webb & Berthel y J. brevifolia (Seub.) Antoine (De Palacios et al. 2014).
Ambas especies de Ephedra (Ephedraceae) tuvieron porosidad anular, placas de perforación foraminada, presencia de fibrotraqueidas, traqueidas y radios multiseriados, pero no presentaron engrosamientos helicoidales como señala Carlquist (1989) para E. trifurca Torr. ex S.Watson y E. aspera. Tampoco se observaron cristales registrados por Carlquist (1989) en los radios de E. trifurca. Ese mismo autor indica que los caracteres cuantitativos delimitan mejor las especies de Ephedra; sin embargo, E. aspera y E. trifurca no mostraron diferencias cuantitativas marcadas, pero se separaron por presentar parénquima paratraqueal escaso y unilateral respectivamente.
Las tres especies de Rhus (Anacardiaceae) compartieron la porosidad anular, vasos agrupados, engrosamientos helicoidales en madera tardía, fibras libriformes no septadas, presencia de traqueidas vasculares y cristales prismáticos en radios. Se considera que la porosidad anular es un carácter que distingue al género Rhus, mientras que la presencia de canales resiníferos en radios puede ser variable (Young 1974). Gupta & Agarwal (2008) asocian especies deciduas de Rhus con la presencia de estos canales. Sin embargo, se trata de un carácter plesiomórfico, al igual que las fibras septadas en la familia, por lo que su ausencia debe interpretarse como un carácter derivado (Terrazas 1999). Las características cuantitativas de la madera de Rhus difieren de lo reportado por Abundiz et al. (2004) y se encuentran entre los intervalos registrados por Terrazas (1999) para la longitud de elementos de vaso y fibras. El índice de mesomorfia para las especies de Rhus fue menor a 200, indicando que se trata de especies xeromórficas a diferencia de las siete especies de Rhus con distribución en India, clasificadas como maderas mésicas (Gupta & Agarwal 2008).
Las cuatro especies de Asteraceae presentaron porosidad anular, traqueidas vasculares, fibras libriformes y depósitos en el parénquima axial. Estos caracteres pueden o no estar presentes en otros miembros de la familia (Carlquist 1966). Solo Flourensia cernua presentó engrosamientos helicoidales y Sidneya tenuifolia fue la única con fibrotraqueidas. Nahuatlea purpusii (Brandegee) V.A.Funk comparte la porosidad anular, vasos agrupados, parénquima paratraqueal escaso, radios heterocelulares y fibras libriformes (Abundiz et al. 2004, Sandoval-García et al. 2023) con las especies aquí estudiadas. Delbón et al. (2021) incluyen en su estudio a F. thurifera DC. y la anatomía de su madera es muy similar a F. cernua excepto en el diámetro de las fibras. Mehta (1982) reporta para Parthenium incanum diámetro de vasos ligeramente mayor, además de la presencia de engrosamientos helicoidales, fibrotraqueidas y depósitos en radios, ausentes en los individuos de esta especie muestreados en la Sierra de Juárez.
Chilopsis linearis es un género monotípico de Bignoniaceae que presentó porosidad anular, vasos solitarios y radios heterocelulares. Pace et al. (2015) reportan para C. linearis menor frecuencia de vasos, valores mayores en diámetros de vasos, alto y ancho de radios; porosidad semi-anular, presencia de engrosamientos helicoidales, fibras septadas y radios tanto homocelulares como heterocelulares que contrasta con las observaciones de este trabajo. Algunas de las sinapomorfías (parénquima paratraqueal escaso, presencia de tílides y punteaduras radio-vaso semirebordeadas) encontradas por estos autores para C. linearis fueron confirmadas en este trabajo. Las tílides también se han registrado en otros géneros de Bignoniaceae (Metcalfe & Chalk 1950).
Tiquilia greggii compartió con otros miembros de Boraginaceae la porosidad anular, vasos agrupados, placas de perforación simple y punteaduras intervasculares alternas (Metcalfe & Chalk 1950, Riedl 1997); así como los radios homocelulares con Antrophora williamsii I.J. Johnston y Lepidocordia punctata Ducke (Gottwald 1982) y las traqueidas vasculares con Bourreria purpusii Brandegee (Barajas-Morales 1981).
Physaria purpurea (Brassicaceae) presentó caracteres distintivos al resto de las especies analizadas en este matorral, como fueron las punteaduras intervasculares pseudoescalariformes y el parénquima que forma la matriz donde los vasos y algunos grupos de fibras se encuentran inmersos. Dickison (1990) menciona que en algunas especies las punteaduras pseudoescalariformes podrían representar un carácter ancestral conservado. Otros autores señalan que es difícil encontrarlo en plantas del desierto (Giménez et al. 2005), por lo que este carácter resalta en el matorral de la Sierra de Juárez. Adicionalmente, los radios por estar constituidos exclusivamente por células erectas, se interpretaron como paedomórficos, uno de los rasgos que Carlquist (1962) toma en cuenta para denominar a una madera paedomórfica. Lens et al. (2012) han sugerido que diversos factores en Arabidopsis thaliana (L.) Heynh como el recorte de flores o cambios en el fotoperiodo pueden estimular la inactivación de los genes SOC1 y FUL, que podrían desencadenar la formación de madera, como podría estar ocurriendo en Physaria purpurea. También asocian un mutante de esta misma especie con la ausencia de radios y concluyen que en Brassicaceae las características paedomórficas son comunes.
Cylindropuntia leptocaulis (Cactaceae) mostró porosidad anular como se ha registrado para otras especies de Cylindropuntia (Gibson 1977). No se observó una transición de madera no fibrosa a madera fibrosa reportada en algunas especies de Opuntia (Gibson 1997, 1978). Los radios altos y anchos con regiones no lignificadas también se han reportado para otros géneros de la familia (Metcalfe & Chalk 1950, Gibson 1973, 1977, Vázquez-Sánchez et al. 2017) y posiblemente favorecen el almacenamiento de fotosintatos y agua en compensación por la ausencia del parénquima axial. Las drusas en los radios de C. leptocaulis también se han registrado en los géneros de la familia (Metcalfe & Chalk 1950).
Glossopetalon spinescens (Crossosomataceae) presentó vasos solitarios, placas de perforación simple, parénquima paratraqueal escaso y fibrotraqueidas, distintivos de la familia (Metcalfe & Chalk 1950). Para otros géneros de Crossosomataceae como Crossosoma se reportan punteaduras intervasculares alternas (Metcalfe & Chalk 1950); pero en este estudio, G. spinescens presentó punteaduras intervasculares opuestas. Carlquist (2007) registra placas de perforación escalarifomes en G. stipuliferum H.St.John (= G. spinescens var. aridum), pero tampoco fueron observadas en este estudio. DeBuhr (1978) reporta además para la madera de Forsellesia nevadensis (= G. spinescens var. aridum) características cualitativas y cuantitativas muy similares a las registradas aquí, excepto por las punteaduras intervasculares alternas y la presencia de traqueidas que en las muestras de G. spinescens no se observaron. Por lo que se sugiere que la especie estudiada podría tratarse de una variedad distinta.
Las tres especies de Fabaceae (Mimosoide) compartieron la presencia de fibras gelatinosas y cristales prismáticos tipo “cámara” con otras especies de Mimosa y Vachellia, así como la porosidad anular con M. aculeaticarpa Ortega y el parénquima axial en bandas confluentes con en V. tortuosa (L.) Seigler & Ebinger y V. farnesiana (L.) Wight & Arn (Metcalfe & Chalk 1950, Montaño-Arias et al. 2017).
Quercus pungens (Fagaceae) al igual que sus congéneres tuvo vasos solitarios, traqueidas vasicéntricas, parénquima apotraqueal difuso en agregados, formando bandas delgadas y radios dimorfos (Metcalfe & Chalk 1950, Pérez-Olvera & Dávalos-Sotelo 2008). La presencia de tílides en vasos y cristales prismáticos en parénquima también es común para Quercus (Metcalfe & Chalk 1950, Arenas-Navarro et al. 2023). Tillson & Muller (1942) reportan para Q. falcata Michx. y Q. alba L. porosidad anular y señalan que especies caducifolias del género tienen porosidad anular y especies siempre verdes porosidad difusa, pero en Q. pungens no se cumple este supuesto. En este género se han registrado especies con porosidad variable y esto se ha relacionado a la estacionalidad de los sitios (Pérez-Olvera & Dávalos-Sotelo 2008, Arenas-Navarro et al. 2023). Cuantitativamente Q. pungens difiere a lo reportado por Arenas-Navarro et al. (2023) para otros robles, posiblemente asociado a que Q. pungens es un arbusto del matorral versus los árboles de los bosques pino-encino de la Sierra Madre del Sur.
Fouquieria splendens compartió con las otras especies de este género en Fouquieriaceae, la porosidad semi-anular, vasos en hileras radiales y placa de perforación simple (Metcalfe & Chalk 1950, Henrickson 1972, Carlquist 2000); la presencia de fibrotraqueidas se comparte con F. columnaris, F. fasciculata, F. leonilae Miranda, F. purpusii Brandegee y F. shrevei I.M.Johnst; las fibras gelatinosas con F. columnaris y la ausencia de cristales con F. macdougalii Nash (Carlquist 2000, Abundiz et al. 2004). Carlquist (2000) incluye en su trabajo a F. splendens y los datos cuantitativos son similares a los reportados en este estudio.
Fendlera rupicola mostró en su madera placas de perforación escalariforme, presencia de fibrotraqueidas y radios heterocelulares características distintivas de Hydrangeaceae (Metcalfe & Chalk 1950). Se había reportado la madera con porosidad anular a semi-anular (Stern et al. 1969) como en el material estudiado, las punteaduras intervasculares opuestas son comunes en Fendlera; sin embargo, F. rupicola presentó punteaduras alternas como Deutzia glabrata Kom., especie de Hydrangeaceae (Metcalfe & Chalk 1950). Stern et al. (1969) señala que F. rupicola tiene vasos exclusivamente solitarios, con tenues engrosamientos helicoidales, traqueidas y ausencia de parénquima axial caracteres no encontrados en los individuos analizados.
Koeberlinia spinosa presentó en su madera porosidad anular, vasos solitarios, punteaduras intervasculares alternas y fibrotraqueidas, características distintivas de Koeberliniaceae (Metcalfe & Chalk 1950). Para Koeberlinia se han registrado vasos con engrosamientos helicoidales y depositos de gomo-resinas, radios homocelulares y ausencia de cristales (Metcalfe & Chalk 1950, Gibson 1979), caracteres que difieren a lo encontrado, con excepción de los cristales que son raros en los radios de los individuos de la Sierra de Juárez. Gibson (1979) analiza la madera de K. spinosa y las amplitudes de variación en los caracteres cuantitativos que registra concuerdan con nuestros datos, con excepción del diámetro de vasos (de 43 a 149 μm) que es mucho mayor al de los individuos analizados (de 9 a 16 μm).
Carlquist (2005) reporta para Krameria erecta y K. bicolor S.Watson (Krameriaceae) vasos solitarios, como ocurre en la especie estudiada y lo relaciona con la presencia de traqueidas como apoyo para la conducción del agua. Además, reporta engrosamientos helicoidales en traqueidas, carácter que no se observó y parénquima axial en bandas angostas con paredes primarias no lignificadas con depósitos inorgánicos. Estos depósitos inorgánicos los asignamos como esferulitos. Carlquist (2005) menciona que la madera de Krameria se distingue por la presencia de radios paedomórficos y podría corresponder a los radios homocelulares exclusivamente de células erectas que se reportan aquí. Notoriamente, Abundiz et al. (2004) describen la madera de K. cytisoides Cav. y mencionan caracteres cualitativos que no observamos como el parénquima apotraqueal difuso y los radios heterocelulares con células procumbentes y erectas con depósitos obscuros, además de diferencias contrastantes en las dimensiones de la mayoría de los caracteres cuantitativos.
Salvia pinguifolia (Fernald) Wooton & Standl. al igual que otros miembros de Lamiaceae tuvo en su madera vasos agrupados, placa de perforación simple, punteaduras intervasculares alternas, fibras con punteaduras simples y radios heterocelulares (Metcalfe & Chalk 1950). Otros autores registran para S. canariensis L., S. lanceolata Brouss y S. pubescens Benth. porosidad anular, elementos de vaso con engrosamientos helicoidales, traqueidas vasculares y fibras septadas, caracteres que también compartió la especie presente en la Sierra de Juárez, excepto por los engrosamientos helicoidales que se observaron en las traqueidas y no en los elementos de vaso. En S. pinguifolia no se observaron cristales, estos contenidos inorgánicos de acuerdo con Carlquist (1992a) y Ceja-Romero et al. (2005), pueden ocurrir o no en el género. Abundiz et al. (2004) describen la madera de S. candicans M.Martens & Galeotti y reportan caracteres cualitativos distintos a los encontrados aquí, como son el arreglo de vasos en hileras radiales o en diagonal, punteaduras intervasculares coalescentes, elementos de vasos con engrosamientos helicoidales y depósitos gomosos, parénquima paratraqueal escaso y fibras también con depósitos obscuros, así como valores ligeramente mayores y solo menor para la frecuencia de vasos (54/mm²).
Ayenia microphylla mostró en su madera las características distintivas de algunas Malvaceae como son placas de perforación simple, punteaduras intervasculares alternas, fibras libriformes y depósitos obscuros (Metcalfe & Chalk 1950, Rojas & León 2019). A. microphylla presentó traqueidas vasculares, igual que en los géneros Malvastrum A.Gray; Plagianthus J.R.Forst. & G.Forst. y Wissadula Medik. (Metcalfe & Chalk 1950); el parénquima paratraqueal fue escaso como en Dombeya Cav; Ruizia cordata Cav. y Trochetia blackburniana Bojer ex Baker, así como radios heterocelulares como en Dombeya (Boura et al. 2011).
Castilleja lanata presentó en su madera porosidad difusa, vasos agrupados en patrón radial, placa de perforación simple, punteaduras intervasculares alternas, parénquima paratraqueal escaso, fibras libriformes y radios homocelulares, características distintivas de Orobanchaceae (Metcalfe & Chalk 1950, Michener 1983). Michener (1983) además menciona la presencia de engrosamientos helicoidales y placas de perforación escalariformes, traqueidas vasculares ocasionales y depósitos cristalinos en algunas especies de Castilleja, así como la ausencia de radios, caracteres no encontrados en este estudio. Para otras especies de Castilleja se han reportado radios homocelulares en C. arctica Krylov & Serg. y C. nubigena Kunth, esta última también con parénquima paratraqueal escaso (Schweingruber et al. 2020), que coincidió con lo aquí observado para C. lanata.
Las dos especies de Rosaceae de la Sierra de Juárez mostraron en su madera porosidad anular, placas de perforación simple, punteaduras intervasculares alternas, parénquima apotraqueal y fibrotraqueidas, caracteres distintivos de la familia (Metcalfe & Chalk 1950, Zhang 1992). Se difiere con estos autores en los caracteres reportados para Cercocarpus como elementos de vaso con engrosamientos helicoidales y presencia de cristales en parénquima axial. Ambas especies comparten vasos solitarios y radios heterocelulares con depósitos obscuros. Con respecto a los caracteres cuantitativos que reporta Zhang (1992) para Cercocarpus y Fallugia, se concuerda con lo aquí encontrado. La madera de C. fothergilloides Kunth analizada por Abundiz et al. (2004), difiere en los caracteres cualitativos (porosidad difusa, presencia de traqueidas y depósitos); así como con valores menores en los caracteres cuantitativos de vasos, fibrotraqueidas y radios de C. breviflorus A.Gray. Futuros estudios que incluyan las otras especies del género serán de gran relevancia para entender su variación.
Ptelea trifoliata L. mostró en su madera las características distintivas de Rutaceae, que de acuerdo con Metcalfe & Chalk (1950), corresponden a placas de perforación simple, punteaduras intervasculares alternas, parénquima paratraqueal vasicéntrico y fibras libriformes. Esos autores reportan engrosamientos helicoidales en elementos de vaso, pero estos solo los registramos en traqueidas. La presencia de traqueidas es rara en la familia, aunque se han descrito en los géneros Acradenia Kippist, Choisya Kunth y Skimmia Thunb. Abundiz et al. (2004) incluyen a P. trifoliata en su investigación y reportan vasos con depósitos gomosos, engrosamientos helicoidales en elementos de vasos y fibras; así como radios homocelulares, caracteres que no observamos.
Lycium berlandieri compartió la porosidad anular, placa de perforación simple y punteaduras intervasculares alternas con otras Solanaceae (Metcalfe & Chalk 1950); así como el arreglo dendrítico de los vasos, los engrosamientos helicoidales en los elementos de vaso, el parénquima apotraqueal difuso y los radios uni y biseriados con otras especies de Lycium L. (Metcalfe & Chalk 1950). Los engrosamientos helicoidales también se han reportado para la madera de L. brevipes Benth, L. carolinianum Walter, L. cestroides Schltdl. y L. europaeum L; las traqueidas vasculares en L. brevipes, L. cestroides, L. elongatum Miers, L. europaeum y L. fremontii A.Gray. Las areniscas se observaron en L. elongatum en fibrotraqueidas y se consideran comunes en el género (Fahn et al. 1986), en este estudio únicamente se encontraron en el parénquima axial. Con respecto a los caracteres cuantitativos son similares a los registrados por Carlquist (1992b) para Solanaceae.
Como otros representantes de Verbenaceae, Aloysia wrightii presentó en su madera porosidad anular, placa de perforación simple y parénquima paratraqueal (Metcalfe & Chalk 1950). Las fibras septadas son comunes en Verbenaceae, pero la ausencia de septos en A. wrightii aquí estudiada también se ha registrado en Petrea L. (Metcalfe & Chalk 1950). A. wrightii compartió con Citharexylum tetramerum Brandegee el parénquima paratraqueal escaso, los radios heterocelulares y las fibras libriformes (Abundiz et al. 2004). Siegloch et al. (2013) analizan la anatomía de la madera de dos especies de Aloysia, A. chamaedryfolia Cham sudamericana y A. gratissima (Gillies & Hook.) Tronc que se distribuye desde Arizona hasta Argentina. La madera de ambas especies difiere de la de A. wrightii, por la presencia de engrosamientos helicoidales en elementos de vaso, punteaduras intervasculares alternas, fibras septadas, presencia de fibras gelatinosas y ausencia de traqueidas; así como en los caracteres cuantitativos, que son mayores a los aquí registrados.
Los resultados de este trabajo son similares tanto cualitativa y cuantitativamente a lo presentado por Carlquist (2005) para Larrea tridentata (Zygophyllaceae), excepto por la porosidad anular y el índice de mesomorfía que es mayor (41). En Plectrocarpa Gillies ex Hook. & Arn. también se ha registrado parénquima axial estratificado (Metcalfe & Chalk 1950).
Comparación de matorrales xerófilos. En la Tabla 2 se sintetizan algunos caracteres de la madera que se comparan con los obtenidos en este trabajo y los trabajos previos para el matorral de California y el de Tehuacán. En los tres estudios la precipitación es menor a 600 mm anuales, de 350 a 600 mm en California y casi 500 mm en Tehuacán, observándose el valor más bajo para la Sierra de Juárez (~250 mm). Hay diferencias no solo en la composición florística sino también en el tipo de porosidad; en California la porosidad anular y semi-anular mantuvieron casi la misma proporción (44 y 46 % respectivamente), en la Sierra de Juárez dominó la porosidad anular (81 %) y en Tehuacán la difusa (59 %), esto posiblemente asociado a las precipitaciones de cada sitio. Los vasos agrupados dominaron en los tres sitios, este rasgo se confirma como una estrategia adaptativa xeromórfica, al aumentar y asegurar la conducción hidráulica (Carlquist & Hoekman 1985, Fahn et al. 1986, Wheeler & Baas 1991). La presencia de engrosamientos helicoidales y traqueidas fue mayor en California sugiriendo que los eventos estresantes en este matorral son más severos que en la Sierra de Juárez y que en Tehuacán.
Tabla 2 Comparación de caracteres de la madera de matorral xerófilo en la Sierra de Juárez con los matorrales xerófilos de California y Tehuacán.
| Variables | Matorrales xerófilos | ||
|---|---|---|---|
| California | Sierra de Juárez | Tehuacán | |
| Promedio de lluvia (mm) | 350-600 | 249 | 478 |
| Porosidad anular (%) | 44 | 81 | 12 |
| Porosidad semianular (%) | 46 | 16 | 29 |
| Porosidad difusa (%) | 10 | 3 | 59 |
| Vasos agrupados (%) | 70 | 52 | 71 |
| Engrosamientos helicoidales (%) | 39 | 22 | 24 |
| Traqueidas (%) | 77 | 47 | 59 |
| Parénquima axial paratraqueal | escaso | abundante | |
Aunque estas comunidades se consideran como matorrales xerófilos, las diferencias encontradas para los vasos entre los tres matorrales podrían asociarse a las variables ambientales como precipitación y temperatura, sugiriendo que el grado de aridez influye directamente en la estructura anatómica de la madera. Estudios adicionales donde se evalúen las variables ambientales con los atributos de los vasos son necesarios para confirmar estas aseveraciones.
Compensaciones en la madera. De acuerdo con Carlquist & Hoekman (1985) cuando la madera muestra caracteres como vasos amplios y solitarios, las especies tienen otros rasgos que compensan el patrón de arreglo y tamaño de los vasos como son presencia de traqueidas o bien raíces profundas, muerte parcial de algunas ramas, capas resinosas en hojas, caída de hojas por sequía o frío o formación de hojas anchas o angostas según la disponibilidad de agua. En la Sierra de Juárez se observaron algunos de estos rasgos en dos de las fabáceas analizadas, Neltuma glandulosa y Vachellia constricta; con diámetro de vasos amplio (> 50 μm) y baja frecuencia de vasos/mm² (< 80); estas especies se reconocen como freatófitas (Nilsen et al. 1987) porque desarrollan raíces profundas en busca de agua y son caducifolias. Otro ejemplo es Quercus pungens, que presentó un diámetro de vaso amplio (> 60 μm), compensado por la presencia de traqueidas vasicéntricas que mantienen el flujo de agua como se indica para otras especies de este género (Percolla et al. 2021, Arenas-Navarro et al. 2023).
Los anillos de crecimiento inconspicuos caracterizó a seis especies. Las dos primeras, Castilleja lanata y Physaria purpurea son las únicas sufrútices incluidas, ambas con una alta frecuencia de vasos (180 y 317/ mm2), agrupados y de diámetro reducido (13 y 19 μm); esta combinación de rasgos anatómicos podría favorecer su presencia en esta comunidad desértica. Fendlera rupicola, que es un arbusto, presentó placas de perforación escalariformes que podrían contribuir a evitar la cavitación a temperaturas bajo cero (Zimmermann 1983), las cuales se presentan en el invierno e inicio de la primavera en la Sierra de Juárez, compensando la porosidad semi-anular. Mientras que Fouquieria splendens y Larrea tridentata son especies bien conocidas por sus mecanismos frente a la sequía que les proporcionan sus hojas (Gibson 2012, Saldívar 2003). Finalmente, Krameria erecta, así como Castilleja lanata son consideradas en la literatura como especies hemiparásitas; sin embargo, son necesarios trabajos más exhaustivos en esta comunidad para comprender si la condición de hemiparásita podría estar influyendo en la anatomía de la madera.
No se encontró una relación evidente entre la porosidad y la fenología foliar como también lo reportaron Aguilar-Rodríguez & Barajas-Morales (2005) para el bosque húmedo de montaña. Tampoco se cumple la asociación que estas autoras proponen entre la presencia de anillos de crecimiento con el origen de las especies; considerando que en algunas especies estudiadas donde los anillos son inconspicuos su origen es boreal, como en Physaria purpurea (Fuentes-Soriano & Al-Shehbaz 2013), en Flendera rupicola (Soltis et al. 1995) o en Castilleja lanata (Méndez-Larios & Villaseñor 2001). Otra posible interpretación es que la porosidad podría estar asociado a la marcada estacionalidad en la zona de estudio.
Las distintas combinaciones de los elementos celulares de la madera se han descrito como el “triángulo de compensación” (Baas et al. 2004), que confiere propiedades como resistencia a embolismos, resistencia mecánica y eficiencia en la conducción y se interpretó como presente en las especies de la Sierra de Juárez. Por ejemplo, en las maderas analizadas, el triángulo se reconoce por los caracteres vasos abundantes (150/mm²) y agrupados; así como por la porosidad anular que aumentan la conductividad hidráulica cuando las lluvias llegan a presentarse. Además de elementos de vaso cortos (191 μm) y de diámetro angosto (36 μm) que pueden reducir la propagación de embolias por sequía, congelación y descongelación. Las fibras de paredes gruesas a muy gruesas que fueron distintivas en todas las especies estudiadas, le confieren resistencia mecánica frente a la formación de embolias (Martínez-Cabrera et al. 2009).
Se concluye que para este matorral las especies presentan caracteres cuantitativos con valores más bajos a lo registrado en otros trabajos, asociado a que las especies incluidas son arbustos menores a los 2 m de altura en la Sierra de Juárez y a la precipitación escasa menor a 250 mm anuales. No encontramos registros previos sobre las punteaduras intervasculares pseudoescalariformes y el parénquima formando la matriz de la madera en Brassicaceae, las punteaduras intervasculares opuestas en Crossosomataceae y los esferulitos en parénquima apotraqueal en Krameriaceae. El alto de los radios permite reconocer grupos de especies y seguramente compensa que el parénquima axial es ausente o escaso en la madera de las especies de este matorral xerófilo de la Sierra de Juárez. Se considera que las especies convergen en la porosidad anular y la presencia fibras con paredes gruesas a muy gruesas.
Material suplementario
El material suplementario de este trabajo puede ser consultado aquí: https://doi.org/10.17129/botsci.3655











 nueva página del texto (beta)
nueva página del texto (beta)



