La acumulación de mantillo en el piso forestal depende de la estacionalidad en el clima. Más del 70 % del piso forestal está formado por material foliar en descomposición y el resto de la necromasa son tallos, ramas, flores y frutos (Barbour et al. 1980, Robertson & Paul 2000). Con la descomposición del mantillo se liberan los nutrientes contenidos en la materia orgánica, por lo que este horizonte orgánico del suelo es un componente fundamental en el ciclo interno de nutrientes de los ecosistemas forestales (Facelli & Pickett 1991, Schlesinger & Bernhardt 2020). Además, el mantillo es el hábitat y la fuente principal de recursos para los organismos heterótrofos degradadores en el suelo (Singh & Gupta 1977) y puede reducir hasta en 90 % la erosión eólica e hídrica del suelo (Maass et al. 1988). En el bosque tropical estacionalmente seco (sensuDirzo et al. 2011), llamado de ahora en adelante bosque estacional, el crecimiento de las plantas, incluyendo el despliegue de las hojas, ocurre principalmente durante el periodo de lluvias, que dura entre 3 y 6 meses al año (de la Peña-Domene et al. 2022). En este ecosistema, la acumulación de mantillo se inicia cuando finaliza la época de lluvias y la mayoría de las especies leñosas dejan caer sus hojas senecentes (Campo et al. 2001, Zhang et al. 2014). La pérdida de masa de mantillo durante la época de secas es baja debido a que la falta de agua limita la lixiviación de los productos de descomposición y la actividad microbiana (Martínez-Yrízar et al. 1992, Campo et al. 1998, Lambers et al. 2008). En contraste, en la época de lluvias, la mayor disponibilidad de agua acelera la descomposición del mantillo (Martínez-Yrízar 1995, Pandey et al. 2013, Bejarano et al. 2014, Campo 2016). Así, en el bosque estacional, en la época seca se favorece la acumulación de mantillo mientras que durante las lluvias, debido a las condiciones favorables para la descomposición, disminuye la masa de mantillo.
La cantidad de mantillo depende de la vegetación en un sitio. En el bosque estacional, la ganadería extensiva es la causa principal de la reducción de la cubierta vegetal (Miles et al. 2006, Mendoza-Ponce et al. 2018, Seixas et al. 2018). Además, el pisoteo del ganado compacta el suelo, disminuyendo el crecimiento de nueva vegetación (Yates et al. 2000), por lo que puede haber necromasa de pastos, pero poca acumulación de mantillo forestal. La exclusión de la ganadería puede favorecer el proceso de sucesión natural (Stern et al. 2002), que incluye un aumento en la riqueza y cobertura de especies leñosas y el recambio de especies (Poorter et al. 2023). Durante este proceso, al incrementarse la cobertura de especies leñosas, aumenta la acumulación de mantillo forestal; por ejemplo, en bosques estacionales de Brasil (Souza et al. 2019) y México (Rojas-Robles 2019, Morffi-Mestre et al. 2020), se ha registrado un aumento en la masa de mantillo forestal con el tiempo sucesional. La acumulación de mantillo forestal aumenta con la cobertura de especies leñosas, resultado del proceso de sucesión natural.
El aumento en la cobertura vegetal durante la sucesión comienza con la llegada de especies colonizadoras. Estas especies, también llamadas pioneras o sucesionales tempranas (Connell & Slatyer 1977) tienen semillas pequeñas con alta vagilidad para ser dispersadas por animales o por el viento (Howe & Smallwood 1982); estas especies se caracterizan por tener altas tasas de crecimiento en condiciones de alta luminosidad (Rincón & Huante 1993). Además, estas especies también producen mucha hojarasca que se descompone rápidamente (Campo et al. 2001, Cárdenas & Campo 2007, Lambers et al. 2008). En algunos paisajes agropecuarios, el proceso de sucesión no comienza porque no hay fuentes de semillas de estas especies sucesionales tempranas (Martínez-Garza et al. 2011). En otros sitios, aunque si lleguen los propágulos, pocas semillas logran germinar y establecerse debido a la compactación del suelo (Vieira & Scariot 2006, Alba-García 2011). Además, en estas condiciones, las plántulas que logran establecerse son consumidas por el ganado (de la O-Toris et al. 2012) por lo que la sucesión natural no prosigue o es muy lenta y se requiere de la intervención humana.
La intervención que busca la recuperación de un ecosistema que ha sido degradado, dañado o destruido es llamada restauración ecológica (Gann et al. 2019). La intervención mínima, también llamada regeneración no asistida, busca la eliminación de la perturbación para que el ecosistema se recupere de forma natural mediante el proceso de sucesión secundaria (Ceccon & Martínez-Garza 2016, Chazdon & Guariguata 2016). Por otra parte, la intervención máxima, también llamada regeneración asistida, incluye el establecimiento de plantaciones de especies nativas (Chazdon & Guariguata 2016, Martínez-Garza et al. 2021). En las plantaciones de restauración, incluir un mayor número de especies puede favorecer la acumulación de mantillo; por ejemplo, en una selva estacional de la India, en áreas dominadas por una sola especie se registró una menor caída de hojarasca que en plantaciones mixtas (Rai et al. 2016). Si además bajo las plantaciones ocurre el proceso de sucesión natural (Lugo 1997, Montagnini 2007), una mayor riqueza de especies puede acelerar la recuperación de la capa de mantillo en sitios degradados.
Para el establecimiento de plantaciones de restauración se pueden elegir especies por su función en el ecosistema. Por ejemplo, muchas leguminosas tienen la capacidad simbiótica para fijar nitrógeno (N) (Sprent 2009). Gracias a esta simbiosis, las leguminosas pueden tener mejor desempeño, probablemente porque se ven menos afectadas por la baja disponibilidad de N en el suelo en los sitios perturbados (Huante et al. 1995, Martínez-Garza et al. 2016), lo que resultaría en una mayor caída de hojarasca. Por ejemplo, en plantaciones de leguminosas en Nicaragua que incluyeron a Samanea saman (Jacq.) Merr. y a Inga laurina (Sw.) Willd. se registró una mayor masa de mantillo que en plantaciones de especies no-leguminosas (Simarouba glauca DC., Simaroubaceae y Tabebuia rosea (Bertol.) DC., Bignoniaceae; Reyes-Trujillo & Rodríguez-Madrigal 2014). Si además las especies leñosas leguminosas mejoran las condiciones del suelo para el establecimiento de otras especies (Espindola et al. 2005, Sharma & Sunderraj 2005, Roa-Fuentes et al. 2015), es posible que una mayor riqueza de especies resulte en un mayor ingreso de hojarasca al piso forestal en las plantaciones con especies de leguminosas. Por otra parte, la velocidad de descomposición del mantillo también depende de la composición de especies; una mayor concentración de N y menor de lignina y componentes secundarios, predicen una mayor descomposición del mantillo (Lambers et al. 2008, Bejarano et al. 2014, Rai et al. 2016). Además, antes de que las plantas dejen caer sus hojas, ocurre el proceso de reabsorción de nutrientes (Cárdenas & Campo 2007), pero se ha visto que las leguminosas conservan una mayor concentración de N en su mantillo aún después de ocurrida la reabsorción (Constantinides & Fownes 1994). Las leguminosas podrían producir más mantillo gracias a sus altas tasas de crecimiento aún en suelos pobres en nutrientes y se espera que esta necromasa se descomponga más rápidamente debido a su mayor concentración de N.
En el 2017 se estableció un proyecto de restauración en áreas excluidas de la ganadería en la localidad de Quilamula, Sierra de Huautla, Morelos que incluyó siete combinaciones de plantación con especies leguminosas y no-leguminosas y áreas bajo sucesión natural de bosque estacional (Márquez-Torres & Martínez-Garza 2022). Después de cuatro años de establecidas estas plantaciones, pusimos a prueba las siguientes predicciones: (1) bajo las plantaciones de restauración se acumula una mayor masa de mantillo forestal que en los sitios bajo sucesión natural donde el crecimiento de la vegetación es lento debido a la falta de propágulos y a suelos altamente compactados, (2) la masa de mantillo forestal se acumula durante los meses de la época de secas cuando las leñosas dejan caer sus hojas mientras que esta se degrada durante los meses de la época de lluvias, (3) las plantaciones de especies leguminosas acumulan una mayor masa de mantillo forestal debido a su mejor desempeño en sitios degradados en comparación con el de las especies no-leguminosas. Además, las hojas senescentes de las leguminosas, al tener mayor concentración de N se descomponen más rápido, por lo que se espera una mayor disminución de la masa de mantillo al final de la época de lluvias, (4) la plantación de una mayor riqueza de especies leñosas predice una mayor masa de mantillo, (5) el proceso de reclutamiento diferencial debido a la intervención de restauración modifica la acumulación y descomposición del mantillo. Revelar que tratamientos de restauración mejoran la dinámica de acumulación y degradación del mantillo permitirá intervenir este ecosistema para asegurar la recuperación de este proceso del ecosistema y de los beneficios que produce en la fertilidad del suelo y, con ello, brinda a las personas locales.
Materiales y métodos
Este proyecto fue establecido en terrenos aledaños a la localidad de Quilamula (Latitud 18.5167, Longitud -99.0333), dentro de la Reserva de la Biosfera Sierra de Huautla (REBIOSH), con una altitud de 1,083 m snm (CONANP 2005). Quilamula pertenece al municipio de Tlaquiltenango, localizado al sur del Estado de Morelos, en el centro de México (Figura 1). El clima en la región es cálido subhúmedo con régimen de lluvias en verano y canícula en el mes de agosto; la temperatura media anual es 24.5 °C y el promedio de precipitación anual es 862 mm; cerca del 90 % de la precipitación se registra entre finales de mayo y octubre (García 2004, CONANP 2005). El promedio histórico anual de lluvia en esta localidad para los últimos 15 años fue de 986 mm (Márquez-Torres & Martínez-Garza 2022). La precipitación del año en que se estableció la plantación (2017) hasta los años en que se realizó este estudio (2021-2022) mostró una variación inter-anual del 16 % (Material suplementario Tabla S1), mientras que el rango de variación intra-anual fue de entre 114 y 140 % (Material suplementario Tabla S1 y Figura S1). En esta región, el material parental está conformado por rocas ígneas del Oligoceno- Mioceno, sedimentarias del Cretácico Inferior, litológicamente clasificadas como calizas y depósitos marinos interestratificados de areniscas y lutitas del Cretácico Superior (Lugo-Hubp 1984). Los suelos dominantes para la REBIOSH son feozem háplicos, regosoles éutricos y litosoles (INEGI 1981). En esta localidad, los suelos han sido clasificados como cambisoles y leptosoles (sensu World Reference Base for Soil Resources; Carrasco-Carballido et al. 2019). El ecosistema original en esta localidad es el bosque tropical estacionalmente seco también llamado selva baja caducifolia (Rzedowski 2006). Las especies dominantes en las áreas conservadas de la REBIOSH son las leguminosas Conzattia multiflora (B.L.Rob.) Standl, Lysiloma acapulcense (Kunth) Benth., L. divaricatum (Jacq.) J.F.Macbr. y no-leguminosas como varias especies de los géneros Bursera (Buseraceae) y Ceiba (Bombacaceae); la mayoría de los árboles dejan caer sus hojas al final de la época de lluvia y permanecen sin hojas de cinco a siete meses (CONANP 2005).
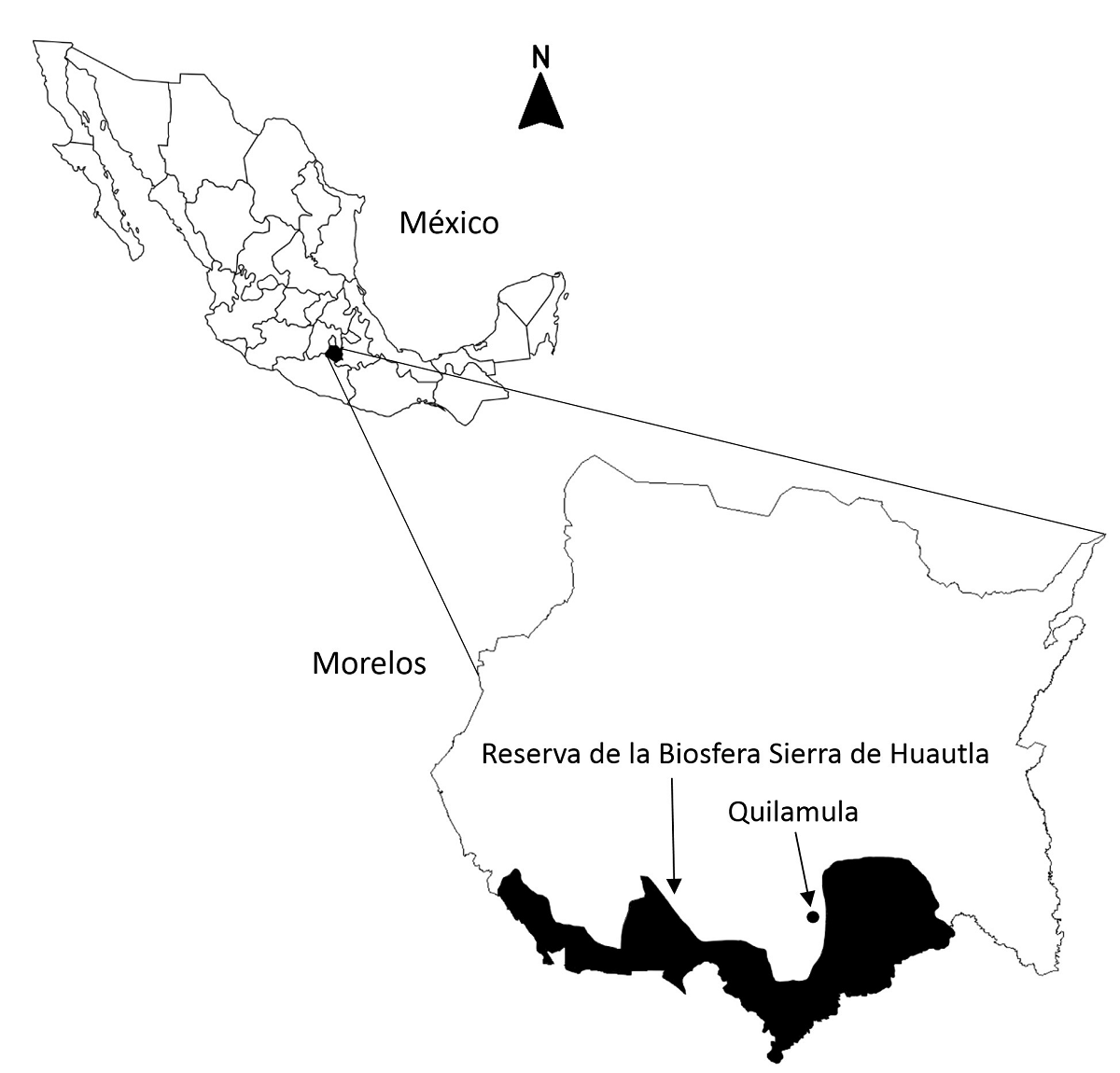
Figura 1 Ubicación del Ejido de Quilamula (punto negro) y de la Reserva de la Biosfera Sierra de Huautla en el estado de Morelos, en el centro de México (área negra).
Un terreno de 1.6 ha fue cercado en julio de 2017 con alambre de púas a cuatro niveles. Este terreno, con una pendiente de 10°, fue destinado inicialmente a la siembra de maíz y en los últimos 20 años para la cría de ganado con la vegetación secundaria que creció naturalmente en el lugar (Sr. Gilberto Quintero, com. pers.). La ganadería de monte, muy extendida en los tropicos de Latinoamérica (Figueroa et al. 2020, Pérez-Lombardini et al. 2021) disminuyó la cobertura secundaria a sólo (20 % de árboles dispersos de Mimosa benthamii J.F.Macbr. (Fabaceae); estos árboles fueron eliminados para establecer los tratamientos de plantación y sucesión natural en condiciones iniciales similares (Márquez-Torres 2022). A partir del 2013, los pastos exóticos africanos Andropogon gayanus Kunth y Pennisetum setaem (Forssk.) Chiov invadieron las áreas dedicadas a la ganadería de monte en la localidad (Sr. Evodio Rendón Alquicira, com. pers.). En ese terreno se establecieron 60 parcelas de 11.5 × 10 m, cada una con una separación de 3 m a lo largo y de 2.5 m a lo ancho (Material suplementario, Figura S2). En las parcelas asignadas a plantaciones se establecieron 30 plántulas de hasta 12 especies de árboles nativos de seis especies leguminosas y/o seis no-leguminosas (Tabla 1). Las plantaciones incluyeron monocultivos de las 12 especies seleccionadas y siete combinaciones de policultivos con la siguiente composición: i) tres leguminosas, ii) tres no-leguminosas, iii) seis leguminosas, iv) seis no-leguminosas, v) mixto 1, vi) mixto 2, y vii) 12 especies. Los tratamientos mixtos 1 y 2 fueron combinaciones de ocho especies cada uno, que incluían cuatro especies leguminosas y cuatro no-leguminosas (Tabla 1). Las plántulas fueron establecidas dentro de las parcelas en una disposición de cinco filas por seis columnas con una separación entre ellas de 1.5 m. Las plántulas de las especies incluidas en cada combinación (Tabla 1) fueron plantadas sistemáticamente dentro de las parcelas para evitar que dos de la misma especie estuvieran juntas. Finalmente, las tres parcelas restantes, donde no se plantaron árboles, se designaron como bajo sucesión natural. Todos los tratamientos tuvieron tres parcelas, consideradas réplicas, teniendo un total 21 parcelas de plantaciones mixtas, tres parcelas bajo sucesión natural y 36 parcelas de monocultivo (no incluidos en este estudio); el tratamiento de cada parcela fue asignado sistemáticamente para maximizar la distancia entre parcelas con el mismo tratamiento. La edad de las plántulas al momento del trasplante fue de aproximadamente un año con excepción de las de Bursera linanoe (La Llave) Rzed., Calderón & Medina (Burseraceae) que tenían dos años. En total se plantaron 1,710 plantas que fueron adquirida en los viveros forestales de las localidades Huajintlán y Ajuchitlán, pertenecientes a la Secretaría de Desarrollo Sustentable del Estado de Morelos.
Tabla 1 Siete composiciones (Comp) de plantación de restauración incluyendo de tres a 12 especies leguminosas (Legu) o no-leguminosas (No-Legu) nativas del bosque tropical estacionalmente seco de Quilamula, Morelos, México. Para cada especie se muestra su nombre científico, autoría y familia. La autoría de las especies fue consultada en tropicos.org.
| Número de especies plantadas | 3 | 3 | 6 | 6 | 8 | 8 | 12 | |
|---|---|---|---|---|---|---|---|---|
| Especie | Familia/Comp | Legu | No-Legu | Legu | No-Legu | Comp 1 | Comp 2 | Todas |
| *Dalbergia congestiflora Pittier | Fabaceae | X | X | X | X | |||
| *Eysenhardtia polystachya (Ortega) Sarg. | Fabaceae | X | X | X | X | |||
| **Gliricidia sepium (Jacq.) Kunth ex Walp. | Fabaceae | X | X | X | ||||
| Haematoxylum brasiletto H.Karst | Fabaceae | X | X | X | X | |||
| **Leucaena leucocephala (Lam.) de Wit | Fabaceae | X | X | X | X | |||
| **Pithecellobium dulce (Roxb.) Benth | Fabaceae | X | X | X | X | |||
| Amphipterygium adstringens (Schltdl.) Standl | Anacardiaceae | X | X | X | X | |||
| Bursera linanoe (La Llave) Rzed., Calderón & Medina | Burseraceae | X | X | X | X | |||
| Dodonaea viscosa Jacq. | Sapindaceae | X | X | X | X | |||
| Jacaratia mexicana A.DC. | Caricaceae | X | X | X | ||||
| Swietenia humilis Zucc. | Meliaceae | X | X | X | X | |||
| Tabebuia rosea (Bertol.) DC. | Bignoniaceae | X | X | X | X | |||
El género (*) o la especie (**) está registrada con capacidad para nodular en Sprent (2009) y/o Allen & Allen (1981)
Muestreo de mantillo. El muestreo de mantillo se realizó cuatro años después de establecida la plantación: al inicio y mediados de la temporada de lluvias (junio y octubre de 2021) y al inicio y mediados de la temporada de secas (enero y marzo de 2022). Dentro cada parcela se tomaron cuatro muestras de mantillo (20 × 20 cm) por fecha de muestreo. La primera colecta se tomó a 2 m de forma horizontal y 2 m de forma vertical de una esquina de la parcela. Los siguientes tres puntos de colecta por parcela para el mismo censo se tomaron de forma diagonal dejando 3 m de distancia entre cada punto de colecta (Material suplementario Figura S3). El muestreo de cuatro muestras de mantillo por censo permitió abarcar una mayor área de la parcela para incluir el mantillo bajo todas las especies (Material suplementario Figura S3). En los siguientes meses de colecta se midieron 2 m de forma horizontal de la colecta anterior para no repetir el punto de colecta y que se subestimara la acumulación de mantillo (Material suplementario Figura S3). En cada mes de colecta se obtuvo un total de 240 muestras de mantillo, 480 muestras por época (i.e., lluvias y secas) y al final un total de 960 muestras de mantillo. De cada muestra se separó la necromasa de pastos de la masa de mantillo forestal; se obtuvieron en total 1,692 muestras, incluyendo 960 muestras de mantillo forestal y 732 muestras de necromasa de pastos.
Las muestras se procesaron en el laboratorio de Biología Integrativa del Centro de Investigación en Biodiversidad y Conservación (CIByC) de la Universidad Autónoma del Estado de Morelos (UAEM) donde se secaron a una temperatura de 48 °C por tres días. Después, todas las muestras secas se pesaron con una balanza analítica (Sartorius CP622). Las cuatro muestras por parcela se mezclaron para formar una muestra compuesta por parcela: 24 muestras compuestas de cada censo que corresponden a las parcelas con plantaciones y a las de sucesión natural, y un total de 96 muestras compuestas. Después del muestreo de marzo del 2022, en todas las parcelas se registraron los atributos de la vegetación en pie: a partir de uno de los puntos del último muestreo de mantillo se trazó un círculo de 3 m de diámetro al interior de la parcela donde se evaluó la cobertura de especies plantadas y reclutadas. El área de muestreo de los atributos de la vegetación representó una cuarta parte de la parcela (28.3 m2).
Análisis Estadísticos. Para comparar la masa de mantillo entre las plantaciones de mayor riqueza (12 especies, N = 3) y la sucesión natural (N = 3) y en las plantaciones mixtas por grupo funcional (i.e., leguminosas y no-leguminosas) se realizaron dos análisis de varianza de medidas repetidas (RANOVA, por sus siglas en inglés). En ambos análisis, la variable repetida fue la masa de mantillo (g/m2) de junio y octubre del 2021 y de enero y marzo del 2022. El factor de variación del primer análisis fue el nivel de intervención de restauración (i.e., plantación y sucesión natural) y para el segundo, el grupo funcional. Para ambos análisis se transformó la masa de mantillo con el logaritmo natural para cumplir con los supuestos de normalidad y homocedasticidad (Zar, 1999). Para analizar el efecto de la riqueza de especies leñosas en la masa de mantillo se realizó una correlación lineal. La sucesión natural (cero especies plantadas) y las plantaciones mixtas con tres, seis, ocho, y 12 especies de leñosas fueron incluidas en este análisis.
Para evaluar el efecto de los atributos de la vegetación en pie después del último muestreo y las propiedades fisicoquímicas y químicas del suelo en la masa de mantillo se realizó un análisis de componentes principales (PCA, por sus siglas en inglés). Las nueve variables incluidas fueron, de la vegetación: (i) la suma de la necromasa de pastos de los cuatro muestreos, (ii) porcentaje de cobertura del pasto A. gayanus, (iii) porcentaje de cobertura del pasto P. setaem, (iv) porcentaje de cobertura de Mimosa affinis B.L.Rob (Fabaceae); y del suelo (primeros 10 cm del horizonte mineral): (v) el pH y la concentración de (vi) materia orgánica, (vii) de amonio (NH4 +), (viii) de nitrato (NO3 -) y (ix) de fósforo (P) total. Las cinco propiedades del suelo fueron evaluadas a mediados de la estación seca (marzo del 2019) (Jiménez-Hernández 2021). De estos atributos se obtuvieron dos variables compuestas (eje 1 y 2) del PCA que fueron usadas para predecir la masa de mantillo usando regresiones lineales simples. Todos los análisis se realizaron en STATISTICA 7 (Statsoft19, Inc.1984-2002).
Resultados
La masa de mantillo fue significativamente mayor en las plantaciones de 12 especies (686 ± 236 g/m2; promedio ± 1 error estándar) que en las áreas bajo sucesión natural (412 ± 97 g/m2; F (1, 4) = 19.58, P < 0.05; Material suplementario, Tabla S2). En promedio, la masa de mantillo fue mayor en junio (881 ± 149 g/m2) y menor en enero (363 ± 146 g/m2); el RANOVA reveló que el mes de colecta afectó la masa de mantillo (F (3,12) = 3.61, P < 0.05; Material suplementario, Figura S4) pero la prueba Post Hoc de Tukey reveló solo diferencias marginalmente significativas en la masa de mantillo de junio y enero (P < 0.06; Material suplementario, Tabla S3). La interacción del nivel de intervención con el mes de colecta no fue significativa (F (3,12) = 0.96, P > 0.44; Material suplementario, Tabla S2).
El análisis por grupo funcional mostró que, en promedio, la masa de mantillo fue mayor en las plantaciones de especies leguminosas (650 ± 104 g/m2) que en las de no-leguminosas (629 ± 104 g/m2) pero el análisis reveló una masa de mantillo estadisticamente similar (F (1,30) = 0.45, P > 0.84; Material suplementario, Tabla S4). La masa de mantillo en estas plantaciones fue significativamente mayor en marzo (949 ± 137 g/m2) y junio (876 ( 164 g/m2) que en octubre (463 ( 55 g/m2) y enero (434 ( 60 g/m2; Figura 2A) y el análisis reveló diferencias significativas por efecto del mes (F (3,30) = 18.70, P < 0.00001). La interacción del grupo funcional con el mes de colecta no fue significativa (F (3,30) = 1.62, P > 0.21; Material suplementario, Figura S5).
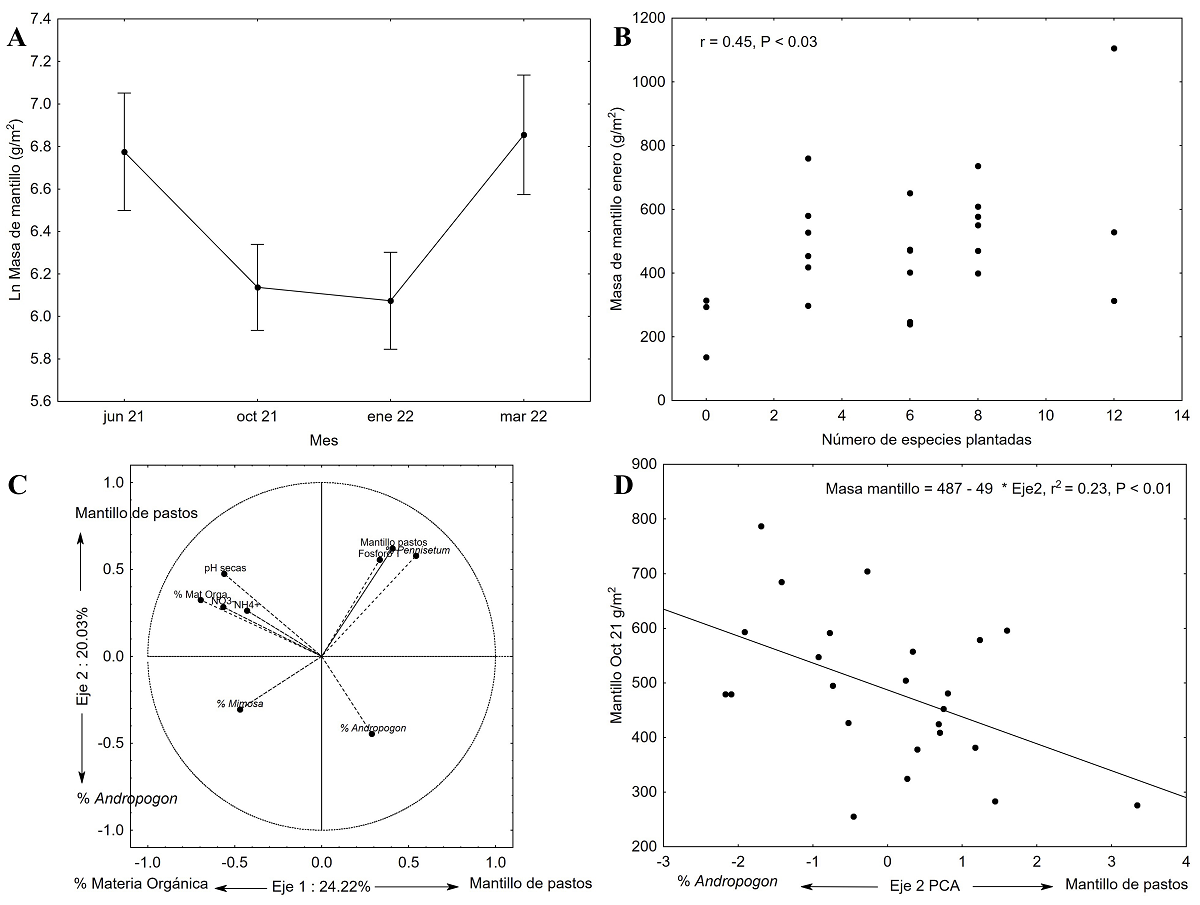
Figura 2 A. Logaritmo natural de la masa de mantillo durante cuatro meses en plantaciones de leguminosas y de no-leguminosas en Quilamula, Morelos, México. - Se muestra el estadistico del análisis de varianza de medidas repetidas. Los puntos negros corresponde a promedios y las líneas verticales son los intervalos de confianza al 75 %. Las letras muestran diferencias significativas evaluadas con la prueba de Post Hoc de Tukey. B. Relación de la masa de mantillo (g/m2) de enero del 2022 con la riqueza de árboles en plantaciones de restauración ecológica de 4 años en Quilamula, Morelos. Se muestra la r y la P. C. Valor de los vectores de nueve atributos del reclutamiento natural y del suelo usados para ordenar 24 parcelas en dos ejes del Análisis de Componentes Principales en áreas bajo restauración en Quilamula, Sierra de Huautla, Morelos. D. Relación de la masa de mantillo (g/m2) con el eje 2 de un Análisis de Componentes Principales en plantaciones de restauración ecológica de 4 años en Quilamula, Morelos. Se muestra la r 2, la línea y la ecuación de regresión.
La masa de mantillo de enero se correlacionó positivamente con el número de especies plantadas (r = 0.45, P < 0.03; Figura 2B).
El análisis de componentes principales (PCA) de los atributos de la vegetación y propiedades del suelo mostró que el 44.3 % de la variación fue explicada por los primeros dos ejes (Figura 2C). El eje 1 explicó el 24.2 % de la varianza total; este eje se relacionó con la necromasa de pastos (0.41) y la concentración de materia orgánica en el suelo (-0.70; Figura 2C). El eje 2 explicó el 20 % de la varianza total; este eje se relacionó con la necromasa de pastos (0.62) y la cobertura del pasto exótico A. gayanus (-0.44; Material suplementario, Tabla S5). El eje 2 del PCA explicó la masa de mantillo de octubre: la masa de mantillo aumentó conforme disminuyó la cobertura del pasto A.gayanus y la necromasa de pastos (Figura 2D).
Discusión
En este trabajo se evaluó la masa de mantillo en áreas bajo sucesión natural y en plantaciones de restauración de tres a 12 especies leñosas nativas después de cuatro años de establecimiento. Tomando en cuenta las plantaciones mixtas y la sucesión natural, la masa promedio de mantillo fue de 6.5 Mg/ha; este valor es similar al registrado en hábitats conservados del bosque estacionalmente seco de Jalisco, México (5.1 Mg/ha, Campo et al. 2001). Acorde a lo esperado, la masa de mantillo fue mayor (i) en las plantaciones de mayor riqueza de especies leñosas en comparación con la sucesión natural y (ii) a mediados de la época de secas (marzo) en comparación con al final de la época de lluvias (octubre). Además, la masa de mantillo en enero se relacionó positivamente con el número de especies plantadas. Por último, una menor cobertura del pasto exótico A. gayanus favoreció una mayor acumulación de mantillo forestal.
De acuerdo con lo esperado, la masa de mantillo fue mayor en las plantaciones de 12 especies en comparación con la registrada bajo sucesión natural, después de cuatro años. Estos resultados demuestras que si bien la masa de mantillo aumenta con el tiempo sucesional (Rojas-Chaves et al. 2015, Souza et al. 2019, Morffi-Mestre et al. 2020), las plantaciones de restauración aceleran este proceso. De acuerdo con nuestros resultados, en la selva húmeda de Costa Rica, plantaciones de restauración de cuatro especies tuvieron cuatro veces más mantillo (6.3 Mg/ha) que sitios bajo sucesión natural (1.4 Mg/ha) después de cinco años (Celentano et al. 2011). Pero, en otro proyecto de restauración en el mismo sitio que este estudio, la masa de mantillo fue similar en plantaciones de restauración con seis especies y en áreas bajo sucesión natural despúes de tres años (7.9 Mg/ha; Rojas-Robles 2019). Los estudios antes mencionados sugieren que además del tiempo sucesional (> cuatro años), el número de especies plantadas afecta la acumulación de masa de mantillo, lo que se discutirá a continuación.
La masa de mantillo aumentó con la riqueza de especies plantadas, como se esperaba. Nuestros resultados concuerdan con lo reportado para otros bosques tropicales: por ejemplo, en plantaciones de cuatro años en la selva húmeda de Panamá, la masa de mantillo fue mayor en plantaciones mixtas con seis especies (3.2 Mg/ha) en comparación con plantaciones monoespecíficas (2.8 Mg/ha; Scherer-Lorenzen et al. 2007). También, en una selva subtropical húmeda en Jiangxi, China, después de seis (Huang et al. 2018) y nueve años (Beugnon et al. 2023) de su establecimiento se registró que la masa de mantillo se duplicó en plantaciones con 16 especies (4.39 Mg/ha) en comparación con la registrada en monocultivos (1.96 Mg/ha). Por otro lado, estudios en plantaciones de restauración en el bosque denso ombrofílico de tierras bajas en Espírito Santo, Brasil revelaron que la masa de mantillo incrementó muy poco con la riqueza de especies en plantaciones con 29 (3.38 Mg/ha) a 114 especies de árboles (4.13 Mg/ha) después de nueve años (Caldeira et al. 2019). Los estudios disponibles para bosques tropicales sugieren que generalmente, la riqueza de especies plantadas favorece la acumulación de mantillo.
La masa de mantillo fue mayor a mediados de la época de secas (marzo) que al final de las lluvias (octubre), como se esperaba. La masa de mantillo se acumula en las secas cuando los árboles dejan caer sus hojas y se reduce en la época de lluvias gracias a condiciones más favorables para la descomposición (Zhang et al. 2014, Campo 2016). Por ejemplo, en la Caatinga, en Brasil se registró una reducción del 36 % en la masa de mantillo al final de la época de lluvias (Lucena et al. 2019) y en una selva semi-estacional en Espíritu Santo, Brasil se registró una reducción del 28 % (Neves et al. 2022). En este estudio se registró una reducción del 46 % de la masa de mantillo, siendo este valor menor a la reducción reportada en sitios conservados del bosque estacional en Chamela, Jalisco, México (68 %) con un régimen de lluvias similar (Martínez-Yrízar 1980). Esta menor reducción puede estar relacionada a diferencias en la calidad de la hojarasca, dado que la calidad nutricional de las hojas se incrementa con la edad del bosque (Cárdenas & Campo 2007, Bretherick et al. 2025). También, es posible que en los sitios bajo restauración haya una menor densidad de mesofauna (i.e., ácaros, colémbolos y gusanos del suelo; Powers et al. 2009) y otros organismos descomponedores, como los hongos saprófitos (Zhou et al. 2024). Además, un estudio reveló la sensibilidad de la descomposición a la precipitación diaria en estos bosques; eventos de precipitación mayores de 10 mm favorecen la descomposición del mantillo (Anaya et al. 2012). En el sitio de estudio, en junio del 2021, solo en 6 días se registró > 10 mm de lluvias (datos proporcionados por la Estación de Quilamula) lo que puede explicar la permanencia del mantillo, aunque la acumulación de precipitación de ese mes haya sido de 196 mm (Material suplementario, Figura S1). Adicionalmente, la masa de mantillo puede disminuir debido a la fragmentación y arrastre de partículas durante las primeras lluvias (Montaña et al. 1988), mientras que en las secas, cuando aumenta la temperatura y el dosel está más abierto debido a la pérdida de hojas, podría ocurrir una descomposición parcial por fotodegradación (Austin & Vivanco 2006). La dinámica de la masa del mantillo está asociada al clima, la presencia de los organismos descomponedores y la calidad de la hojarasca; el efecto de la composición de especies en la degradación del mantillo se discutirá a continuación.
Contrario a lo esperado, la masa de mantillo fue similar en plantaciones de especies leguminosas y de no-leguminosas sin importar el mes. En las plantaciones de leguminosas se esperaba una menor acumulación de mantillo al final de las lluvias porque hojas con una mayor concentración de N se descomponen más rápido (Constantinides & Fownes 1994, Rai et al. 2016). Además, bajo las leguminosas se esperaba una mayor acumulación de mantillo en secas favorecido por su simbiosis con bacterias fijadoras de N (Sprent 2009), aunque esta simbiosis es sensible a la sequía (Perroni-Ventura et al. 2010) y a la disponibilidad de N en el suelo (Barron et al. 2011). En este estudio, la sobrevivencia de seis especies leguminosas en los primeros 28 meses de la plantación fue mayor (25 %) que la de seis no-leguminosas (22 %, Márquez-Torres & Martínez-Garza 2022). Pero dos leguminosas con capacidad de nodulación (Gliricidia sepium (Jacq.) Kunth ex Walp. y Pithecellobium dulce (Roxb.) Benth.) mostraron porcentajes de sobrevivencia muy bajos (< 4 %, Márquez-Torres & Martínez-Garza 2022) mientras que Haematoxylum brasiletto H.Karst., especie que nunca ha sido registrada con nódulos (ver Tabla 1), presentó mayor sobrevivencia (28-46 %) y la no-leguminosa Dodonaea viscosa Jacq. (Sapindaceae) fue superior en sobrevivencia (73 %) a todas las especies plantadas (Márquez-Torres & Martínez-Garza 2022). También en Quilamula, México, en otra plantación de restauración con seis especies, tres especies leguminosas mostraron mayor sobrevivencia (> 65 %) que dos no-leguminosas (< 50 %) en los primeros 3 años de la plantación, mientras que una especie leguminosa con capacidad de nodulación (Erythrina americana Mill.) (Sprent 2009) sufrió la más alta mortalidad (> 98 %, Carrasco-Carballido et al. 2019). También, en plantaciones de restauración en la selva húmeda, en el primer año, después de una sequía extendida, tres especies leguminosas tuvieron sobrevivencias de entre 34-48 % mientras que 15 especies no-leguminosas mostraron un intervalo más amplio de sobrevivencia (1-82 %, Martínez-Garza et al. 2013). Estos estudios muestran que la sobrevivencia de las especies leñosas leguminosas no siempre es la más alta ni está relacionada a su capacidad de nodulación. Además, es posible que haya restricciones de humedad y de nutrientes que limiten el proceso de la fijación de N atmosférico.
La variabilidad en el crecimiento de las especies dentro de los grupos funcionales pudo haber afectado la acumulación de mantillo. En este estudio, el crecimiento fue similar para las seis especies leguminosas en comparación con las seis no-leguminosas y varió dependiendo de la combinación de especies plantadas (Márquez-Torres 2022). También, en otra plantación de restauración establecida en esta localidad, el crecimiento de cuatro especies leguminosas fue similar al de dos no-leguminosas (Carrasco-Carballido et al. 2019). Por otra parte, en plantaciones de restauración con 24 especies en la selva húmeda, en los primeros seis años, tres especies leguminosas tuvieron mayores tasas de crecimiento en diámetro que cinco no-leguminosas (Martínez-Garza et al. 2016). El mayor crecimiento de las plantas está relacionado con una mayor producción de hojarasca; por ejemplo, la relación positiva entre el crecimiento de los árboles y la producción de hojarasca se ha revelado en plantaciones en ecosistemas semiáridos de México (Ngangyo-Heya et al. 2017). Estos hallazgos muestran la relevancia de la identidad de las especies dentro de cada grupo funcional para explicar la acumulación de mantillo. En un estudio con menos especies, el patrón fue más claro: en sistemas de producción de Coffea arabica L. (Rubiaceae) dentro de un bosque estacionalmente seco en Nicaragua se registró que la masa de mantillo fue mayor en plantaciones de leguminosas (Samanea saman e Inga laurina) que en plantaciones de no-leguminosas (Simarouba glauca [Simaroubaceae] y Tabebuia rosea [Bignonaceae]; Altamirano-Tinoco 2005, Reyes-Trujillo & Rodríguez-Madrigal 2014). También, en este estudio, dado que se registró un desempeño diferencial de las especies en las combinaciones establecidas, el muestreo utilizado pudo haber oscurecido los patrones de acumulación de mantillo, por lo que el análisis de la dinámica del mantillo en los monocultivos podría revelar el efecto del desempeño y fenología foliar de cada especie. Finalmente, el reclutamiento natural en cada tratamiento también pudo afectar estos resultados.
El proceso de reclutamiento diferencial debido a la intervención de restauración modificó la masa de mantillo, como se esperaba. El análisis de la vegetación en pie al final del estudio evidenció el efecto negativo que tuvo la invasión de dos especies de pastos perennes de origen africano (CANEI 2010) en la acumulación de mantillo forestal: (i) Pennisetum setaceum es un pasto dispersado por el ganado (Areces-Berazain 2023), (ii) Andropogon gayanus (Figura 3) es un pasto resistente al manejo del fuego con una gran capacidad de rebrote y que puede alcanzar hasta 3 m de altura (Keller-Grein & Schultze-Kraft 1989, Ramírez-Reynoso et al. 2020). Además, en los sitios con mayor cobertura de A. gayanus y mayor necromasa de pastos, se registró una menor acumulación de mantillo forestal al final de la época de secas. Por otra parte, en todos los tratamientos, los reclutas de la leguminosa sucesional temprana, Mimosa affinis, nativa de la REBIOSH (Wang et al. 1999), fueron los más abundantes. Otros estudios han revelado que la exclusión de la perturbación aumenta el reclutamiento de varias especies del género Mimosa; por ejemplo, M. benthami J.F.Macbr. fue la recluta más abundante en áreas bajo restauración en El Limón de Cuauchichinola, Morelos, México en los primeros cuatro años de intervención (Alba-García 2011); esta especie también dominó la regeneración de avanzada de estos sitios a los seis años de la intervención (Martínez-Pérez 2014). Además, en un campo experimental en Seropédica, Brasil, se registró que después de un año, M. caesalpiniifolia Benth., aportó más masa al mantillo que otras leguminosas sucesionales tempranas como Acacia mangium Willd. y A. holosericea A.Cunn. ex G.Don (Andrade et al. 2000). También, en Permanbuco, Brasil se registró que M. caesalpiniifolia aportó más masa de mantillo que otra leguminosa sucesional temprana, Gliricidia sepium (Jacq.) Kunth ex Walp durante los primeros dos años de establecimiento (de Oliveira Apolinário et al. 2016). La cobertura de Mimosa affinis en este estudio también pudo obscurecer la diferencia en la dinámica del mantillo en plantaciones de leguminosas y no-leguminosas (ver Material suplementario, Figura S5). Por otra parte, una mayor concentración de N en el suelo puede beneficiar a las invasoras; por ejemplo, se sabe que P. setaceum se beneficia de una mayor disponibilidad de N en el suelo (Areces-Berazain 2023). El efecto negativo de la cobertura de pastos en la masa de mantillo forestal sugiere que, en los sitios bajo restauración, los árboles plantados y reclutados compitieron con los pastos exóticos que antes habían sido controlados por el ganado.

Figura 3 Andropogon gayanus (Poaceae) en lluvias (A) y en secas (B) en plantaciones de restauración en Quilamula, Sierra de Huautla, Morelos. Fotos de Gerardo A. Rojas-Robles.
Implicaciones para la restauración ecológica del bosque estacionalmente seco. En este ecosistema, la restauración del mantillo forestal evita la erosión eólica en la prolongada estación seca y la erosión hídrica al inicio de la temporada de lluvias. A pesar del efecto del mantillo en el éxito de las plantaciones en este ecosistema (Barajas-Guzmán et al. 2006, González-Tokman et al. 2018), su recuperación es poco considerado en las prácticas de restauración (Mesa-Sierra et al. 2025). Los resultados de este estudio muestran que para restaurar la masa de mantillo se debe (i) establecer plantaciones de restauración en sitios donde la sucesión natural sea lenta, (ii) dado que la plantación de leguminosas no asegura su buen desempeño, se debe plantar una mezcla de especies, sobre todo de aquellas para las que ya se conoce su desempeño en sitios degradados; por ejemplo, una revisión sistemática reveló que hasta el 2022 había información sobre el desempeño de al menos 65 especies leñosas nativas del bosque estacional de México (Hernández-Barrera 2024); además, se sugiere plantar un mayor número de individuos de aquellas especies de interés con desempeño bajo y siempre plantar nuevas especies para generar conocimiento sobre ellas (Restauración experimental sistemática sensuHowe & Martínez-Garza 2014), (iii) plantar el mayor número de especies disponibles si no es posible producirlas en vivero, llevar a cabo la siembra directa de semillas sucesionales tempranas y tardías una vez que exista cierta cobertura vegetal (Martínez-Garza et al. 2022) y, (iv) realizar un monitoreo constante para controlar el crecimiento de pastos exóticos invasores. Si se identifica que la sucesión está siendo detenida por ellos, se sugiere realizar acciones de manejo adaptativo (Gann et al. 2019). Adicionalmente, la literatura disponible recomienda no eliminar toda la vegetación establecida, ya que protege el suelo cuando las plantaciones son jóvenes, además de que favorece el reclutamiento (Martínez-Garza et al. 2022). En suelos desnudos, considerar el uso de acolchados que mejoren el desempeño de las especies plantadas (Barajas-Guzmán & Barradas 2013). Estudios adicionales sobre la recuperación de los nutrientes en el suelo gracias al restablecimiento del mantillo forestal permitirán seleccionar tratamientos para acelerar la restauración del bosque estacionalmente seco.
Material suplementario
El material suplementario de este trabajo puede ser consultado aquí: https://doi.org/10.17129/botsci.3576.











 nueva página del texto (beta)
nueva página del texto (beta)



