INTRODUCCIÓN
La industria procesadora de carne es una de las mayores consumidoras del agua dulce total utilizada en la industria agrícola y ganadera a nivel mundial; genera grandes volúmenes de aguas residuales, debido al sacrificio de animales y a la limpieza de las instalaciones (Bustillo-Lecompte y Mehrvar 2015). Las aguas residuales contienen altos valores de fósforo total (PT), nitrógeno total (NT), carbono orgánico total (COT), demanda química de oxígeno (DQO), sólidos suspendidos totales (SST), demanda bioquímica de oxígeno (DBO) y aceites y grasas, que desencadenan una serie de impactos ambientales como disminución del oxígeno disuelto en el cuerpo receptor y presencia elevada de nitrógeno con el efecto de provocar eutrofización (de Sena et al. 2009, Bustillo-Lecompte y Mehrvar 2015). Además, la inadecuada gestión de las aguas residuales de los camales tiene como consecuencia depósitos de lodo, emanaciones de gases (olores) y elevada carga bacteriológica (Qamar et al. 2022).
El desinterés por el control y tratamiento de los efluentes convirtió esta actividad en un problema ambiental; frente a ello, los procesos de oxidación avanzada (POA) Fenton y foto-Fenton son alternativas de tratamiento favorables y convenientes para la oxidación de compuestos orgánicos, hasta lograr la mineralización de los contaminantes (de Sena et al. 2009).
Los POA se fundamentan en procesos físicos y químicos capaces de alterar profundamente la estructura química de los contaminantes, formando radicales hidroxilos altamente reactivos y con baja selectividad, lo necesario para producir y acelerar reacciones de oxidación (de Sena et al. 2009, García et al. 2013).
El proceso Fenton consiste en una reacción entre el H2O2 y las sales de hierro (Fe2+) como catalizadoras, en medio ácido (pH 2.5-4), para la producción de radicales •OH. El catalizador suele ser sulfato de hierro (II) que no se consume en el proceso; por el contrario, el Fe2+ se regenera a partir del hierro férrico (Fe3+) (Silva et al. 2018), como se aprecia en la ecuación 1.
En la ecuación 2, la especie oxidada Fe3+ reaccionará nuevamente con el peróxido de hidrógeno, para producir radicales hidroperóxidos (HO2 •) con un potencial menor de oxidación-reducción (Eo = 1.76 V).
Cabe resaltar que los iones férricos Fe3+ se forman más rápidamente en la reacción 1 que en la reacción 2, y se van acumulando paulatinamente en solución acuosa hasta promover la aparición de precipitados de hidróxido férrico (Fe[OH]3) (Behrouzeh et al. 2022).
Entre los factores que intervienen en el proceso Fenton, es importante destacar que el proceso de degradación de contaminantes orgánicos requiere que el valor óptimo del pH sea de 2 a 4 (Gogate y Pandit 2004, Behrouzeh et al. 2022). Del mismo modo, la dosis de H2O2 influye directamente en la eficacia del proceso, mientras que la concentración de hierro está relacionada con la cinética de la reacción (Neyens y Baeyens 2003).
En el proceso foto-Fenton, la combinación de peróxido de hidrógeno y radiación UV con un ion Fe+2 o Fe+3 produce más radicales hidroxilos y, a su vez, aumenta la tasa de degradación de los contaminantes orgánicos. La regeneración fotoquímica de iones ferrosos por foto reducción de iones férricos se produce en la reacción foto-Fenton (ecuaciones 3 y 4). Los iones ferrosos generados reaccionan nuevamente con H2O2, generando un radical hidroxilo y un ion férrico. De esta manera, el ciclo continúa (Ameta et al. 2018).
Para evaluar la eficiencia del proceso foto-Fenton es importante mencionar los siguientes factores influyentes:
pH en rangos recomendables de 2 a 3, en los cuales los complejos de hidroxi-Fe+3 son más solubles y el Fe (OH)+2 es más fotoactivo; en valores menores a este rango, el ion férrico es más estable y con valores superiores el hidróxido férrico puede precipitarse (Terán 2016).
Velocidad de degradación, que está directamente relacionada con la cantidad de H2O2. Es decir, a mayor cantidad de H2O2 se incrementa la velocidad de degradación, ya que existe una mayor generación de radicales •OH. En cambio, es posible que a partir de una determinada cantidad de H2O2 ocurra una autodescomposición de éste por recombinación con •OH, afectando negativamente a la velocidad de reacción (Silva et al. 2018, Zhang et al. 2019).
Radiación UV, que es otro factor importante en el proceso foto-Fenton. Se aplica utilizando la radiación solar o iluminación artificial mediante lámparas como fuente de fotones. La eficiencia de esta tecnología no sólo depende del nivel de radiación y la longitud de onda, sino también de la distribución de la luz dentro del reactor, la cual afecta la absorción de la irradiancia por el catalizador (de la Obra et al. 2017). Se ha reportado que al aplicar iluminación artificial, el reactor de contacto incrementa la acción desinfectante de la luz UV en el agua a tratar, debido a la reflexión de los rayos en las paredes del reactor, la cual interviene en la distribución del flujo de luz en el agua (Anotai et al. 2006, O’Dowd y Pillai 2020).
Los procesos de oxidación avanzada (POA) constituyen una tecnología prometedora para la remediación de aguas residuales con altos contenidos de materia orgánica. Dentro de los POA más eficientes están los procesos Fenton y foto-Fenton como opciones potencialmente viables para la purificación de aguas residuales (García et al. 2013, Ameta et al. 2018, O’Dowd y Pillai 2020).
En ese contexto, la presente investigación tuvo como objetivo comparar la eficiencia de los procesos Fenton y foto-Fenton en el decaimiento de la DBO5 del efluente del Camal Municipal de Cusco-Perú.
MATERIALES Y MÉTODOS
Método de muestreo
Para el muestreo del efluente del Camal Municipal del Cusco-Perú se utilizó el Protocolo nacional para el monitoreo de la calidad de los recursos hídricos superficiales (R.J. Nº010-2016-ANA; ANA 2016). Se recolectó una muestra del tipo compuesta, constituida por porciones de muestras recolectadas por un periodo de 3 h en intervalos de 30 min, la cual estuvo debidamente homogenizada, a fin de conocer las condiciones promedio y asegurar la representatividad de la muestra. La toma de muestras para los procesos Fenton y foto-Fenton se realizó en diferentes días debido al volumen de muestra requerido para evaluar cada proceso, de acuerdo con el diseño experimental empleado.
Para el cálculo del volumen de cada porción de muestra se consideró la siguiente ecuación:
donde Vi es el volumen de cada porción de muestra, V el volumen total a componer, Qi el caudal instantáneo medido en el momento de la toma de muestra, Qp el caudal promedio durante el muestreo y n el número de alícuotas tomadas.
Análisis de la DBO5
El análisis inicial de la DBO5 y las muestras después de la aplicación de los procesos Fenton y foto-Fenton fue realizado con métodos estandarizados de la APHA-AWWA-WEF (2017).
Procedimiento experimental del proceso Fenton
La metodología empleada se adaptó con base en las investigaciones realizadas por Anotai et al. (2006) y Behrouzeh et al. (2022). Se realizaron 15 experimentos en un sistema discontinuo por lotes en condiciones controladas de temperatura y presión ambiente. Para cada experimento se utilizaron 1000 mL de la muestra compuesta, se ajustó el pH deseado utilizando HCl al 37 % (v/v) de la marca Merck; se colocaron los vasos precipitados en la prueba de jarras, y se añadieron sulfato ferroso heptahidratado (FeSO4•7H2O) y peróxido de hidrógeno (H2O2) al 30 % (v/v). La solución permaneció en agitación constante de 150 rpm por 1 h, después de lo cual se neutralizó añadiendo KOH (Merck) al 25 % (m/v). Se dejó decantar por 5 min y se realizó una filtración rápida. Posteriormente se realizó la medición de la DBO5.
Procedimiento experimental del proceso foto-Fenton
De manera similar al proceso Fenton, se realizaron 15 experimentos mediante un sistema discontinuo en condiciones controladas de temperatura y presión ambiente. Se realizó el montaje del fotorreactor con una lámpara UV de 13 W antes de iniciar el tratamiento. El volumen de cada alícuota proveniente de la muestra compuesta y filtrada a fin de retirar el material grueso fue de 1000 mL. Se ajustó el pH añadiendo HCl al 37 % (v/v) de la marca Merck. Se añadió el FeSO4•7 H2O y el H2O2 al 30 % (v/v) con un tiempo de reacción de 1 h. Finalizado dicho proceso, se neutralizó la solución añadiendo KOH grado reactivo de la marca Merck al 25 % (m/v), se dejó decantar por 5 min y se realizó una filtración rápida. Luego de ello se procedió a realizar le medición de la DBO5.
Diseño experimental de los procesos Fenton y foto-Fenton
Se aplicó el diseño de caja Behnken para determinar la dosis óptima de las variables del proceso Fenton, las mismas que fueron aplicadas en el proceso foto-Fenton. Se empleó el programa Statgraphics para obtener la matriz de distribución de los 15 experimentos para cada tratamiento, cuyos tres factores estuvieron constituidos por los parámetros de eficiencia del proceso Fenton: FeSO4•7 H2O, H2O2 y pH.
En el proceso foto-Fenton, además de los parámetros de eficiencia, los 15 tratamientos ejecutados fueron sometidos a radiación UV-C. El reactor estuvo expuesto a la irradiación de una lámpara de luz ultravioleta con una potencia de 13 W y una longitud de onda de 254 nm. En cuanto a los niveles, se tuvieron los siguientes: nivel alto (+), nivel intermedio (0) y nivel bajo (-), cuya variable de respuesta fue el porcentaje de decaimiento de la DBO5, tal como se muestra en el cuadro I.
CUADRO I DISEÑO DE CAJA BEHNKEN DE LOS PARÁMETROS DE PROCESO FENTON Y FOTO-FENTON.
| Factores | Código de niveles | ||
| - | 0 | + | |
| FeSO4•7H2O (mg/L) | 1200 | 1700 | 2200 |
| H2O2 (mg/L) | 700 | 900 | 1100 |
| pH | 2.5 | 3.0 | 3.5 |
| Variable respuesta | Decaimiento de la DBO5 (mg/L) | ||
DBO5: demanda bioquímica de oxígeno; FeSO4•7H2O; sulfato ferroso heptahidratado; H2O2: peróxido de hidrógeno; pH: potencial de hidrógeno.
En relación con el análisis de los datos obtenidos y su procesamiento para los procesos Fenton y foto-Fenton, se empleó el programa SPSS para la prueba de hipótesis. De igual modo, se empleó el programa Statgrafics Centurión XVI para desarrollar los diferentes gráficos y diagramas que permitieron visualizar los porcentajes de remoción de la DBO5 en función de los valores de los parámetros de proceso.
RESULTADOS Y DISCUSIÓN
Caracterización física y química del efluente del Camal Municipal de Cusco. Procesos Fenton y foto-Fenton
Los resultados obtenidos en el cuadro II muestran que el efluente del camal presenta una elevada cantidad de compuestos orgánicos, con valores de DBO5 entre 1200 y 3900 mg/L DQO entre 2500 y 5200 mg/L. Asimismo, se puede inferir que la composición física y química del efluente presenta una alta variabilidad relacionada con los días de monitoreo debido a una variación diaria en el número de animales sacrificados.
CUADRO II RESULTADOS DEL ANÁLISIS FÍSICO Y QUÍMICO DEL EFLUENTE DEL CAMAL MUNICIPAL DEL CUSCO.
| Muestra compuesta | Día de monitoreo | pH | Temperatura (ºC) | Oxígeno disuelto (mg/L) | Conductividad (uS/cm) | TDS (mg/L) | Turbiedad (NTU) | DBO5 (mg/L) | DQO (mg/L) |
| Fenton | 1 (inicio de semana) | 7.5 | 17.79 | > 0.05 | 1526 | 796 | 559 | 1208 | 2501 |
| Foto-Fenton | 2 (último día de la semana) | 7.5 | 19.0 | > 0.05 | 1668 | 831 | 718 | 3947 | 5202 |
DBO5: demanda bioquímica de oxígeno; DQO: demanda química de oxígeno; pH: potencial de hidrógeno; TDS: total de sólidos disueltos.
Eficiencia de remoción de la DBO5 del efluente del camal empleando el proceso Fenton
En el cuadro III se presentan los resultados del proceso Fenton. Se observa que todos los experimentos presentaron un porcentaje de decaimiento de la DBO5 superior al 70 %, lo cual demuestra que este proceso degradó eficientemente la materia orgánica presente en el efluente del Camal Municipal del Cusco. En la figura 1 se presenta el esquema del proceso de degradación.
CUADRO III RESULTADOS DEL TRATAMIENTO FENTON.
| Experimento | FeSO4•7H2O (mg/L) | H2O2 (mg/L) | pH | DBO5 Antes del tratamiento (mg/L) | DBO5 después del tratamiento (mg/L) | Porcentaje de decaimiento de la DBO5 |
| 1 | 1200 | 700 | 3.0 | 1207.89 | 116.09 | 90.39 |
| 2 | 2200 | 700 | 3.0 | 1207.89 | 360.91 | 70.12 |
| 3 | 1200 | 1100 | 3.0 | 1207.89 | 103.17 | 91.46 |
| 4 | 2200 | 1100 | 3.0 | 1207.89 | 94.23 | 92.20 |
| 5 | 1200 | 900 | 2.5 | 1207.89 | 72.91 | 93.96 |
| 6 | 2200 | 900 | 2.5 | 1207.89 | 100.59 | 91.67 |
| 7 | 1200 | 900 | 3.5 | 1207.89 | 113.31 | 90.62 |
| 8 | 2200 | 900 | 3.5 | 1207.89 | 80.13 | 93.37 |
| 9 | 1700 | 700 | 2.5 | 1207.89 | 121.78 | 89.92 |
| 10 | 1700 | 1100 | 2.5 | 1207.89 | 139.13 | 88.48 |
| 11 | 1700 | 700 | 3.5 | 1207.89 | 99.73 | 91.74 |
| 12 | 1700 | 1100 | 3.5 | 1207.89 | 102.05 | 91.55 |
| 13 | 1700 | 900 | 3.0 | 1207.89 | 110.26 | 90.87 |
| 14 | 1700 | 900 | 3.0 | 1207.89 | 115.43 | 90.44 |
| 15 | 1700 | 900 | 3.0 | 1207.89 | 108.27 | 91.04 |
DBO5: demanda bioquímica de oxígeno; FeSO4•7H2O; sulfato ferroso heptahidratado; H2O2: peróxido de hidrógeno; pH: potencial de hidrógeno.
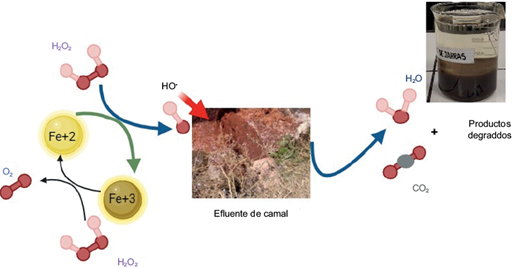
Fig. 1 Esquema del proceso Fenton en la degradación de la materia orgánica del Camal Municipal del Cusco.
De acuerdo con los resultados obtenidos en el cuadro III destaca el experimento 5, el cual presenta un 93.96 % de decaimiento de la DBO5. Este resultado corresponde a una interacción óptima de los variables del proceso, probablemente por la mayor cantidad de radicales hidroxilos generados a través de la reacción a pH de 2.5.
Al comparar estos valores los reportados en la literatura, Páramo (2015) obtuvo resultados similares con el 95 % de decaimiento de la DQO del efluente de un rastro municipal, aplicando las siguientes condiciones experimentales: Fe2+ 111.6 mg/L, H2O2 = 200 mg/L y pH = 3. En otro estudio, Montero del Águila et al. (2018) lograron un decaimiento máximo del 78.81% de la DQO del efluente del Camal Municipal de Chota con las siguientes condiciones experimentales: 1875 mg/L de FeSO4, H2O2 = 1000 mg/L y pH = 3, por lo que se infiere que, al añadir mayor cantidad de FeSO4 se incrementa la velocidad de degradación.
En la figura 2 se muestra la interacción de los factores de concentración del H2O2 y el FeSO4•7H2O, así como el nivel de pH. Este gráfico muestra la magnitud e importancia de estos efectos estandarizados en el decaimiento de la DBO5. Asimismo, se observa una línea vertical de referencia que indica cuáles efectos son estadísticamente significativos, de la cual se infiere que siete de éstos tienen influencia significativa en el decaimiento de la DBO5. El mayor efecto positivo observado corresponde a las concentraciones del catalizador y el oxidante. Neyens y Baeyens (2003) afirman que la concentración del H2O2 influye directamente sobre la eficacia del proceso, mientras que la concentración del FeSO•7H2O está relacionada con la cinética de la reacción: a mayor concentración de esta sal, la cinética disminuye. De acuerdo con O’Dowd y Pillai (2020), el Fe+3 puede reaccionar con el H2O2 para formar radicales hidroxilos, pero a un ritmo mucho más lento que el del Fe+2. Por su parte, Wang et al. (2016) afirman que si la carga de catalizador en la solución acuosa excede el rango óptimo, el exceso de catalizador consumirá el •OH generado.
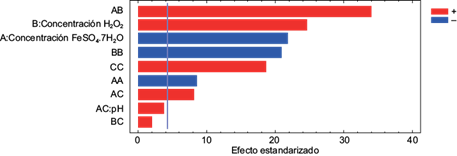
Fig. 2 Diagrama de Pareto del proceso Fenton. (A: concentración de sulfato ferroso heptahidratado [FeSO4•7H2O]; B: concentración de peróxido de hidrógeno [H2O2]; C: potencial de hidrógeno [pH].)
A partir de la figura 3 se puede inferir que el incremento en la concentración del catalizador FeSO4•7H2O hasta 2200 mg/L tiene un efecto negativo en el decaimiento de la DBO5, debido a que se excede el rango óptimo de dosis de catalizador. Por el contrario, el incremento en la concentración de H2O2 favorece el decaimiento de la DBO5 por la mayor generación de radicales •OH. Finalmente, en cuanto al pH, se logró una reducción del 94 % de la DBO5 en el rango de 2.5-3.5. Según Wang et al. (2016) , el rango óptimo de pH para la degradación de la mayoría de los compuestos orgánicos es de 2.5 a 3.0.
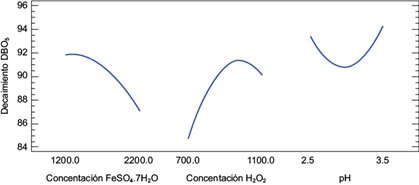
Fig. 3 Efectos principales del proceso en el decaimiento de la DBO5. (DBO5: demanda bioquímica de oxígeno; FeSO4•7H2O: sulfato ferroso heptahidratado; H2O2: peróxido de hidrógeno; pH: potencial de hidrógeno.)
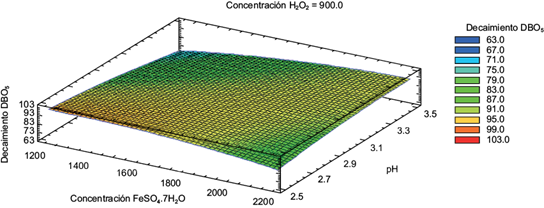
En la figura 4 se muestra que el porcentaje más alto de decaimiento de la DBO5, mediante el proceso Fenton corresponde a un 97 % y se lograría con una concentración de FeSO4•7H2O = 1200 mg/L, pH de 2.5 y un valor intermedio de la concentración de H2O2 = 900 mg/L.
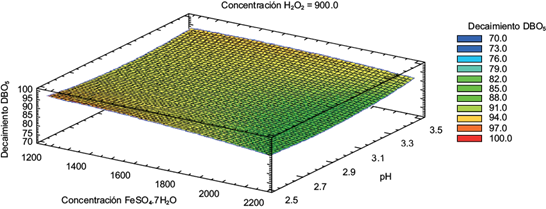
Fig. 4 Superficie de respuesta estimada en el proceso Fenton. (DBO5: demanda bioquímica de oxígeno; FeSO4•7H2O: sulfato ferroso heptahidratado; H2O2: peróxido de hidrógeno; pH: potencial de hidrógeno.)
Una de las principales desventajas del proceso Fenton es la generación de mayores cantidades de lodos de iones férricos; asimismo, es necesaria la adición continua de este catalizador para que la reacción continúe (Babuponnusami y Muthukumar 2014). De acuerdo con Ameta et al. (2018), estas desventajas podrían superarse mediante el uso del proceso foto-Fenton, que es un proceso cíclico y regenera el ion Fe2+.
Eficiencia de remoción de la DBO5 del efluente del camal empleando el proceso foto-Fenton
En los resultados presentados en el cuadro IV se observa que, al igual que en el proceso Fenton, el experimento 5 logró un mayor porcentaje de decaimiento de la DBO5, con un valor de 94.63 % alcanzado mediante las siguientes condiciones de experimentación: concentración FeSO4•7H2O = 1200 mg/L, concentración de H2O2 = 900 mg/L, pH = 2.5 y 1 h de exposición a la radiación UV-C (254 nm). Cabe resaltar que, para este proceso, la DBO5 a degradar fue de 3957 mg/L y el porcentaje de decaimiento en todos los experimentos fue superior al 63.5 %. De acuerdo con Ameta et al. (2018) , la combinación de peróxido de hidrógeno, catalizador de Fe+2 o Fe+3 y radiación UV produce más radicales hidroxilos que un proceso Fenton, lo que, a su vez, aumenta la tasa de degradación de los contaminantes orgánicos. De Sena et al. (2009) estudiaron la efectividad de los POA para el tratamiento de aguas residuales de la industria cárnica utilizando UV/H2O2 y foto-Fenton a escala de laboratorio, alcanzando tasas de decaimiento de la DBO5 de hasta 97.60 y 95.70 %, respectivamente. Por lo tanto, con base en los porcentajes de decaimiento obtenidos en la presente investigación, se podría considerar que los procesos Fenton y foto-Fenton mejoran la calidad de los efluentes de aguas residuales para fines de reutilización del agua.
CUADRO IV RESULTADOS DEL TRATAMIENTO FOTO-FENTON.
| Experimento | FeSO4•7H2O (mg/L) | H2O2 (mg/L) | pH | DBO5 antes del tratamiento (mg / L) | DBO5 sespués del tratamiento (mg/L) | Porcentaje de decaimiento de la DBO5 |
| 1 | 1200 | 700 | 3 | 3946.84 | 313.69 | 92.05 |
| 2 | 2200 | 700 | 3 | 3946.84 | 669.84 | 83.03 |
| 3 | 1200 | 1100 | 3 | 3946.84 | 263.56 | 93.32 |
| 4 | 2200 | 1100 | 3 | 3946.84 | 276.41 | 93 |
| 5 | 1200 | 900 | 2.5 | 3946.84 | 211.91 | 94.63 |
| 6 | 2200 | 900 | 2.5 | 3946.84 | 466.87 | 88.17 |
| 7 | 1200 | 900 | 3.5 | 3946.84 | 1440.33 | 63.51 |
| 8 | 2200 | 900 | 3.5 | 3946.84 | 243.7 | 93.83 |
| 9 | 1700 | 700 | 2.5 | 3946.84 | 228.47 | 94.21 |
| 10 | 1700 | 1100 | 2.5 | 3946.84 | 218.53 | 94.46 |
| 11 | 1700 | 700 | 3.5 | 3946.84 | 482.1 | 87.79 |
| 12 | 1700 | 1100 | 3.5 | 3946.84 | 298 | 92.45 |
| 13 | 1700 | 900 | 3 | 3946.84 | 271.51 | 93.12 |
| 14 | 1700 | 900 | 3 | 3946.84 | 268.2 | 93.2 |
| 15 | 1700 | 900 | 3 | 3946.84 | 377.47 | 90.44 |
DBO5: demanda bioquímica de oxígeno; FeSO4•7H2O; sulfato ferroso heptahidratado; H2O2: peróxido de hidrógeno; pH: potencial de hidrógeno.
Según Chimbolema et al. (2020), a mayor potencia de la luz ultravioleta empleada en el proceso foto-Fenton se tiene un incremento en la mineralización de la materia orgánica, debido a la regeneración fotoquímica de iones ferrosos por fotorreducción de iones férricos. Estos iones ferrosos recién generados reaccionan nuevamente con el H2O2 generando radicales hidroxilos y iones férricos; de esta manera, el ciclo continúa.
En la figura 5 se observan los tres factores que tienen influencia significativa en el decaimiento de la DBO5. Cabe resaltar que la interacción de mayor efecto positivo corresponde a las concentraciones del catalizador y el pH. Según indican Chimbolema et al. (2020), la influencia del pH en el proceso foto-Fenton radica en la capacidad de modificar la prevalencia de las especies de hierro.
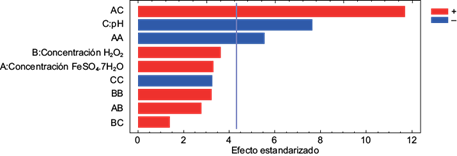
Fig. 5 Diagrama de Pareto del proceso foto-Fenton. (A: concentración de sulfato ferroso heptahidratado [FeSO4•7H2O]; B: concentración de peróxido de hidrógeno [H2O2]; C: potencial de hidrógeno [pH].)
En la figura 6 se puede observar que, a medida que se incrementa la concentración de FeSO4•7H2O aumenta también el porcentaje de decaimiento de la DBO5 hasta un 92.5 %; pero un exceso de este compuesto reduce el proceso de degradación fotoquímica, ya que el Fe+3 puede reaccionar con el H2O2 para formar radicales hidroxilos a un ritmo mucho más lento que el del Fe+2. En el caso del incremento de la concentración de H2O2 hasta 1100 mg/L, también aumenta el decaimiento de la DBO5, alcanzando un 97 %. Respecto del pH, niveles de 2.5 a 3.0 favorecen el porcentaje de decaimiento de la DBO5, debido a que los complejos hidroxi-Fe+3 son más solubles y el Fe (OH)+2 es más fotoactivo. Con un incremento del pH disminuye esta solubilidad (Ameta et al. 2018).

Fig. 6 Efectos principales del proceso foto-Fenton en el decaimiento de la DBO5. DBO5: demanda bioquímica de oxígeno; FeSO4•7H2O: sulfato ferroso heptahidratado; H2O2: peróxido de hidrógeno; pH: potencial de hidrógeno.)
La figura 7 muestra que el porcentaje más alto de decaimiento de la DBO5 mediante el proceso foto-Fenton corresponde a un 95 %, con una concentración de FeSO4•7H2O = 1400 mg/L, pH de 2.5 y un valor intermedio de la concentración de H2O2 = 900 mg/L.
CONCLUSIONES
Se demostró que los procesos Fenton y foto-Fenton son eficientes para inducir el decaimiento de la DBO5 de las aguas residuales del Camal Municipal del Cusco, Perú, efluente que presenta variabilidad en cuanto a su concentración de carga orgánica, con valores de DBO5 entre 1200 a 4000 mg/L, concentración dependiente de la cantidad de animales sacrificados por día.
Las condiciones óptimas para la remoción de materia orgánica del efluente del camal mediante el proceso Fenton corresponden al experimento 5 con los siguientes parámetros de proceso: FeSO4•7H2O = 1200 mg/L, H2O2 = 900 mg/L y pH = 2.5. En estas condiciones se logró un decaimiento de la DBO5 del 93.96 %.
Respecto del proceso foto-Fenton, la condición óptima para la remoción de materia orgánica corresponde también al experimento 5, con los siguientes parámetros: FeSO4•7H2O = 1200 mg/L, H2O2 = 900 mg/L, pH = 2.5 y exposición a radiación UV-C (254 nm). En estas condiciones se obtuvo un 94.63 % de decaimiento de la DBO5, ligeramente superior al obtenido durante la aplicación del proceso Fenton.











 nueva página del texto (beta)
nueva página del texto (beta)