Introducción
México es rico en una diversidad de ambientes climáticos que fomenta la producción de una gama de cultivos de importancia nacional e internacional. Ejemplo de ello, es el cultivo de cebolla (Allium cepa) que se produce en la mayoría de las entidades del país. En 2023, se registró una producción de 1,528,450 toneladas concentrada en 10 estados, destacando Chihuahua (SIAP, 2023). Pese a su importancia, se ve afectado por enfermedades virales, como el virus rayado amarillo del puerro (Leek yellow stripe virus-LYSV) (Pérez-Moreno et al., 2004; VelasquezValle et al., 2010), el virus de la marchitez manchada del jitomate (Tomato spotted wilt orthotospovirus-TSWV), el virus del jaspeado del tabaco (Tobacco etch virus-TEV), el virus latente común del ajo (Garlic latent common virus-GLCV) (Velasquez-Valle et al., 2010) y el virus de la mancha amarilla del iris (Iris yellow spot orthotospovirus-IYSV) (Velásquez-Valle y Reveles-Hernández; 2011). Este último, de mayor importancia económica en cebolla en el mundo (Jones, 2005; Bag et al., 2009) y otros cultivos del género Allium (Bag et al., 2015; Weilner y Bedlan, 2013), con pérdidas en producción de semilla y mermas en el tamaño del bulbo (Bag et al., 2010; Bag et al., 2012b).
El IYSV es el más devastador en Allium (Brewster, 2008) y tiene mayor importancia por su amplia distribución geográfica y rango de hospedantes reportados en los últimos años (Smith et al., 2011; Ghotbi et al., 2005; Sampangi y Mohan, 2007). En las últimas décadas, el impacto económico de los Orthotospovirus se ha incrementado, causando pérdidas económicas en una diversidad de hortalizas y ornamentales (Turina et al., 2016), esto debido a la dificultad de combatir los insectos vectores con insecticidas, e implementar diferentes estrategias de manejo para limitar y prevenir la introducción de Orthotospovirus en áreas agrícolas (Turina et al., 2016). Es por ello, la importancia de conocer el IYSV en México, su rango de hospedantes que pueden ser reservorios del virus y eventual surgimiento de la enfermedad; aunado a ello, los hospederos alternos del vector del virus.
Clasificación taxonómica y genómica del IYSV. El Iris yellow spot orthotospovirus pertenece a la familia Tospoviridae (Orden: Bunyavirales) y género Orthotospovirus (Adams et al., 2017). Su genoma consta de tres segmentos de ARN: segmento pequeño (Small-S) (2.9 kb), mediano (Medium-M) (4.8 kb) y largo (Large-L) (8.9 kb) (Cortês et al., 1998). El ARN largo contiene 8,880 nucleótidos, con un marco de lectura abierta (Open Reading Frame-ORF) en la cadena viral complementaria (vc). El ARN codifica para la proteína ARN polimerasa del ARN dependiente (RdRp) de 331.17 kDa en sentido negativo (Figura 1) (Bag et al., 2010). La terminación 5’ y 3’ del ARN L (vc) contiene dos regiones no traducidos de 33 y 226 nucleótidos, ambos extremos tienen nucleótidos terminales conservados (característica común del género) (Bag et al., 2010).
El ARN M consta de 4,817 nucleótidos con dos marcos de lectura abierta (Open Reading Frame-ORF) con arreglo ambisentido, separados por una región intergénica (IGR) de 380 nucleótidos (Bag et al., 2009). El ORF pequeño contiene 935 nucleótidos que codifica una proteína de 311 aminoácidos y 34.7 kDa. Este ORF
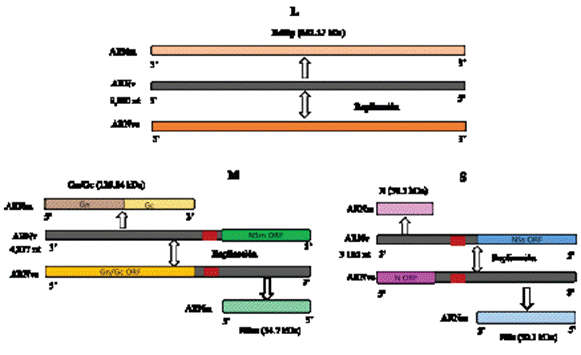
Figura 1 Representación de la organización segmentada del genoma de ARN de Iris yellow spot orthotospovirus (L, M y S). Modificado de Bag et al. (2015).
codifica en sentido positivo para la proteína de movimiento no estructural (NSm). El ORF largo es de 3,410 nucleótidos y codifica una proteína de 1,136 aminoácidos y 128.84 kDa, donde se encuentra la glicoproteína precursora (Gn/Gc) en sentido viral complementario. Ambos ORF’s son separados por una región intergénica de 395 nucleótidos (Bag et al., 2009). Tanto el ARN M y S son de codificación ambisentido y ambos contienen dos ORFs (Granval de Millán y Gracia, 1999). Finalmente, el ARN S consta de 3,105 nucleótidos, con dos ORFs; un ORF de 1,329 nucleótidos y codifica la proteína no estructural (NSs) en sentido positivo y otro de 816 nucleótidos que codifica la nucleoproteína (N) en sentido negativo (Figura 1) (Cortês et al., 1997; Cortês et al., 1998).
Síntomas en cebolla. En cebolla los síntomas suelen ser específicos (Weilner y Bedlan, 2013), y consisten en lesiones elongadas o en forma de diamante, cloróticas o color café claro a blanco y con presencia o ausencia de una isla verde en el centro de las lesiones de las hojas (Figuras 2 A-D) y tallos florales (Gent et al., 2006). Al inicio de la infección los síntomas pueden confundirse con lesiones originadas por trips u otros patógenos (hongos o bacterias) (Weilner y Bedlan, 2013); sin embargo, estas lesiones se observan en la parte interna de las hojas próximas al bulbo, donde los trips prefieren alimentarse (Figuras 2 E-F). Cuando las lesiones del virus coalescen, las hojas colapsan y se reduce el área fotosintética (Kritzman et al., 2001), afectando la formación del bulbo (Gent et al., 2006) e inclusive causa la muerte de la planta cuando el daño es severo (Weilner y Bedlan 2013). Los síntomas son más frecuentes cuando la planta se encuentra en edad avanzada o en la formación del bulbo (Weilner y Bedlan, 2013). Los síntomas reportados en el cultivo de cebolla en México, son similares a los reportados en otros países, lesiones cloróticas, amarillentas o blancas, secas y alargadas (Figura 2A y 2B) (Ramírez-Rojas et al., 2016), y en ocasiones se observa una isla verde en el centro de la lesión (Figura 2 C y D) (Ávila-Alistac et al., 2017).

Figura 2. A y B Síntomas asociados a la infección de Iris yellow spot orthotospovirus consistentes en lesiones cloróticas de color blanco pajizo en forma elongada; C y D) Lesiones cloróticas de color blanco pajizo con presencia de una isla verde en el centro de la lesión; E-G) Presencia de altas poblaciones de T. tabaci (inmaduros y adultos) en el cultivo de la cebolla.
En otros hospedantes como N. benthaminana, el IYSV causa mosaicos y deformación en hojas (Ghotbi et al., 2005; Ávila-Alistac et al., 2017; Ornelas-Ocampo et al., 2018). En tomate de cáscara (Physalis ixocarpa) los síntomas se asocian a un amarillamiento y necrosis en la planta (Ríos-Domínguez et al., 2017). A pesar de reportes sintomatológicos similares en México y otros países, la diversidad genética de las poblaciones de IYSV puede generar una diversidad de síntomas (Iftikhar et al., 2014). En México, la información sobre la diversidad de IYSV es limitada, solo existe el reporte de Ornelas-Ocampo y colaboradores (2018) quienes observaron variabilidad de síntomas en cebolla infectadas con IYSV, clasificándolos como síntomas típicos y severos; no obstante, genómicamente, no presentó diferencias entre los fragmentos del genoma de IYSV analizados. Pese a esto, no se descarta la probabilidad de la variabilidad en las zonas productoras de cebolla, considerando la presencia de otros Orthotospovirus en áreas agrícolas.
Distribución nacional y hospedantes alternos de IYSV. El IYSV está distribuido en la mayoría de las entidades productoras de cebolla en el mundo (Gent et al., 2006). En México se reportó en 2010, en Delicias, Chihuahua con severas pérdidas económicas en el cultivo (Velázquez-Valle et al., 2010). En el mismo año también se reportó en Zacatecas (Velásquez-Valle y Reveles-Hernández, 2011). Posteriormente, en 2012, se observó una incidencia del 100 % en 2,500 ha cultivadas de cebolla en Morelos (Ramírez-Rojas et al., 2016), y en 2013 en Vista Hermosa y Tanhuato, Michoacán (Ávila-Alistac et al., 2017). Estos reportes se registraron en cebolla, y solo en Guanajuato se reportó su presencia en ajo (Allium sativum) (Pérez-Moreno et al., 2010) donde confirmaron la presencia del vector (Thrips tabaci) y el virus en el insecto (García-Rodríguez et al., 2014).
Además, IYSV se ha detectado en tomate de cáscara en Malinalco y Tonatico, Estado de México (Ríos-Domínguez et al., 2017; Ríos-Domínguez et al., 2018), y jitomate (Solanum lycopersicum) en Coatepec Harinas, Edo. de México (RíosDomínguez et al., 2018). La infección en otros hospedantes diferentes a Allium demuestran la capacidad del virus para infectar especies de otras familias de importancia económica en el país. Por ello, no se descarta la probabilidad de distribución del virus en otras especies.
Por ejemplo, inicialmente el rango de hospedantes del IYSV era limitado (Kritzman et al., 2001), pero con el tiempo la gama de hospedantes se ha diversificado en varias plantas ornamentales (Jones, 2005), cultivos y arvenses de todo el mundo (Cuadro 1) (Hsu et al., 2011; Sampangi et al., 2007; Schwartz et al., 2014; Weilner y Bedlan, 2013; Szostek y Schwartz, 2015). El estudio del papel de los hospedantes alternos y vectores secundarios (Schoonhoven et al., 2005) es primordial para entender el patosistema de IYSV-Vector-Hospedante-Arvense para implementar estrategias asertivas para el manejo holístico y sistémico. En Zacatecas, México, Velásquez-Valle et al. (2013) resalta la importancia de Amaranthus spp., Bidens odorata, Brassica campestris, Chenopodium spp., Eruca sativa, Malva parviflora, Medicago sativa, Sisymbrium spp. y Sonchus oleraceus como hospedantes de IYSV. Interesantemente, IYSV se ha detectado en al menos 20 familias de plantas con predominancia en Asteraceae, arvenses abundantes en el país (Cuadro 1).
Cuadro 1 Rango de hospedantes de Iris yellow spot orthotospovirus.
| Familia | Nombre científico | Nombre común | Referencias |
|---|---|---|---|
| Alliaceae | Allium tuberosum | Cebolla silvestre | Gawande et al., 2014 |
| A. fistulosum | Cebollín | Tabassum et al., 2016 | |
| Amaranthaceae | Amaranthus retroflexus | Amaranto | Gent et al., 2006; Sampangi et al., 2007; Schwartz et al., 2014; Birithia et al., 2018 |
| A. hybridus | Quelite blanco | Karavina y Gubba, 2017 | |
| A. spinosus | Quelite espinoso | Karavina y Gubba, 2017 | |
| Amaranthus spp. z | Quelite | Velásquez-Valle et al., 2013 | |
| Atriplex micranth | Atriplex | Evans et al., 2009ª | |
| Asteraceae | Arctium minus | Lampazo menor | Hsu et al., 2011; Smith et al., 2012 |
| Tripleurospermum inodorum | Falsa manzanilla | Weilner y Bedlan, 2013 | |
| Artemisia vulgaris | Artemisa | Weilner y Bedlan, 2013 | |
| Arctium tomentosum | Bardana tormentosa | ||
| Cichorium intybus | Achicoria común | Hsu et al., 2011; Smith et al., 2012; Weilner y Bedlan, 2013 | |
| Taraxicum officinale | Diente de león | Hsu et al., 2011; Smith et al., 2012; Schwartz et al., 2014; Szostek y Schwartz, 2015 | |
| Sonchus asper | Lechuguilla espinosa | Nischwitz et al., 2007 | |
| Lactuca serriola | Lechuga silvestre | Sampangi et al., 2007; Schwartz et al., 2014; Szostek y Schwartz, 2015 | |
| S. oleraceus z | Lechuguilla común | Schwartz et al., 2014; Velásquez-Valle et al., 2013 | |
| Senecio vulgaris | Senecio | Schwartz et al., 2014 | |
| Bidens odorata z | Aceitilla | Velásquez-Valle et al., 2013 | |
| Chrysothamnus nauseosus | Chamiza | Schwartz et al., 2014 | |
| Conyza canadensis | Pegajosa | Schwartz et al., 2014 | |
| Tragopogon dubius | Barbaja amarilla | Schwartz et al., 2014; Szostek y Schwartz, 2015 | |
| Amaryllidaceae | Bessera elegans | Arete | CABI, 2015 |
| Brassicaceae | Chorispora tenella | mostaza azul | Schwartz et al., 2014 |
| Descurainia sophia | Hierba sofía | Schwartz et al., 2014; Szostek y Schwartz, 2015 | |
| Capsella bursapastoris | Bolsa de pastor | Weilner y Bedlan, 2013 | |
| Eruca sativa z | Rucola silvestre | Velásquez-Valle et al., 2013 | |
| Brassica campestris z | Nabo del campo | Velásquez-Valle et al., 2013 | |
| Sisymbrium spp z | Mataandil | Velásquez-Valle et al., 2013 | |
| B. kaber | Mostaza de campo | Schwartz et al., 2014 | |
| Convolvulaceae | Convolvulus arvensis | Correhuela | Schwartz et al., 2014; Weilner y Bedlan, 2013 |
| Chenopodiaceae | Kochia scoparia | Coquia | Sampangi et al., 2007; Schwartz et al., 2014 |
| C. album | Quínoa | Sampangi et al., 2007; Schwartz et al., 2014; Birithia et al., 2018 | |
| Chenopodium spp. z | Quenopodium | Velásquez-Valle et al., 2013 | |
| Salsola iberica | Bola de fuego | Schwartz et al., 2014 | |
| Euphorbiaceae | Ricinus communis | Higuerilla | Schwartz et al., 2014 |
| Euphorbia dentata | Lechosilla | Schwartz et al., 2014 | |
| Fabaceae | Medicago sativa z | Alfalfa | Velásquez-Valle et al., 2013 |
| Geraniaceae | Erodium cicutarium | Alfilerillo | Schwartz et al., 2014 |
| Polygonaceae | Rumex crispus | Lengua de vaca | Hsu et al., 2011; Smith et al., 2012; Weilner y Bedlan, 2013 |
| Portulacaceae | Portulaca oleracea | Verdolaga | Cosmi et al., 2003; Schwartz et al., 2014 |
| Plantaginaceae | Linaria canadensis | Linaria azul | CABI, 2015 |
| Plantago lanceolata | Llantén de hoja angosta | Schwartz et al., 2014 | |
| Poaceae | Setaria viridis | Almorejo | Evans et al., 2009b |
| Aegilops cylindrica | Zacate cara de cabra | Schwartz et al., 2014 | |
| Dactylis glomerata | Pasto ovillo | Weilner y Bedlan, 2013 | |
| Eleusine indica | Pata de gallina | Karavina y Gubba, 2017 | |
| Poa sp. | Pasto | Weilner y Bedlan, 2013 | |
| Polygonaceae | Polygonum lapathifolium | Polígono pata perdiz | Schwartz et al., 2014 |
| Malvaceae | Hibiscus trionum | Flor de una hora | Schwartz et al., 2014 |
| Malva palviflora z | Quesitos | Velásquez-Valle et al., 2013 | |
| M. neglecta | Malva | Szostek y Schwartz, 2015 | |
| Solanaceae | Solanum nigrum | Hierba mora | Schwartz et al., 2014; Birithia et al., 2018 |
| S. sarrachoides | Belladona | Schwartz et al., 2014 | |
| Datura stramonium | Toloache | Birithia et al., 2018 | |
| S. lycopersicum y | Tomate | Ríos-Domínguez et al., 2018 | |
| Physalis minima | Grosella espinosa | Birithia et al., 2018 | |
| P. ixocarpa y | Tomate de cáscara | Ríos-Domínguez et al., 2017; Ríos-Domínguez et al., 2018 | |
| Zygophyllaceae | Tribulus terrestres | Abrojo de flor amarilla | Sampangi et al., 2007 |
| Geraniaceae | Pelargonium hortorum | Geranio común | Ghotbi et al., 2005 |
| Cycadaceae | Cycas sp. | Palama sago | Ghotbi et al., 2005 |
| Rosaceae | Rosa sp. | Rosa | Ghotbi et al., 2005 |
| Araceae | Scindapsus sp. | Potos | Ghotbi et al., 2005 |
| Gentianaceae | Eustoma russellianum | Lisianthus | Kritzman et al., 2000 |
| E. grandiflorum | Lisianthus | Mumford et al., 2008 | |
| chrysanthemum | Crisantemo | Rafizadeh et al., 2013 |
yDetectado por RT-PCR.
zDetectado mediante ELISA.
Formas de transmisión y vectores del IYSV. Hasta el momento no existen evidencias de transmisión del virus por semillas (Kritzman et al., 2001) y bajo condiciones controladas la transmisión mecánica en plantas de cebolla es menor a 30 % (Bag et al., 2015). El principal vector es T. tabaci (Terebrantia: Thripidae) (Cortês et al., 1998), también conocido como “trips de la cebolla”, el cual transmite al virus de una manera persistente y propagativa (Diaz-Montano et al., 2011). También se demostró a Frankliniella fusca bajo condiciones de invernadero la capacidad de transmitir al virus en bajo porcentaje (Srinivasan et al., 2012). Las especies de Orthotospovirus se transmiten naturalmente por trips de manera persistente (Bag et al., 2015); es decir, una vez que el virus infecta al insecto, éste será capaz de transmitirlo por el resto de su vida.
El trips de la cebolla es una plaga importante en este cultivo (Diaz-Montano et al., 2011), y de un extenso número de plantas de importancia económica, como hortalizas y plantas ornamentales (Schoonhoven et al., 2005; Alford, 1999; Gent et al., 2004). Este vector, adquiere mayor relevancia al transmitir no solo a IYSV, sino también a Tomato spotted wilt orthotospovirus (TSWV) (Jenser et al., 2011) e Impatiens necrotic spot orthotospovirus (INSV) (Ghotbi et al., 2005). Es una plaga cosmopolita y polífaga, que puede sobrevivir fácilmente en plantas alternas como arvenses, especialmente ante la ausencia del cultivo (Schoonhoven et al., 2005). Tanto INSV como TSWV están presentes en cultivos hortícolas en México; el INSV se ha reportado en P. ixocarpa, Capsicum spp. y jitomate (Torre-Almaraz et al., 1998; González-Pacheco y Silva-Rosales, 2013; Zuñiga-Romano et al., 2019) y el TSWV en varios cultivos hortícolas y ornamentales del país e incluso en el cultivo de cebolla (Torre-Almaraz et al., 1998; Holguín-Peña y Rueda-Puente, 2007; Morales-Díaz et al., 2008; Velásquez-Valle et al., 2009; Velásquez-Valle et al., 2012).
Existe la posibilidad que T. tabaci tenga la capacidad de transmitir los tres Orthotospovirus en mezclas virales, ya que existen evidencias de que dos o más virus se pueden complementar para infectar a su hospedante. Bag et al. (2012a) sustenta lo mencionado previamente al resaltar que TSWV facilitó el movimiento de la proteína viral de IYSV desde el área de inoculación hasta las hojas jóvenes de Datura, volviéndose una infección sistémica. Dicho de otra forma, la doble infección de IYSV y TSWV en Datura aumentó la severidad de los síntomas en hojas inoculadas, así como en hojas jóvenes (infección sistémica), generando un sinergismo. Cabe mencionar que el comportamiento de TSWV e IYSV en plantas de Datura son diferentes, TSWV infecta de forma sistémica e IYSV es localizado (infección limitado en las áreas inoculadas). La redistribución y/o la complementación genética entre los segmentos genómicos de los virus podrían contribuir a mayor variabilidad, lo que no es limitativo la infección de dos o más Orthotospovirus en la naturaleza (Bag et al., 2012a). Lo anterior refuerza la teoría de que el insecto vector tiene la capacidad de transmitir virus de forma aislada y en mezclas virales.
Hospedantes alternos de Thrips tabaci . Las plantas hospederas de T. tabaci incluyen no solo cultivos de importancia económica, también diversas arvenses que al fenecer o ser eliminadas puede favorecer la dispersión de los insectos virulíferos a cultivos de interés (Doederlein y Sites, 1993; Ghotbi et al., 2005). En México, se ha estudiado el papel de las arvenses de la familia de las Cucurbitaceae y Solanaceae como potenciales fuentes de inóculo para el desarrollo del Tomato apex necrosis virus (ToANV), Zucchini yellow mosaic virus (ZYMV), Watermelon mosaic virus (WMV), Papaya ring spot virus (PRSV-W) y Cucumber mosaic virus (CMV) en cultivos de importancia agronómica (Félix-Gastélum et al., 2023). En cebolla, es limitada la información concerniente a las arvenses; solo en Morelos y Michoacán se estudió la presencia de IYSV en arvenses asociadas al cultivo (Ramírez-Rojas et al., 2016; Ávila-Alistac et al., 2017); sin embargo, solo se registró la presencia de T. tabaci en arvenses asociadas al cultivo, sin evaluar la presencia del virus en el insecto (Cuadro 2). No obstante, las arvenses reportadas en otros países positivas a IYSV, están presentes en México e interaccionan con el cultivo de cebolla y además, son hospedantes del vector (Beltran et al., 2011; Velásquez-Valle et al., 2013;
Cuadro 2 Hospederos alternos de Thrips tabaci e Iris yellow spot orthotospovirus en México y el mundo.
| Especie | Hospedante de T. tabaci en México | Hospedante de IYSV Nacional/Mundial | Referencias | |
|---|---|---|---|---|
| Amaranthaceae | ||||
| Chenopodium spp | + | +/+ | Velásquez-Valle et al., 2013; Sampangi et al., 2007; Schwartz et al., 2014 | |
| Amaranthus spp. | + | +/- | Velásquez-Valle et al., 2013 | |
| A. hybridus | + | -/+ | Ávila-Alistac et al., 2017 | |
| A. spinosus | + | -/+ | Ávila-Alistac et al., 2017; Karavina y Gubba, 2017 | |
| Solanaceae | ||||
| Solanum eleagnifolium | + | -/- | Velásquez-Valle et al., 2013 | |
| Solanum tuberosum | + | -/- | Velásquez-Valle et al., 2013 | |
| Capsicum annumm | + | -/- | Beltran et al., 2011; Velásquez-Valle et al., 2009. | |
| Asteraceae | ||||
| Sonchus spp. | + | -/+ | Velásquez-Valle et al., 2013; Nischwitz et al., 2007 | |
| Sonchus oleraceus | + | -/+ | Ávila-Alistac et al., 2017; Schwartz et al., 2014 | |
| Parthenium hysterophorus | + | -/- | Ávila-Alistac et al., 2017 | |
| Tithonia tubiformis | + | -/- | Ávila-Alistac et al., 2017 | |
| Lactuca serriola | + | -/- | Ávila-Alistac et al., 2017 | |
| Bidens odorata | - | +/- | Velásquez-Valle et al., 2013 | |
| Fabaceae | ||||
| Phaseolus vulgaris | + | -/- | Velásquez-Valle et al., 2013 | |
| Medicago sativa | - | +/- | Velásquez-Valle et al., 2013 | |
| Brassicaceae | ||||
| Brassica spp. | + | -/- | Velásquez-Valle et al., 2013 | |
| Sisymbrium spp. | + | +/- | Velásquez-Valle et al., 2013 | |
| Lepidium virginicum | + | -/- | Ávila-Alistac et al., 2017 | |
| Brassica campestris | - | +/- | Velásquez-Valle et al., 2013 | |
| Eruca sativa | - | +/- | Velásquez-Valle et al., 2013 | |
| Liliaceae | ||||
| A. cepa | + | -/- | Magos, 2011; VelásquezValle et al., 2013; Ávila-Alistac et al., 2017 | |
| Acanthaceae | ||||
| Dicliptera peduncularis | + | -/- | Ávila-Alistac et al., 2017 | |
| Convolvulaceae | ||||
| Ipomoea purpurea | + | -/- | Ávila-Alistac et al., 2017 | |
| Euphorbiaceae | ||||
| Acalypha ostryifolia | + | -/- | Ávila-Alistac et al., 2017 | |
| Ricinnus comunis | + | -/+ | Ávila-Alistac et al., 2017; Schwartz et al., 2014 | |
| Acalypha arvensis | + | -/- | Ávila-Alistac et al., 2017 | |
| Malvaceae | ||||
| Malva parviflora | + | +/- | Velásquez-Valle et al., 2013; Ávila-Alistac et al., 2017 | |
| Anoda cristata | + | -/- | Ávila-Alistac et al., 2017 | |
| Malvastrum coromandelianum | + | -/- | Ávila-Alistac et al., 2017 | |
| Portulacaceae | ||||
| Portulaca oleracea | + | -/+ | Ávila-Alistac et al., 2017; Cosmi et al., 2003; Schwartz et al., 2014 |
+ Hospedante de T. tabaci y/o IYSV
Ávila-Alistac et al., 2017). Estas arvenses se han reportado en altas poblaciones al igual que T. tabaci; p.e. se ha reportado a Portulaca oleracea como hospedero de IYSV (Cosmi et al., 2023; Schwartz et al., 2014), arvense ampliamente distribuido en zonas productoras de cebolla (Figura 3) (Ávila-Alistac et al., 2017). La frecuencia de las arvenses dentro y fuera de plantaciones de cebolla constituyen la principal causa de prevalencia de T. tabaci, vectores potenciales en área productivas sin presencia de IYSV (Gent et al., 2006; Tanveer et al., 2015). Por consiguiente, no se descarta la presencia de IYSV en arvenses presentes en el país como las reportadas

Figura 3 Arvenses interaccionando dentro y fuera del cultivo de cebolla (Allium cepa). A) Escoba amarga (Parthenium hysterophorus); B) Verdolaga (Portulaca oleracea); C) Plantas de acalifa (Acalypha ostryifolia); D) Acahual o falso girasol (Tithonia tubiformis) en el borde del cultivo de cebolla.
por Velásquez-Valle et al. (2013) (Cuadro 2). En México, al menos 14 especies de arvenses son hospedantes de T. tabaci y estos se han reportado como hospedantes de IYSV en México y zonas fuera del país (Cuadro 2).
Epidemiología y manejo de IYSV. El IYSV al igual que el resto de los virus del mismo género necesitan la interacción de factores básicos para causar una epidemia: el vector, el hospedante, hospedante alterno y el virus (Ullman et al., 2002). Aunado a ello, las condiciones ambientales pueden condicionar la epidemia en un área determinada (German et al., 1992). Estos virus tienen la capacidad de utilizar al insecto vector para infectar nuevos hospedantes, ampliando su adaptabilidad al portar el virus; influyendo en su incidencia y distribución bajo diferentes condiciones ambientales y nuevos hospedantes (Jones, 2005).
La severidad del IYSV en el cultivo de cebolla es complejo y dependerá de la población de trips sanos e infectivos y del número de plantas sanas e infectadas, así como de plantas asintomáticas. Una vez que la planta está infectada por el virus, no existe un tratamiento para su control; no obstante, estas plantas sirven como fuente de alimentación de trips sanos, y éstos infectar a plantas sanas. Adicionalmente, la densidad poblacional en campo tanto de trips como de plantas hospederas del IYSV, dependen de factores ambientales bióticos y abióticos, así como del manejo agronómico que se realice (Figura 4). Se ha observado que el impacto del IYSV en el cultivo depende de la etapa fenológica en que aparecen los primeros síntomas, si aparecen los síntomas cuando los bulbos están aún en desarrollo, el tamaño y calidad del bulbo se verá afectado (Drost et al., 2019).
Por otro lado, la presencia de T. tabaci en cultivos hortícolas es un tema fitosanitario de importancia en México (Palomo et al., 2015), por ser vectores de virus y, por el daño directo que generan al alimentarse del hospedante ocasionando marchitez prematura, retardo del desarrollo de la hoja y distorsión de los brotes vegetativos (Aguilar et al., 2017). Tanto los estados inmaduros como adultos perforan las células con su aparato bucal y succionan la savia (Jones, 2005). De los seis estados de vida del insecto (huevo, dos instares larvales, prepupa, pupa y adulto) (Jones, 2005; Pourian et al., 2009), las larvas del primer y segundo instar pueden adquirir el virus en la alimentación, pero solo la larva de segundo instar y los adultos lo transmiten (Sastry, 2013; Hull, 2001; Chatzivassiliou et al., 2002). Si el insecto adquiere el virus en etapa adulta, no lo podrá trasmitir (Jones, 2005; Whitfield et al., 2005). Es inminente que una vez que el insecto adquiere el virus, éste se reproducirá y se moverá eficientemente por el intestino medio y glándulas salivales de los trips, sin afectar el desarrollo, fecundidad y mortalidad del insecto ante la infección del virus (Inoue et al., 2010). Este insecto es prolifero, registrando hasta seis generaciones en el ciclo de cultivo sin verse afectado por las lluvias (Palomo et al., 2015).
Los hospederos alternos son imprescindibles en la epidemiología del IYSV, sobre todo si T. tabaci completa su desarrollo en los hospederos (Hsu et al., 2011). Por lo anterior, el manejo de los hospederos alternos son determinantes para el manejo integral de la enfermedad (Schwartz et al., 2014; Wisler y Norris, 2005). Esto aumenta el interés en estudios sobre el insecto-IYSV-Allium cepa-hospedantes alternos (arvenses), ya que estas interacciones tienden ser complejas. Rodríguez et al. (2007) enfatizan, la pertinencia de conocer ampliamente esta relación para optimizar un manejo integrado. Dichas interacciones pueden afectar en el surgimiento de nuevas variantes del virus, gama de hospedantes y/o frecuencia de transmisión (Syller, 2012). Así mismo, la capacidad que tienen los trips para desarrollarse en otras plantas favorece este tipo de interacción, ya que la ausencia del principal hospedante incentiva la migración a otras partes vegetativas o inflorescencias de otras plantas (Milne y Walter, 1998).
En general, todas las estrategias de manejo del IYSV se han enfocado básicamente a actividades preventivas que reduzcan poblaciones de T. tabaci y evitar el crecimiento de arvenses en el cultivo (Drost et al., 2019). La determinación de los patrones del vector y hospedantes alternos del virus y/o vector podrían ayudar a los productores a plantear estrategias de manejo integrado en el cultivo (Birithia et al., 2018).
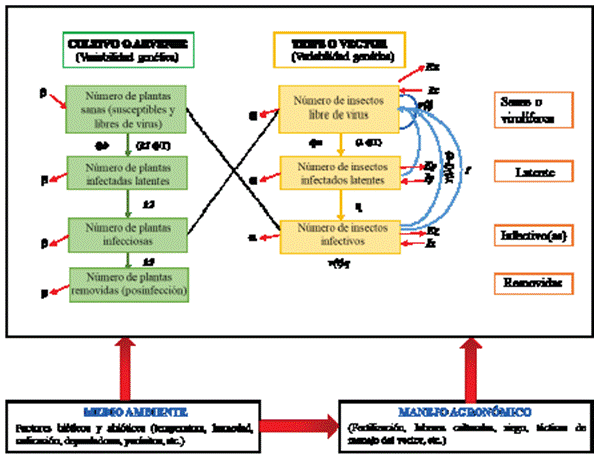
Figura 4 Sistema epidemiológico de un patosistema viral encauzado a Iris yellow spot orthotospovirus (basado y modificado de Madden et al., 2000). Acotaciones utilizadas: v(t)= Tasa de fecundidad total de la población del insecto por día dentro del cultivo. Ґ= Tiempo de incubación del virus dentro del vector. q= Probabilidad de que la descendencia del vector sea virulifera. β= Tasa de mortalidad de plantas y recuperación (resiembra). α= Tasa de mortalidad y natalidad del insecto. ɸ b= (Plantas visitadas por insectos al día) (Probabilidad de que el insecto virulífero inocule al virus en una planta por una visita). 1/k1= Tiempo en que el vector inocula la planta. 1/k2= Periodo de latencia del virus en la planta. 1/k3= Periodo infeccioso del virus en la planta. ɸT= (Plantas visitadas por insectos al día) (Tiempo en que el insecto prueba la planta en una visita). Ex= Tasa de emigración de insectos libres de virus. Ix= Tasa de inmigración de insectos libres de virus. Ey= Tasa de emigración de insectos latentes. Ez= Tasa de emigración de insectos infectivos. Iy= Tasa de inmigración de insectos latentes. Iz= Tasa de inmigración de insectos infectivos. 1/λ = Tiempo de adquisición del vector. ɸ a= (Plantas visitadas por insectos al día) (Probabilidad de que un insecto adquiera al virus con una sola visita a la planta infectada). 1/ƞ= Tiempo en que el virus pasa de latente a infectivo dentro del vector (periodo de latencia). Para mayor información consultar a Madden et al. (2000).
Sin embargo, no solo se debe considerar controlar químicamente al vector; sino, se debe hacer más investigaciones para entender su comportamiento en el país. En Zacatecas se ha analizado de acuerdo sus necesidades, estudiar el comportamiento del virus, donde se observó la presencia del IYSV en plántulas de cebolla en almácigos a campo abierto, imposibilitando la presencia del vector (Velásquez-Valle et al., 2017). Este tipo de problemas, conlleva a pensar que la comercialización de plántulas de cebolla entre los estados productores de cebolla, acrecienta la posibilidad del movimiento del virus y vector. Ante la imposibilidad de una comercialización exitosa de su producto, los productores de cebolla optan por abandonar sus parcelas, con riesgo al incremento del virus y poblaciones de trips (Velásquez-Valle et al., 2013). Muchos casos el manejo ha sido fundamental para minimizar los riesgos de infección del virus o al menos evitar daños severos al cultivo. Para Turina et al. (2016) señalan que ante la dificultad de combatir los vectores de trips con los insecticidas, la mejor manera de mitigar o prevenir las enfermedades inducidas por los Orthotospovirus implica una estrategia de semillas con resistencia al virus. En México, se ha hecho estudios en 20 variedades en torno a su rendimiento ante la infección del virus en Morelos. Estos resultados revelaron que las variedades “Blanca Morelos”, “Doña Blanca F1”, “Línea INIFAP 19” y “Chona” tienen rendimientos superiores al resto de las variedades ante la presencia de IYSV (Magos, 2011).
Conclusiones
Se debe considerar un manejo integral donde se considere todos los factores que influyen en la epidemia de IYSV con el fin de contrarrestar la enfermedad. Desde el primer reporte en el país (2010) en el cultivo de cebolla fue un tema de preocupación; no obstante, a través del tiempo su severidad fue mermando. Caso similar pasó con Tomato brown rugose fruit virus (ToBRFV), el cual se reportó con daños severos en jitomate y chile en 2018 (Cambrón-Crisantos et al., 2019); pero en la actualidad se ha reportado síntomas atenuados y presencia de haplotipos que puede estar influyendo en la intensidad sintomatológica en plantas de jitomate y chile (Ávila-Alistac et al., 2024). En ToBRFV se han hecho estudios de diagnóstico temprana, preciso y eficiente (Zamora-Macorra et al., 2023), así como estudios en variabilidad del virus en diferentes variedades de jitomate y chile (Ávila-Alistac et al., 2024) y alternativas de manejo del virus (Ramos-Villanueva et al., 2023). Sin embargo, se conoce poco sobre su rango de hospedantes y factores que influyen en la epidemiología del virus. En IYSV, se tiene un mayor conocimiento de sus hospedantes y vector; no obstante, es importante indagar con mayor interés este problema de índole nacional, ya que se ha reportado en solanáceas, mismas que son de valor económico en el país. Así mismo, considerar la reemergencia del virus, de acuerdo al manejo del cultivo, recombinación genética entre especies del mismo género e incluso la influencia del cambio climático que incide en las dinámicas poblacionales de T. tabaci.
En la actualidad, la información sobre las arvenses como hospederos de IYSV y el vector, proporciona mayor comprensión de la enfermedad, al igual que las plantas voluntarias de cebolla. Por ello, es importante conocer estos aspectos, así como el manejo que realizan los productores, ya que es otro factor primordial para el establecimiento del vector e IYSV en las diferentes etapas fenológicas del cultivo. Evidentemente, existe una relación compleja entre el IYSVT. tabaci -Allium cepa-arvenses y otros Orthotospovirus que transmite T. tabaci; p.e., es pertinente estudiar las arvenses como trampa vegetal, por la preferencia alimenticia de T. tabaci aun en presencia del cultivo; adicionalmente, se debe considerar que estas arvenses no sean hospederas del virus, ya que serían un problema al ser hospederos del vector y el virus. En suma, el conocimiento del virus, hospedantes alternos y vector en el país, permitirá encausar las investigaciones futuras para ayudar al productor a contrarrestar este problema y minimizar las pérdidas causadas por el virus en el cultivo de cebolla y ajo principalmente.















