Introducción
H. diminuta es un cestodo gastroentérico de distribución frecuente en ratas y ratones; el ser humano es un hospedador accidental1. El gusano adulto se establece en el intestino delgado, tiene un escólex desarmado y los proglótidos grávidos miden de 20 a 60 mm de largo por 4 mm de ancho. Los huevos de forma redonda, miden entre 60 y 79 µm de diámetro y no presentan filamentos polares. La forma larvaria (cisticerocoide) se establece en el hemoceloma de insectos coprófagos, como las pulgas (Nosopsyllus y Xenopsyllus) y los coleópteros de los cereales (Tribolium y Tenebrio); sin embargo, cucarachas, lepidópteros, miriápodos y coleópteros coprófilos también pueden actuar como hospedadores intermediarios2. En general, la parasitosis es asintomática, aunque una infección masiva puede ser causa de enteritis catarral. La transmisión zoonótica puede evitarse mediante la protección de los alimentos y el agua de consumo humano para impedir el acceso de los roedores. El diagnóstico se realiza mediante la identificación coproparasitológica de los huevos3. La factibilidad y la viabilidad de mantener y propagar el ciclo de vida de H. diminuta en el laboratorio, lo convierte en un modelo experimental con un sin número de aspectos inmunológicos, moleculares y bioquímicos, entre los que se encuentran la búsqueda de tratamientos alternativos a los fármacos.
En los últimos años se ha informado que varios de los helmintos que impactan a los animales con importancia pecuaria, han desarrollado resistencia al tratamiento farmacológico antiparasitario; por lo que se han instrumentado varias estrategias para prevenir esta resistencia, que incluyen desde el recambio del animal de producción por una raza con resistente a los parásitos hasta la aplicación de fármacos en diferentes esquemas de rotación y combinación4. Una estrategia alternativa, para controlar las parasitosis es el uso de hierbas medicinales.
Las hierbas aromáticas de Chenopodium spp. (epazote del zorrillo, paico o té mexicano) y Artemisia spp. (estafiate), se utilizan en la medicina tradicional mexicana; el primero se ha utilizado como antihelmíntico, antiespasmódico y antirreumático, mientras que el segundo, además de utilizarse como diurético y se utiliza como analgésico y antiinflamatorio gastrointestinal5. El constituyente primario del aceite de Chenopodium es el monoterpeno bicíclico ascaridol6, el cual tiene propiedades sedantes, antifúngicas y analgésicas con efecto antiparasitario en infecciones experimentales para abatir la carga parasitaria de Cryptosporidium parvum y Eimeria spp. en pollos y de H. diminuta en ratones7. Los aceites esenciales de Artemisia tienen componentes con actividad antimicrobiana, antioxidante, pesticida, nematicida8 y ovicida en ratones infectados naturalmente con Hymenolepis nana9.
Los extractos no-acuosos se han utilizado en la fabricación de cosméticos, nutracéuticos, pinturas, lubricantes y biodiesel. Los aceites vegetales, como disolventes alternativos, son valorados por sus propiedades fisicoquímicas, alta disponibilidad mundial, biodegradabilidad, bajo costo y baja toxicidad para humanos y animales; incluso, son efectivos para extraer clorofila y compuestos antioxidantes de las hojas de aguacate para la industria alimentaria10. Por lo que este estudio tuvo como objetivo investigar el efecto de los extractos no- acuosos de Artemisia ludoviciana mexicana y Chenopodium vulvaria en la infección experimental murina con H. diminuta.
Material y métodos
Hymenolepis diminuta
Para propagar el ciclo de vida de H. diminuta, se infectaron de manera experimental ratas hembras jóvenes de 6 a 8 semanas de edad y con un peso aproximado de 180 a 200 g. A cada rata se le administraron 20 cisticercoides usando una sonda gástrica. Los cisticercoides se obtuvieron del hemotórax de imagos de Tenebrio molitor. Se emplearon 100 escarabajos adultos porque a diferencia de las larvas, los adultos buscan activamente alimentos con humedad favoreciendo de esa manera la parasitosis. Para obtener los cisticercoides, los coleópteros adultos con exoesqueleto color pardo rojizo, recién liberados de la crisálida y privados de alimentos durante 12 h se alimentaron con heces recién expelidas de ratas infectadas con H. diminuta. A los 10 días posteriores los insectos fueron sacrificados y se recuperaron los cisticercoides del hemotórax; estos fueron contados y se administraron utilizando la sonda intragástrica11.
Dinámica de huevos expelidos
Un total de 20 ratones hembra, Mus musculus cepa Balb/c de 14 meses de edad se infectaron individualmente por vía gástrica con 10 cisticercoides. Para determinar la cinética de oviposición, las heces de los ratones se analizaron durante 30 días utilizando una técnica coproparasitológica de concentración por sedimentación con formalina-éter12. Diariamente, durante las primeras horas del día, se colectaron cinco muestras de heces de cada ratón y se hidrataron en solución salina fisiológica antes de ser procesadas. Para construir la cinética, se tomó la decisión arbitraria de contar a 10x usando un microscopio de campo claro (CME; Leica Microsystems; Wetzlar, Alemania) el total de número de huevos encontrados en tres campos y luego se calculó el promedio diario de todas las muestras.
Extractos no-acuosos de Artemisia ludoviciana y Chenopodium vulvaria
Los extractos de Artemisia y Chenopodium se elaboraron con los tallos y las hojas de la planta deshidratada en etapa de floración. Las plantas se adquirieron de manera comercial (Las Plantas Medicinales de América; CDMX, México). La materia vegetal se pulverizó con una licuadora Oster® de acero inoxidable con interruptor de palanca (Oster®,modelo BLST4125, Acuña, Coahuila, México) hasta obtener partículas de 0.2 a 0.7 mm de diámetro. Para preparar el extracto no-acuoso de cada hierba, el material biológico pulverizado se homogeneizó en aceite de maíz (Maceite, Promotora de Productos y Mercados Mexicanos S.A. de C.V.; Jalisco, México), porque es biodegradable, de fácil acceso, de bajo costo y de nula toxicidad. La extracción se realizó utilizando un Robot de cocina Thermomix® (Thermomix®, modelo TM31, Vorwerk & Co.; Wuppertal, Alemania) programando los siguientes parámetros: 60 ºC, homogeneizando a 1,100 rpm, durante 45 min, en una proporción de 2 g de materia seca por 5 g de aceite, equivalente a 0.4 g/ml. Posteriormente, el aceite se filtró usando una gasa estéril con una bomba de vacío para constituir el extracto-no acuoso. Cada extracto se almacenó a temperatura ambiente en un frasco ámbar herméticamente sellado durante 15 días hasta su uso10.
Tratamiento y dosificación
Los ratones infectados con H. diminuta se dividieron al día 30 post-infección en cuatro grupos de cinco individuos cada uno y se trataron durante 3 días consecutivos (días 30, 31, y 32 post-infección), determinando diariamente el número de huevos excretados por animal mediante un examen coproparasitoscópico de sedimentación, de acuerdo a lo descrito en la sección de Dinámica de huevos expelidos. El grupo 1 se administró con dimetilsulfóxido (DMSO) al 1%, el grupo 2 con 50 mg/kg de nitazoxanida (Cryptofin, Laboratorio Aranda, S.A. de C.V., CDMX, MX), el grupo 3 con el extracto no-acuoso de Artemisia y el grupo 4 con el extracto de Chenopodium. Los grupos 3 y 4 recibieron una dosis de 375 mg/kg de peso corporal, según la dosis de mayor efectividad reportada previamente7,13. El bienestar animal se condujo de acuerdo con la normatividad mexicana para el cuidado y uso de animales de laboratorio14. A las 24 h de haber finalizado la administración del tratamiento (día 33 post-infección), los gusanos adultos se recuperaron de cada ratón y se determinó la carga parasitaria por hospedador.
Evaluación de los helmintos adultos
Los helmintos recuperados se lavaron con solución salina fisiológica y se fijaron durante 3 h con formaldehído al 10 % luego, se colocaron en un recipiente con etanol al 70 %, donde se mantuvieron hasta su evaluación. Los especímenes se tiñeron de acuerdo al procedimiento descrito por Beltrán-Fabián-de-Estrada et al15, con algunas modificaciones. Brevemente, cada helminto se tiñó con carmín ácido al 1.6 % durante 15 min y el exceso de colorante se retiró con tres lavados de etanol al 70 %. Los helmintos se deshidrataron en un “tren” de etanol al 80, 90, 96 y 100 %; incubando durante 10 min en cada paso. Finalmente, los helmintos se transportaron en esencia de clavo durante 24 h. La evaluación se llevó a cabo en microscopía de campo claro para identificar alteraciones morfológicas en el escólex y en los proglótidos grávidos de cada cestodo recuperado. Particularmente, en los proglótidos se buscaron alteraciones en ramas uterinas y en tegumento, el cual, además fue evaluado por microscopía electrónica de barrido, de acuerdo a un procedimiento previamente descrito16. Los datos obtenidos se registraron de manera cualitativa.
Análisis estadístico
Todos los resultados se expresaron como los valores medios y desviación estándar. El análisis de los resultados entre muestras se realizó con una prueba ANOVA de dos factores; las diferencias estadísticas se determinaron al 95 % de confianza con la prueba de contraste de Tukey (Prism, GraphPad Software, Boston, USA).
Resultados y discusión
Infección experimental de Tenebrio molitor
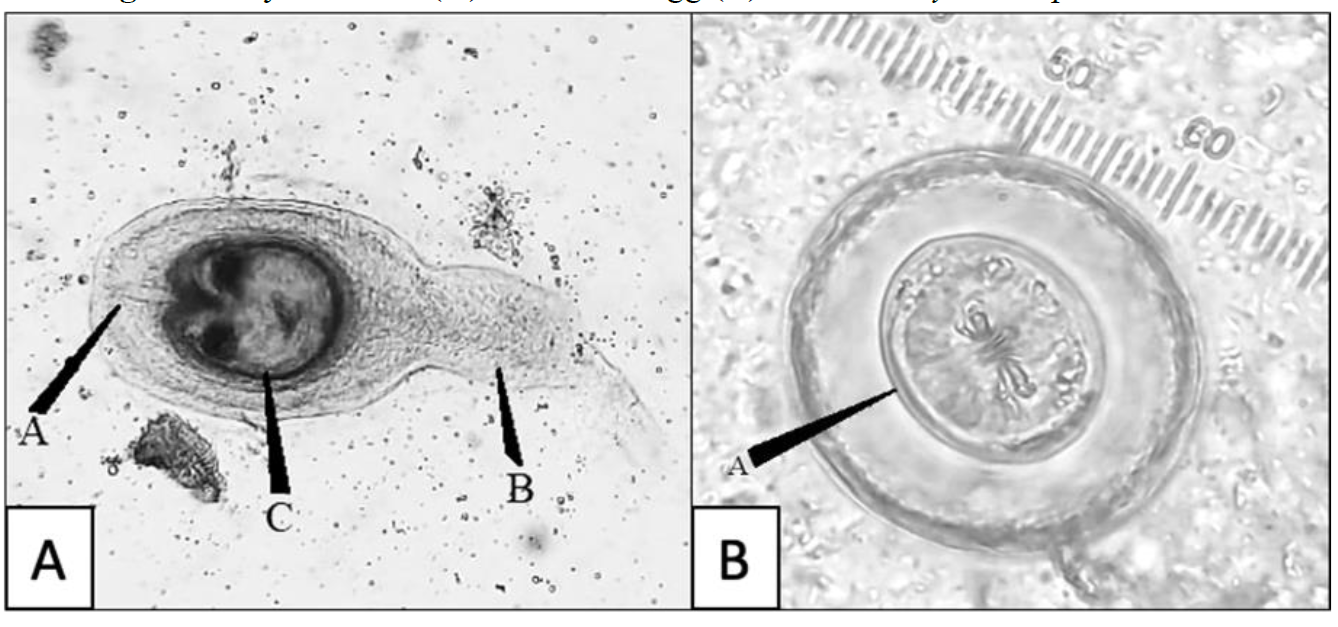
A los 10 días post-infección, los escarabajos se decapitaron y se encontró una frecuencia de infección del 60 %. Los cisticercoides tuvieron un tamaño promedio de 80 a 100 µm de longitud. Previamente otros autores reportaron para escarabajos Tribolium confusum una frecuencia de infección experimental del 39 al 41.7 %11; sin embargo, al igual que en este estudio, no se cuantificó la dosis por escarabajo. Los cisticercoides se recuperaron macerando manualmente el hemotórax en solución salina (Figura 1A).
Dinámica de huevos expelidos
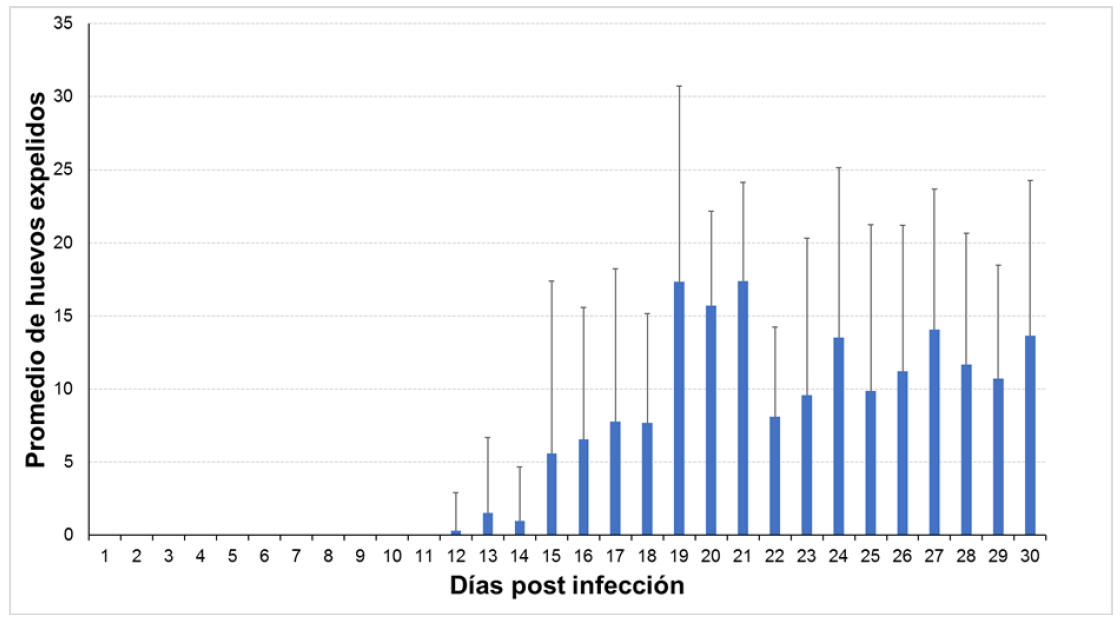
Para vigilar el establecimiento de H. diminuta, las muestras de heces de cada uno de los ratones infectados experimentalmente, se analizaron diariamente durante 30 días, previo a la administración de cualquier tratamiento. Los huevos del cestodo se detectaron a partir del día 12 post-infección y se mantuvieron presentes hasta el fin del experimento. Los huevos midieron entre 30 y 38 µm de diámetro (Figura 1B). Previamente, otros autores han reportado que la longitud máxima alcanzada por el helminto es a los 9 días post-infección, seguido de una disminución de tamaño a partir del día 11, debido al desprendimiento de proglótidos grávidos17, lo cual correlaciona con los datos que se registraron en este trabajo, ya que la detección de huevos comenzó el día 12 post-infección. Con respecto a la dinámica de huevos expelidos, los datos contrastan con una dinámica de 21 días en ratas infectadas experimentalmente, donde los autores registraron un aumento gradual en la cantidad de huevos excretados, comenzando con 1,106 y alcanzando 1,722 huevos por gramo de heces18. La cinética que aquí se reporta está constituida por datos de 30 días, en la que se observa un comportamiento con elevaciones cada 8 días. La Figura 2 muestra que la mayor cantidad de huevos detectados se encontró entre los días 19 y 21 post-infección.
Efecto de extractos no-acuosos sobre la excreción de huevos
En general, se observó una reducción del 50 % en la excreción de huevos a las 24 h post-tratamiento; sin embargo, entre las 48 y 72 h se registró una reducción del 75 % en los grupos de nitazoxanida y de Chenopodium, mientras que en el grupo tratado con Artemisia, mantuvo la reducción del 50 % el análisis de varianza de dos factores mostró diferencias estadísticamente significativas entre los grupos, por lo que se muestran en la Figura 3 los resultados de las comparaciones no significativas (ns) y las significativas, P<0.05 (*), P<0.001 (***) y P<0.001 (****) de la prueba de contraste de Tukey.
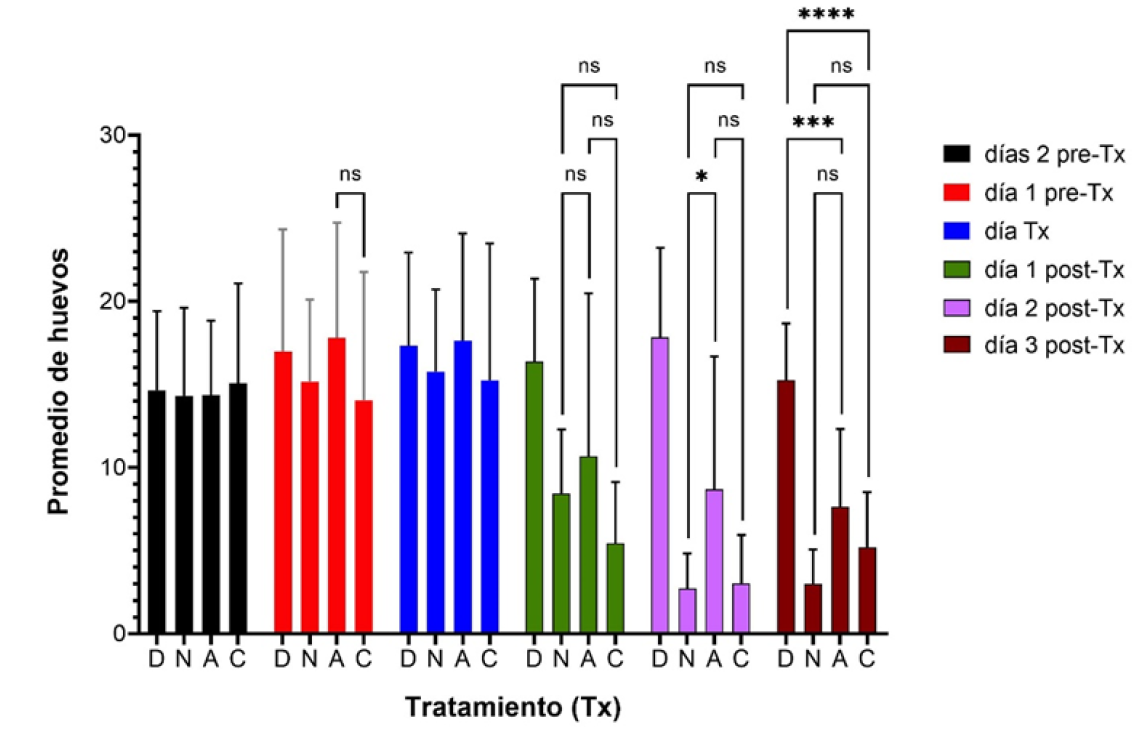
Resultados obtenidos con DMSO (D), nitazoxanida (N), Artemisia ludoviciana (A) y Chenopodium vulvaria (C). Comparaciones no significativas (ns) y significativas, P<0.05 (*), P<0.001 (***) y P<0.001 (****).
Figura 3 Excreción de huevos de Hymenolepis diminuta post-tratamiento
Los resultados, con el extracto no-polar de Artemisia, son similares a los previamente publicados por otros autores, donde se observó que en ratones infectados experimentalmente con Hymenolepis nana, el extracto acuoso de A. absinthium induce de manera dosis-dependiente, la reducción de la excreción de huevos en 61.8 % (400 mg/kg) y 98.8 % (800 mg/kg)19, mientras que el extracto etanólico de A. abrotanum induce una reducción del 75 % (150 mg/kg)9. Sin embargo, los resultados de este trabajo contrastan con los obtenidos con ovinos naturalmente infectados, donde se observó una reducción del 20 % en la excreción de huevos de nematodos, empleado un extracto acuoso de A. campestris (1:1.5; 50 ml/animal; 21 días) (20. Para explicar esta controversia se tienen que tomar en cuenta al menos cuatro factores, la región geográfica de origen de la planta, la región anatómica de la planta de la cual se prepara el extracto, la naturaleza del extracto (acuoso o alcohólico) y el tipo de parásito que se encuentre en estudio19. El aumento de la resistencia antiparasitarias en adición al riesgo residual de los fármacos, ha llevado a considerar que algunas plantas usadas en la medicina tradicional podrían ser una alternativa a este problema y, lo primero que se ha buscado es estudiar a las plantas que se han utilizado en algunas culturas como método antiparasitario9. Aunque muchas plantas se han estudiado, sólo algunas han sido apropiadamente caracterizadas, sobre todo considerando que las condiciones de cultivo no son necesariamente homogéneas a nivel mundial y no necesariamente todas las especies de plantas, aún del mismo género, necesariamente tienen el mismo metabolismo y por lo tanto los principios activos pueden diferir en variedad y en cantidad20; incluso pueden variar en una misma planta, dependiendo de la región anatómica de la cual se prepare el extracto y evidentemente el método de extracción, acuoso o etanólico también influirá en los metabolitos obtenidos.
Una vez que se ha considerado la heterogeneidad de los extractos, debe considerarse que los parásitos también son heterogéneos y aunque la palabra helminto considera cestodos y nematodos, los primeros llevan a cabo todos los intercambios nutritivos y gaseosos a través de su tegumento y el daño del mismo ocasionará pérdidas irreversibles en su metabolismo. En el caso de nematodos20, la alimentación se lleva a cabo por ingesta y su cuerpo se encuentran rodeado por una cutícula de composición escleroprotéica muy resistente, que protege al gusano de su entorno, por lo que, el efecto de los extractos de las plantas está asociado a la ingesta.
Con respecto al extracto no-acuoso de Chenopodium, los resultados difieren de los reportados para los extractos oleosos convencionales de C. graveolens (100 mg/kg) y C. ambrosioides (400 mg/kg), los cuales no mostraron reducción en la excreción de huevos de H. diminuta después de cinco días de tratamiento7. Sin embargo, extractos metanólicos y acuosos de C. album indujeron la reducción gradual (de 86 a 63.5 %) en la excreción de huevos de Haemonchus contortus en animales naturalmente infectados y tratados durante 15 días con una dosis de 2 mg/kg de peso corporal21. Aunque en el trabajo que aquí se reporta, no se comprobó la viabilidad de los huevos excretados, se ha sugerido que los extractos de C. ambrosioides solubilizados con Tween 80 tienen efecto ovicida contra H. diminuta7 y nematicida contra H. contortus6.
Efecto de extractos sobre el número de helmintos adultos
Durante el curso de la infección o del tratamiento, no se observaron ratones con efectos clínicos adversos, con heces pastosas o diarreicas, ni tampoco se observó la expulsión de gusanos. Los helmintos recuperados midieron entre 27 y 35 cm de longitud (Figura 4B), tamaño esperado en ratones infectados experimentalmente17. En los grupos administrados con Artemisia y con Chenopodium, el número de adultos disminuyó 50 % (P<0.005), mientras que en el grupo con nitazoxanida, disminuyó hasta 75 % (P<0.001) con respecto al grupo tratado con DMSO. Resultados similares a los de este trabajo, han reportado que ratones infectados experimentalmente con H. nana y tratados con un extracto acuoso de A. absinthium, obtuvieron una reducción del 56.5 % con 400 mg/kg y del 98.5 % con 800 mg/kg 19; mientras que los extractos hidroalcohólicos de A. dracunculus y A. absinthium mostraron in vitro efectos cestocidas, dosis-dependiente (50 a 250 mg/ml) contra protoescólices de Echinococcus granulosus22. De esta manera el extracto de Artemisia, independientemente de la especie, puede ser una estrategia alternativa para el control de los cestodos gastrointestinales aunque aún se encuentra en estudio la dosis en la que debe administrarse y la caracterización de los metabolitos que constituyen el extracto de Artemisia, lo cual es importante porque los extractos acuosos de A. herba-alb y C. ambrosioides, el primero, administrado vía oral en palomas, no tuvo efecto sobre el número de cestodos de Raillietina spp23 y, el segundo, no tuvo efecto en el número de cestodos recuperados de roedores infectados naturalmente7. Lo cual podría llevar a plantear una nueva estrategia para el control de las infecciones por cestodos mediante la combinación de los fármacos antiparasitarios usados de manera tradicional y los extractos de Artemisia, lo que además tendría como ventaja la disminución del desarrollo de resistencia antiparasitaria y la contaminación ambiental.
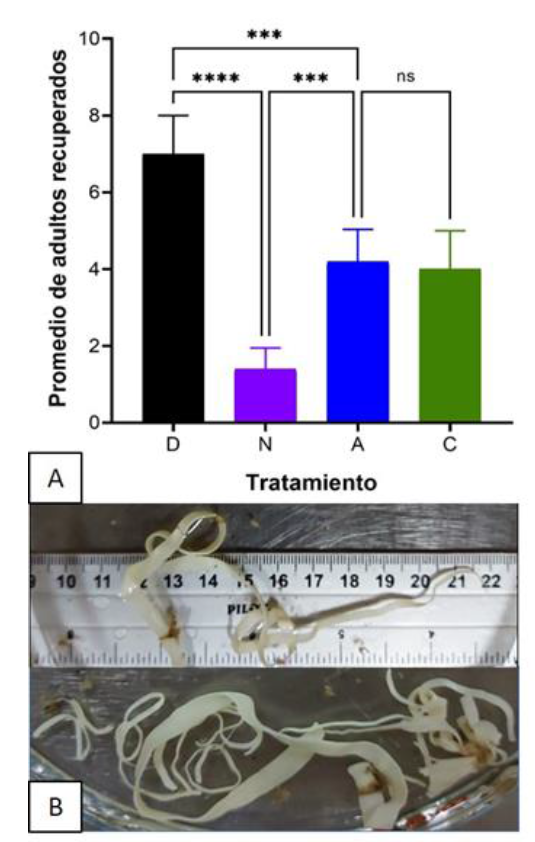
Resultados obtenidos con DMSO (D), nitazoxanida (N), Artemisia ludoviciana (A) y Chenopodium vulvaria (C). En el panel A, comparaciones no significativas (ns) y significativas a P>0.001 (***) y a P>0.001 (****). En panel B es un cestodo recuperado de un ratón tratado con DMSO-1%.
Figura 4 Cestodos adultos recuperados post-tratamiento
Efecto sobre el tegumento del helminto adulto
Los proglótidos grávidos tratados con DMSO 1% mostraron una tinción uniforme que permitió observar las ramificaciones internas de útero con huevos (Figura 5), mientras que la microscopía electrónica de barrido mostró un tegumento con estriaciones uniformes (Figura 6). El análisis de los proglótidos tratados con nitazoxanida y luego teñidos con carmín-ácido mostró que los proglótidos retienen colorante de manera homogénea, i.e., hay regiones con cúmulos de colorante y regiones sin teñir, lo que sugiere daño en las estructuras internas. Por otro lado, con el aceite de clavo, utilizado como medio para aclarar los tejidos, se observaron secciones del tegumento que tomaron una coloración café-verdosa, lo cual sugiere daño.
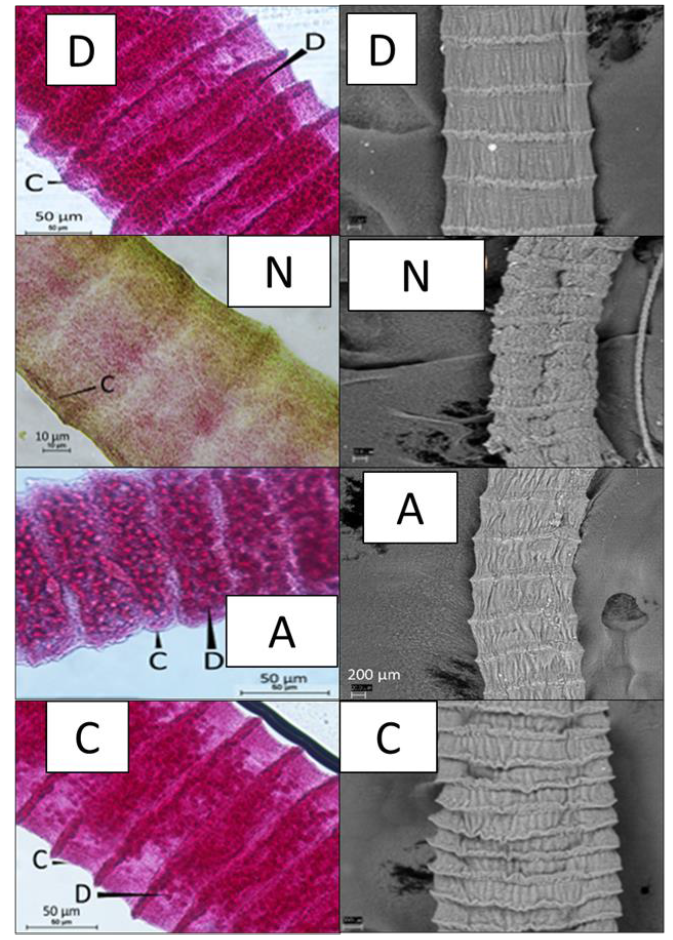
Los proglótidos se tiñeron con carmín-ácido (paneles izquierdos) y se sometieron a microscopía electrónica de barrido (paneles derechos). La figura muestra los resultados obtenidos con DMSO (D), nitazoxanida (N), Artemisia ludoviciana (A) y Chenopodium vulvaria (C). Atrio genital (C) y huevos en las ramas uterinas (D).
Figura 5 Proglótidos grávidos de Hymenolepis diminuta post-tratamiento
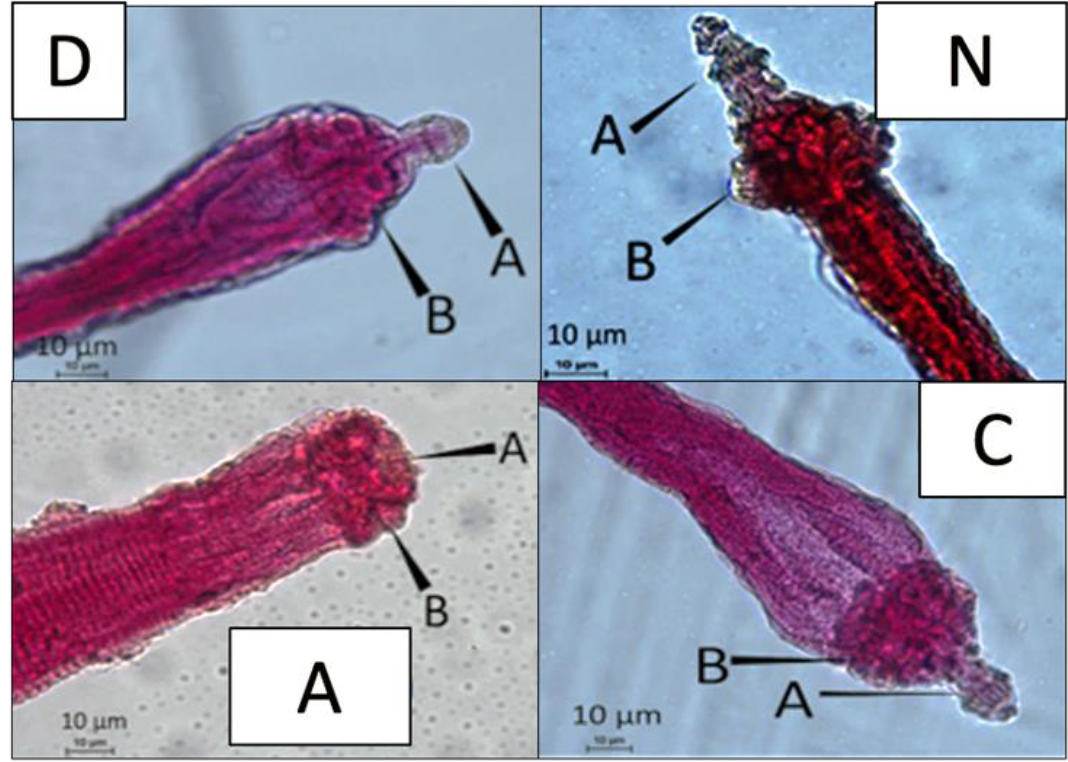
Resultados obtenidos con DMSO (D), nitazoxanida (N), Artemisia ludoviciana (A) y Chenopodium vulvaria (C). Cada panel muestra rostelo (A) y ventosas (B).
Figura 6 Escólex recuperado a las 72 horas post-tratamiento
En resumen, la nitazoxanida provocó deformaciones y surcos anormales en el tegumento del proglótido, así como daño en úteros con ausencia de huevos. El análisis de los proglótidos en microscopía electrónica de barrido mostró deformación del tegumento asociada a fisuras y a la generación de vesículas que dan una apariencia aterciopelada sin patrón de estrías. Con anterioridad se ha descrito que las lesiones en el tegumento de los cisticercoides de Taenia crassiceps provocadas por el tratamiento con nitazoxanida, consiste en la separación del tegumento del cuerpo del parásito, así como ruptura de la vesícula; de igual manera, en la microscopía electrónica de barrido, se observa desintegración del tegumento24.
En los proglótidos tratados con Artemisia, se observó que la tinción con carmín-ácido fue uniforme; las ramas uterinas se observaron intactas. En el tegumento se observaron depresiones. La microscopía electrónica de barrido mostró incremento en las rugosidades del tegumento, zonas de fisuras, depresiones en algunas porciones de los proglótidos, pequeñas regiones con vesículas y tejido degradado. Beshay en 201719 demostró por microscopía electrónica de transmisión, que el efecto cestocida (1 mg/ml durante 7 h de exposición) de A. absinthium contra H. nana adulta, está asociado con cambios morfológicos del tegumento por la acumulación de lípidos e, internamente, el proglótido mostró destrucción del canal nefridial y de los óvulos intrauterinos, así como procesos de apoptosis y autofagia, lo que podría atribuirse a la alteración de la absorción de nutrientes debido a el daño tegumental19. Existen reportes de la inducción de la expulsión de nematodos con daños observables macroscópicamente, cuando el hospedador es tratado con Artemisia25.
En los proglótidos tratados con Chenopodium graveolens, se observó que la tinción con carmín-ácido mostró áreas no teñidas en el interior de los proglótidos, pero no se observó daño en las ramas uterinas ni cambios morfológicos en los huevos. Con microscopía electrónica se observó que el cambio principal fueron depresiones en el tegumento; sin embargo, al observar los huevos, luego de la tinción con carmín-ácido no mostraron cambios en la morfología de los huevos. Previamente se ha documentado que de manera dosis dependiente, el extracto de Artemisia es capaz de inducir apoptosis en los proglótidos grávidos de H. nana19 y por lo tanto inducir daño en los huevos; sin embargo, si el daño en el tegumento es superficial, como en los datos que aquí se reportan, no habría daño en los huevos. Por otro lado, otros autores han descrito que los extractos de C. ambrosioides y C. album tienen efecto paralizante en los anélidos Pheretima posthuma26 y Eisenia foetida27.
A nivel del escólex, el tratamiento con nitazoxanida mostró daño de ventosas y rostellum, a igual que lo han reportado otros autores usando la combinación nitazoxanida-albendazol (40 mg/kg) en el modelo de cisticercosis murina. La combinación resultó en deformaciones de las ventosas y el rostellum28. Los extractos de Chenopodium y Artemisia no mostraron daño en el rostellum, aunque la tinción con carmín-ácido, mostró ligera deformación de las ventosas. Previamente se ha reportado por otros autores que el extracto de Senna alexandrina produce rugosidades en los proglótidos de H. diminuta y deformación en las ventosas del parásito16.
Conclusiones e implicaciones
En este estudio se determinó el efecto de los extractos no-acuosos de Artemisia ludoviciana mexicana y Chenopodium vulvaria durante la infección experimental murina con H. diminuta. Los extractos abatieron la carga parasitaria en 50 % durante las primeras 24 h de su administración; pero con el extracto de Chenopodium la carga parasitaria se abate hasta del 70 % en las siguientes 72 h. Estudios adicionales deben hacerse para determinar dosis, principios activos y en su caso, combinación con fármacos para establecer el efecto cestocida. También debe verificarse el efecto con otros géneros de cestodos, trematodos y nematodos gastroentéricos, incluidos los estados larvarios. La ausencia de reacciones adversas posibilita la utilización de los extractos como estrategia alternativa para el control de las infecciones por cestodos gastroentéricos.