En las últimas dos décadas, los efectos del cambio climático sobre las especies, la estructura y función de los ecosistemas se han hecho más evidentes (Yang & Rudolf 2010). El cambio climático ha producido cambios en la fenología y ontogénesis de diversas especies de plantas, animales y hongos, así como en sus interacciones (Kauserud et al. 2008).
Diversos estudios a mediano y largo plazo han mostrado que la fenología y los patrones de la formación de esporomas en los macrohongos son modificados por las variables ambientales como la precipitación, humedad y temperatura (Kauserud et al. 2008, 2012, Baptista et al. 2010, Sato et al. 2012, Boddy et al. 2014, Li et al. 2018). Estudios a largo plazo en zonas templadas, entre 1940 y 2006, han mostrado los efectos del cambio climático en el patrón temporal de formación de esporomas de los hongos, sugiriendo que el aumento en la temperatura global de hasta 4 °C para el 2100 tendrá efectos drásticos en la fenología de estos organismos (Kauserud et al. 2008).
Varios estudios realizados en los últimos 30 años en bosques templados han revelado que el inicio de la formación de esporomas de los macrohongos se adelanta entre dos y tres semanas, en comparación con registros históricos, observándose ahora los primeros esporomas a mediados de julio, así como una prolongación del periodo medio anual de formación de esporomas hacia finales de otoño entre noviembre y diciembre (Gange et al. 2007, Büntgen et al. 2013). En la década de 1950, el periodo de duración de los esporomas fue de un promedio de 33.2 ± 1.6 días, mientras que en 2009 se extendió más del doble, con valores de 69.1 ± 6.8 días (Gange et al. 2007). Esta extensión de la temporada de esporomas en los bosques templados está relacionada con la prolongación de la temporada de crecimiento de la vegetación (Menzel et al. 2006).
Los macrohongos son componentes esenciales de los ecosistemas terrestres debido a su papel en el transporte, almacenamiento y liberación de nutrientes como carbono (C), fósforo (P) y nitrógeno (N) (Bortier et al. 2018). Además, cumplen con diversas funciones ecológicas como descomponedores, simbiontes y parásitos (Setälä & McLean 2004, Niego et al. 2023); asimismo, contribuyen al reciclaje de materia orgánica, enriqueciendo los suelos de selvas, bosques y otros hábitats, y ayudan a mantener la estabilidad de la biodiversidad (Zotti et al. 2013, Wu et al. 2019, Wang et al. 2020).
Se estima que existen entre 53,000 y 110,000 especies de macrohongos a nivel mundial, aunque hasta el 2007 sólo se conocían aproximadamente 21,600 especies (Mueller et al. 2007, Hawksworth & Lücking 2017). En México, se estimó entre 2014 y 2016 que hay cerca de 200,000 especies de hongos, pero hasta ese momento solo se habían documentado alrededor del 2.25 % de macrohongos (Aguirre-Acosta et al. 2014, Sarukhán et al. 2017). Este bajo porcentaje de conocimiento, refleja una brecha significativa en la exploración de la biodiversidad fúngica mexicana, especialmente si se compara con grupos mejor estudiados como plantas o vertebrados (Sarukhán et al. 2017).
En las regiones tropicales, la información es todavía más escasa. En específico para la Península de Yucatán (PY) en 2014, reportaron un total de 754 especies de hongos; Quintana Roo (447); Campeche (154); Yucatán (153) (Ancona-Méndez et al. 2010, Yuridia-López et al. 2011). De las 754 especies de hongos, poco más de 450 especies son macrohongos (Aguirre-Acosta et al. 2014) que representa el 10 % de las especies registradas para México; de las especies reportadas para la PY, Quintana Roo alberga 401 especies (de la Fuente et al. 2020) que representa aproximadamente el 89 % del total en la península, por lo tanto, es la entidad con mayor riqueza documentada.
La mayoría de los estudios sobre macrohongos en Quintana Roo se han centrado en inventarios como los de Chio & Guzmán (1982), Guzmán-Dávalos & Guzmán (1982), Guzmán (1983, 2003), Pérez-Silva & Herrera (1992), Ryvarden & Guzmán (1993), San Martin & Rogers (1995), San Martin et al. (1998), Pompa-González et al. (2011) y de la Fuente et al. (2020); sin embargo, es necesario continuar con estudios de la diversidad de macrohongos, así como explorar diversos sitios y ecosistemas del trópico, tanto en hábitats conservados y transformados por el cambio de uso de suelo. Además, se debe evaluar la relación entre las variables climáticas y su influencia en la composición, fenología de los macrohongos, así como los efectos en la estructura y función de los ecosistemas.
Por lo anterior, el presente estudio tuvo como objetivo analizar la dinámica de la formación de esporomas de los macrohongos en una selva mediana subperennifolia en el sur de Quintana Roo, y su relación con las condiciones ambientales estacionales como temperatura y humedad, durante el verano y otoño; además de evaluar cómo estas variables microclimáticas influyen en la composición y abundancia de los diferentes grupos de macrohongos.
Materiales y métodos
Área de estudio. El área de estudio se localiza en el ejido de Allende perteneciente al municipio de Othón P. Blanco, ubicado en el sur de Quintana Roo con coordenadas 18° 22' 10.7" N 88° 33' 25.6" W. Se encuentra al noroeste de Belice, delimitado por la frontera natural del Río Hondo, y al suroeste de la ciudad de Chetumal, capital del estado (Figura 1). La zona donde se ubica el área de estudio presenta una vegetación de selva mediana subperennifolia, considerada como uno de los tipos de vegetación con mayor extensión en Quintana Roo con una superficie aproximada de 1.2 millones de hectáreas lo que equivale a un 25 % de la superficie total del estado (INEGI 2018). Esta vegetación presenta predominantemente las siguientes especies arbóreas: Brosimum alicastrum (L.) Swart, Bursera simaruba (L.) Sarg., Manilkara zapota (L.) P.Royen, Lysiloma bahamensis (Griseb.) E.Wiley, Vitex gaumeri (Standl.) S.F.Blake, Bucida buceras L., Alseis yucatanensis C.Wright, y Swietenia macrophylla King. En la ribera del río crece Pachira aquatica Aubl., además, se encuentran helechos y musgos en el estrato arbustivo, así como una gran diversidad de epífitas como orquídeas, bromeliáceas y aráceas (Bautista & Palacio-Aponte 2012).
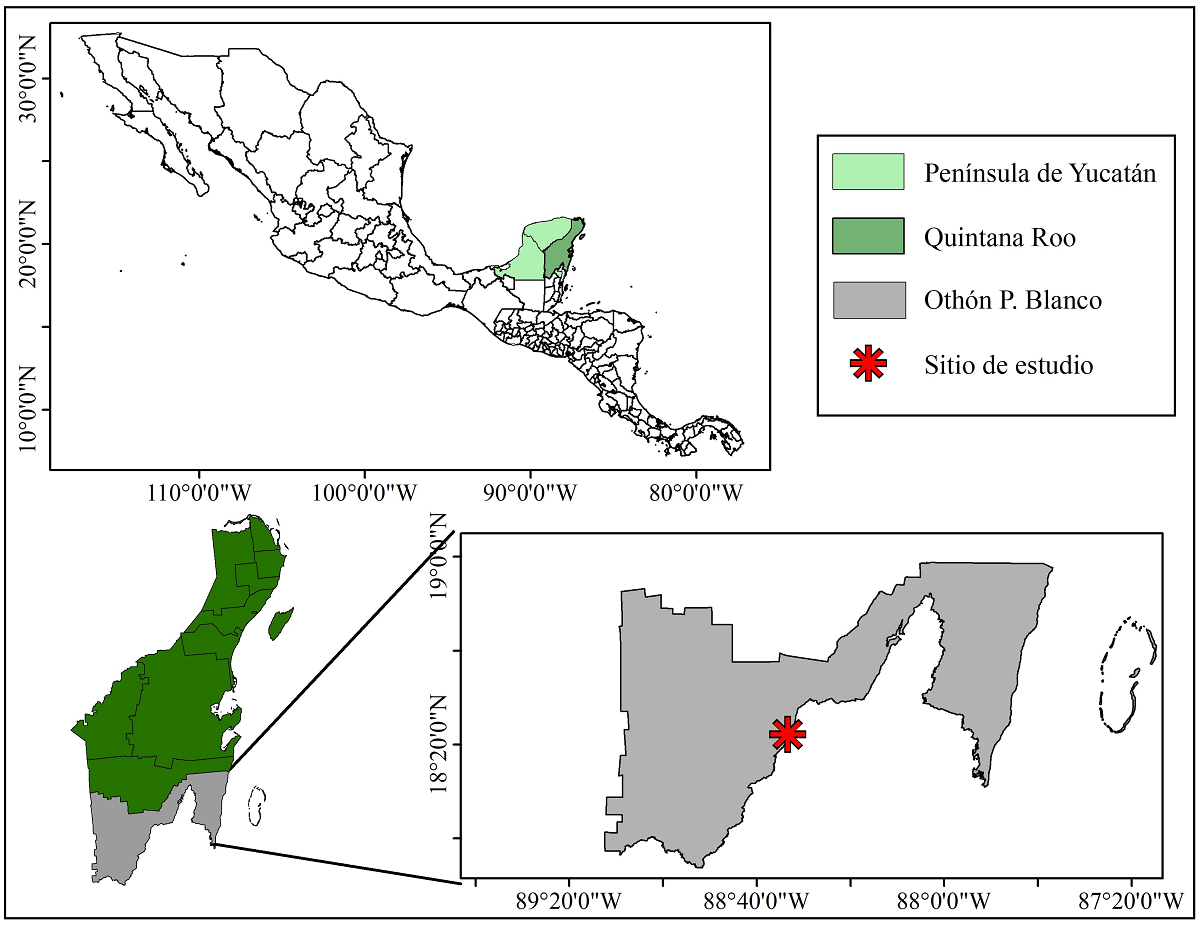
Figura 1 Ubicación geográfica del sitio de estudio establecido en una selva mediana subperennifolia en el sur de Quintana Roo.
El clima de la región es cálido-subhúmedo de acuerdo con la clasificación de Köppen, con precipitaciones que ocurren principalmente durante los meses de junio a noviembre abarcando las estaciones de verano y otoño. La temperatura media oscila entre 26 °C y 30 °C, con una precipitación anual de 1,350 mm, el suelo predominante es vertisol (INEGI 2010). La vegetación en esta zona ha sido afectada significativamente por actividades agrícolas y ganaderas, resultando en un paisaje con parches de vegetación rodeados en su mayoría por cultivos de caña de azúcar (Ellis et al. 2020).
Parcelas de muestreo. Se seleccionó un fragmento de vegetación secundaria con una extensión que abarca aproximadamente 100 hectáreas; sin evidencia de perturbación antropogénica durante los últimos 30 años. Se establecieron 10 parcelas de 10 × 10 m de manera aleatoria para alcanzar una cobertura total de muestreo de 0.1 hectáreas. Este diseño de muestreo siguió protocolos estandarizados para estudios de diversidad fúngica en selvas tropicales (Mueller 2004).
La recolección se realizó de junio a noviembre de 2023, con cuatro colectas por mes, sumando un total de 24 colectas. Con la ayuda de medidores ambientales (HOBO U23 Pro v2; Onset Computer Corporation, Bourne, Massachusetts, EE. UU.), se registraron datos de temperatura y humedad ambiental durante todo el periodo de muestreo en tres de las 10 parcelas. La selección de las tres parcelas fue al azar.
Para medir la temperatura y humedad del suelo, se empleó un higrómetro digital (YY-1000; Shenzhen YIERYI Technology Co., Ltd., Guangdong, China), con mediciones y registros semanales. La recolección de macrohongos se limitó a los esporomas observables mayores a 0.5 cm (Redhead 1997).
La abundancia fue considerada de acuerdo a los conteos de individuos por especie, para evitar sobreestimar este parámetro; los esporomas recolectados que presentaron grupos conexos, tipo cespitoso o gregario, y dentro de un radio menor a 100 cm, se registraron como un solo individuo (Gómez-Hernández et al. 2016), según lo sugieren Straatsma et al. (2001) y Lodge et al. (2004).
Identificación y procesamiento de macrohongos. Los especímenes recolectados, se llevaron al Laboratorio de Estudios Avanzados en Agroecosistemas del Instituto Tecnológico de la Zona Maya para observarlos y describir detalladamente sus características macroscópicas y microscópicas del píleo, himenóforo, contexto, estípite y base o volva, entre otros. Posteriormente se deshidrataron por 24 a 48 horas a una temperatura entre 38 a 40 °C (Caiafa et al. 2017).
Una vez deshidratadas, se hicieron preparaciones temporales y se observaron con un microscopio compuesto (DM750; Leica Microsystems GmbH, Wetzlar, Alemania), para examinar características como el grosor de las hifas del píleo, himenio, basidios, basidiolos, cistidios, ascas, paráfisis y esporas. Para los Ascomycota, se documentaron adicionalmente la morfología de los ascomas (apotecios, periticios, o cleistotecios), la disposición de las ascas y la presencia de estructuras especializadas como pelos o apéndices en las esporas (Lumbsch & Huhndorf 2010). Se midieron 50 esporas por individuo en el microscopio. También se utilizaron diversos reactivos como Azul de metileno, KOH 10 %, Rojo Congo y Reactivo de Melzer, para observar ornamentaciones y cambios de coloración en las microestructuras fúngicas. Los especímenes estudiados se encuentran en resguardo en el Laboratorio de Estudios Avanzados del Instituto Tecnológico de la Zona Maya. Los esporomas se identificaron a nivel de género y especie con literatura especializada (Largent 1977, Pegler 1983, Guzmán 2003, Lodge et al. 2004, Mueller et al. 2011). Los nombres científicos están actualizados de acuerdo con la base de datos Index Fungorum (https://www.indexfungorum.org/names/names.asp).
Análisis de datos. Se evaluó la riqueza de especies (S), la abundancia total y la abundancia relativa. La riqueza se refiere al número de taxones recolectados, durante cada mes de la temporada de lluvias. La abundancia es el número total de esporomas recolectados por especie, taxón o morfoespecie, mientras que la abundancia relativa es la proporción de esporomas de cada especie, taxón o morfoespecie en relación con el número total de esporomas recuperados. La frecuencia de aparición se expresa como la proporción del número de visitas en que se recuperó cada especie con respecto al número total de días de muestreo desde junio a noviembre de 2023.
Para cuantificar la diversidad de macrohongos se calculó el índice de diversidad de Shannon-Wiener (H´) y el índice de diversidad verdadera del orden q = 2, esta última considerada como una medida robusta de diversidad efectiva que pondera las especies según su abundancia (Chao et al. 2014). El índice de Shannon-Wiener se calculó como la suma de las proporciones (pi) de esporomas de cada especie multiplicadas por el logaritmo natural de dichas proporciones:
La diversidad verdadera del orden q = 2 corresponde al inverso de la suma de los cuadrados de las proporciones de todas las especies:
La cual se interpreta como el número de especies igualmente abundantes necesarias para obtener el mismo nivel de diversidad observado, con mayor sensibilidad a las especies comunes (Jost 2006, Chao et al. 2014).
Las curvas de acumulación de especies se generaron mediante el paquete en línea iNEXT (Chao et al. 2016), utilizando un enfoque de interpolación-extrapolación con 1,000 réplicas de bootstrap para estimar intervalos de confianza al 95 %. El análisis se estratificó en dos períodos estacionales (junio-agosto y septiembre-noviembre) ya que estos meses corresponden al verano y otoño respectivamente. Cada colecta mensual fue considerada como unidad de muestreo independiente. Para cada período se calcularon la riqueza observada y los estimadores no paramétricos de Chao1 e iChao1, los cuales, incorporan correcciones para especies raras no detectadas. El esfuerzo de muestreo se considera adecuado cuando las curvas tienden a la asíntota o cuando los estimadores indican una cobertura superior al 70 %, criterio establecido para estudios ecológicos de diversidad fúngica (Hortal et al. 2006, Chao & Jost 2012). Estas curvas se construyeron a partir de matrices de presencia-ausencia y abundancia relativa de los taxones registrados.
Para determinar una correlación de las variables temperatura del suelo (TemS), humedad del suelo (HumS), temperatura ambiental (TemA), humedad ambiental (HumA), área basal (AB), diámetro normal (DM) y riqueza arbórea (Riq), con el número de especies y su abundancia se realizó un análisis de correspondencia canónica (CCA) en donde se incluyeron 118 morfoespecies registradas en el sitio. También se realizó un Escalamiento Multidimensional No Métrico (NMDS) para determinar las distancias entre los meses de muestreo y si estos presentan similaridad o difieren entre ellos.
Las correlaciones de Spearman, determinan si alguna variable genera una relación positiva o negativa con las especies de macrohongos registradas. Los análisis NMDS, CCA y correlaciones de Spearman se realizaron con el entorno estadístico de R v. 4.3.2 (R Core Team 2024), mediante la interfaz RStudio (RStudio Team 2020), utilizando la paquetería vegan (Oksanen et al. 2013).
Resultados
Riqueza y diversidad de macrohongos. Durante los meses junio a noviembre del 2023, se recolectaron un total 1,234 esporomas en el sitio de estudio. Estos se clasificaron en 118 morfoespecies (Tabla S1). De estos taxones, 35.59 % se identificaron a nivel de especie, 36.44 % a nivel de género, 7.63 % hasta familia y el 20.34 % aún no se han identificado. El 89.83 % de los taxones identificados pertenecen al filo Basidiomycota, quien fue el grupo dominante, representado por nueve órdenes, 23 familias, 35 géneros y 106 morfoespecies. Por otro lado, el filo Ascomycota está conformado por dos órdenes, tres familias, tres géneros y 12 morfoespecies.
La familia Agaricaceae fue la más diversa con 21 especies, seguida de Polyporaceae con 19, Marasmiaceae 16 y Xylariaceae con ocho, que en conjunto representan el 54.24 % del total de los taxones recolectados (Figura 2). Los géneros más abundantes fueron Agaricus, Marasmius, Xylaria y Conocybe, con 16, 12, 8 y 5 % respectivamente (Figura 3).
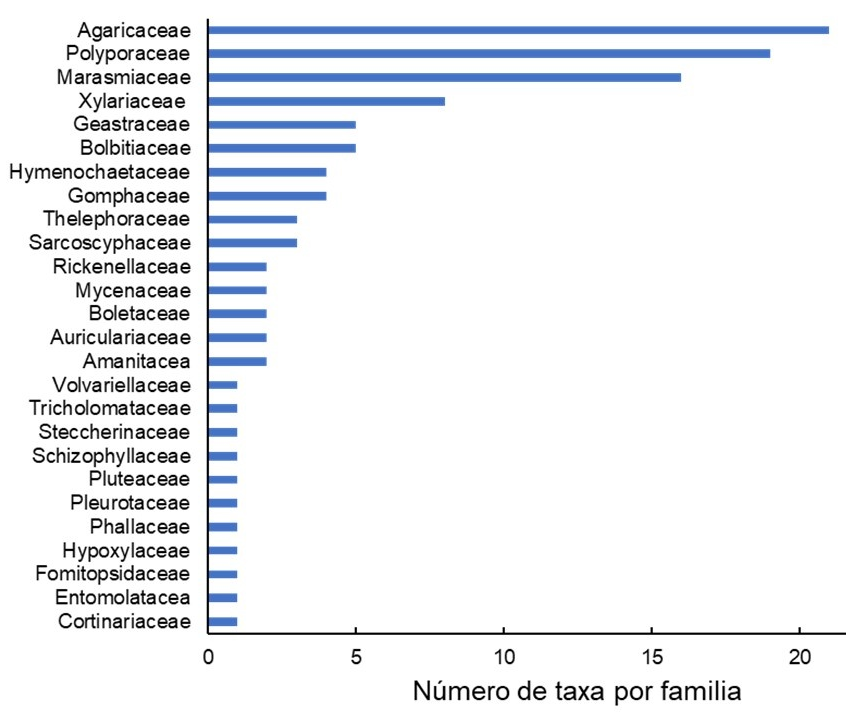
Figura 2 Número total de especies por familia de macrohongos registradas en un fragmento de vegetación de selva mediana subperennifolia en el trópico subhúmedo.
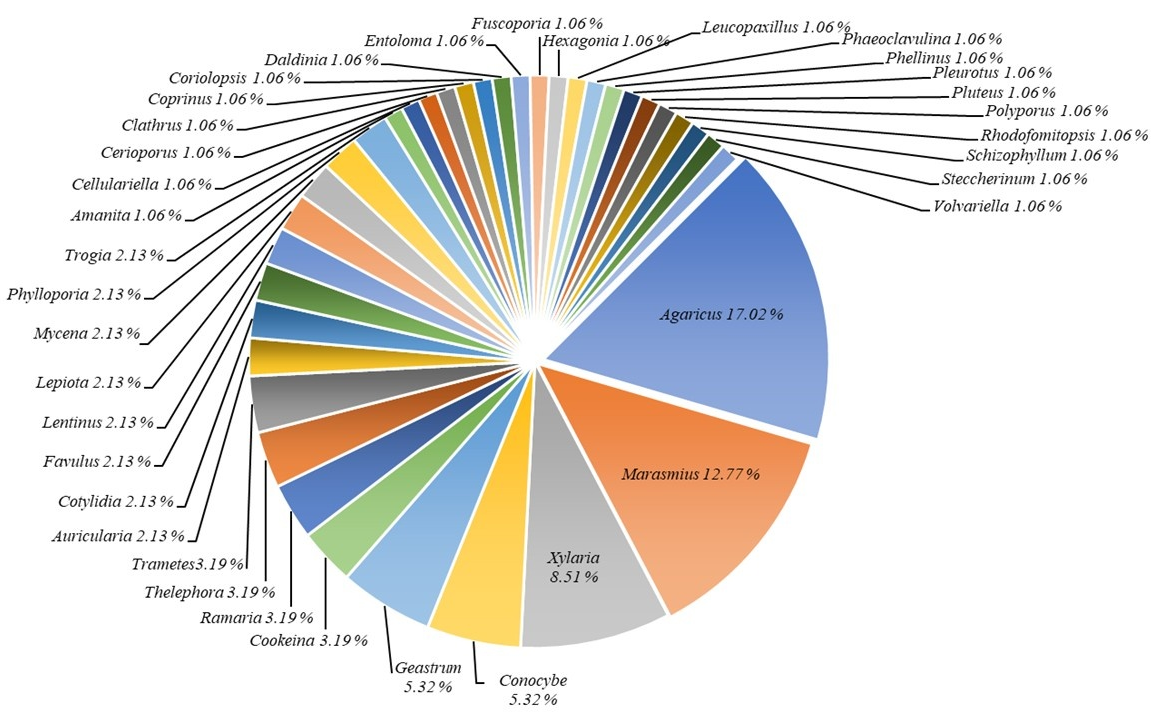
Figura 3 Porcentaje total de especies por género de macrohongos registradas en un fragmento de vegetación de selva mediana subperennifolia en el trópico subhúmedo.
El mayor número de familias se registró durante los meses de septiembre y noviembre, con 18 y 17 registros respectivamente, mientras que junio presentó el menor número de familias, con solo cinco. En cuanto al hábito ecológico, los saprótrofos fueron el grupo más predominante con un 90.15 % de las especies recolectadas, mientras que los hongos ectomicorrízicos constituyeron solo el 9.85 %. Al considerar el sustrato donde se desarrollan los macrohongos, se encontró que los lignícolas representaron el 61.34 %, los humícolas el 20.77 % y los terrícolas el 17.89 %.
Los macrohongos estudiados en un fragmento de selva mediana, presentan un marcado patrón de formación de esporomas durante la estación de lluvias en los meses de junio a noviembre. Únicamente la familia Polyporaceae presentó esporomas durante todos los meses de estudio, misma que representa un 16.10 % de la diversidad total. Esto es debido a que esta familia presenta esporomas de longevidad anual, bienal o perenne, además poseen hifas esqueléticas y generativas que mantienen la integridad estructural y retienen humedad, retardando la descomposición (Zoberi 1972). A su vez, la familia Marasmiaceae, aunque solo estuvo presente en cinco meses, fue la más abundante con un 21.24 % de la abundancia relativa y representa el 13.56 % de la diversidad total. Las familias Steccherinaceae, Phallaceae y Mycenaceae se encontraron en meses específicos; junio, julio y septiembre respectivamente. De estas últimas familias solo se registró una recolección (Figura 4).
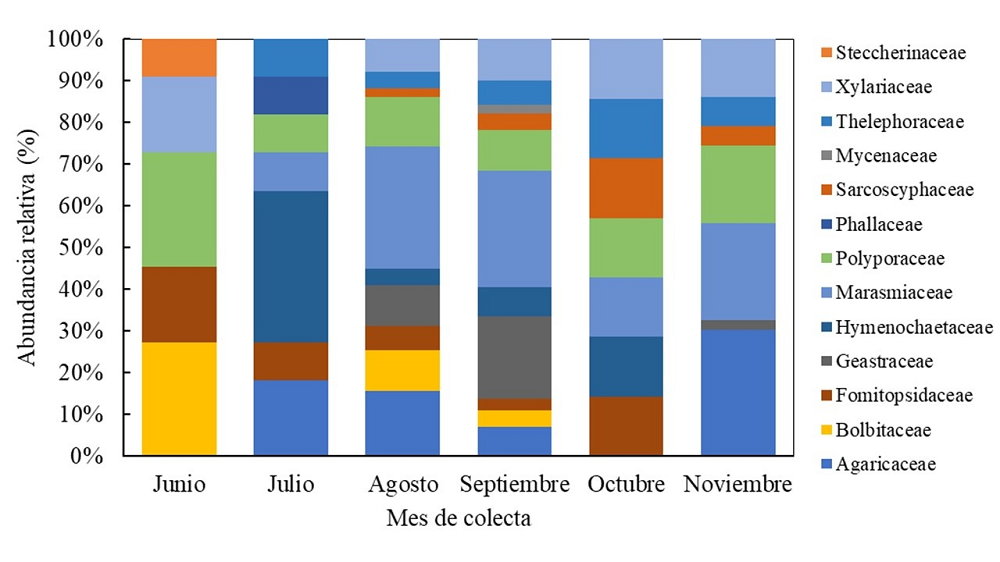
Figura 4 Abundancia relativa de familias de macrohongos registradas en un fragmento de vegetación de selva mediana subperennifolia en el trópico subhúmedo.
Los datos muestran que septiembre presentó el mayor número de esporomas, registrando un total de 402 pertenecientes a 59 especies. Seguido de agosto con 309 esporomas y 45 especies, y noviembre, con 216 esporomas y 41 especies. En contraste, octubre presentó la menor abundancia, con solo 31 esporomas pertenecientes a 8 especies (Figura 5).
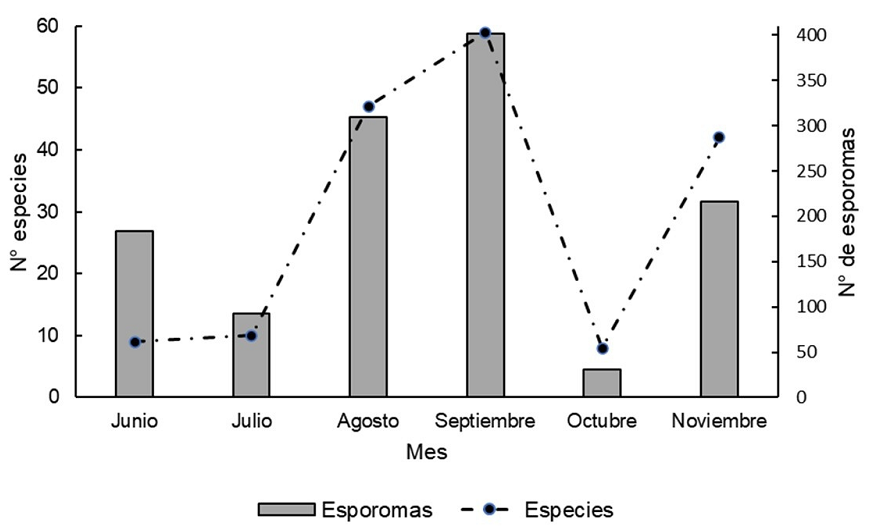
Figura 5 Número de especies y esporomas de macrohongos por mes registradas en un fragmento de vegetación de selva mediana subperennifolia en el trópico subhúmedo.
Índices de diversidad y curvas de acumulación. Se calculó el índice de diversidad de Shannon (H´), para evaluar la diversidad de macrohongos en el sitio de muestreo. El valor obtenido fue de 4.36, lo que indica que el sitio presenta una alta diversidad, particularmente si se considera que el valor máximo teórico posible, calculado a partir del logaritmo natural de la riqueza de especies, (ln S = ln 118), es de 4.77. Este resultado sugiere que en el sitio la comunidad de macrohongos no solo presenta una riqueza considerable de especies, sino que también presenta una distribución relativamente equitativa de individuos entre ellas. Por otro lado, el índice de diversidad verdadera del orden q = 2, alcanzó un valor de 24.43 en una comunidad con 118 taxones registrados. Este valor representa un 20.72 % de la riqueza total, lo cual refleja que a pesar de la alta diversidad, la comunidad presenta una estructura de abundancias desigual, donde algunos taxones son más abundante que el resto (Chao et al. 2014). A pesar de esta estructura de abundancias desigual, la estimación de una diversidad alta, sugiere un ecosistema saludable (Magurran 2004, Jost 2006).
De acuerdo a las curvas de acumulación de especies, el estimador Chao1 arrojó un valor de 55.6 % de cobertura, con un total de 53 especies observadas para el primer periodo (jun-ago), mientras que, en el segundo periodo (sep-nov) mostró un 71.1 % de cobertura y 90 especies registradas. Aunque el periodo jun-ago nos indica que no hubo un buen esfuerzo de muestreo, el periodo sep-nov, nos señala una extrapolación buena. La curva de acumulación de especies contemplando ambos periodos presentó una cobertura de 74.6 % con 118 especies registradas, lo que sugiere, que al aumentar el esfuerzo de muestreo se podrán encontrar hasta 170 especies (Figura 6).
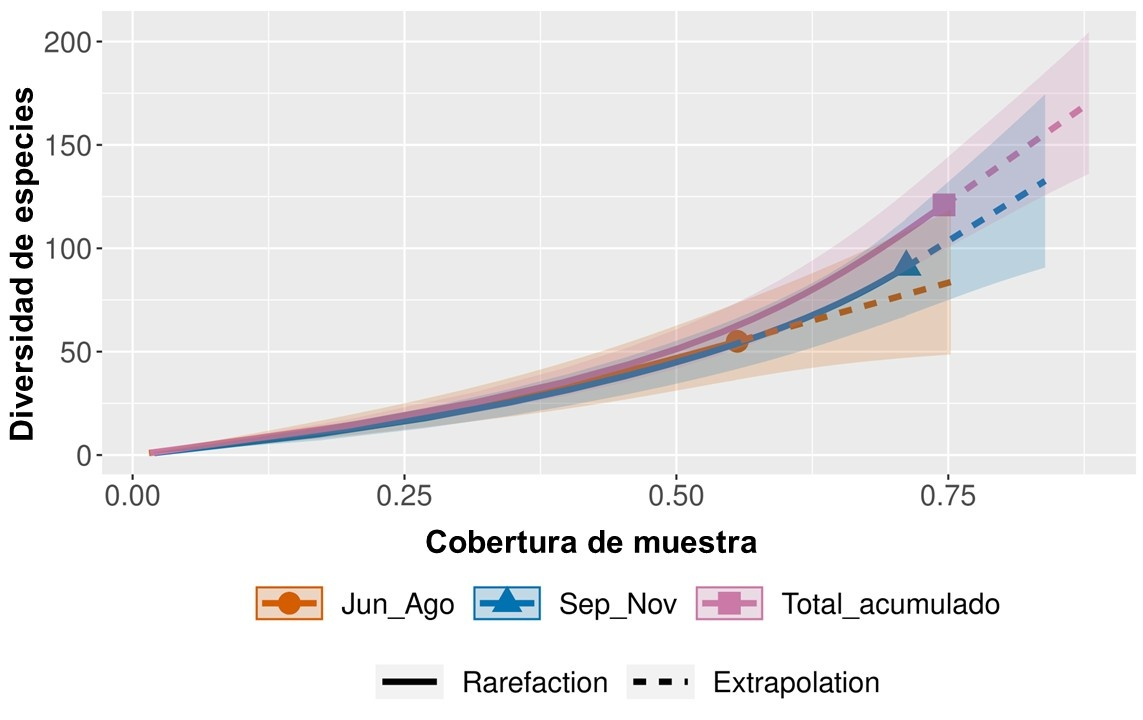
Figura 6 Curvas de acumulación de especies observadas en un fragmento de vegetación de selva mediana subperennifolia en el trópico subhúmedo.
Datos microambientales. Se registraron datos ambientales como la temperatura y humedad relativa, así como del suelo, en donde el mes que registró el punto más alto de temperatura ambiental fue agosto con 34.7 °C, seguido de junio con 34.5 °C, julio y septiembre reportaron 34.4 °C como su temperatura máxima, mientras octubre y noviembre presentaron una temperatura de 33.3 °C y 31.1 °C respectivamente (Figura 7A). También se obtuvieron los promedios de precipitación por mes, en el que junio presentó menos lluvia con 97.7 mm, seguido de octubre y julio con 103.3 mm y 109.5 mm respectivamente, los meses con un promedio de precipitación más alto se registraron para noviembre con 159.1 mm, septiembre con 136 mm y agosto con 114.1 mm (Figura 7A).
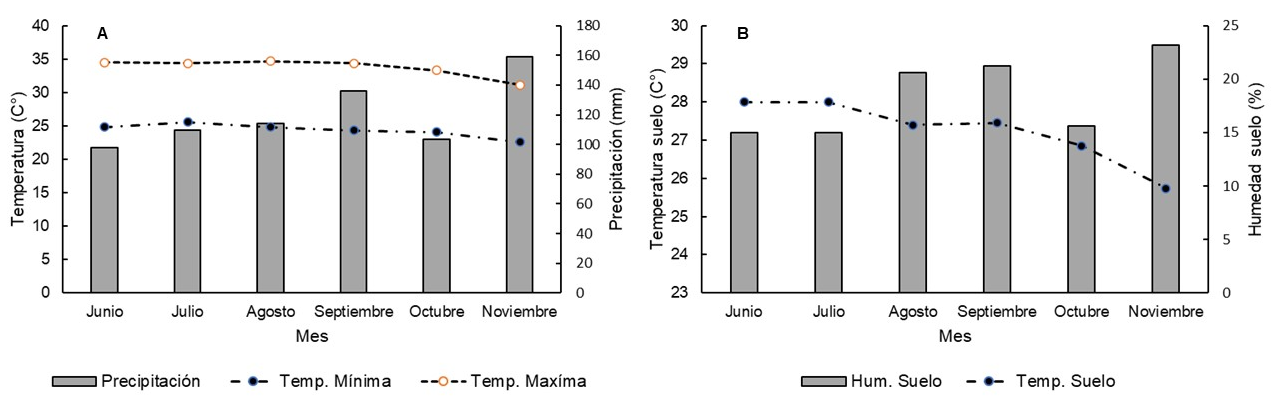
Figura 7 A) Temperatura y humedad ambiental; B) Temperatura y humedad del suelo en un fragmento de vegetación de selva mediana subperennifolia en el trópico subhúmedo.
En relación a la temperatura del suelo, los datos más altos se presentaron durante los meses de junio y julio con 28 °C, mientras que noviembre tuvo la temperatura más baja con 25.74 °C. El porcentaje más bajo de humedad del suelo se presentó en los meses de junio, julio y octubre con 15 y 15.62 %, mientras el mes con mayor porcentaje de humedad fue noviembre con 23.18 % (Figura 7B).
Las correlaciones de Spearman mostraron que algunas especies como Clathrus ruber y Steccherinum nitidum presentan una correlación positiva moderada con la temperatura del suelo (r s = 0.53) para ambas especies, mientras que con la misma variable especies como Xylocoremium sp. (r s = -0.66) y Thelephora aff. versatilis (r s = -0.70), presentan una fuerte correlación negativa, lo que sugiere que estas especies se ven afectadas por las temperaturas. Variables como la humedad del suelo presenta a especies como Schizophyllum commune (r s = 0.85) y Favolus tenuiculus (r s = 0.84) con una correlación fuerte positiva. La precipitación presenta una alta correlación acumulada entre las variables ambientales y las especies de macrohongos (r s = 0.8406, P = 0.036).
La abundancia y riqueza de macrohongos estudiados se relacionaron positivamente con el incremento de la humedad del suelo y una ligera disminución de la temperatura. El primer periodo mostró un porcentaje promedio de humedad del 16 %, el cual es menor al 20 % de humedad promedio del segundo periodo. La temperatura disminuyó durante octubre y noviembre con respecto a los meses anteriores.
El análisis NMDS reveló que los meses de julio y octubre tienen valores similares en la composición de las especies de macrohongos, lo que sugiere una relación con las condiciones ambientales registradas en esos meses, así mismo sucede en los meses de agosto y septiembre. Mientras tanto, junio y noviembre, mostraron ser los meses más disímiles coincidiendo con los extremos del gradiente de temperatura y humedad. Estos resultados sugieren, que las condiciones abióticas como la temperatura y la humedad son determinantes en la composición de las comunidades de macrohongos (Figura 8).
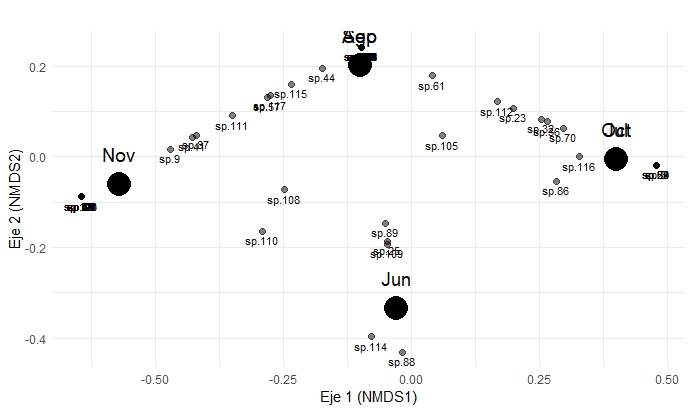
Figura 8 Análisis de escalamiento multidimensional no métrico (NMDS) para la complementariedad de las especies de macrohongos entre los meses de junio (Jun), julio (Jul), agosto (Ago), septiembre (Sep), octubre (Oct) y noviembre (Nov). “sp.1, sp2, sp.3, sp.n…” corresponden a las especies recolectadas en un fragmento de vegetación de selva mediana subperennifolia en el trópico subhúmedo.
El modelo CCA muestra como la mayoría de las especies se acumuló cerca de las variables temperatura ambiental, temperatura del suelo, área basal, diámetro del árbol y riqueza arbórea, el CCA1 (valor propio = 0.5027) y el CCA2 (valor propio = 0.4729), mientras las variables humedad del ambiente, humedad del suelo y precipitación se alejan, aunque ciertas especies se acercan más a estas variables. El eje 1 representa el 18.22 % y el eje 2 el 35.36 %, que en conjunto explican el 53.58 % de la varianza total (Figura 9).
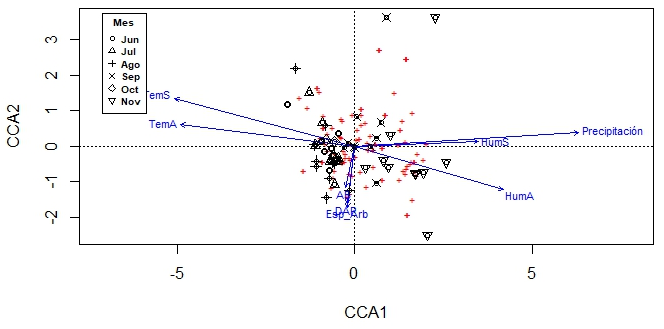
Figura 9 Análisis de correspondencia canónica (CCA) de las variables ambientales y las especies de macrohongos colectadas durante junio (Jun), julio (Jul), agosto (Ago), septiembre (Sep), octubre (Oct) y noviembre (Nov). Los vectores corresponden a las variables explicativas TemS (Temperatura del suelo), TemA (Temperatura del ambiente), AB (Área basal), Esp. Arb (Especies arbóreas), DAP (Diámetro a la altura del pecho), HumS (Humedad del suelo), HumA (Humedad del ambiente) y Precipitación.
Discusión
En Quintana Roo, se han registrado 401 especies de macrohongos (de la Fuente et al. 2020), mientras que en nuestro estudio se documentan 118 taxones (Material suplementario Tabla S1), lo que representa aproximadamente el 30 % de la diversidad reportada para el estado. Esta diversidad es considerable en comparación con el estudio previo en la región, como el de Guzmán (1983), quien reportó 150 especies.
Se reportan especies como Steccherinum nitidum, Schizophyllum commune y Favolus tenuiculus (Material suplementario, Figura S2 y Figura S3) que son lignícolas. Sus correlaciones significativas con variables del suelo pueden explicarse por la relación indirecta entre las condiciones microclimaticas del suelo y los sustratos leñosos en selvas tropicales. Estudios en ecosistemas similares han demostrado que la humedad del suelo influye en la disponibilidad de agua para la madera en contacto con él, especialmente en etapas avanzadas de descomposición (Osono 2014, Bässler et al. 2022). Además, la temperatura del suelo puede reflejar condiciones térmicas generales que afectan la actividad enzimática de hongos lignícolas, incluso en sustratos no enterrados (Wu et al. 2022), estos hallazgos subrayan la importancia de considerar las variables ambientales indirectas en estudios fenológicos de macrohongos.
Los valores obtenidos mediante los índices de diversidad verdadera (q = 2) y de Shannon en nuestro estudio reflejan una alta diversidad de macrohongos, lo cual es consistente con lo reportado en otras selvas tropicales. Por ejemplo, los estudios por Mohd-Nordin et al. (2024) y Gogoi et al. (2024) reportaron un índice de Shannon 2.103 y 3.54 respectivamente, lo que indica una alta diversidad en estos ecosistemas. En contraste, en bosques templados, como el estudio de Ruiz-Almenara et al. (2019) presenta un índice de Shannon de 1.54 lo que representa una diversidad moderada. Estas diferencias respaldan la idea de que las selvas tropicales albergan una mayor diversidad de macrohongos, y a pesar de esto, los bosques templados concentran el mayor número de estudios sobre este grupo de organismos (Lodge & Cantrell 1995).
Las familias de macrohongos más representativas en nuestro estudio fueron Agaricaceae (21), Polyporaceae (19), Marasmiaceae (16) y Xylariaceae (8). Estos hallazgos coinciden con estudios realizados en la Península de Yucatán (Guzmán 1995) y en otras selvas tropicales (Tibuhwa 2011, Li et al. 2018, Alem et al. 2021, Putra et al. 2023). La dominancia de Polyporaceae resalta su rol como descomponedores primarios de madera, favorecida por la abundancia de sustratos leñosos en selvas tropicales, que proveen nichos diversificados (Adarsh et al. 2015), y su capacidad de degradar eficientemente lignina/celulosa bajo condiciones de alta humedad y temperatura (Zhao et al. 2024). Esta familia muestra además una notable plasticidad ecológica, permitiéndole colonizar madera en descomposición como tejidos vegetales vivos (Wu et al. 2022). Esta familia también presenta, en la mayoría de sus especies, hifas esqueléticas, las cuales son muy resistentes en bajos porcentajes de humedad, tardan en descomponerse y algunas especies son perennes (Halme et al. 2009).
La co-ocurrencia de las familias Agaricaceae y Marasmiaceae sugiere una partición de recursos, es decir, mientras que la familia Polyporaceae coloniza troncos en descomposición, estas familias prosperan en la hojarasca y materia orgánica superficial como lo reportan otros estudios en selvas tropicales (Putra et al. 2023).
La menor riqueza de especies de la familia Xylariaceae, en otros estudios tropicales (Alem et al. 2021) podría deberse a diferencias en la disponibilidad de sustratos en descomposición avanzada, lo que es crítico para este grupo (Tibuhwa 2011), o bien, a variaciones microclimaticas locales que afectan su establecimiento. Estos patrones resaltan cómo la disponibilidad de sustratos y la especialización funcional estructuran las comunidades de macrohongos en selvas tropicales.
La investigación sobre la fenología de los macrohongos en el trópico es aún limitada. Sin embargo, estudios recientes como el de Krah et al. (2023), quienes analizaron 6.1 millones registros de macrohongos en la base de datos de la Biodiversidad Global (GBIF), sugieren que no hay un patrón específico de fructificación de macrohongos en los trópicos.
En nuestro estudio, observamos que la abundancia y riqueza de las distintas familias de macrohongos aumentaron cuando la humedad del suelo superó el 20 % y la humedad relativa fue superior al 88.5 %, esto coincide con los trabajos que realizaron Shuhada et al. (2020) y Pérez-Rosas et al. (2022), donde el aumento de esporomas ocurre cuando la humedad ambiental es superior al 80 %. Estos trabajos no mencionan el porcentaje de humedad del suelo; sin embargo, en este estudio, observamos que cuando los porcentajes de humedad ambiental eran mayores a 80 %, en el suelo se presentaban porcentajes mayores del 20 %, por lo que podría ser una variable importante a tomar en cuenta en futuros estudios.
Estudios en bosques templados han documentado que las familias Boletaceae, Cantharellaceae, Russulaceae y Tricholomataceae, presentan preferencias marcadas para formar esporomas en ambientes con humedad del suelo superior al 25 % (Haq 2020, Ponce et al. 2022). En selvas tropicales, este patrón se modifica, las familias Marasmiaceae, Mycenaceae, Polyporaceae y Tricholomataceae que forman esporomas, predominan cuando la humedad del suelo supera el 20 % y la humedad relativa ambiental es alta (> 88 %) (Lodge et al. 2004). Sin embargo, como demuestra Pinna et al. (2010) en bosques boreales, existe un umbral crítico donde el exceso de humedad en el suelo puede tener un efecto limitante en la formación de esporomas de los macrohongos, con lo cual la riqueza y abundancia podría disminuir.
El mayor número de esporomas se registró en septiembre y noviembre, meses en los que se registró la mayor humedad del suelo, estos resultados concuerdan con estudios previos que indican que la humedad del suelo es un factor crucial para los esporomas en ambientes tropicales (Salerni et al. 2002, Yang et al. 2012). Nuestros resultados robustecen la idea de que el cambio climático, al influir en los patrones de precipitación y temperatura, podría impactar negativamente en la biodiversidad fúngica, como sugiere Krah et al. (2023).
Además del cambio climático, la deforestación y el cambio de uso de suelo en Quintana Roo constituyen una amenaza adicional para la diversidad de macrohongos. En este estado, más de 115 mil hectáreas se destinan para actividades agrícolas y pecuarias, con una pérdida anual de selva de aproximadamente 5,904 hectáreas por agricultura, 4,900 por la ganadería y 1,882 por el sector turístico (CONAFOR 2020). Esto ha propiciado un aumento constante en la deforestación y el cambio de uso del suelo provocando la pérdida de especies vegetales y fúngicas (CONAFOR 2009, 2020). El hecho de que la temperatura tenga una relación negativa con algunas especies como Leucopaxillus gracillimus, Marasmius elegans, Marasmius fulvoferrugineus, Pluteus oligocystis y Thelephora aff. versatilis (Figura S2 y Figura S3), también sugiere que estas podrían ser vulnerables a los incrementos futuros en la temperatura (Sato et al. 2012, Krah et al. 2023). Aunque, la humedad también se ha destacado como un factor clave en la aparición de macrohongos (Straatsma et al. 2001, Salerni et al. 2002, Osono 2014).
En nuestro estudio, comparamos los dos meses con mayor riqueza de familias, (septiembre y noviembre); donde se registraron 18 y 17 familias respectivamente, sin embargo, la abundancia en cada una de ellas varió. En el caso de, la familia Agaricaceae, en el mes de septiembre se recolectaron cinco esporomas de cinco taxones, mientras que en noviembre se recolectaron 13 esporomas de ocho taxones, esto se debe a que muchas de las especies dentro de esta familia tienen requerimientos altos de humedad (Amandeep 2015, Robinson et al. 2019).
Otras familias también mostraron comportamientos distintos en cuanto a su abundancia y riqueza de especies; de la familia Geastraceae se registraron 20 esporomas y tres taxones en septiembre, mientras que en noviembre solo se recolectó un esporoma. De la familia Marasmiaceae fueron registradas 27 esporomas y ocho especies en septiembre, pero solo 10 esporomas de seis especies en noviembre.
Entre las familias más abundantes identificadas en este estudio, varios géneros son reconocidos por su potencial alimenticio. En la familia Agaricaceae, el género Agaricus incluye especies comestibles como Agaricus bisporus, ampliamente cultivado para el consumo humano (Wasser 2002). La familia Marasmiaceae incluye el género Lentinula, destacando Lentinula edodes, valorado en la gastronomía asiática (Hibbett et al. 2007). En la familia Polyporaceae, géneros como Pleurotus son recolectados tradicionalmente por comunidades locales (Boa 2004).
Estudios en bosques templados han documentado que el aumento de la temperatura y humedad puede retrasar las temporadas de los esporomas, especialmente en bosques caducifolios de haya (Fagus sylvatica), bosques boreales alpinos y bosques mixtos de coníferas, lo que a su vez aumentan su riqueza y abundancia (Gange et al. 2007, Büntgen et al. 2013, Bässler et al. 2022). No obstante, Li et al. (2018) sugieren que en las selvas tropicales, tanto la temperatura como la precipitación influyen en prolongar el periodo de los esporomas.
Aunque los datos de nuestro estudio, señalan que únicamente se presenta correlación significativa con la precipitación, algunas especies, Leucopaxillus gracillimus, Marasmius elegans, Marasmius fulvoferrugineus, Pluteus oligocystis y Thelephora aff. versatilis, presentan correlaciones negativas con la temperatura, por lo que disminuyen su riqueza y su abundancia, estos resultados son similares a estudios en Oaxaca (Ruiz-Almenara et al. 2019, Pérez-Rosas et al. 2022), donde del mismo modo, las variables humedad absoluta y relativa del suelo presentan una correlación positiva con ciertas especies (Auricularia aff. cornea, Cookeina speciosa, Cookeina sulcipes, Cotylidia aurantiaca, Geastrum campestre, Geastrum spegazzinianum) (Figura S1 y Figura S3), lo que sugiere que no todos los conjuntos responden de la misma forma a las condiciones ambientales o bien, estas especies se relacionan con algún otro factor que no es la humedad.
Se ha demostrado que la humedad y la temperatura son de los principales factores que influyen en producción de esporomas. Sin embargo, estudios recientes como el de Villarruel-Ordaz et al. (2024) en bosques tropicales caducifolios revelan que factores topográficos como la altitud, orientación y pendiente del terreno pueden explicar hasta 62 % de la variación en la distribución de macrohongos, superando en algunos casos la influencia de las variables climáticas locales. Otros estudios señalan que grupos específicos de macrohongos como los saprótrofos-lignícolas se asocian significativamente con laderas norte de pendiente pronunciada (> 15) donde se acumula mayor cantidad de madera muerta, mientras que los hongos ectomicorrícicos predominan en altitudes medias (800-1,200 m snm) asociados a bosques de Quercus. Estos hallazgos coinciden con nuestros resultados y refuerzan la evidencia de que, además de las condiciones microclimaticas se requieren de otras condiciones ambientales. Entre estos factores adicionales, la altitud, las características topográficas influye de manera significativa en la composición de especies de la comunidad de macrohongos. Así mismo, los recursos del sitio como lo son, el tamaño y la cantidad de madera muerta, la diversidad de especies arbóreas y las condiciones físico-químicas del suelo, impactan de manera significativa en la riqueza de especies, así como en su abundancia (He et al. 2017, Olou et al. 2019, Adamo et al. 2021, Tomao et al. 2020). Particularmente en ecosistemas tropicales, estos resultados destacan la necesidad de investigar más a fondo, los distintos factores que influyen en la riqueza y abundancias de las comunidades de los distintos grupos funcionales de los macrohongos.
Comprender las condiciones bióticas o abióticas que influyen en las comunidades de macrohongos en las selvas tropicales, ayudaría a gestionar los recursos forestales de estas selvas, comprender sus ciclos biogeoquímicos, fenológicos y nutricionales y qué meses son los más productivos de estos organismos, además que son un recurso forestal no maderable de alto valor ecológico y económico (Ruiz-Almenara et al. 2019, Adamo et al. 2021).
Aunque estudios clásicos como Lodge & Cantrell (1995), recomiendan series temporales de 5 a 10 años para evaluar completamente la dinámica fúngica interanual realizando mediciones continuas de parámetros clave como la producción de esporomas, diversidad y condiciones ambientales asociadas como la temperatura, humedad y disponibilidad de sustrato, investigaciones recientes demuestran que diseños estacionales rigurosos pueden generar datos robustos y capturar patrones fenológicos fundamentales, si estos se enfocan en ventanas de máxima productividad fúngica por ejemplo Pérez-Rosas et al. (2022), quienes registraron > 70 % de la riqueza anual de macrohongos en bosques templados durante una sola temporada de lluvias, se estandarizan y se vinculan los meta-análisis con la información existente para el ecosistema (Niskanen et al. 2023).
Nuestro estudio utilizó este enfoque y nos centramos en la temporada de producción de esporomas óptima reportado para selvas tropicales (Lodge et al. 2004), lo que nos permitió identificar patrones fenológicos fundamentales y establecer correlaciones ambientales iniciales, reconociendo explícitamente que estos hallazgos representan la base para futuros monitoreos multi-anuales que capturen la variabilidad interanual que permitan validar estos patrones a largo plazo.
En conclusión, este estudio proporciona información sobre la diversidad y fenología de los macrohongos en un fragmento de selva mediana, registrando 118 taxones, esto representa la cuarta parte de la diversidad conocida del estado, por lo que subraya el potencial para encontrar más diversidad y registrar más especies en la región. Los hallazgos y el análisis fenológico indican que la humedad relativa y la humedad del suelo es clave para la formación de los esporomas, ya que la mayor riqueza de macrohongos ocurre en los meses más húmedos, sugiriendo que es esencial, mientras que la temperatura también influye en el desarrollo de algunas especies, mostrando correlaciones positivas y negativas. Las familias Agaricaceae, Polyporaceae, Marasmiaceae y Xylariaceae son las más representativas, aunque su abundancia varía a lo largo del tiempo, reflejando el impacto de condiciones ambientales como la humedad relativa. Los resultados de los factores ambientales como temperatura y humedad resaltan la importancia de considerar el cambio climático en la conservación de ecosistemas tropicales y la necesidad de monitoreo a largo plazo para desarrollar estrategias de mitigación.
Material suplementario
El material suplementario de este trabajo puede ser consultado aquí: https://doi.org/10.17129/botsci.3760.











 nueva página del texto (beta)
nueva página del texto (beta)



