Introducción
La manía de aparición tardía se define por manifestarse entre los 60 y 65 años, o incluso en una edad más avanzada.1,2 Se estima que afecta entre 0.5 y 1% de los adultos mayores, y que 10% de los casos están asociados con cambios vasculares u otras patologías cerebrales, dentro de las cuales son relevantes los síndromes paraneoplásicos en el contexto de pacientes con neoplasias. Por otra parte, los síntomas maniaco-psicóticos suelen ser menos frecuentes que los episodios depresivos.1
La encefalitis mediada por anticuerpos es la tercera causa más frecuente de encefalitis.3 Esta patología no se presenta con mecanismos fisiopatológicos homogéneos,2 ya que en algunos casos los anticuerpos se unen a epítopes extracelulares de superficie generando una disfunción neuronal reversible, mientras que, en otros, como los generados en síndromes paraneoplásicos, se unen a epítopes intracelulares. En este escenario, los anticuerpos pueden no ser directamente etiopatogénicos.3 Por ende, es posible que la pérdida neuronal juegue un papel fundamental en la presentación sindromática de estos casos.
Los síndromes neurológicos paraneoplásicos se caracterizan por efectos remotos de neoplasias primarias debidos a mecanismos inmunomediados que producen daño directo al tejido nervioso, ya sea central o periférico, sin llegar a invadirlo.4 No obstante, ha habido un avance en su diagnóstico, puesto que actualmente no solo se considera la identificación de anticuerpos onconeuronales,5 y se ha optado por una clasificación de fenotipos según el riesgo de asociarse a un cáncer, dividiéndolos en fenotipos de riesgo alto e intermedio. Asimismo, se requiere de la exclusión de causas más prevalentes, como enfermedades neurodegenerativas y alteraciones tóxicas o metabólicas.5 Por último, el diagnóstico se realiza según tres niveles de certeza, de acuerdo con los hallazgos obtenidos por medio del PNS-Care Score.5 Este también depende de otros criterios para establecer la probabilidad de encefalitis autoinmune6,7 o psicosis autoinmune,8 y así mejorar los valores predictivos. Sin embargo, se ha cuestionado el valor clínico de estos criterios en contextos donde existe una presentación puramente psiquiátrica,9 los cuales representan aproximadamente un 4% de los casos.10
La ausencia de alteraciones en el líquido cefalorraquídeo no excluye el diagnóstico. Al respecto, 60% de pacientes con alteraciones a nivel del sistema nervioso central presenta títulos de anticuerpos,4 y no todos tienen la misma sensibilidad o especificidad. Existen anticuerpos bien caracterizados en el contexto de síndromes paraneoplásicos, los cuales aumentan la sospecha diagnóstica de esta entidad, incluso si no hay indicios de la neoplasia primaria.4
La ausencia de anticuerpos puede significar la presencia de nuevos anticuerpos frente a epítopes todavía no identificados, o una respuesta mediada por células T.11 A su vez, esto se asocia a otras alteraciones paraclínicas: 58-71.8% está relacionado con pleocitosis; 9.4%, con bandas oligoclonales positivas; 31.6%, con un aumento en el índice de IgG en el líquido cefalorraquídeo, y 83% con alteraciones en el trazado del electroencefalograma.11,12 Se considera que la prevalencia e incidencia de este grupo seronegativo son similares a aquellas de los casos con anticuerpos positivos,11,12 esto es, que representan de 7 a 11% de los casos de encefalitis autoinmune.13Dada la heterogeneidad de este grupo no existe un claro panorama a nivel pronóstico,12 el cual puede empeorar debido a los mecanismos fisiopatológicos que involucran procesos citotóxicos, que a su vez pueden interrelacionarse con otros procesos, como el envejecimiento, generando una regulación alterada de la microglía que amplifique la respuesta inflamatoria.12 Por otra parte, las recaídas se asocian generalmente a un tratamiento inmunológico insuficiente o a un retiro temprano de la terapia inmune,14 y la resolución espontánea es rara.
Para los casos con presencia de anticuerpos onconeuronales no hay evidencia de alta calidad que guíe las decisiones terapéuticas, sin embargo, se ha reportado que el tratamiento de la neoplasia subyacente previene la progresión de los síntomas neurológicos y puede incluso mejorarlos. En casos donde los anticuerpos onconeuronales y el síndrome son altamente específicos, existe evidencia en la literatura que apoya la realización de tratamientos oncológicos empíricos.4
Finalmente, no existe evidencia confiable que recomiende el uso de tratamiento inmunosupresor, el cual tiene una pobre tasa de respuesta, ni la estimulación del crecimiento tumoral.4
Presentación del caso
Presentamos el caso de una mujer caucásica de 75 años con antecedente de timoma con compromiso pleural en esquema de quimioterapia paliativa. La paciente consultó por un cuadro de un mes de evolución de ánimo triste y discurso incoherente con ansiedad flotante y desorientación en espacios públicos, sin ideación delirante. Debido a esto, se consideró que cursaba un episodio depresivo con síntomas ansiosos. Se inició manejo con escitalopram 10 mg y alprazolam 0.5 mg, ambos en dosis diarias. Dos semanas después del inicio del tratamiento, la paciente se tornó irritable y por momentos presentó afecto eufórico asociado a labilidad afectiva. Posteriormente, asistió a un control ambulatorio, en el cual se sospechó la presencia de un trastorno neurocognitivo mayor, por lo que se suspendió el alprazolam y se aumentó la dosis de escitalopram en conjunto con quetiapina (20 mg al día y 25 mg al día, respectivamente). Quince días después, la paciente acudió nuevamente a urgencias debido a una exacerbación de los síntomas afectivos, presentando logorrea, hipertimia, actitud seductora, hiperprosexia e ideas delirantes megalomaníacas.
Como antecedentes patológicos, la paciente presentó hipertensión arterial, hipotiroidismo y SAHOS, en manejo con levotiroxina, valsartán y amlodipino. En el examen físico y neurológico general, hubo hallazgos positivos de disprosexia, apraxia ideomotora bilateral y conductas perseverantes. A su vez, en el examen mental de ingreso, la paciente mostró actitud hiperfamiliar e intrusiva, logorrea, hiperprosexia, afecto exaltado, taquipsiquia, asociación laxa de ideas, e ideas delirantes megalomaníacas, con marcada inquietud motora.
En los análisis paraclínicos, se solicitó perfil tiroideo (TSH 0.19 mUI/L, T4 libre 1.4 nmol/L, T3 libre 3.27 nmol/L), que reveló anticuerpos antitiroideos tiroglobulínicos positivos (301.36 UI/mL). En el análisis del líquido cefalorraquídeo (LCR) se encontró hiperproteinorraquia acelular con bandas oligoclonales positivas, sin identificación de anticuerpos (test inmunoblot EUROLINE para síndrome paraneoplásico amfifisina, CV2, PNMA2, Ri, Yo, Hu, Recoverina, SOX1, Titina, Zic4, GAD65 y test de inmunofluorescencia indirecta en células HEK293 NMDA, AMPA 1 y 2, GABA B1/B2, LGI2CASPR2, DPPX). La resonancia magnética con gadolinio no mostró lesiones intracraneales sugestivas de procesos neoplásicos secundarios (Figura 1), así como la telemetría, que no presentó trazos anormales.
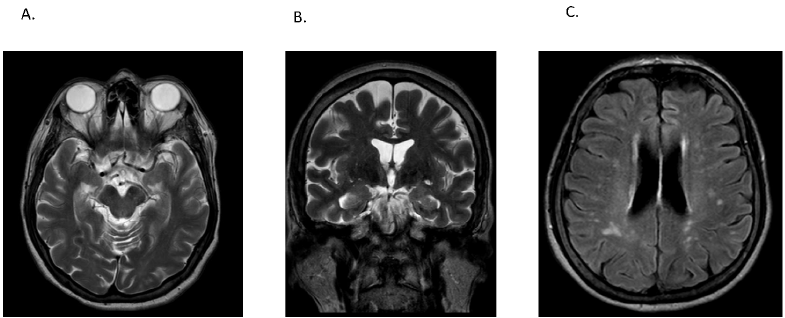
Figura 1 Resonancia magnética cerebral. A) Corte axial en T2 sin evidencia de hiperintensidades a nivel temporal y sin alteraciones volumétricas apreciables. B) Corte coronal en T2 sin evidencia de hiperintensidades a nivel temporal. C) Corte axial en FLAIR con evidencia de múltiples hiperintensidades en sustancia blanca de predominio posterior Fazekas I.
Se concluyó que la paciente cursaba un primer episodio de manía de aparición tardía con un puntaje de 35 en la escala de Young para la evaluación de la manía, en el contexto de una enfermedad neoplásica de base. Como primera posibilidad diagnóstica se consideró un síndrome paraneoplásico fenotipo de riesgo intermedio (Tabla 1). Por ende, se indicó manejo con metilprednisolona, 1 gr diario por 5 días, e inmunoglobulina en dosis de 0.4 gr/kg/día por 5 días.
Tabla 1 Diagnósticos diferenciales según diversos criterios5,7,8
| Presentes | Ausentes | |
|---|---|---|
| Encefalitis autoinmune posible (debe cumplir los tres criterios) | Progresión rápida (menos de 3 meses) de
síntomas psiquiátricos. Al menos una de las siguientes: pleocitosis (conteo de leucocitos > 5 cél/mm3), focalización SNC de novo, convulsiones de novo, alteraciones en RMN sugestivas de encefalitis. Exclusión razonable de causas alternativas. |
Ausencia de anticuerpos específicos en suero y
LCR, y al menos dos de los siguientes: -Anormalidades en RMN sugestivas de encefalitis autoinmune. -Biopsia cerebral que evidencie infiltrados inflamatorios y excluya otros síndromes. |
| Encefalitis autoinmune probable (anticuerpos negativos) | Progresión rápida (menos de 3 meses) de
síntomas psiquiátricos. Ausencia de anticuerpos específicos en suero y LCR. Pleocitosis, bandas oligoclonales o aumento índice IgG en LCR. Exclusión de otros tipos de encefalitis autoinmunes bien definidos. |
Al menos uno de los siguientes: -Trastorno del movimiento (catatonía o disquinesia). -Respuesta adversa a antipsicóticos, sospecha de síndrome neuroléptico maligno. -Disfunción cognitiva severa o desproporcionada. -Disminución del estado de consciencia. -Convulsiones de novo. Disautonomía clínicamente significativa. |
| Encefalitis de Hashimoto | RMN normal o con anormalidades no específicas.
Anticuerpos antitiroideos positivos. Ausencia de anticuerpos neuronales específicos en suero y LCR. |
Enfermedad tiroidea subclínica o leve
(usualmente hipotiroidismo). Encefalopatía con convulsiones/mioclonos/ alucinaciones/episodios similares a ACV. Exclusión razonable de otras causas alternativas. |
| PNS Care Score: 6 puntos (fenotipo de riesgo intermedio 2 y presencia de cáncer 4) | Síndrome neurológico paraneoplásico probable. |
Asimismo, se suspendió el manejo con escitalopram y quetiapina, y se inició la administración de ácido valproico, 750 mg al día, y olanzapina, 5 mg al día, cuyas dosis aumentaron a 1000 mg al día y 25 mg al día, respectivamente, para el control de síntomas maniformes. Secundario al tratamiento con corticoides, se evidenció exacerbación de la sintomatología afectiva, con aumento a 38 puntos en la escala de Young, lo cual presentó mejoría al terminar dicho manejo sin ajustes psicofarmacológicos. Teniendo en cuenta la adecuada evolución clínica y la mejoría de los síntomas se indica egreso hospitalario con mantenimiento de ácido valproico, 1000 mg al día, y olanzapina, 20 mg al día. La paciente egreso con puntaje de 11 en la escala de Young. Durante la hospitalización no se realizaron pruebas neurocognitivas.
Desde el egreso, la paciente presentó una resolución de los síntomas afectivos y psicóticos. Se realizó una disminución progresiva de la dosis de olanzapina a 5 mg diarios por somnolencia. Adicionalmente, en el seguimiento ambulatorio se realizó la evaluación cognitiva de Montreal (MoCA), en la cual la paciente obtuvo un puntaje de 23/30, con presencia de fallas en memoria de trabajo y funciones ejecutivas que no comprometen las actividades básicas de la vida diaria. Discusión
Este caso muestra la aparición de un cuadro maníaco con síntomas psicóticos de inicio tardío en una paciente con proceso neoplásico irresecable en manejo paliativo y antidepresivo, sin inicio de quimioterapia y sin invasión cerebral. Esta paciente no presentaba antecedentes personales ni familiares de trastornos afectivos. Como parte del proceso diagnóstico, se consideró de baja probabilidad que este episodio fuera parte de un trastorno mental primario, por lo que se buscaron causas secundarias,2 en particular, neurológicas, debido a la evidencia de alta correlación con afecciones de este tipo en el grupo etario de la paciente.1 Dentro de la evaluación diagnóstica se descartó que la paciente estuviese en delirium y que tuviera alteraciones metabólicas, tóxicas o déficits de vitaminas como posibles causas del cuadro. Adicionalmente, se descartó un compromiso metastásico cerebral o procesos infecciosos primarios a nivel cerebral. También se revisaron los medicamentos tomados por la paciente previamente, y se planteó la posibilidad que el manejo antidepresivo fuese un factor contribuyente en el viraje, puesto que la manía inducida por antidepresivos representa un riesgo latente. Sin embargo, no existe mucha evidencia de que esto se presente en etapas tardías de la vida, y se considera que las edades tempranas son las que se encuentran en mayor riesgo de viraje,15 además
de que dicho riesgo depende del antidepresivo utilizado.16Asimismo, dados los hallazgos en el análisis neurológico y del LCR se consideró que la paciente cursaba concomitantemente un proceso autoinmune (encefalitis autoinmune posible). En un nivel neuroimagenológico, se evidenciaron hiperintensidades de predominio occipital, sin la presencia de procesos agudos o subagudos concomitantes. Debido a esto, se contempló la posibilidad de una manía vascular.17 No obstante, existen limitaciones en el uso clínico de este concepto debido a la poca disponibilidad de reportes de caso, los cuales no siempre presentan una relación entre el desarrollo de síntomas neurológicos y los síntomas maniformes, y tampoco criterios uniformes sobre qué considerar como lesiones significativas. Debido a que la paciente tenía lesiones caracterizadas como Fazekas I, y dada la posibilidad de factores de confusión debido a la asociación entre factores de riesgo cardiovascular, la manía de inicio tardío18 y las hiperintensidades de sustancia blanca, no específicas del síndrome maníaco,17 esto no se consideró como un factor etiológico sino de vulnerabilidad.
Por otro lado, se evidenció la presencia de anticuerpos antitiroglobulina positivos, lo cual planteó la posibilidad de una encefalopatía de Hashimoto, la cual implica dificultades al momento del diagnóstico, ya que su presentación clínica puede ser similar a otras encefalitis autoinmunes. Sin embargo, la paciente no cumplía con los criterios para dicha patología, la cual se presenta en 13% de la población sana.6
Debido a estos factores, la etiología inmunomediada continuó siendo una de las más probables.8 La paciente, al ser evaluada según el PNS-Care Score, alcanzó una clasificación de encefalitis posible con un fenotipo de riesgo intermedio (Tabla 1). Asimismo, presentó hallazgos sugestivos de inflamación a nivel del LCR. Una de las dificultades que implican estos criterios, es la necesidad del cumplimiento de encefalitis autoinmune sin considerar la psicosis autoinmune como parte de los criterios,5 así como las potenciales limitaciones en presentaciones puramente psiquiátricalls.9 Por otro lado, hubo dificultades en el tratamiento, ya que debió haber incluido la resección de la neoplasia y el manejo con quimioterapia, los cuales, por las características del compromiso, no fueron realizadas.
Conclusiones
La manía de inicio tardío supone un desafío para el clínico debido a su alta asociación con comorbilidades de salud general, como los factores de riesgo cardiovascular y enfermedades neurológicas, así como su presentación heterogénea dentro de un espectro clínico con múltiples posibilidades etiológicas. Dichos desafíos se acrecientan en el contexto de un proceso neoplásico concomitante. Debido a la edad de inicio y el curso subagudo, sin antecedentes significativos de vulnerabilidad, la búsqueda de causas secundarias es central en este caso. No obstante, la determinación del agente etiológico fue obstaculizado debido a los múltiples factores que interactúan a nivel central para asignar el fenotipo. Como primer diagnóstico de trabajo se presenta una etiología inmunomediada, en la cual la ausencia de anticuerpos podría ser un reflejo del desconocimiento de los mecanismos fisiopatológicos subyacentes, y conducir a la infraestimación de este tipo de casos.5 Esto plantea la importancia de continuar la descripción y estudio de este tipo de patologías, en las cuales predominan los síntomas psiquiátricos,19 sin presencia de convulsiones, con alteraciones en el examen neurológico no explicadas por la sintomatología psiquiátrica y sin evidencia en el momento de un proceso neurodegenerativo concomitante.
Financiación
Los autores no han recibido apoyo financiero para la investigación, autoría y/o publicación de este artículo.
Conflicto de intereses
Los autores del presente manuscrito no presentan conflictos de intereses que declarar.
Contribuciones de los autores
JC, AO y LM concibieron la idea general del informe. JC obtuvo el consentimiento de la familia del paciente. JC desarrolló los criterios de búsqueda para la revisión de la literatura, que fue realizada por JC, AO y LM. JC, AO y LM escribieron el borrador original, el cual fue editado por JC y RE. Todos los autores contribuyeron al artículo y aprobaron la versión sometida a evaluación.











 text new page (beta)
text new page (beta)



