Antecedentes
La esquizofrenia es una condición crónica que afecta a 1 % de la población a nivel mundial, es decir, hasta 1 de cada 300 personas la padece.1 Algunos reportes señalan que la tasa de incidencia de esta enfermedad se ha mantenido estable a lo largo del tiempo entre las distintas poblaciones, lo cual podría sugerir que afecta a los individuos de modo similar2 Sin embargo, durante la última década se ha observado que existe una variabilidad respecto a la incidencia y la prevalecía de esta condición.3 En este sentido, se han identificado factores que pueden aumentar el riesgo de desarrollar esquizofrenia, como son la genética y los antecedentes de complicaciones perinatales que alteren el adecuado desarrollo neurológico durante el periodo gestacional.4 Debido a que la sintomatología inicia por lo general en la adultez temprana, la esquizofrenia representa una carga económica y social significativa.4 Esta condición se considera uno de los trastornos psiquiátricos más graves, principalmente por las altas tasas de mortalidad de quienes la padecen; se estima que los pacientes con esquizofrenia tienen una esperanza de vida hasta 20 años menor que la población general.5,6,7Como síndrome clínico, la esquizofrenia se caracteriza por una amplia gama de signos y síntomas que se presentan de manera distinta en cada paciente. Se consideran síntomas positivos la presencia de alucinaciones, por lo general auditivas o visuales, e ideas delirantes, así como las alteraciones en el lenguaje y el comportamiento. Estos síntomas suelen ser los primeros en identificarse y el motivo por el cual se busca atención médica4 Existen otros síntomas, conocidos como negativos, que se manifiestan como pérdida de la motivación, del interés y retraimiento social, y suelen asociarse con un mal funcionamiento y disminución de la calidad de vida del paciente. Por lo general, estos síntomas presentan mala respuesta a los esquemas actuales de tratamiento y contribuyen a que exista un incremento en el riesgo de padecer enfermedades crónico degenerativas, como enfermedad cardiovascular y diabetes mellitus.5,6,7 Finalmente, los síntomas cognitivos constituyen alteraciones en la atención, la memoria de trabajo y las funciones ejecutivas.4
Con respecto a la etiología de esta condición, se sugiere que existe una hipofunción en los receptores de glutamato N-metilD-aspartato (NMDA), teoría sustentada principalmente por la evidencia en modelos animales, según los cuales, al administrar de manera aguda y crónica un antagonista de los receptores NMDA como el MK-801 (dizocilpina), se observan características conductuales que reproducen los signos de este padecimiento.8,9 Dentro de la fisiopatología de la esquizofrenia se han localizado áreas cerebrales fuertemente involucradas, como la corteza prefronatal (PFCx), responsable de procesos cognitivos complejos por medio de la interconexión de áreas corticales sensoriales y motoras y de estructuras subcorticales.10,11,12 La PFCx está formada principalmente por neuronas glutamatérgicas piramidales (75 a 80% del total de las células neuronales) e interneuronas gabaérgicas.7 Por otro lado, se ha reportado que el estrés oxidante juega un papel significativo en la fisiopatología de distintas enfermedades psiquiátricas, como la esquizofrenia y el trastorno afectivo bipolar.13,14 Este proceso origina alteraciones funcionales que pueden contribuir al desarrollo de una mayor propensión a las recaídas, una menor respuesta al tratamiento y un incremento en el decline funcional y cognitivo.15 El estrés oxidante se observa cuando existe un desbalance entre la producción de radicales libres (RL) y la capacidad de las defensas antioxidantes para contrarrestarlos. El exceso de RL produce alteraciones en la estructura molecular de los componentes celulares, provocando daño en proteínas, lípidos y el DNA.16,17,18 El daño por RL a los ácidos grasos poliinsaturados de las membranas celulares se denomina lipoperoxidación (LP). Existen defensas y moléculas antioxidantes como el glutatión reducido (GSH) -un tripéptido no protéico compuesto por los aminoácidos glutamato, cisteína y glicina21,16,17- que contribuyen al balance redox de la célula.19,20
Los fármacos antipsicóticos constituyen el tratamiento central para la esquizofrenia; su mecanismo de acción antipsicótico se debe a la regulación de los receptores D2 de dopamina a nivel estriatal.4,22,23 Es importante destacar que, pese a la disponibilidad de diversos fármacos, se ha reportado que entre el 20 y 30 % de los pacientes presentan falta de respuesta al tratamiento,24,25 por lo que el desarrollo de alternativas que resulten seguras y eficaces continúa siendo un reto.
La olanzapina (OLZ) es un fármaco antipsicótico atípico de segunda generación que posee un mejor perfil de tolerabilidad en comparación con antipsicóticos típicos como el haloperidol. La OLZ causa menos efectos extrapiramidales y menor efecto de sedación e hiperprolactinemia, no solo en dosis antipsicóticas moderadas sino también en dosis mayores. Además, se ha reportado una mejoría superior de los síntomas negativos con su uso en comparación con los antipsicóticos típicos.26,27 En un inicio, este fármaco fue aprobado para el tratamiento de pacientes con esquizofrenia y, posteriormente, para pacientes con trastorno afectivo bipolar y depresión resistente al tratamiento 28 Sin embargo, su uso como agente de primera línea se ve limitado en pacientes con alguna condición comórbida que aumente el riesgo metabólico, debido a que no solo se asocia de manera consistente con ganancia de peso, si no que implica un alto riesgo cardio metabólico al incrementar de manera importante los niveles de triglicéridos en ayunas y la resistencia a la insulina, lo que lleva al aumento en los niveles de glucosa en la sangre.29,26 De acuerdo con estudios realizados en modelos animales con MK-801, los antipsicóticos atípicos han mostrado ser superiores a los antipsicóticos típicos en la reversión del déficit cognitivo inducido por el bloqueo del receptor NMDA, ya que generan una mejoría en el aprendizaje espacial, el aprendizaje de reversión y la memoria de reconocimiento 30,31,32Específicamente, se observó que la OLZ revirtió de manera parcial dichos déficits cognitivos, así como la disminución de la expresión de las subunidades GluN1 y GluN2B fosforilado del receptor NMDA inducida por MK-801.33,34,35 Por otra parte, en un modelo in vitro realizado con células hipotalámicas de roedores, el uso de la OLZ se asoció con incremento del estrés oxidante. Debido a esto, una terapia combinada con un antioxidante podría representar una buena opción de tratamiento.36
La N-acetilcisteína (NAC) es un mucolítico aprobado clínicamente que, al ser un precursor del glutatión, puede atravesar la barrera hematoencefálica, y actúa como una molécula antioxidante disminuyendo los niveles de RL y restableciendo la depleción de GSH.17,37,38,39 Se ha demostrado que tiene un papel importante en distintos trastornos psiquiátricos, ya que interviene en la modulación de procesos como la neuro-inflamación, el estrés oxidante y la regulación de los sistemas de neurotransmisión de glutamato y dopamina.17,14,15,40,41 Por dicha evidencia y su buen perfil de seguridad, se ha considerado a la NAC como un agente adyuvante que potencializa la eficacia de antipsicóticos atípicos como la OLZ, y regula los procesos de oxidación y muerte celular tanto de la propia enfermedad como los relacionados con el uso prolongado de dosis altas de OLZ. Consecuentemente, el tratamiento combinado constituye una opción viable para pacientes con esquizofrenia o psicosis asociadas, en particular, aquellos con un curso crónico y poca respuesta a los actuales esquemas de tratamiento.17,42,43 Con base en esta información, el objetivo del presente estudio fue evaluar el efecto antioxidante de la terapia sola o en combinación (OLZ + NAC) en un modelo de esquizofrenia inducido por MK-801 en ratón.
Material y métodos
Animales
Se utilizaron 30 ratones albinos de la cepa CD1, machos adultos de 25 a 30 g, donados por el bioterio de la Universidad Autónoma Metropolitana Unidad Xochimilco, los cuales se mantuvieron en condiciones estándares de bioterio, con ciclos de luz-oscuridad 12:12, una temperatura de 22°C y acceso libre al agua y al alimento. Todos los procedimientos para el manejo de los animales fueron realizados de acuerdo con las guías regulatorias para el cuidado y uso de animales de laboratorio según la NOM-062-ZOO-1999. Asimismo, el protocolo fue registrado en el Instituto Nacional de Neurología y Neurocirugía Manuel Velasco Suarez con el número 38/20.
Diseño experimental y tratamiento farmacológico
Los animales fueron divididos en 5 grupos experimentales con las siguientes características:
Sano: animales intactos,
MK-801/Veh: se les administró tratamiento con solución salina al 0.9% (i. p.) cada 12 horas durante 14 días previos a la administración de MK-801 (dizocilpina) (0.25 mg/kg, i. p.), que es un antagonista de los receptores NMDA para inducir el modelo de esquizofrenia siguiendo la metodología de AquinoMiranda et al.,8
MK-801/OLZ: animales tratados con olanzapina (4 mg/kg, i. p.) cada 12 horas en dosis de 0.25 mg/kg (i.p.), según lo reportado por Reddy, et al.,35 durante 14 días previos a la administración de MK-801, para inducir efectos adversos por efecto de la OLZ, de acuerdo con lo reportado por Ng et al.,44
MK-801/NAC: ratones tratados con N-acetilcisteína (80 mg/kg, i. p.) cada 24 horas durante 14 días previos a la administración de MK-801 (0.25 mg/kg, i. p.),
MK-801/OLAZ+NAC: animales que recibieron el tratamiento con la combinación de olanzapina (4 mg/kg, i. p.) cada 12h horas y NAC (80 mg/kg, i. p.) cada 24 horas, durante 14 días previos a la administración de MK-801 (0.25 mg/kg, i. p.). 44
Determinación de los niveles de glucosa sérica
Dado que se ha reportado que el tratamiento con OLZ puede desarrollar resistencia a la insulina,26 en el día catorce se evaluaron los niveles de la glucosa sérica en todos los animales al concluir la administración de los tratamientos, tres horas después de la administración del MK801. Se usó un glucómetro Accu-chek de la marca Roche.
Ensayo de lipoperoxidación
Se obtuvo la corteza frontal de los ratones para medir los productos finales fluorescentes de la LP mediante la técnica descrita por Triggs y Willmore 45 y modificada por Diaz-Ruiz et al.46 La corteza frontal fue homogeneizada en 3 mL de solución salina (NaCl al 0,9%), posteriormente, se separó en alícuotas de 1 mL, a las cuales se agregó 4 mL de una mezcla de cloroformo-metanol (2: 1, v / v). Después de agitar, la mezcla se mantuvo en hielo durante 30 minutos para permitir la separación de las fases. Finalmente, se midió la fluorescencia de la fase clorofórmica en un espectrofotómetro de luminiscencia Perkin-Elmer LS50B a 370 nm de excitación y 430 nm de emisión. La sensibilidad del espectrofotómetro se ajustó a 150 unidades de fluorescencia con una solución estándar de quinina (0.1 g / mL). Los resultados se expresaron como unidades internacionales de fluorescencia por gramo de tejido fresco.
Determinación de la concentración de glutatión reducido Tres horas después de la administración de MK-801, los animales fueron sacrificados por decapitación (previa anestesia con pentobarbital sódico) y se realizó la disección de la corteza frontal. El estándar de GSH se preparó en fosfato de sodio 0.1 M y un buffer de EDTA 5 mM (pH 8) y se mantuvo en hielo hasta su uso. La solución de o-ftalaldehído (OPA) se preparó en metanol absoluto de grado reactivo justo antes de su empleo. Las muestras se homogenizaron en 3.75 mL de buffer EDTA-fosfato (pH 8.0) más 1 mL de HPO3 (25 %). Los homogeneizados se centrifugaron a 3,000 x g durante 15 minutos, los sobrenadantes fueron separados en alícuotas de 500 µL y se les adicionaron 4.5 mL de buffer de fosfato más 100 µL de o-ftalaldehído. Las muestras se incubaron a temperatura ambiente durante 15 minutos y fueron medidas en un espectrofotómetro de fluorescencia Perkin-Elmer LS50B a 350 nm de excitación y 420 nm de emisión.47
Análisis estadístico
Se obtuvieron los valores promedio ± error estándar. La estimación del tamaño de la muestra para este estudio experimental aleatorizado y controlado se obtuvo por medio de la siguiente fórmula:
En esta fórmula, n es el número de sujetos para cada grupo de tratamiento, µτ - µ2 es la diferencia detectable entre la media de los dos grupos, σ es la desviación estándar común de cada grupo, y Zα y Zß son los valores que incluyen alfa en las dos colas y beta en la cola inferior de la distribución normal estándar, de acuerdo con lo descrito por Greenberg y colaboradores en 1998. σ2, µτ y µ2 se estimaron con datos de un ensayo piloto.
En todos los casos se realizó un análisis exploratorio de los datos para determinar si existía una distribución normal, mediante la prueba de Kolmogorov-Smirnov, y homogeneidad de varianzas, usando la prueba de Levene. Una vez determinado esto, se emplearon pruebas estadísticas paramétricas o no paramétricas según las suposiciones de cada análisis. En este sentido, se realizó una prueba ANOVA de una vía seguida de la prueba post hoc de Dunnett; la significancia estadística fue establecida con p<0.05, utilizando el software SPSS 20.0.
Resultados
Niveles de glucosa sérica
El valor basal de glucosa sérica fue de 128.50 ± 6.29 (mg/ dL) y 131.20 ± 12.62 en el caso del grupo con MK-801 sin tratamiento. Con respecto a los grupos con MK-801 y tratamientos OLZ, NAC y OLZ+NAC, los valores fueron de 153.60 ± 17.39, 128.60 ±13.48 y 146.60 ±24.47, respectivamente. Se observó una tendencia al aumento solo en el grupo de ratones que recibió tratamiento únicamente con olanzapina, así como una tendencia a la baja en los ratones que recibieron la combinación de OLZ+NAC, sin registrarse diferencias estadísticamente significativas.
Niveles de lipoperoxidación
En la Figura 1 se muestran los resultados del análisis de los niveles de LP evaluados en la corteza frontal, 14 días después de la administración de los tratamientos y 3 h después de la inyección del MK-801. El nivel basal de productos finales de la LP en los animales sanos fue de 441.52 ± 66.53, y de 630.50 ± 58.68 en los ratones con MK-801 tratados con vehículo, observándose un incremento de 42%, siendo esta diferencia estadísticamente significativa. En todos los grupos tratados con OLZ, NAC y su combinación (OLZ+NAC) y MK-801 se muestra una disminución estadísticamente significativa (p<0.05) de la LP, del 35.22, 29.55 y 51.43%, respectivamente, en comparación con el grupo control (MK801/Veh). Los valores incluidos son el promedio ± error estándar y están expresados en unidades internacionales de fluorescencia por gramo de tejido fresco.
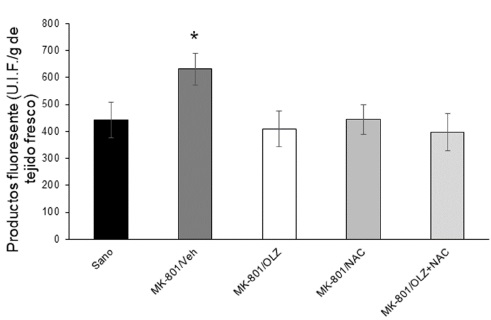
Figura 1 Gráfica en la que se muestran los resultados de los niveles de lipoperoxidación evaluados en la corteza frontal. Los valores son el promedio ± E.E. de 5 a 6 animales por grupo y están expresados en unidades internacionales de fluorescencia (U.I.F.) por gramo de tejido fresco. Sano: animales intactos; MK-801/Veh: animales con MK801 y vehículo; MK-801/ OLZ: ratones con MK-801 y OLZ en dosis de 4 mg/Kg (i.p.) administradas cada 12 horas durante 14 días; MK-801/NAC: ratones con MK-801 y NAC en dosis de 80 mg/kg (i.p.) administradas cada 24 horas durante 14 días; MK-801+ OLZ/NAC: animales con MK-801 y con ambos tratamientos en las dosis antes mencionadas. ANOVA de una vía seguida de la prueba de Dunnett * p<0.05.
Niveles de glutatión reducido
Los niveles de GSH fueron avaluados en la corteza frontal tres horas después de la administración de MK-801. Los resultados se muestran en la Figura 2. El nivel basal de GSH en los animales sanos fue de 0.99 ± 0.12 (mm/ mg), mientras que en los ratones con MK-801 tratados con vehículo fue de 0.50 ± 0.07; se observa una disminución de 49.5%, siendo esta diferencia estadísticamente significativa. En todos los grupos tratados con OLZ, NAC y su combinación (OLZ+NAC) y MK-801 observamos incrementos estadísticamente significativos (p<0.05) de los niveles de GSH, de 66, 72 y 46%, respectivamente, en comparación con el grupo control (MK-801/Veh).
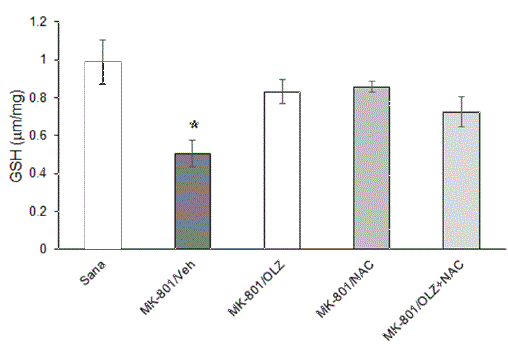
Figura 2 Gráfica en la que se muestran los resultados de los niveles de glutatión reducido (GSH) evaluados en la corteza frontal. Los valores son el promedio ± E.E. de 5 a 6 animales por grupo y están expresados en micro moles por miligramos. Sano: animales intactos; MK-801/Veh: animales con MK-801 y vehículo; MK-801/OLZ: ratones con MK-801 y olanzapina en dosis de 4 mg/Kg (i.p.) administradas cada 12 horas durante 14 días; MK-801/ NAC: ratones con MK-801 y NAC en dosis de 80 mg/kg (i.p.) administradas cada 24 horas por 14 días; MK-801/OLA+NAC: animales con MK-801 y ambos tratamientos en las dosis antes mencionadas. ANOVA de una vía seguida de la prueba de Dunnett * p<0.05.
Discusión
La hipofunción en los receptores de glutamato NMDA constituye una de las principales teorías sobre la etiopatogenia de la esquizofrenia. La hipofunción en estos receptores se asocia con alteraciones en la memoria, cognición y plasticidad neuronal, y con alteraciones en la liberación de glutamato en estructuras neuronales específicas, como el hipocampo y la corteza frontal.48 Con base en esto, en este estudio se utilizó el modelo de administración aguda de MK-801 en ratones según la metodología reportada por Aquino-Miranda et al.,8 ya que se trata de un modelo estandarizado y reproducible que causa una hipofunción glutamatérgica, estrés oxidativo y muerte celular, tal como se observa en la esquizofrenia.48
Reportamos un incremento de la lipoperoxidación en el grupo con MK-801 que fue tratado con vehículo, demostrando que el MK-801 incrementa el estrés oxidante y el daño a las membranas celulares. Estos hallazgos concuerdan con lo reportado en el estudio de Ozyurt et al.,49 en el cual la administración del MK-801 por vía intraperitoneal en ratas incrementó el estrés oxidante en la corteza frontal, observándose un aumento de la lipoperoxidación.
Asimismo, nuestros hallazgos demostraron que el tratamiento con NAC disminuye la lipoperoxidación después de la administración de MK-801. Este efecto es apoyado por los resultados del estudio de Turkmen et al.,50 en el que probaron el efecto antioxidante de la NAC después de la administración de MK-801 en testículo de ratones, observando que el tratamiento con NAC aumentó la actividad de las defensas antioxidantes y disminuyó el estrés oxidante inducido por el MK-801. Por otro lado, debe considerarse que la NAC administrada en altas dosis puede ser pro oxidante, por lo que las dosis elegidas para nuestro modelo fueron establecidas de acuerdo a los ensayos realizados por Smaga et al., 51 en cuyo estudio se administró NAC en dosis de 50 y 100 mg/kg vía intra peritoneal en ratas Wistar, tanto de manera aguda como crónica, durante 10 días. Los resultados demostraron que ambas dosis tienen efecto antioxidante, ya que incrementaron la eficacia de los mecanismos de defensa antioxidante en la corteza prefrontal sin alterar el estado antioxidante endógeno del cerebro de los animales que recibieron de manera crónica o aguda las dosis de NAC y de aquellos que no fueron sometidos a estrés oxidante. Nuestros hallazgos coinciden con dichos resultados, puesto que se observó que la dosis de 80 mg/Kg disminuye la lipoperoxidación en comparación con el grupo control no tratado (Mk-801/Veh).
Es importante destacar que la mayoría de los estudios realizados con NAC han sido en animales, sin embargo, recientemente ha sido probada en más de 20 ensayos clínicos como tratamiento adyuvante en distintos padecimientos neuropsiquiátricos. Es el caso del estudio realizado por Nucifora et al.52 en pacientes con esquizofrenia y trastorno afectivo bipolar, en el cual se reportó una disminución notable en los niveles séricos de GSH en los pacientes al ser comparados con los controles, además se observó una asociación entre la disminución de estos niveles y la magnitud de los síntomas psicóticos. Por otro lado, se han reportado disminuciones de hasta 27% (p<0.05) del GSH total en el líquido cefalorraquídeo de pacientes con esquizofrenia sin tratamiento farmacológico en comparación con los controles.53 En esta misma línea se encuentra un ensayo clínico aleatorizado doble ciego y controlado con placebo en pacientes con esquizofrenia tratados con antipsicóticos convencionales, que recibieron 1200 mg de NAC como tratamiento adyuvante. El estudio reportó que los pacientes tratados mostraron una mejoría significativa en la escala PANSS tanto para síntomas positivos como negativos, así como en el rendimiento cognitivo, en áreas como atención, memoria de trabajo y de corto plazo, funcionamiento ejecutivo y velocidad de procesamiento.54
Estos hallazgos son acordes con los resultados de nuestro estudio, ya que la administración de MK-801 en los ratones que no recibieron tratamiento con antipsicótico, antioxidante, o la combinación, generó una disminución estadísticamente significativa del glutatión reducido en la corteza frontal, lo que sugiere un incremento del estrés oxidante y posible daño celular. Por lo tanto, el tratamiento con OLZ y con NAC, administrados solos o en combinación, reduce los niveles de lipoperoxidación e incrementa los niveles de GSH, regulando posiblemente el daño oxidante propio de esta enfermedad. Lo anterior indica que la administración de NAC podría considerarse un tratamiento adyuvante, principalmente en pacientes con un curso crónico. De igual modo, los resultados de este protocolo de investigación apoyan la teoría existente relacionada al papel del estrés oxidante y la apoptosis neuronal en enfermedades psiquiátricas como la esquizofrenia. Nuestros resultados reforzarían también la posible modificación de los esquemas actuales de tratamiento, sobre todo en pacientes con un curso crónico de la enfermedad y con mala respuesta a dichos esquemas.
Conclusiones
Dados los hallazgos del presente estudio podemos concluir que el MK-801 incrementa los niveles de lipoperoxidación y disminuye los niveles de GSH en la corteza frontal. Asimismo, los tratamientos con OLZ en dosis de 4 mg/kg y con NAC en dosis de 80 mg/kg, administrados solos o en combinación, revierten estos efectos, es decir, son eficaces para disminuir el estrés oxidante en la corteza frontal del ratón.
Fuente de Financiamiento
Los hallazgos de este trabajo forman parte del protocolo de investigación registrado en el Instituto Nacional de Neurología y Neurocirugía Manuel Velasco Suarez con el número 38/20.
Conflictos de interés
Los autores del presente trabajo declaramos que no existen conflictos de interés.
Contribución de autores
Todos los autores han contribuido al diseño del estudio, la aprobación del comité de ética y la redacción, revisión crítica y versión final del manuscrito. RLA: redacción del manuscrito, estandarización del modelo de esquizofrenia en ratón; IPN: revisión del manuscrito, asesoría para la estandarización de los métodos bioquímicos; CR: concepción y diseño del estudio, análisis estadísticos; AMB, EM y NM: administración del tratamiento, toma de muestra, estandarización de los métodos bioquímicos; ADR: redacción del manuscrito, asesoría para el análisis estadístico, concepción y diseño del estudio.











 text new page (beta)
text new page (beta)



