Introducción
El síndrome de dificultad respiratoria aguda (SDRA) es una afección crítica caracterizada por una inflamación difusa y daño severo en el tejido pulmonar, que resulta en insuficiencia respiratoria aguda y conlleva alta mortalidad.1 La incidencia de SDRA en unidades de cuidados intensivos (UCI) varía, pero se estima que afecta a una proporción significativa de pacientes críticos, con tasas de mortalidad que pueden alcanzar hasta 40% en casos graves.2 Entre las complicaciones comunes de SDRA se encuentra la lesión renal aguda (LRA), que puede empeorar el pronóstico y prolongar la estancia en la UCI.3
La LRA se define por un deterioro rápido de la función renal, evidenciado por aumento en los niveles de creatinina sérica y disminución en la tasa de filtración glomerular (TFG).4 En el contexto del SDRA, la LRA puede ser provocada por múltiples factores, incluyendo hipoxia, inflamación sistémica y la administración de medicamentos nefrotóxicos.5
La interleucina 6 (IL-6) es una citocina proinflamatoria que juega un papel clave en la respuesta inmune y la inflamación.6 Elevados niveles de IL-6 están asociados con un aumento en la severidad de la inflamación y el daño a diversos órganos, incluido el riñón.7 En el contexto de SDRA, la IL-6 puede contribuir a la exacerbación del daño pulmonar y renal a través de la activación de vías inflamatorias y la disfunción endotelial.8
La utilidad de IL-6 como predictor de LRA en pacientes con SDRA grave ha sido objeto de investigación con resultados variados. Algunos estudios han encontrado una asociación significativa entre niveles elevados de IL-6 y el desarrollo de LRA, sugiriendo que IL-6 podría ser un biomarcador útil en el monitoreo de la función renal.9 Sin embargo, otras investigaciones no han logrado establecer una relación clara, indicando que la asociación entre IL-6 y LRA puede depender de factores específicos del paciente y del contexto clínico.10
Dado el papel potencialmente crucial de IL-6 en la inflamación y el daño renal, esta investigación se centra en evaluar si los niveles séricos de IL-6 al ingreso pueden predecir el desarrollo de LRA en pacientes con SDRA grave, con el objetivo de proporcionar información adicional sobre su valor como biomarcador en esta población crítica.
Material y métodos
Estudio de cohorte histórica. Se calculó un tamaño de muestra de 100 pacientes. Se realizó el cálculo de tamaño de muestra con diferencia de medias con un intervalo de confianza de 95%, potencia de 80% y diferencia esperada de 15%.
La población de estudio son adultos mayores de 18 años ingresada a la UCI del Centro Médico ABC en el periodo de marzo de 2020 a marzo de 2024. Se utilizarán los expedientes clínicos electrónicos del Centro Médico ABC campus Santa Fe y campus Observatorio.
Criterios de inclusión: pacientes mayores de 18 años ingresados a la UCI, de uno u otro sexo, pacientes bajo ventilación mecánica invasiva, pacientes con diagnóstico de SDRA grave según criterios de Berlín, de etiología indistinta, con niveles de IL-6 a su ingreso y niveles de creatinina seria al ingreso, 48 y 72 horas.
Criterios de exclusión: pacientes con LRA diagnosticada antes del ingreso en la UCI, pacientes con enfermedad renal crónica (ERC) previa al ingreso, pacientes con terapia de reemplazo renal previa al ingreso, pacientes con trasplante renal, pacientes con tratamiento previo de tocilizumab o glucocorticoides, mujeres embarazadas y sujetos con voluntad anticipada.
La descripción de las características generales de la población se realizó utilizando la prueba de normalidad con Kolmogórov-Smirnov, para las variables cuantitativas (como la edad y las pruebas bioquímicas), donde un valor de p > 0.05 se consideró distribución normal, por lo que se resumen con media y desviación estándar; para las variables de libre distribución (p < 0.05), se utilizó mediana y rango intercuartílico; mientras que para las variables cualitativas nominales, tales como sexo y comorbilidades, se presentan como frecuencia (número y porcentaje).
La comparación de variables categóricas se realizó utilizando la prueba χ2 de Pearson y para las variables continuas se empleó la prueba t de Student para aquellas con distribución normal y la prueba U de Mann-Whitney como opción no paramétrica. Para ambos casos, se estimó la respectiva razón de momios (RM) a través de modelos de regresión logística considerando la lesión renal aguda como variable dependiente.
Se realizó un análisis de curva ROC y área bajo la curva para determinar el rendimiento predictivo de la interleucina 6 (IL-6) para el diagnóstico de lesión renal aguda y se evaluaron diferentes puntos de corte. Posteriormente, se evaluó la correlación lineal de los valores de IL-6 con la creatinina al ingreso, a las 48 y 72 horas, y la tasa de filtración glomerular al ingreso, a través de coeficientes de correlación de Spearman. Finalmente, se evaluó la asociación y el cambio porcentual de creatinina a las 72 horas con respecto a la IL-6 en su forma continua y, de acuerdo con su distribución en cuartiles, utilizando modelos de regresión lineal con la variable dependiente transformada en su logaritmo natural. Para todas las estimaciones se calculó su respectivo intervalo de confianza al 95% (IC95%) y se consideró un valor p < 0.05 como estadísticamente significativo. El procesamiento de los datos y análisis estadístico se realizó con el paquete IBM SPSS Statistics 25.0 y en STATA versión 14.
Resultados
Se analizó la información de 98 pacientes con diagnóstico de SDRA grave atendidos en la UCI del Centro Médico ABC en el periodo de marzo del 2020 a marzo del 2024, para evaluar la asociación de los niveles séricos de IL-6 y el desarrollo de LRA. La muestra de estudio tuvo una media de edad de 61.5 ± 18.0 años (rango: 18-97). La edad se asoció positiva y significativamente con el diagnóstico de LRA con una razón de momios de 1.03 (IC95% 1.01-1.06), mientras que no hubo diferencias significativas en cuanto al sexo. Los pacientes con LRA presentaron mayores proporciones de antecedente de diabetes mellitus, hipertensión arterial sistémica, enfermedad pulmonar obstructiva crónica (EPOC), cirrosis, insuficiencia cardiaca congestiva, infarto agudo al miocardio y fibrilación auricular; sin embargo, estas diferencias no fueron estadísticamente significativas. De la misma forma, no hubo diferencias en cuanto al diagnóstico de neumonía por COVID, a pesar de que los individuos con LRA mostraron mayores proporciones de neumonía no COVID. En cuanto a la creatinina sérica, se observaron concentraciones significativamente mayores en los individuos que desarrollaron LRA, a partir de la medición de 48 y 72 horas. En contraste, la tasa de filtración glomerular se asoció negativamente con LRA desde el ingreso con una razón de momios de 0.97 (IC95% 0.95-0.98). No se observó asociación entre los niveles de IL-6 al ingreso y el desarrollo de LRA (RM: 1.0004; IC95% 0.999-1.001) (Tabla 1).
Tabla 1: Características de la muestra de estudio y su asociación con lesión renal aguda (LRA).
| Característica | Total (N = 98) n (%) |
LRA (N = 39) n (%) |
Sin LRA (N = 59) n (%) |
RM (IC95%) |
|---|---|---|---|---|
| Edad [años]* | 61.5 ± 18.0 | 67.2 ± 16.9 | 57.8 ± 16.9 | 1.03 (1.01-1.06) |
| Sexo | ||||
| Masculino | 53 (54.1) | 24 (61.5) | 29 (49.2) | 1.25 (0.85-1.65) |
| Femenino | 45 (45.9) | 15 (38.5) | 30 (50.8) | 0.60 (0.27-1.38) |
| Comorbilidades | ||||
| Diabetes mellitus | 14 (14.29) | 7 (18.0) | 7 (11.9) | 1.63 (0.52-5.06) |
| Hipertensión arterial | 28 (28.6) | 14 (35.9) | 14 (23.8) | 1.80 (0.74-4.37) |
| EPOC | 5 (5.1) | 3 (7.7) | 2 (3.4) | 2.38 (0.38-14.91) |
| Cáncer | 12 (12.2) | 4 (10.3) | 8 (13.4) | 0.73 (0.20-2.61) |
| Cirrosis | 2 (2.0) | 1 (2.6) | 2 (1.7) | 1.53 (0.09-25.15) |
| Insuficiencia cardiaca | 2 (2.0) | 2 (5.1) | 0 (0.0) | – |
| Infarto agudo del miocardio | 7 (7.1) | 4 (10.3) | 3 (5.1) | 2.13 (0.45-10.11) |
| Fibrilación auricular | 9 (9.2) | 6 (15.4) | 3 (5.1) | 3.39 (0.80-14.50) |
| Neumonía | ||||
| COVID | 36 (36.7) | 11 (28.2) | 25 (42.4) | 1 |
| No COVID | 62 (63.3) | 28 (71.8) | 34 (57.6) | 1.87 (0.78-4.46) |
| Creatinina (mg/dL), p50 [p25, p75] | ||||
| Ingreso | 0.77 [0.65, 0.95] | 0.86 [0.65, 0.98] | 0.74 [0.61, 0.90] | 3.07 [0.36, 25.95] |
| 48 horas | 0.90 [0.72, 1.16] | 1.22 [0.98, 1.56] | 0.76 [0.61, 0.87] | 1,208.95 [66.92, 21,840.76] |
| 72 horas | 0.90 [0.71, 1.18] | 1.23 [1.05, 1.43] | 0.78 [0.62, 0.90] | 3,848.91 [132.08, 112,155.80] |
| Tasa de filtración glomerular (mL/min/1.73 m2)* | 87.6 ± 26.8 | 74.6 ± 29.6 | 96.2 ± 20.8 | 0.97 (0.95-0.98) |
| Interleucina 6 (pg/mL), p50 [p25, p75] | 42.9 [15.6, 109.7] | 47.4 [17.6, 173.0] | 35.9 [15.0, 89.5] | 1.0004 [0.999, 1.001] |
EPOC = enfermedad pulmonar obstructiva crónica. LRA = lesión renal aguda. RM = razón de momios. IC95% = intervalo de confianza al 95%. Los números en negrita corresponden a razones de momios cuyos intervalos de confianza no cruzan el valor nulo = 1.
* Valores expresados en media ± desviación estándar.
Consistentemente con los resultados previos, al evaluar el valor predictivo de concentración de IL-6 al ingreso para LRA, se estimó un área bajo la curva no significativa de 0.568 (IC95% 0.449-0.686, p = 0.259) (Figura 1). Adicionalmente, de acuerdo con las coordenadas de la curva ROC de la variable continua, se evaluaron los puntos de corte de (pg/mL): 5.0, 10.0, 15.0, 20.0, 25.0, 30.0, 35.0, 40.0, 45.0 y 50.0, sin encontrar un valor que predijera de forma significativa la LRA.
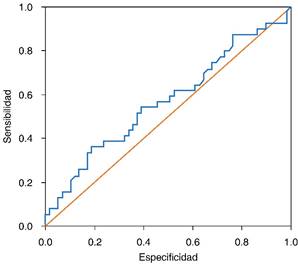
Figura 1: Evaluación del área bajo la curva ( AUC ) de las concentraciones de interleucina 6 al ingreso para el desarrollo de lesión renal aguda. AUC 0.568 (IC95% 0.449-0.686, p = 0.259).
A pesar de no observarse una asociación significativa entre la IL-6 al ingreso y el desarrollo de LRA, se observó una correlación lineal positiva con las concentraciones séricas de creatinina a las 72 horas, con un coeficiente de correlación de Spearman de 0.278 (p = 0.006) (Figura 2) y un coeficiente de regresión de 0.05 (IC95% 0.004-0.94) (Tabla 2), para las variables en su forma logarítmica. En contraste, no se observó correlación significativa con la creatinina al ingreso (rho: 0.021, p = 0.838), creatinina al a las 48 horas (rho: 0.154, p = 0.129), ni con la tasa de filtración glomerular al ingreso (rho: 0.068, p = 0.506). Se identificó que, a partir de 25.00 pg/mL de IL-6 al ingreso, los pacientes presentan concentraciones de creatinina a las 72 horas significativamente mayores (p = 0.047). Sin embargo, de acuerdo con la distribución de cuartiles de IL-6 al ingreso, se identificó un incremento porcentual de la creatinina a las 72 del ingreso para los individuos con concentraciones de IL-6 ≥ 42.0 pg/mL de 21.3%, lo que representa ~0.18 mg/dL, mientras que para concentraciones de IL-6 ≥ 109.0 pg/mL el incremento estimado es de 30.9%, lo que representa ~0.22 mg/dL (Tabla 2).
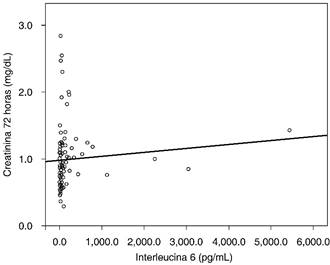
Figura 2: Correlación de las concentraciones de interleucina 6 al ingreso y de creatinina a las 72 horas. Rho: 0.278 (p = 0.006). Se excluye un valor extremo de interleucina 6 para facilitar la representación gráfica.
Tabla 2: Incremento porcentual de las concentraciones séricas de creatinina a las 72 horas del ingreso, de acuerdo con los cuartiles de distribución de la interleucina 6 al ingreso.
| Interleucina 6 (pg/mL) | β* | IC95% | Incremento porcentual |
|---|---|---|---|
| Continua | 0.05 | 0.004-0.94 | 5.1 |
| ≥ 16 | 0.12 | –0.06-0.31 | 13.3 |
| ≥ 42 | 0.19 | 0.03-0.35 | 21.3 |
| ≥ 109 | 0.27 | 0.09-0.45 | 30.9 |
* Coeficiente de regresión lineal tomando en cuenta la variable de respuesta transformada al logaritmo natural de la concentración de creatinina a las 72 horas; los números en negrita corresponden a coeficientes de regresión cuyos intervalos de confianza no cruzan el valor nulo = 0.
Discusión
En este estudio sobre pacientes con síndrome de distrés respiratorio agudo (SDRA) grave, no se encontró una asociación significativa entre los niveles séricos de interleucina 6 (IL-6) al ingreso y el desarrollo de lesión renal aguda (LRA). La evaluación del valor predictivo de IL-6 para LRA, medida mediante el área bajo la curva ROC, no mostró significancia estadística (AUC = 0.568, IC95% 0.449-0.686, p = 0.259). A pesar de esto, se observó una correlación positiva entre los niveles de IL-6 y las concentraciones séricas de creatinina a las 72 horas, lo que sugiere una posible relación con la función renal en etapas posteriores.
Nuestros resultados indican que los niveles de IL-6 al ingreso no predicen de manera significativa el desarrollo de LRA en pacientes con SDRA grave. Esta falta de asociación contrasta con estudios previos que han encontrado que IL-6 podría tener valor predictivo en otros contextos. Por ejemplo, un estudio de Yang y colaboradores (2017) encontró que los niveles elevados de IL-6 estaban asociados con el desarrollo de LRA en pacientes con sepsis severa. Sin embargo, la discrepancia en nuestros resultados podría reflejar diferencias en las características de los pacientes, la gravedad de la enfermedad o los métodos de medición utilizados.
A pesar de la falta de un valor predictivo claro al ingreso, los niveles de IL-6 se correlacionaron positivamente con las concentraciones de creatinina a las 72 horas. Este hallazgo es consistente con estudios que han encontrado asociaciones entre marcadores inflamatorios y daño renal en etapas más avanzadas. Por ejemplo, Zhang y asociados (2020) observaron correlación entre niveles elevados de IL-6 y marcadores de daño renal en pacientes críticos, aunque la relación no fue lineal. Esto sugiere que IL-6 podría reflejar un componente de la inflamación que contribuye al deterioro renal progresivo.
Nuestros resultados indican que niveles más altos de IL-6 al ingreso se asociaron con incremento en los niveles de creatinina a las 72 horas, lo que es coherente con otros estudios que han explorado el papel de IL-6 en el deterioro de la función renal. Sin embargo, la falta de una asociación significativa entre IL-6 y LRA al ingreso sugiere que IL-6 no debería ser utilizado de manera aislada para predecir la LRA en pacientes con SDRA grave. No obstante, la correlación observada con la creatinina en etapas posteriores podría ofrecer información adicional para el seguimiento de la función renal.
Este estudio tiene varias limitaciones que podrían influir en los resultados. En primer lugar, el tamaño de la muestra es relativamente pequeño, lo que podría limitar la capacidad para detectar asociaciones significativas. Además, la medición de IL-6 en un solo momento (al ingreso) puede no captar adecuadamente las variaciones dinámicas en los niveles de inflamación. Finalmente, la presencia de múltiples comorbilidades podría haber complicado la interpretación de la relación entre IL-6 y LRA.
Futuras investigaciones podrían beneficiarse de estudios longitudinales que midan los niveles de IL-6 y otros biomarcadores inflamatorios a lo largo del tiempo para comprender mejor su relación con la LRA. Asimismo, sería valioso explorar el papel de otros mediadores inflamatorios en la predicción y manejo de la LRA en pacientes con SDRA.
Conclusiones
Aunque la IL-6 no demostró ser un predictor significativo de LRA en nuestro estudio, los parámetros tradicionales de función renal como la creatinina sérica y la tasa de filtración glomerular siguen siendo indicadores clave en el manejo de pacientes con SDRA grave. Se requieren más estudios para clarificar el papel de IL-6 y otras citocinas en la LRA y para mejorar las estrategias de monitoreo y tratamiento en estas poblaciones vulnerable.











 text new page (beta)
text new page (beta)


