1. Introducción
La pérdida de tejidos y órganos puede deberse a accidentes, enfermedades, trastornos genéticos y el envejecimiento natural, que, en la mayoría de los casos, el cuerpo humano no tiene la capacidad de regenerar. Para su tratamiento o recuperación los trasplantes han sido empleados, no obstante, la escasez de donaciones de tejidos impide cubrir la demanda de la población afectada. La ingeniería tisular es la ciencia que se encarga de construir sustitutos biológicos en el laboratorio para su potencial uso en medicina regenerativa (1) y está basada en una triada: células (troncales o diferenciadas), andamios, y factores de crecimiento o inductores.
Las células troncales mesenquimales poseen la capacidad de auto renovación, alta tasa de proliferación y plasticidad de diferenciarse a linajes adipogénicos, condrogénicos y osteogénicos (2,3), sus fuentes de obtención son diversas (4) entre las que se encuentran la médula ósea (5), cordón umbilical (6) e incluso tejidos bucales (7,8).
Respecto a las células troncales de pulpa dental (7) las cuales son un tipo de célula no diferenciada de fácil acceso para su obtención (9), y con alta tasa de proliferación respecto a las células troncales de médula ósea (10), lo que las hace ser buenas candidatas para realizar ensayos in vitro, además de su probable aplicación en medicina regenerativa.
Los andamios (scaffolds en inglés) se utilizan como un soporte físico y biológico en el que se siembran las células, para posteriormente ser trasplantadas en un organismo. Los andamios son críticos en el éxito de regeneración tisular ya que intervienen en aspectos de adhesión, proliferación, diferenciación, distribución, retención y crecimiento celular, así como de distribución de nutrientes y oxígeno, promoviendo el establecimiento de un ambiente mecánico y biológico apropiado para la regeneración tisular de una manera organizada (11, 12, 13,14).
Para la construcción de andamios se han empleado biomateriales tanto naturales como sintéticos. Ejemplos de los primeros son el ácido hialurónico (15), la gelatina (16) y la matriz extracelular (17). Sin embargo, los polímeros naturales tienen varias desventajas, como propiedades mecánicas muy bajas, rápida degradación, dificultad para plastificar, riesgo de respuestas inmunitarias desfavorables y la falta de reproducibilidad en propiedades fisicoquímicas de un lote a otro, ya que dependen de la historia del individuo (animal o vegetal) donde se obtuvo el polímero natural. Entre los biomateriales sintéticos, la policaprolactona (PCL) ha sido utilizada por su biocompatibilidad, biodegradabilidad, estabilidad estructural y propiedades mecánicas; sin embargo, presenta baja bioactividad y energía superficial (alta hidrofobicidad), lo que conlleva a la reducción de la afinidad celular y tasas de regeneración tisular bajas (18). Otro biomaterial sintético es el ácido poli (láctico-co-glicólico) (PLGA), que en comparación con la PCL presenta mayor adhesión y proliferación celular debido a que es más hidrofílico. Un andamio fabricado a partir de PCL y PLGA podría promover una buena adhesión y proliferación celular, así como una buena resistencia mecánica, además de que ambos polímeros son aceptados por la Food and Drug Administration (FDA) de los Estados Unidos de Norteamérica y han sido utilizados para elaborar andamios por medio de la técnica de electrohilamiento (19,20,21).
Dentro de las múltiples técnicas para la fabricación de andamios, el electrohilamiento (electrospinning en inglés), permite la producción de fibras a escala micrométrica, pudiendo utilizarse prácticamente cualquier polímero para mimetizar una matriz extracelular. El proceso de electrohilamiento consiste en inyectar una disolución del polímero a través de una aguja de cero inoxidable hacia la placa receptora, también de acero inoxidable. Entre la aguja y la placa receptora se aplica un alto voltaje crenado un campo eléctrico entre ellas. Al salir la disolución de la aguja adquiere una carga positiva la cual hace que la disolución se acelera debido al campo eléctrico y en el trayecto se evapora el disolvente, llegando a la placa únicamente el polímero con forma de microfibras (22) (Figura 1). Los factores de crecimiento o biomoléculas han demostrado un efecto de diferenciación o inducción celular in vitro e in vivo, entre las que se encuentran las proteínas morfogenéticas de hueso (BMPs por sus siglas inglés), el factor β de crecimiento transformante (TGF-β en inglés), y los factores de crecimiento tipo insulina (22,23,24).
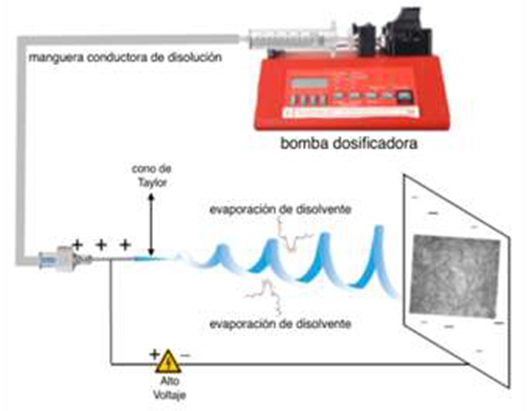
Figura 1 Proceso de electrohilamiento (Diseño por: Fernando Hernández Sánchez, CICY, Mérida, Yucatán, México).
La combinación PCL/PLGA a diferentes proporciones ha sido utilizada previamente para la elaboración de andamios, habiéndose demostrado que permite la adhesión de celular (25,26). Los andamios de estos dos polímeros construidos con técnicas combinadas de impresión 3D y electrohilamiento permiten la diferenciación de células madre mesenquimales derivadas de cordón umbilical hacia linajes condrogénicos y osteogénicos sin tener efectos citotóxicos (27). No obstante, en nuestro conocimiento, no existen reportes del empleo combinado de dichos polímeros que hayan evaluado su efecto en células troncales de pulpa dental, por lo que el presente estudio pretende evaluar su citotoxicidad en dichas células con fines de regeneración tisular.
2. Materiales y Métodos
Fabricación del andamio
Los andamios se elaboraron utilizando un electrohilador marca NABOND model TL-01 de manofactura China. Se hizo una disolución de policaprolactona (PCL) (Perstorp®, Mn=80000, Tm de 58ºC-60ºC y Tg = -60ºC) y poli(láctico-co-glicólico) (PLGA) (Aldrich, Mn= 76000-115000 y Tg = 49ºC-55ºC). Se prepararon andamios PCL/PLGA en relaciones 90:10 y 80:20 respectivamente. Los disolventes utilizados fueron cloroformo y etanol de grado reactivo (JALMEK®). Las mezclas fueron disueltas al 12% m/v en cloroformo/etanol (90:10) durante un período de 12 h continuas. (28).
Las mezclas poliméricas fueron electrohiladas utilizando una diferencia de potencial de 20 kV, una distancia entre el ánodo y el cátodo de 13 cm, una rapidez de giro del cilindro de 3 rev/s y una rapidez de flujo de 0.2 ml/h (28).
Microscopía electrónica de barrido (MEB)
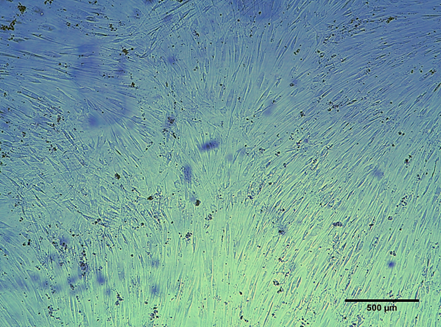
La caracterización morfológica de cada tipo de andamio se realizó mediante microscopía electrónica de barrido utilizando el software Image-j. Cada microfotografía fue dividida en 4 cuadrantes para la evaluación del diámetro de las fibras (25 fibras por cuadrante, dando un total de 100 fibras), y tamaño de poro. Este último se calculó trazando una circunferencia entre fibras sobrepuestas en forma de triángulo o cuadrado, realizándose 10 medidas de diámetro de poro en cada cuadrante, dando un total de 40 medidas por tipo de andamio (Figura 2b) (28).
Espectroscopia de infrarrojos por transformada de Fourier (FTIR)
Para determinar la existencia de nuevos grupos funcionales cuando la PCL y el PLGA fueron mezclados se realizaron ensayos FTIR. Los análisis fueron llevados a cabo por la técnica de reflexión total atenuada (RTA) con un cristal de Germanio en un intervalo de número de onda 500 cm-1 a 4000 cm1, analizando un total de 100 escaneos (28).
Obtención de las pulpas dentales humanas y cultivo celular
El presente estudio fue aprobado por la comisión de Ética y Bioseguridad de la Facultad de Estudios Superiores Iztacala de la UNAM. El consentimiento informado previo por escrito fue leído y firmado por cada uno de los donantes. Se recolectaron terceros molares humanos incluidos de 5 pacientes sistémicamente sanos (18 a 22 años de edad) en la clínica Cuautepec de la Facultad de Estudios Superiores Iztacala, UNAM (CE/FESI/012017/1098).
Los dientes se descontaminaron y se cortaron a nivel de la unión cemento-esmalte mediante un disco de diamante para acceder a la cámara pulpar; el enfriamiento durante el proceso de cortado se realizó irrigando constantemente con solución salina estéril (Solución CS Pissa). Para la obtención del tejido pulpar se utilizaron cucharillas de dentina (Hu-Friedy) y limas endodóncicas (Densply), se trabajó en condiciones asépticas: en una cabina de flujo laminar (Telstar Bio II Advance) previamente limpiada con alcohol etílico al 70% y expuesta a luz ultravioleta durante 20 minutos. Todo el tejido pulpar aislado se colocó en cajas Petri estériles y se procedió a fragmentarlas mediante mango de bisturí con una hoja del número 20, los fragmentos de tejido se transfirieron a tubos cónicos de 15 ml (Biologix) para realizar la digestión enzimática con 3 mg/ml de Colagenasa l (Collagenase from Clostridium histolyticum, Sigma-Aldrich) y 4 mg/ml de Dispasa (Dispase II, Sigma-Aldrich), por mililitro de DMEM (Dulbecco's Modified Eagle Medium Low-Glucose, Biowest) durante 15 minutos a 37 °C. Trascurrido ese tiempo se inactivó la solución enzimática agregando medio de cultivo, la suspensión celular se centrifugó a 1000 rpm durante 10 minutos a 24 °C para obtener el botón celular, se re-suspendió en medio fresco y se sembraron las células en cajas de cultivo tipo T de 25 cm2 (Nunclon) agregándoles 5 ml de medio de cultivo DMEM bajo en glucosa (Dulbecco's Modified Eagle Medium Low-Glucose, Biowest), adicionado con Suero Bovino Fetal (FBS, Biowest) al 10%, antibióticos y antimicótico al 1% (penicilina 100U/ml, estreptomicina 100µg/ml, anfotericina B 5µg/ml, Sigma-Aldrich), y se incubó a 37 °C con una atmósfera humidificada de 95% de O2 y 5% de CO2. El medio de cultivo fue cambiado dos veces por semana hasta alcanzar una confluencia del 80% para llevar a cabo los subsecuentes ensayos (Figura 3) (29, 30).
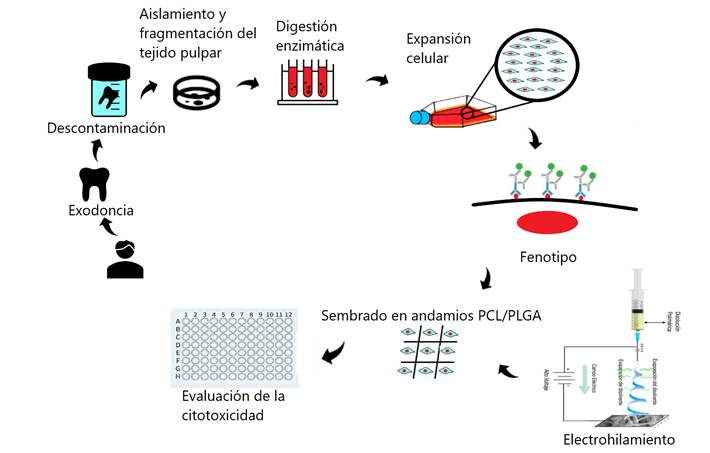
Figura 3 Esquema del proceso para la obtención de células de la pulpa dental por medio de digestión enzimática, la expansión celular hasta obtener confluencia celular para realizar la caracterización de células troncales de pulpa dental (DPSCs, por sus siglas en inglés), también se ejemplifica la siembra de las células en los andamios de PCL/PLGA para evaluar el efecto citotóxico de los mismos con las DPSCs.
Inmunofenotipo
Las células troncales de la pulpa dental (DPSC por sus siglas en inglés) se caracterizaron por inmunofluorescencia con los anticuerpos antihumano-CD44 y antihumano-STRO-1. Se sembraron DPSC (5x103 células/ml) en una placa de 24 pozos (TPP, Techno Plastic Products) y se incubó a 37 °C con una atmósfera humidificada con 95% de O2 y 5% de CO2 durante 48 horas, hasta lograr una semi-confluencia, transcurridas esas horas, se eliminó el medio de cultivo, se lavó la placa de 24 pozos con PBS (Biowest) para remover células muertas y eliminar restos de medio de cultivo, posteriormente, las células se fijaron con formalina 10% (Sigma-Aldrich) durante 20 minutos a temperatura ambiente, se permeabilizaron con Tritón TMX-100 (Sigma-Aldrich) al 0.50% durante 20 minutos, y se bloqueó con albumina de suero bovino (Santa Cruz) al 1% durante 30 minutos. A continuación, se agregaron los anticuerpos primarios contra los marcadores de superficie: anti-humano-CD44 (Santa Cruz) a una dilución de 1:200, y el anticuerpo anti-humano-STRO-1(Santa Cruz) a una dilución de 1:100. La placa con las células se colocó en un refrigerador marca LG a una temperatura controlada de 4 °C durante toda la noche. Al día siguiente se descartó la solución con los anticuerpos primarios y se lavaron las células con PBS. Para la visualización del fenotipo, se agregó el anticuerpo secundario Alexa Fluor® 488 (Thermo Fisher) y se incubo durante 1 hora a temperatura ambiente, se descartó el anticuerpo secundario y nuevamente se lavó nuevamente con PBS para agregar 200µl por pozo de DAPI (4',6-Diamidino-2-Phenylindole, Dihydrochloride Invitrogen™) en una dilución de 1:1000 para teñir los núcleos, se lavaron las células con agua destilada y se observó en microscopio confocal (Nikon A1R+ STORM) ubicado en el Instituto de Investigaciones Biomedicas, C.U, UNAM (29,30,31).
Viabilidad celular
En el presente estudio se utilizó el ensayo colorimétrico por absorbancia MTT (3-(4,5-dimetiltiazol-2-yl) 2,5-difeniltetrazolium bromuro) (Roche) para evaluar la viabilidad celular de las DPSC en andamios PCL/PLGA (90:10) y PCL/PLGA (80:20). Para cada tipo de andamio se sembraron 5x103 células por pocillo en placas de 96 pozos (TPP, Techno Plastic Products) de la siguiente manera: células en pozo, células en andamios de PCL:PLGA (90:10) y PCL:PLGA (80:20), evaluando a diferentes tiempos 3, 7 y 10 días. Las células en pozo sirvieron como grupo control y las células en cada uno de los andamios sirvieron como grupos experimentales, todos los grupos se realizaron por triplicado. Después de cada tiempo, el medio de cultivo de los pozos seleccionados para este ensayo se desechó con la ayuda de micropipetas e inmediatamente se lavó con PBS y se añadieron 70 µl de solución MTT al 10% por pozo, las placas de cultivo se resguardaron de la luz y se colocaron y se incubó durante tres horas a 37 °C con una atmósfera de 5% de CO2, posteriormente se añadieron 100µl de isopropanol para solubilizar las sales de formazán y realizar la lectura mediante un lector de placas de ELISA (Biotek Elx808) equipado con un filtro de 562-630 nm (30,31).
Análisis estadístico
Se usó el software Stata versión 14 (Stata Corp, College Station, TX, USA) para el análisis estadístico de los resultados del ensayo MTT. Los datos obtenidos se expresaron como media con sus respectivas desviaciones estándar. Cuando se realizó la comparación estadística entre el grupo control (células en pozo) con cada uno de los grupos experimentales (células en andamios de PCL/PLGA) se analizaron mediante la prueba "t" de Student. Se consideró como diferencia significativa un valor de p < 0.05.
3. Resultados
Microscopía electrónica de barrido
Los diámetros de fibra y tamaños de poro de los andamios se muestran en la Tabla 1. Los resultados muestran que ambos parámetros se encuentran a una escala micrométrica, con valores de diámetro de fibra de 3.23 ± 0.9 µm para la mezcla PCL/PLGA 90:10, y de 2.95 ± 1.1 µm para la mezcla 80:20. Por su parte, el tamaño de poro fue de 9.10 ± 1.02 µm y de 11.45 ± 1.22 µm respectivamente para cada mezcla de polímeros.
Tabla 1 Diámetros de fibra y tamaños de poro de los andamios.
| Andamio | Diámetro de fibras (µm) | Diámetro de poro (µm) |
|---|---|---|
| PCL/PLGA (90:10) | 3.23 ± 0.9 | 9.10 ± 1.02 |
| PCL/PLGA (80:20) | 2.95 ± 1.1 | 11.45 ± 1.22 |
En la Figura 4 se muestra la micrografía de andamios hechos a partir de PCL/PLGA (90:10) y PCL/PLGA (80:20).
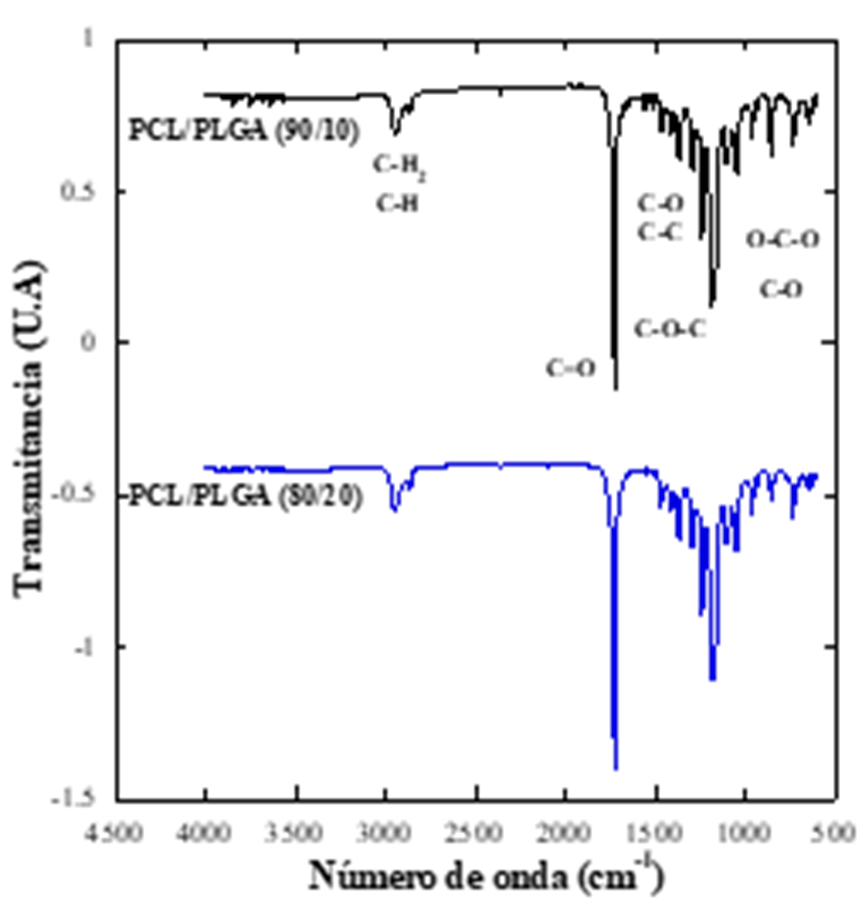
Espectroscopia de infrarrojos por transformada de Fourier (FTIR)
En el espectro de la Figura 5 se muestran los picos pertenecientes a los andamios (PLGA 20% y PLGA 10%), en donde se identificaron bandas del carbonilo (tensión) en 1733 cm-1, así como tensión asimétrica del grupo CH2 en 2862 cm-1. También se observan los grupos C-O y C-C a tensión en 1300 cm-1 que pertenecen a la fase cristalina de la policaprolactona. En 1244 cm-1 se identificó el pico C-O-C en tensión asimétrica, y en 1188 cm-1 se observa el pico O-C-O en tensión. Los picos C-O y C-C en tensión que aparecen en 1152 cm-1 pertenecen a la fase amorfa de la policaprolactona (Elzein T et al., 2004). Todos estos grupos funcionales son correspondientes a los polímeros utilizados (PCL y PLGA), por lo que no existieron formaciones de nuevos enlaces durante la disolución polimérica.
Cultivo celular
Se obtuvieron las células por la técnica de digestión enzimática, las cuales se adhirieron a la superficie de la placa de cultivo de acuerdo a los criterios de Dominici M., 2006 (Figura 6) (32). Las células proliferaron extensamente exhibiendo una morfología fibroblastoide homogénea, agrupándose en gran número y formando colonias (33).
Inmunofenotipo
El análisis inmunofenotípico de DPSC reveló la expresión positiva para los marcadores mesenquimatosos, CD44 (Figura 7-A) y STRO-1 (Figura 7-B). Estos resultados indicaron la presencia de marcadores de células troncales.
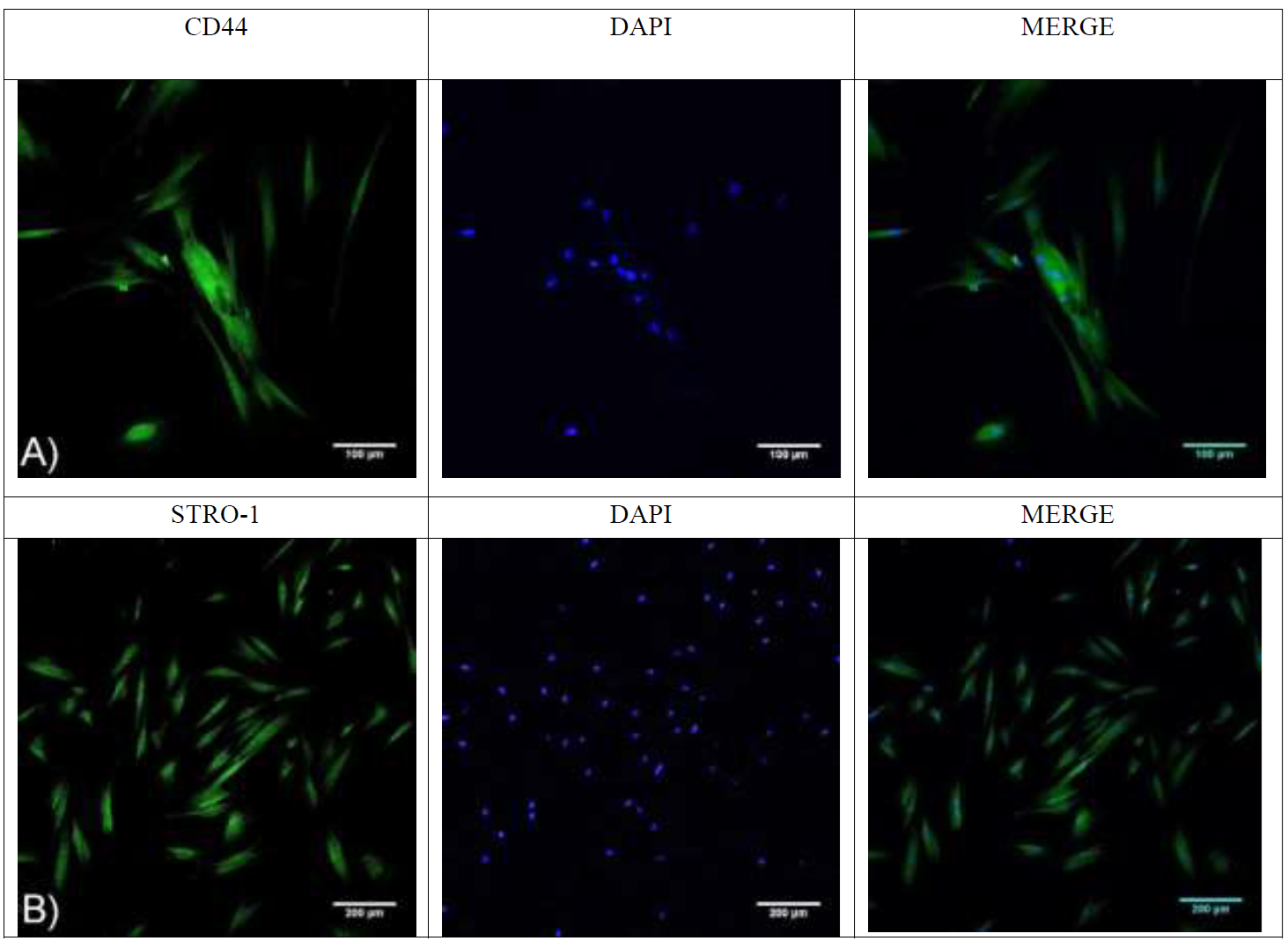
Figura 7 Imágenes de inmunofenotipo de células troncales de pulpa dental de humano con los anticuerpos anti humano-CD44 y anti humano-STRO-1. (A y B) anticuerpo secundario Alexa Flúor 488, denótese la membrana celular en fluorescencia en color verde y los núcleos celulares teñidos con DAPI en color azul por microscopio confocal (Nikon A1R+ STORM).
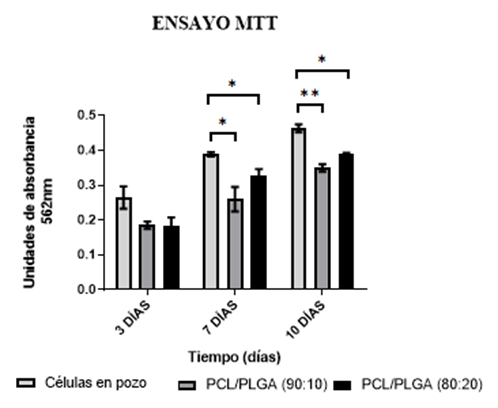
Viabilidad celular
Los resultados de la viabilidad celular se presentan en la Figura 8. Después de 3 días, la viabilidad celular de las células en pozo mostró una media de 0.264 ± 0.03, las células en andamios de PCL/PLGA (90:10) exhibieron una media de 0.185 ± 0.106, y las células en andamios de PCL/PLGA (80:20) expresaron una media de 0.184 ± 0.023. Sin embargo, no hubo diferencia estadísticamente significativa (p > 0.05). Después de 7 días, tanto la media de la viabilidad celular en el andamio PCL/PLGA 90:10 (0.260 ± 0.035), como en el PCL/PLGA 80:20 (0.328 ±0.017), fueron significativamente menores (p < 0.05) respecto al de las células en pozo (0.388 ± 0.006). De igual manera a los 10 días, tanto la viabilidad celular en el andamio PCL/PLGA 90:10 (0.349 ± 0.010), como en el PCL/PLGA (80:20) (0.389 ± 0.003) fueron significativamente menores (p< 0.05) en comparación con las células en pozo (0.463 ± 0.011).
4. Discusión
La poli-caprolactona (PCL) y el ácido poliláctico glicólico (PLGA) son dos de los polímeros más empleados en la elaboración de andamios para aplicaciones en ingeniería tisular y aprobados por la administración de alimentos y medicamentos de los Estados Unidos de Norteamérica (FDA en inglés) para su uso en humanos. Diferentes publicaciones han reportado el amplio uso de la PCL, ya que es un polímero relativamente barato, estable en el manejo y almacenamiento (34); además, es flexible y se ha utilizado para superar la fragilidad y baja elongación de otros polímeros, como el PLGA (35). Una de las grandes desventajas de la PCL es su hidrofobicidad, pero al mezclarla con el PLGA mejoran las propiedades de adhesión y proliferación celular (35). Por otro lado, Jay W et al. (2003) recomiendan no emplear altos porcentaje de PLGA cuando se realiza una mezcla con la PCL (36), lo mismo concluyen Hiep y Lee (2010), Milosevic M, et al. (2020) y Steven Elder et al. (2022), quienes mencionan que la presencia de PLGA en constructos tisulares aumentaron la adhesión celular, en contraste con un andamio hecho solo con PCL (25,26,37). Cabe mencionar que la concentración PCL/PLGA (90:10) y PCL/PLGA (80:20) fue acorde a la metodología empleada por Hielp y cols, posteriormente, nuestro grupo de trabajo publicó (Sánchez-Pech et al, 2020) una investigación con resultados muy alentadores empleando la misma concentración de PCL/PLGA (90:10) y PCL/PLGA (80:20) al usar células uretrales de cerdo, esos andamios no fueron tóxicos y permitieron la viabilidad y proliferación celular.
Respecto a la fabricación de los andamios, el método de electrohilado es uno de los más simples, entre todos los métodos para la elaboración de matrices o andamios con fibras de naturaleza polimérica, esto con el fin de simular las matrices extracelulares. En ese sentido, Fioretta, E. S. et al. (2014) señalan que en los andamios un tamaño de poro en el orden micrométrico propicia infiltración y adhesión celular, además de permitir que los nutrientes y el oxígeno penetren en el andamio (38); por lo que estas condiciones probablemente puedan aumentar la viabilidad celular. Respecto a la morfología de las microfibras se encuentra influenciada por diferentes parámetros, tales como el voltaje aplicado, la rapidez de flujo de la disolución polimérica, la distancia entre el ánodo y el cátodo; así como las propiedades de la disolución, ya sea concentración, tensión superficial y composición química de los disolventes. En nuestro caso los andamios fueron elaborados bajo las mismas condiciones, el aumento del 26% en el diámetro de los poros se atribuye al incremento en la proporción de PLGA en la mezcla de polímeros durante la elaboración de los andamios (39).
Por otro lado, las células troncales de diferentes fuentes han sido empleadas en muchas investigaciones in vitro, in vivo y en tratamientos en humanos. Nuestro grupo de investigación se caracteriza por emplear esta fuente de tejido humano (29-31) y de cerdo (40), para evaluar andamios de diferente naturaleza. En ese sentido, queremos resaltar cuatro propiedades de este tipo de células, en primer lugar las células troncales de la pulpa de los molares ha ido ganando terreno por la facilidad de obtener los dientes, generalmente de manera sencilla y ambulatoria, cuando es un molar erupcionado; además estas células son altamente viables (41), tienen una mejor taza de proliferación respecto a las obtenidas de médula ósea (42) y una capacidad multipotente para diferenciarse a mínimo trilinaje mesodérmico (43).
En la elaboración de andamios (44) el éxito es la interacción célula-andamio, ya que esto se verá reflejado en la adhesión, viabilidad y proliferación (45,46) en su proceso fisiológico hacia la formación de la matriz extracelular (47,48). En ese sentido, el ensayo de MTT evidenció diferencias en el comportamiento de la viabilidad de las células en los andamios a los diferentes tiempos evaluados. Aunque al tercer día de cultivo la viabilidad celular fue similar entre los andamios, para el séptimo y décimo días el andamio con mayor proporción de PLGA (80:20), presentó mayor viabilidad, lo que podría explicarse por el incremento de tamaño del poro en el andamio, y la mayor capacidad hidrofílica del PLGA en comparación con la PCL; siendo esta última una característica importante en la absorción de fluidos fisiológicos y en la transferencia de nutrientes a través del andamio (49). En 2017, Zou H y colaboradores, mencionan que el andamio de PLGA no es lo suficientemente amigable para la adhesión y proliferación celular (50); proponiendo mezclar el PLGA con colágeno, para mejorar la bioactividad de la superficie de los andamios elaborados (51); nuestros resultados evidencian que, en una proporción adecuada en los andamios, el PLGA incrementa la proliferación celular.
Por último, entre los requisitos en ingeniería tisular para la elaboración de constructos tisulares, están las evaluaciones in vitro, las cuales deben demostrar, entre otros aspectos, que favorecen la viabilidad y la proliferación celular; así como las posteriores evaluaciones de biocompatibilidad que deben ser realizadas en modelos in vivo(52), con el propósito de evaluar el rechazo de los constructos tisulares para que el huésped no lo reconozca como cuerpo extraño. Finalmente, Gangolli y colaboradores en 2019 (53) hacen énfasis en el uso de materiales, como PCL y PLGA ya que están aprobados por la FDA, los cuales fueron empleados en este proyecto.
5. Conclusiones
Se comprobó que la técnica de electrohilado favorece la creación de andamios con una arquitectura microscópica estable y reproducible, misma que puede favorecer la adhesión y proliferación de células troncales de pulpa dental. Las células cultivas dieron positivo para fenotipo de troncalidad.
Los andamios de PCL/PLGA (80:20) mostraron mayor viabilidad celular en los días 7 y 10 que la mezcla PCL/PLGA (90:10), demostrándose que ninguna de las dos mezclas evidenció efectos citotóxicos sobre las células troncales de pulpa dental.











 text new page (beta)
text new page (beta)