Introducción
En México el cultivo de la sandía es importante por la mano de obra que genera y el valor de su producción que asciende a 5 365 millones de pesos. En nuestro país, los principales estados productores de sandía son Sonora, Veracruz y Jalisco, que acumulan cerca del 50% de la producción nacional (1 134 016 t); el estado de Sonora, ocupa actualmente el primer lugar a nivel nacional con 318 593 t (SIAP 2023). No obstante, el rendimiento y calidad de este cultivo se ve afectado severamente por la marchitez causada por Fusarium oxysporum f. sp. niveum (Fon), que es la principal enfermedad fúngica de la sandía en todo el mundo. Esta enfermedad pueda causar pérdidas de alrededor del 30-80% o incluso más, en campos altamente infestados donde se cultivan variedades susceptibles (Egel y Martyn 2007, Rahman et al. 2021).
Los síntomas que causa Fon en plantas afectadas son coloración verde claro en hojas, perdida de turgencia, clorosis o marchitez generalizada (o de un solo lado de la planta), menor crecimiento de la planta, necrosis o decoloración del tejido vascular y muerte de plantas (Fernández-Herrera et al. 2021); las plantas que no mueren crecen poco y producen pocos frutos y más pequeños. El manejo de la marchitez por Fusarium es difícil debido a que este patógeno puede sobrevivir por largos períodos en el suelo como clamidospora (Everts et al. 2014), y su control se ha enfocado principalmente en el uso de injertos y variedades con resistencia, rotación de cultivos y fungicidas. Esta enfermedad se ha convertido en las últimas dos décadas en un problema emergente en todo el mundo, pues las prácticas de producción de sandías están cambiando, debido la reducción obligatoria del uso de bromuro de metilo, la expansión y aparición de nuevas razas de Fon, así como, la elección por cultivar sandías triploides (sin semillas), las cuales son preferidas por los consumidores, y tienen poca o nula resistencia a la marchitez por Fon (Everts y Himmelstein 2015). F.o. f. sp. niveum tiene cuatro razas (0, 1, 2 y 3) y la única que ha sido reportada en México es la raza 1 (Vargas-Arispuro et al. 2023), la cual es considerada la más preponderante en las áreas productoras de sandías en el mundo (Rahman et al. 2021).
Hoy en día, la presión pública sobre los residuos de agroquímicos en los alimentos y el ambiente, ha obligado a la búsqueda de alternativas seguras y eficientes para el tratamiento de las enfermedades en los cultivos agrícolas (Ishii et al. 1999, Quiróz-López et al. 2021). En este sentido, el uso de inductores de resistencia de amplio espectro, como el acibenzolar-S-metil (ASM), es un enfoque prometedor para el manejo de las enfermedades de las plantas. El ASM es un análogo sintético del ácido salicílico, que induce la resistencia sistémica adquirida (RSA), la cual es efectiva contra enfermedades causadas por virus, bacterias y hongos (Malolepsza 2006, Ito et al. 2024). Este compuesto ayuda a las plantas a expresar los mecanismos de defensa de la RSA (especies reactivas de oxigeno-ROS, fitoalexinas y proteínas relacionadas con patogénesis-PRs), además de que esta estrategia no contamina el ambiente (Ishii et al. 2018). El ASM ha suprimido algunas enfermedades ocasionadas por Fusarium en cultivos como ciclamen y gladiolo (Elmer 2004, 2006). No obstante, el uso del ASM para el manejo de la marchitez vascular causada por Fusarium en el cultivo de la sandía ha sido poco estudiada. Con base en lo anterior, el presente trabajo tuvo como objetivos evaluar la efectividad del acibenzolar S-metil en el crecimiento micelial, la germinación de esporas y en la severidad de la marchitez vascular causada por F. oxysporum f. sp. niveum raza 1 en plántulas de sandía.
Materiales y métodos
Obtención del hongo fitopatógeno
Para este trabajo se utilizó un aislamiento de F.o. f. sp. niveum raza 1 (Fon1, UESFON03), obtenido de una planta de sandía que presentaba síntomas de marchitez y necrosis vascular, ubicado en la Costa de Hermosillo, Sonora. El hongo se aisló en medio PDA y se identificó molecularmente a nivel de raza con primers específicos, y pruebas de patogenicidad en cultivares diferenciales de sandía (Vargas-Arispuro et al. 2023).
Efecto de acibenzolar-S-metil sobre el crecimiento micelial de Fon1
Se evaluó el efecto in vitro de acibenzolar-S-metil (Syngenta) en el crecimiento micelial de Fon1 acorde a lo descrito por Yao y Tian (2005) y Quiróz-López et al. (2021). El acibenzolar S-metil se adicionó al medio PDA antes de vaciarse en las cajas de Petri. Las concentraciones finales de acibenzolar-S-metil en el medio PDA fue de 15, 20, 30 y 40 mg L-1. Un disco de medio PDA de 9 mm de diámetro con Fon1, se colocó en el centro de cada caja Petri y se incubó a 28 °C. El diámetro del crecimiento de la colonia se determinó a las 96 y 168 h después de la incubación; cada tratamiento constó de cuatro replicas y el experimento completo se realizó dos veces.
El efecto de acibenzolar-S-metil en la inhibición del crecimiento micelial de Fon1 se evaluó con la siguiente fórmula:
Efecto de acibenzolar-S-metil sobre la germinación de esporas de Fon1
El efecto fungitóxico del ASM se evaluó en medio líquido Caldo Papa Dextrosa (CPD) acorde con lo descrito por Quiróz-López et al. (2021). Para esto alícuotas de 1 mL de una suspensión conidial del patógeno se adicionaron a tubos de ensayo (150 mm x 10 mm) con 5 mL de CPD, para obtener una concentración final de 5 x 105 conidias mL-1. Los tubos con medio CPD tuvieron una concentración final de 15, 20, 30 y 40 mg L-1 de ASM. Tubos con medio CPD sin ASM e inoculados con Fon1 se utilizaron como tratamiento testigo. Todos los tubos se colocaron en un agitador orbital a 150 rpm a temperatura ambiente durante 24 horas. Cada tratamiento constó de cinco repeticiones y se evaluó 100 esporas del patógeno por repetición. Las esporas se consideraron germinadas cuando presentaron emisión del tubo germinativo, independientemente de su longitud.
Preparación del inóculo
La inoculación de Fon raza 1 en las plantas de sandía, se realizó mediante el método de grano de trigo colonizado por el hongo. Para la realización de este método se seleccionaron granos de trigo en buen estado (100 g) y se colocaron en un matraz de 250 mL, se hidrataron con 100 mL de agua destilada durante 24 horas, para después esterilizarlos a 121 °C durante 1 hora en autoclave, en dos ocasiones distintas. Una vez esterilizados los granos, se agregaron tres trozos de ~1 cm de medio PDA con crecimiento de Fon1 y se incubó el matraz a 28 °C durante 10 días.
Efecto de ASM sobre la severidad de la marchitez causada por Fon1
Semillas de la variedad Sugar Baby se sembraron en macetas (13 cm de diámetro por 10 cm de alto) con sustrato esterilizado. Las macetas con las plantas de sandía (una planta por maceta) se crecieron en condiciones controladas a una temperatura de 29 ± 2 °C y una humedad relativa de 70-80%, y riegos cada tercer día (40 mL de agua por planta). Cada planta de sandía en etapa de dos hojas verdaderas se inoculó con 2 granos de trigo colonizados por Fon raza 1; un grano a cada lado de la planta. La inoculación se realizó enterrando, a 1 cm de profundidad, el grano de trigo en el sustrato a 2 cm de distancia de la base de la planta. El ASM se aplicó de dos maneras distintas, vía foliar y por riego; la aplicación foliar se realizó con la aspersión de ASM a concentraciones de 15, 20, 30 y 40 mg L-1 hasta cubrir el follaje de cada planta, mientras que, la aplicación vía riego se realizó con 40 mL, por maceta, con soluciones de ASM a las mismas concentraciones que la aplicación foliar. El ASM se aplicó tres veces (cada siete días) a partir de que las plantas presentaron la primera hoja verdadera; la primera aplicación se realizó cuatro días antes de la inoculación con el hongo. Se contó con dos tratamientos testigos; plantas de sandía tratadas sólo con agua (sin ASM y sin hongo) y plantas inoculadas únicamente con el hongo (sin ASM). Se tuvieron seis tratamientos (4 concentraciones y dos testigos) y cada tratamiento constó de 15 repeticiones en un diseño completamente al azar. El estudio completo se realizó dos veces (experimento 1 y experimento 2) bajo condiciones experimentales similares, sólo que, en el segundo experimento, con la finalidad de evaluar la toxicidad del ASM en el crecimiento de las plantas, también se evaluaron las variables de altura, número de hojas y peso fresco aéreo de las plantas.
Medición de la severidad de la enfermedad
El índice de severidad de la enfermedad se evaluó a los 28 días después de la inoculación de Fon en las plantas, usando la escala de evaluación propuesta por Grattidge y O`Brien (1982) y Amini y Sidovich (2010): 0 = 0-24% de hojas amarillas o marchitas; 1 = 25-49% de hojas amarillas o marchitas; 2 = 50-74% de hojas amarillas o marchitas; 3 = 75-99% de hojas amarillas o marchitas; 4 = planta muerta.
Fórmula para determinar severidad:
Dónde: ∑n = la suma de los rangos individuales; N = número total de plantas medidas; 4 = valor más alto de la escala de severidad.
Análisis estadístico
El efecto del acibenzolar-S-metil en el crecimiento micelial, germinación de esporas y severidad de la marchitez causada por Fon1, y en el crecimiento de las plántulas de sandía, se analizó mediante un análisis de varianza (ANOVA) y una comparación de medias de Tukey (P < 0.05) utilizando el paquete estadístico R.
Resultados
Efecto del ASM en la germinación de esporas y el crecimiento micelial de F. o. f. sp. niveum
Se observó que el ASM redujo en 10 a 22.6% la germinación de esporas de Fon1, en comparación al tratamiento testigo, después de 24 horas de incubación (Tabla 1). La concentración de 40 mg L-1 de ASM fue la que mostró el menor porcentaje de germinación, lo cual contrastó significativamente con el 90.8% de esporas germinadas del tratamiento testigo. Así mismo, para la variable del crecimiento micelial, hubo un efecto fungitóxico del ASM sobre el hongo a los tiempos evaluados en este estudio (Figura 1). A los cuatro días de crecimiento en PDA, Fon1 mostró decrementos de 6.2 y 14.2% con las dosis de 30 y 40 mg L-1 de ASM, respectivamente, las cuales fueron significativamente diferentes (P < 0.05) en comparación con el tratamiento testigo (Fon1). A los siete días, el menor crecimiento fúngico de Fon1 se mantuvo con las dosis de 30 y 40 mg L-1, con decrementos de 12 y 13%, respectivamente, en comparación con las cajas testigos.
Tabla 1 Efecto de ASM en la germinación de Fon1 a las 24 horas después de la inoculación en medio líquido caldo papa dextrosa.
| Tratamiento | Germinación de esporas (%) |
|---|---|
| ASM 15 mg L-1 | 80.8 b |
| ASM 20 mg L-1 | 74.8 bc |
| ASM 30 mg L-1 | 73 c |
| ASM 40 mg L-1 | 68.2 c |
| Fon1 | 90.8 a |
Valores con la misma letra son iguales estadísticamente (Tukey, p < 0.05). ASM = acibenzolar S-metil; Fon1 = Fusarium oxysporum f. sp. niveum raza 1.
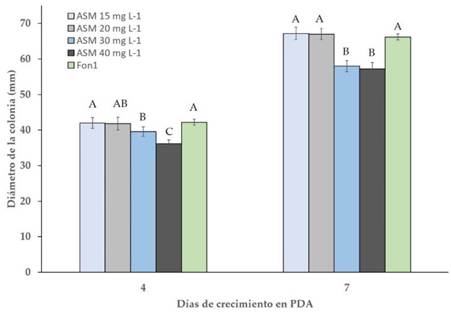
Figura 1 Efecto de concentraciones de acibenzolar S-metil en el crecimiento micelial de Fusarium oxysporum f. sp. niveum raza 1 en medio PDA a los 4 y 7 días después de incubación a 28 °C. La barra en cada columna representa la desviación estándar de los datos del tratamiento. Columnas con la misma letra en cada tiempo de evaluación son iguales estadísticamente (Tukey, p < 0.05)
Efecto del ASM en la severidad de F. o. f. sp. niveum
Los primeros síntomas del marchitamiento en las plantas de sandía, ocurrieron a los 10 días después de la inoculación (ddi) con el hongo en el tratamiento testigo (sólo con Fon). En los dos ensayos realizados, la aplicación del inductor de defensa ASM redujo la severidad causada por Fusarium 28 ddi en comparación con las plantas testigo (sólo con Fon1), las cuales tuvieron una severidad del 100% a los 21 ddi. En general, se observó que la aplicación de ASM vía riego, tuvo los mayores rangos de reducción de la severidad, en comparación con las dosis aplicadas vía foliar, en ambos experimentos.
En el experimento 1, la aplicación vía riego del ASM, mostró ser más eficaz para reducir la severidad por Fon en las plantas de sandía, en comparación con la aplicación vía foliar; ya que mostró rangos de reducción de la enfermedad de 84 al 100%, siendo la mejor dosis 15 mg L-1, pues las plantas no mostraron síntomas de clorosis o marchitez (índice de severidad de 0), en comparación con las plantas inoculadas (Tabla 2). En contraste, cuando el ASM se aplicó vía foliar, la dosis de 15 mg L-1 mostró la mayor severidad de la enfermedad, incluyendo muerte de plantas. No obstante, al incrementar la dosis de ASM a 20, 30 y 40 mg L-1 la severidad se redujo en 72, 90 y 77%, respectivamente, en comparación con las plantas testigo inoculadas.
Tabla 2 Experimento 1. Efecto de la aplicación de cuatro dosis de ASM (mg L-1) en la severidad de la marchitez vascular por Fusarium en plantas de sandía a los 28 ddi.
| Tratamiento (ASM mg L-1) | Índice de severidad* | % de reducción de la marchitez (eficacia) | ||
|---|---|---|---|---|
| AF | AR | AF | AR | |
| 15 | 2 b | 0 a | 48.5 | 100 |
| 20 | 1.1 bc | 0.4 a | 72 | 90 |
| 30 | 0.2 c | 0.1 a | 90 | 94.5 |
| 40 | 0.8 bc | 0.3 a | 77 | 84 |
| Testigo SH | 0 a | 0 a | --- | --- |
| Testigo CH | 4c | 4 b | --- | --- |
SH - Testigo sin hongo, CH - Testigo con hongo. ddi - días después de la inoculación. AF- aplicación foliar, AR- aplicación vía riego. Valores de medias dentro de una misma columna con diferentes letras indican diferencias significativas entre los tratamientos de acuerdo a Tukey (P = 0.05). * Escala de severidad: 0: 0-24% de hojas amarillas o marchitas; 1: 25-49% de hojas amarillas o marchitas; 2: 50-74% de hojas amarillas o marchitas; 3: 75-99% de hojas amarillas o marchitas; 4: 100% de hojas machitas o planta muerta.
En el experimento 2, la mayor reducción de la severidad se obtuvo, otra vez, con la aplicación de ASM vía riego con rangos de 82 al 100% (Tabla 3). Para la aplicación foliar, se observó que a mayor concentración de ASM, mayor es la reducción de la severidad, pues a 15 mg L-1 de ASM se obtuvo 10.5% de severidad, mientras que a 40 mg L-1 la severidad fue de 67.5%, en comparación con las plantas inoculadas con Fon, las cuales tuvieron 100% de severidad a los 21 ddi (Figura 2). En contraste, las plantas sin ASM y no inoculadas, no mostraron síntomas de clorosis o marchitez durante el desarrollo del experimento (Figura 2). En este experimento, se observó fitotoxicidad en las plantas de sandía con las dosis altas de ASM (30 y 40 mg L-1), la cual se vio reflejada significativamente (P < 0.05) en menor altura, número de hojas y peso fresco aéreo de las plantas, en comparación con las plantas no inoculadas y sin tratar con ASM. En este sentido, es importante resaltar que la dosis de 15 mg L-1 en aplicación vía riego, fue la más efectiva para reducir la severidad de la marchitez causada por Fon, además en esta dosis, las plantas no manifestaron daños por fitotoxicidad, ni hubo diferencias significativas para las variables altura, números de hojas y peso fresco, con respecto a las plantas testigo no tratas y sin inocular (Tabla 3).
Tabla 3 Experimento 2. Efecto de la aplicación de dosis de ASM en la severidad de la marchitez vascular por Fusarium y en el crecimiento de plantas de sandía a los 28 ddi.
| Tratamiento ASM (mg L-1) | Índice de severidad* | % de reducción de la marchitez (eficacia) | Variables de crecimiento en aplicación vía riego | ||||
|---|---|---|---|---|---|---|---|
| AF | AR | AF | AR | Altura (cm) | Número de hojas | Peso fresco (g) | |
| 15 | 3.5 bc | 0 a | 10.5 | 100 | 19.65 a | 7.9 a | 1.7 a |
| 20 | 2 ab | 0.3 a | 50 | 82 | 20.05 a | 7.1 bc | 1.66 a |
| 30 | 2.3 bc | 0.2 a | 40.5 | 90 | 11.5 b | 6.4 cd | 1.11 b |
| 40 | 0.2 ab | 0 a | 67.5 | 99 | 12.25 b | 6.3 d | 1.22 b |
| Testigo SH | 0 a | 0 a | --- | --- | 19.95 a | 7.6 ab | 1.89 a |
| Testigo CH | 4 c | 4 b | --- | --- | --- | --- | --- |
SH - Testigo sin hongo, CH - Testigo con hongo. ddi - días después de la inoculación. AF- aplicación foliar, AR-aplicación vía riego. Valores de medias dentro de una misma columna con diferentes letras indican diferencias significativas entre los tratamientos de acuerdo a Tukey (P ≤ 0.05). * Escala de severidad: 0: 0-24% de hojas amarillas o marchitas; 1: 25-49% de hojas amarillas o marchitas; 2: 50-74% de hojas amarillas o marchitas; 3: 75-99% de hojas amarillas o marchitas; 4: 100% de hojas amarillas, machitas o planta muerta.

Figura 2 Efecto de la aplicación de ASM en la severidad de la marchitez vascular causada por F. oxysporum f. sp. niveum raza 1 en plantas de sandía. A) Testigo sin Fon1, sin tratar, B) Testigo con Fon1, sin tratar, C) dosis foliar de 15 mg L-1 de ASM e inoculadas con Fon1, D) dosis vía riego de 15 mg L-1 de ASM e inoculadas con Fon1, E) dosis foliar de 20 mg L-1 de ASM e inoculadas con Fon1, F) dosis vía riego de 20 mg L-1 de ASM e inoculadas con Fon1, G) dosis foliar de 30 mg L-1 de ASM e inoculadas con Fon1, H) dosis vía riego de 30 mg L-1 de ASM e inoculadas con Fon1, I) dosis foliar de 40 mg L-1 de ASM e inoculadas con Fon1, J) dosis vía riego de 40 mg L-1 de ASM e inoculadas con Fon1.
Discusión
Efecto del ASM en la germinación de esporas y el crecimiento micelial de Fon1
La reducción de la germinación de esporas y del crecimiento micelial de Fon1 con las dosis de ASM evaluadas en este estudio, sugiere que este producto no sólo estimula las defensas de las plantas de sandía asociadas con la RSA, sino que también, afecta directamente el crecimiento fúngico de este hongo. En este sentido, diversos estudios han reportado que el efecto tóxico directo del ASM en contra de patógenos varía en función del tipo de patógeno y la dosis evaluada. Nuestros resultados concuerdan con los reportados por Amini (2015)), quien señala que las concentraciones de 5, 50, 100 y 500 mg L-1 de ASM reducen significativamente el crecimiento micelial de Verticillium dalhiae en 5.4, 11.2, 15.4 y 16.9%, respectivamente, en comparación con el tratamiento testigo. Así mismo, Faessel et al. (2008) reportan que las dosis de 5, 40, 80 y 500 mg de ASM, reducen significativamente en 5, 34, 36 y 40%, respectivamente, el crecimiento micelial de Rhizoctonia solani AG-4 en comparación con el tratamiento testigo. Además, Bussabong et al. (2021) reportan una reducción del crecimiento micelial de Curvularia eragrostidis de 41.5%, con la dosis de 5 mM, en comparación con el tratamiento testigo. No obstante, otros autores como Felipini et al. (2015) y Costa et al. (2017) señalan que el ASM (50 mg L-1 y 250 mg L-1, respectivamente) no afectó el crecimiento micelial de Cercospora beticola o Colletotrichum lindemuthianum, sugiriendo que el ASM actúa principalmente como un inductor de la defensa de las plantas y que no tiene efecto tóxico directo en contra de estos patógenos. De igual forma, Zhang et al. (2011) reportan que la dosis de 30 mg L-1 no afectó el crecimiento micelial de P. capsici. Mientras que Ishii et al. (1999) señalan que sólo Didymella bryoniae mostró sensibilidad al ASM en dosis bajas (2 mg L-1), en comparación a Colletotrichum cucumerinum, C. lagenarium, F. oxysporum f. sp. cucumerinum, Corynespora cassiicola, Venturia nashicola, A. alternata y B. cinerea, los cuales no mostraron reducción del crecimiento micelial a esta misma dosis. Por lo anterior, se sugiere que el ASM tiene un efecto fungitóxico directo hacia Fon1, pues en este estudio se observó menor germinación de esporas y crecimiento micelial del hongo con las dosis de ASM evaluadas.
Efecto del ASM en la severidad de Fon1
Los resultados de este estudio indican que el ASM aplicado en el riego o las hojas, reduce la severidad de la marchitez causada por Fon en las plantas de sandía, lo que sugiere que el ASM puede representar una opción viable para su uso en los programas de manejo integrado de la marchitez por Fusarium. El efecto protector del ASM contra diferentes enfermedades o patógenos se ha reportado en cultivos como chile serrano (Capsicum annuum) para la marchitez causada por Phytophthora capsici (Cosme-Velázquez et al. 2015), en tomate de árbol (Solanum betaceum Cav.) para la virosis causada por potyvirus y el tizón tardío causado por Phytophthora infestans (Mejía et al. 2009, Castaño-Monsalve et al. 2015), en trigo (Triticum aestivum L.) para la cenicilla causada por Blumeria graminis f. sp. tritici (Santos et al. 2018), en jitomate (Solanum lycopersicum) para la mancha bacteriana causada por Xanthomonas spp. (Pontes et al. 20016), en pepino (Cucumber sp.) para el control de la cenicilla y el mildiu causado por Podosphaera xanthii y Pseudoperonospora cubensis (Ishii et al. 2018), entre otros cultivos. En el cultivo de sandía, el uso del ASM para el manejo de la marchitez vascular por Fusarium se ha estudiado muy poco; entre estos trabajos resalta el de Everts et al. (2014), quienes señalan que la aplicación vía riego del ASM reduce la marchitez causada por Fusarium en el cultivo de la sandía, tanto en condiciones de invernadero como en campo. En nuestro estudio, la aplicación de ASM redujo significativamente la severidad causada por Fon1 e incluso, para la dosis de 15 mg L-1 en aplicación riego, las plantas no presentaron síntomas de marchitez o clorosis característicos de la enfermedad después de 28 ddi con el hongo, lo cual contrastó con las plantas inoculadas, las cuales habían muerto 21 ddi. Lo anterior sugiere que los mecanismos de defensa relacionados con la RSA fueron expresados en las plantas de sandía como respuesta a la aplicación del ASM. Hasta donde sabemos, los mecanismos de defensa que son expresados por la aplicación del ASM en plantas de sandía durante la interacción con F. o. f. sp. niveum son desconocidos. No obstante, en interacciones de otros cultivos y patógenos, la aplicación de ASM induce la expresión de proteínas PR´s (β-1,3 glucanasas, quitinasas, peroxidasas) y fenoles totales durante la interacción de chicharo (Pisum sativum)-Uromyces pisi (Barilli et al. 2010), quitinasas en la interacción soya (Glycine max cv. Amphor)-Rhizoctonia solani AG-4 (Faessel et al. 2008), cierre de estomas asociado al incremento de ROS en la interacción de rábano japonés (Rhaphanus sativus var. longipinnatus)-Pseudomonas cannabina pv. alisalensis (Sakata et al. 2020), fenil alanina amonio liasa, peroxidasas y β-1,3 glucanasas durante la interacción banana (Musa acuminata L.)-Curvularia eragrostidis (Bussabong et al. 2021), entre otros mecanismos.
En este estudio, la aplicación de las dosis de 30 y 40 mg L-1 de ASM vía riego, causó toxicidad en las plantas de sandía, haciendo que estas tuvieran menor altura, número de hojas y menor peso fresco aéreo, en comparación con las plantas no tratadas y sin inocular. En concordancia con nuestros resultados, diversos autores han documentado que la aplicación de ASM en plantas puede provocar daños en los tejidos o efectos adversos en el crecimiento y desarrollo de las plantas; por ejemplo, en chile serrano se observó una disminución del peso seco de la parte aérea, número de hojas, altura y lesiones en hojas (Cosme-Velázquez et al. 2015), en tomate de árbol se observó hojas deformadas, con ampollas, amarillamiento y una disminución de la altura y desarrollo de las plantas (Mejía et al. 2009, Castaño-Monsalve et al. 2015), en tabaco provoca manchas foliares y enanismo de las plantas (Mandal et al. 2008), en ciclamen redujo la biomasa seca de la planta, aunque no afecto la cantidad y número de flores (Elmer 2006), entre algunos otros síntomas de fitotoxicidad en otros cultivos. En este estudio, se corrobora que la aplicación de ASM en plantas de sandía reduce significativamente la marchitez vascular causada por Fusarium, lo cual podría ser una alternativa prometedora y ecológica para el manejo de esta enfermedad, pues los inconvenientes asociados con el uso indiscriminado de fungicidas, como el desarrollo de resistencia a fungicidas y la contaminación ambiental, se reducen al mínimo, pues es menos probable que los patógenos superen fácilmente los mecanismos de defensa de la RSA inducida por el ASM (Ishii et al. 2018).
Conclusiones
En condiciones in vitro, se observó que el acibenzolar S-metil redujo el crecimiento micelial y la geminación de esporas de F. oxysporum f. sp. niveum raza 1, por lo que se sugiere, que este producto tiene un efecto tóxico directo en contra de este hongo. En planta, la aplicación de ASM redujo la severidad de Fon1. Sin embargo, la aplicación vía riego mostró ser más eficaz para reducir la severidad de la marchitez por Fusarium, en comparación a la aplicación foliar, y las plantas tratas sólo con el hongo. La dosis de 15 mg L-1 de ASM redujo 100% la marchitez causada por Fusarium y no causó síntomas de toxicidad en las plantas de sandía. Las dosis de 30 y 40 mg L-1 de ASM causaron síntomas de toxicidad en las plantas, lo cual se vio reflejado en menor altura, número de hojas y menor peso fresco aéreo. Finalmente, se puede concluir que ASM podría significar una alternativa más para el manejo de la marchitez por Fusarium en el cultivo de la sandía.











 text new page (beta)
text new page (beta)



