Introducción
En el mundo, la diversidad de organismos vivos está sistematizada por las especies que se registran taxonómicamente a nivel genérico; a veces sin considerar las especies que se extinguen por múltiples razones biológicas y antropogénicas (McKinney 1997, Chichorro et al. 2019). Así también, aquellas especies crípticas en las que la taxonomía clásica no ha sido suficiente, y que se han identificado por poseer atributos genéticos a nivel molecular y reproductivo que las hacen diferentes de sus congéneres fenotípicos (Arias-Rodriguez et al. 2007b, 2009a). En tal contexto, se han distinguido grupos de organismos con mayor o menor vulnerabilidad, estando entre ellos los anfibios, siendo este grupo uno de los más sensibles al cambio climático global por los efectos de la evaporación, la pérdida de hábitats acuáticos y el incremento de la temperatura (Lertzman-Lepofsky et al. 2020).
El sapo costero o sapo verrugoso (Incilius valliceps Wiegmann 1833), es una especie nativa de la vertiente Mesoamericana, catalogada en preocupación menor (LC) por la Unión Internacional para la Conservación de la Naturaleza (IUCN 2020). En México no es considerada como una especie en riesgo (Barragán-Vázquez et al. 2022) con distribución que incluye los estados de Puebla, Oaxaca, Veracruz, Tabasco, Chiapas, Campeche, Yucatán y Quintana Roo; y hacia el sur hasta Costa Rica (Mendelson III et al. 2011, IUCN 2020, Klank et al. 2020). Mientras que, en las tierras bajas de Tabasco, forma parte de las tres especies de sapos de la familia Bufonidae con presencia en esta zona del trópico húmedo: sapo costero (I. valliceps), sapo de cresta larga (I. macrocristratus Firschein y Smith 1957) y el sapo de caña (Rhinella horribilis Wiegmann 1833) (Barragán-Vázquez et al. 2022).
La información biológica y la distribución geográfica del género Incilius ha sido enriquecida durante la última década (Mendelson III et al. 2011); así como todo aquello relacionado con caracteres citogenéticos (Cole et al. 1968) en número y forma de los cromosomas, que han sido importantes para establecer parámetros cromosómicos constantes en el género. Con todo ello, se ha aceptado 23 especies en México (Frost 2024).
Los estudios de citogenética en el género Incilius son mínimos y desactualizados, los últimos con más de 50 años de antigüedad (Sanders y Cross 1964, Cole et al. 1968). En dicho contexto, los antecedentes corresponden con la época donde se clasificaba a I. valliceps en el género Bufo, por lo que, se desconocía que se trataba de dos especies simpátricas con distribución en Texas, Estados Unidos de América y el Norte de México. Posteriormente, Mulcahy y Mendelson III (2000), logran separar y renombrar la especie como Bufo nebulifer; y en revisiones posteriores la reclasifican en géneros distintos (Mendelson III et al. 2015, Frost 2024, Frost et al. 2006a, 2006b). Finalmente, Frost et al. (2009) logran ubicar la especie en el género Incilius, siendo I. nebulifer o sapo nebuloso el nombre aceptado durante el desarrollo del presente trabajo. El sapo nebuloso (I. nebulifer), carece de caracterización cromosómica en la actualidad. Sin embargo, la información cariotípica que fue descrita por Cole et al. (1968), debe ser considerada para I. nebulifer, y no para el actual I. valliceps o sapo costero, debido a la idea conespecífica que se tenía en la época para ambas especies (Mendelson III et al. 2015).
Lo anterior, es un ejemplo de la necesidad de actualizar la información citogenética en I. valliceps para dilucidar todos los caracteres cariotípicos posibles, de acuerdo con su estatus taxonómico actual, como el número de cromosomas 2n, la clasificación cromosómica, el número fundamental y la posible presencia de heteromorfismo cromosómico. Por todo ello, el objetivo del presente estudio fue el de extender el discernimiento de la citogenética básica y los mecanismos que determinan el sexo genético en el sapo costero I. valliceps, mediante la caracterización de los cromosomas mitóticos de hembras y machos de especímenes recolectados en dos localidades de Tabasco, México.
Materiales y métodos
Área de recolección y determinación taxonómica
Los especímenes adultos de I. valliceps fueron recolectados en la temporada de seca (marzo-mayo) y precipitación (septiembre-noviembre) durante el 2010-2013 y 2018, debido a su poca abundancia. Se recolectaron dos hembras y cinco machos, en los márgenes y playones de la laguna El Guapacal, que es un cuerpo de agua dulceacuícola y pantanoso que se ubica en la Villa Luis Gil Pérez (17° 52՚43.05՚՚ LN y 93° 04՚25.03՚՚ LO). Así también, un espécimen macho fue obtenido de los márgenes de la planta de tratamiento de aguas residuales de la zona habitacional denominada La Lima (17° 54՚31.65՚՚ LN y 92° 56՚09.35՚՚ LO), ambas localidades del Centro, municipio del estado de Tabasco, sureste de México. La determinación taxonómica, se basó en los caracteres merísticos y morfométricos señalados en las claves para la identificación de los sapos mexicanos de la familia Bufonidae recomendados por Oliver-López et al. (2009), Canseco-Márquez y Gutiérrez-Mayén (2010), y González-Hernández et al. (2021). Así también, considerando el listado actualizado de la herpetofauna de México (Frost 2024) y la lista renovada de las especies de sapos con distribución en Tabasco por Barragán-Vázquez et al. (2022). Los adultos, se identificaron por las particularidades de la piel en la región ventral que es de tipo inmaculada, en comparación con la coloración oscura que es típica de las etapas tempranas posteriores a la metamorfosis y de manchas ventrales en los juveniles (Oliver-López et al. 2009).
Este estudio y su protocolo, fue evaluado y aprobado por la Comisión Institucional de Ética en Investigación “CIEI” de la Universidad Juárez Autónoma de Tabasco, con registro: 0726. La especie aquí mencionada, no se encuentra en la lista de especies protegidas por la NOM-059-SEMARNAT-2010 (SEMARNAT 2019). A lo largo del desarrollo de esta investigación, se atendieron y cumplieron con las Normas Oficiales Mexicanas para el uso y manejo de fauna silvestre en laboratorio, establecidos en la NOM-126-ECOL-2000 (SEMARNAT 2001a) y NOM-062-ZOO-1999 (SEMARNAT 2001b).
Procedimiento citológico y elaboración de preparaciones cromosómicas
La técnica empleada es una adaptación de la utilizada por Arias-Rodriguez et al. (2008), 2009b). Para ello, todos los especímenes fueron tratados individualmente con colchicina al 0.1% (45 µg g de peso) diluida con citrato de sodio al 0.1% a temperatura ambiente (27.0 ± 0.10 °C), mediante la inyección con una jeringa de insulina sobre la región intraperitoneal y con seis horas de exposición. Posteriormente, fueron sacrificados por hipotermia y se les extrajo el tejido hematopoyético de la médula ósea, corazón y gónadas. Después, los tejidos fueron disgregados delicadamente, mientras se hidrataron empleando una solución de citrato de sodio al 2.0% durante una hora a 38.0 ± 1.0 °C. El tejido fue prefijado (en proporción 1:1) durante 72 h con citrato de sodio al 2.0% y una solución fijadora compuesta por metanol frío (4 °C) y ácido acético (4:1). En una centrífuga, los tejidos prefijados fueron concentrados en frío (4 °C) durante 15 min a 7 000 r.p.m. y el sobrenadante se reemplazó por el fijador 4:1. Dicha operación, se realizó por cuatro o más veces o hasta que los tejidos quedaran libres de impurezas o de color blanquecino (lo que indica un buen fijado celular), para posteriormente ser conservados a 4 °C por aproximadamente un mes.
Para elaborar las preparaciones cromosómicas, las células de cada tejido fueron goteadas sobre portaobjetos fríos (previamente mantenidos en etanol a 4 °C) desde 1.80 m de altura para que reventaran y con ello, favorecer la dispersión de los campos cromosómicos. Las preparaciones cromosómicas, fueron secadas con la flama de un mechero de alcohol y teñidas (a 37.0 °C) por 50 min con Giemsa diluida al 10% en búfer de fosfatos a pH 7.0. Los residuos depositados en las preparaciones, fueron eliminados con agua destilada.
El sexo fenotípico de los especímenes, se determinó con la disección de un fragmento de tejido gonádico, posteriormente la tinción con la solución madre de Giemsa y observación bajo el microscopio óptico con el protocolo de Arias-Rodriguez et al. (2008).
Observación microscópica y elaboración del cariotipo
Las preparaciones cromosómicas fueron analizadas con el microscopio Axio Scope.A1 (Carl Zeiss®) y las mejores metafases se fotografiaron digitalmente con los objetivos 40X + 1.25X y 100X + 1.25X, mediante la AxioCam ERc5s (Carl Zeiss®) y las herramientas del programa ZEN/2011 (Carl Zeiss Michroscopy GmbH®).
La frecuencia de los números cromosómicos de las mejores dispersiones metafásicas, definidas por tener cromosomas bien dispersos, se emplearon para establecer el número modal diploide de cromosomas. Para determinar el cariotipo típico, se emplearon seis metafases mitóticas de excelente calidad y se tomaron imágenes que fueron recortadas en cromosomas individuales, de los cuales se tomaron las medidas en micrómetros (µm) del brazo corto (p) y largo (q) que sirvieron de base para constituir los pares homólogos de cromosomas.
A los valores de p y q, de cada par homólogo de cromosomas, les fue calculada la media y desviación estándar y posteriormente se les calculó la longitud relativa (LR), es decir, la longitud promedio en μm de p ó de q, fue dividida por la sumatoria total de p más q del complemento cromosómico en μm, multiplicando el valor por 100.
Los cromosomas, se ordenaron y clasificaron con base en los parámetros citogenéticos propuestos por Levan et al. (1964), como se describe a continuación:
Resultados y discusión
En los tejidos gonádico y somático que fueron empleados para el estudio; solo el de los machos de origen mitótico mostró dispersiones metafásicas, el hematopoyético de la médula ósea fue el que posibilitó el menor número de observaciones cromosómicas; y el tejido cardiaco dio la posibilidad de mayor número de dispersiones cromosómicas que permitieron el desarrollo del presente estudio. En total, se analizaron 24 preparaciones cromosómicas en mitosis, obteniéndose 72 dispersiones metafásicas de excelente calidad, buena dispersión cromosómica y enrollamiento apropiado de la cromatina.
A partir de 72 metafases analizadas, se determinó el número modal diploide de I. valliceps con 2n= 22 cromosomas, de las cuales 64 (2n= 22) dispersiones cromosómicas representaron el 89% del total examinado, seis (2n= 18) metafases el 8% y dos (2n= 26) el 3%. Por otro lado, mediante el análisis de los cálculos citogenéticos realizadas a los cromosomas mitóticos, se estableció que el cariotipo típico diploide (2n) se conforma del par cromosómico primero al sexto (pares del 1-6) de cromosomas birrámeos de tipo metacéntrico-submetacéntrico (msm) y del par cromosómico séptimo al décimo (pares del 7-10) cuatro pares de cromosomas monorrámeos de tipo telocéntrico (T) (Figuras 1a-d, Tabla 1). Mientras los cromosomas del último par cariotípico, correspondientes al par décimo primero (par 11), mostraron dos grupos o tipos de conformación: El primer grupo pertenece a los especímenes de la Villa Luis Gil Pérez, el cariotipo mostró un par cromosómico (cromosomas 21 y 22) con elementos de morfología monorrámea de posición centromérica estrictamente terminal y clasificación acrocéntrica (A) (Figuras 1a-b, Par 11).
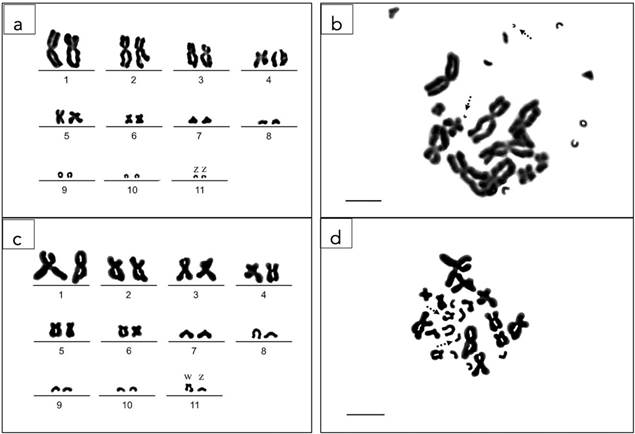
Figura 1 Cariotipo en mitosis, representativo de machos genéticos con cromosomas homogaméticos (ZZ) del sapo costero I. valliceps (a). Metafase con 2n= 22 cromosomas mitóticos (b). Cariotipo diploide de un macho fenotípico (macho no genético) con cromosomas genético sexuales de hembra heterogamética (ZW) (c). Metafase mitótica con 2n= 22 cromosomas (d). Las flechas discontinuas representan el par de cromosomas sexuales en cada metafase en b, d y las barras en b y d, representan 10 μm.
Tabla 1 Parámetros citogenéticos del cariotipo típico en mitosis del sapo I. valliceps desde la longitud promedio (µm), longitud relativa promedio (L.R.) y hasta la clasificación cromosómica.
| Par Cromosómico | Longitud (µm) p ± D.E. | Longitud (µm) q ± D.E. | L.R. de p | L.R. de q | r | i | d | Clasificación |
|---|---|---|---|---|---|---|---|---|
| 1 | 7.58 ± 0.78 | 9.60 ± 1.07 | 9.49 | 12.0 | 1.27 | 44.1 | 1.18 | msm |
| 2 | 6.30 ± 1.85 | 9.53 ± 1.54 | 7.89 | 11.9 | 1.51 | 39.8 | 2.04 | msm |
| 3 | 5.33 ± 1.14 | 7.50 ± 1.42 | 6.67 | 9.39 | 1.41 | 41.5 | 1.70 | msm |
| 4 | 3.98 ± 1.03 | 5.10 ± 1.08 | 4.98 | 6.39 | 1.28 | 43.8 | 1.24 | msm |
| 5 | 3.60 ± 1.03 | 4.95 ± 1.07 | 4.51 | 6.20 | 1.38 | 42.1 | 1.58 | msm |
| 6 | 2.40 ± 0.37 | 3.00 ± 0.42 | 3.01 | 3.76 | 1.25 | 44.4 | 1.11 | msm |
| 7 | 3.68 ± 0.96 | 4.60 | 10.0 | T | ||||
| 8 | 2.55 ± 0.47 | 3.19 | 10.0 | T | ||||
| 9 | 1.63 ± 0.25 | 2.07 | 10.0 | T | ||||
| 10 | 1.28 ± 0.32 | 1.60 | 10.0 | T | ||||
| 11 (ZZ) | 1.84 ± 0.32 | 2.30 | 10.0 | A | ||||
| 11 (Z)* | 1.01 ± 0.17 | 2.84 ± 0.22 | 10.0 | A | ||||
| 11 (W)* | 1.79 ± 0.12 | 10.0 | stt |
D.E.= Desviación estándar, p= brazo corto de cromosoma, q= brazo largo de cromosoma, msm= metacéntrico-submetacéntrico, T= telocéntrico, A= acrocéntrico, sttt= subtelocéntrico-telocéntrico, ZZ= Par cromosómico homogamético de los machos, ZW= par cromosómico heterogamético o sexual de las hembras, *= cromosoma individual.
En el análisis de las metafases del único espécimen macho de la localidad La Lima, se identificó un segundo grupo cromosómico, que manifestó conformación heterogénea del cromosoma 21; con aparente morfología birrámea de un cromosoma tipo subtelocéntrico-telocéntrico (stt) y el cromosoma 22 del citado par once, mostró morfología monorrámea de posición centromérica estrictamente terminal y clasificación acrocéntrica (A) (Figuras 1c-d, Par 11).
La longitud promedio del primer par cromosómico del grupo de los birrámeos de tipo metacéntrico-submetacéntrico (msm) fue de 17.18 ± 1.85 µm y del último par sexto de tipo msm birrámeo fue de 5.40 ± 0.79 µm. Así mismo, los cálculos de los cromosomas del cariotipo que corresponden al grupo de los monorrámeos y al séptimo par cromosómico telocéntrico (T), fue de 3.68 ± 0.96 µm y al décimo par de tipo T de 1.28 ± 0.32 µm. Finalmente, el par cromosómico onceavo del grupo único de monorrámeos de tipo acrocéntrico (A) tienen medidas promedio de 1.84 ± 0.32 µm en su último par cromosómico (Tabla 1).
El complemento cariotípico de I. valliceps se caracterizó de dos fórmulas cromosómicas en mitosis; la primera de 12 msm + 8 T + 2 A (con número total de brazos cromosómicos o número fundamental (NF) de NF= 34 brazos) y la segunda fórmula de 12 msm + 8 T + 1 stt + 1 A (con NF= 36 brazos) (Figuras 1 a-d, Tabla 1). En ninguna de las metafases que fueron analizadas detalladamente, se pudieron observar presencia de estructuras secundarias como constricciones satelitales o presencia de microcromosomas.
La presencia estable del número modal de 2n= 22 cromosomas mitóticos en el cariotipo típico del sapo costero I. valliceps que se reporta en este estudio y los datos de los escasos estudios citogenéticos descritos en el género Incilius (Bachmann 1970, Bogart 1972), indican que el número cromosómico de 2n= 22 cromosomas reportado en I. valliceps, confirma la correlación citotaxonómica y filogenética de las especies de Incilius con los miembros basales de la familia Bufonidae.
Así también, con los conteos cromosómicos diploides de los estudios tempranos en el grupo (Bachmann 1970, Beck y Mahan 1979) y los más recientes (Córdova y Descailleaux 1996, Franco-Navia et al. 1999). Mientras que, los escasos registros de metafases con conteos cromosómicos de 2n= 18 y 2n= 26 cromosomas observados en este estudio, se atribuyen a variaciones de la técnica citogenética, como son la pérdida de elementos cromosómicos, el aislamiento o la integración de uno o más cromosomas, originado por el traslape de metafases cercanas durante el goteo del material biológico, como ha sido reportado en diferentes especies de moluscos, peces, anfibios y reptiles por Arias-Rodriguez et al. (2007a, 2011) y Hernández-Guzmán et al. (2011, 2014, 2015).
Por otro lado, con base en las observaciones de los cromosomas metafásicos en mitosis de los machos adultos, el cariotipo típico diploide (2n) de I. valliceps está conformado por dos fórmulas cromosómicas no esperadas; la primera de 12 msm + 8 T + 2 A (con número total de brazos cromosómicos o número fundamental de NF= 34 brazos) y la segunda fórmula de 12 msm + 8 T + 1 stt + 1 A (con NF= 36 brazos). La abundante presencia de cromosomas birrámeos de tipo metacéntrico-submetacéntrico (msm) en los cariotipos de los bufónidos, es una particularidad citogenética común en los miembros del grupo con muy pocas excepciones en reducido número de especies (Bachmann 1970, Bogart 1972, Skorinov et al. 2018, Bruschi et al. 2019); en ello, la confirmación de que los cromosomas cariotípicos que corresponden a los pares cromosómicos del primero al sexto (pares del 1-6) son birrámeos, siendo congruentes con los hallazgos previos en la familia (Figuras 1 a-d) y en acuerdo con Bachmann (1970), Bogart (1972), Skorinov et al. (2018) y Bruschi et al. (2019). Sin embargo, la abundante presencia de cromosomas monorrámeos de tipo telocéntrico (T) del par cromosómico séptimo al décimo primero (pares del 7-11) del cariotipo típico del sapo costero encontrados en el presente estudio y de dos variantes cariotípicas para un mismo sexo fenotípico, se desvían del patrón citológico común en los bufónidos.
En el caso particular del hallazgo en los machos fenotípicos del sapo I. valliceps, los resultados de las observaciones citológicas hacen referencia a la presencia de dos tipos de cariotipos; debido a las diferencias observadas en el par cromosómico once (cromosomas 21 y 22) o último par del cariotipo de I. valliceps. Lo anterior, posiblemente es un caso excepcional de reversión sexual de la hembra genética a macho fenotípico, situación que se ha comprobado en otros anuros de vida silvestre, especialmente en Rana clamitans (Lambert et al. 2019).
Las diferencias identificadas son complejas de comparar desde el punto de vista del valor muestral, reproductivo y citológico, esto último debido a la escasez de estudios de tipo cariológico en los miembros del género Incilius. Si bien el hallazgo de la variación genética en un espécimen de I. valliceps en la localidad La Lima es significativo, surge la interrogante sobre la prevalencia de esta variación en el resto de la población de la especie en dicha localidad. Esta incertidumbre se relaciona con la escasa abundancia de I. valliceps, lo que limita la cantidad de muestras disponibles para un estudio más amplio. En el caso del reducido número de individuos recolectados y empleados para el presente estudio o valor muestral, obedeció a que I. valliceps es una especie poco abundante en la zona de recolecta (localidades de La Lima y Villa Luis Gil Pérez, municipio de Centro, Tabasco, México) en comparación con la abundancia de R. horribilis o sapo cañero a pesar de que ambas especies son nativas de la región sureste y península de Yucatán en México (Lee 2000).
Desde el punto de vista estadístico-muestral, el número de individuos recolectados, no afecta las observaciones cariológicas registradas bajo el microscopio óptico; es decir no hay efectos en la estructura de los cariotipos, debido a que los caracteres cariotípicos o citológicos son estables en número cromosómico, forma y tamaño de los brazos cromosómicos, entre las células de los especímenes y entre los especímenes de una misma especie (Hernández-Guzmán et al. 2011, Bruschi et al. 2019). Así también, por ejemplo, en los estudios de citogenética realizados por Bruschi et al. (2019) en siete especies de Rhinella, en dos de ellas, el número de especímenes empleados para el estudio fue de tan solo tres individuos para dos de estas especies, y de estos individuos, dos fueron macho y uno hembra. Tal circunstancia indica que la disponibilidad de especímenes, es una condicionante que no depende del investigador o recolector, pero sí de la abundancia relativa de la especie. En dicho sentido, en el estudio de riqueza y abundancia de anfibios del Parque Estatal de la Sierra de Tabasco, México por Gerónimo-Torres et al. (2022), se señala que solo registraron doce especímenes de I. valliceps a lo largo de un estudio de siete meses, dos de ellos en la selva y ocho en vegetación secundaria. Por ello, el estudio realizado en I. valliceps, es congruente con el número de especímenes recolectados, pues se enfatiza que la abundancia del sapo costero en las tierras bajas del sureste de México es reducida en diferentes áreas geográficas. Estudios previos en R. clamitans o rana clamitans indican que la presencia de reversión sexual natural, puede llegar a representar del 2 al 16% de los individuos en una población (Lambert et al. 2019); por lo que, el hallazgo de solo un ejemplar revertido en la localidad de La Lima (Tabasco, México) resulta plausible, siendo que ello representa el 12.5% del total de especímenes muestreados.
Desde el punto de vista citológico las variaciones en la estructura cariotípica, es posible que se originen por dos tipos de circunstancias. La primera está asociada a los efectos de los tratamientos citológicos y la segunda posibilidad, debido a efectos secundarios durante el desarrollo embrionario y la diferenciación sexual. En el primer caso, se ha documentado en varias especies, que la colchicina como alcaloide necesario para inhibir la división celular durante la metafase, puede originar en dependencia del tiempo de exposición y de la concentración, reducción en el tamaño de los cromosomas debido al alto grado de compactación, como secuela secundaria que se produce durante la formación de la cromatina, en la profase del ciclo celular (Morais et al. 1991, Arias-Rodriguez et al. 2006, Koyani y Saiyad 2011). Sin embargo, los efectos de la colchicina no ocasionan deformaciones drásticas en la estructura del cromosoma, por lo que las diferencias identificadas en los cromosomas (par 11) no pueden adjudicarse como efectos derivados del uso de la colchicina (Figuras 1 a-c), que es necesaria y empleada para el desarrollo de estudios citológicos como el actual (Morais et al. 1991, Arias-Rodriguez et al. 2006, Arias-Rodriguez et al. 2009b). La segunda circunstancia o explicación sobre el origen de las diferencias cariotípicas del par cromosómico once (Figuras 1 a y 1c); puede estar ligada al heteromorfismo entre uno de los pares cromosómicos de los cariotipos de las hembras y el homomorfismo cromosómico de los machos de una especie en particular. Normalmente esta situación es el reflejo de un mecanismo de determinación sexual regulado por el sexo heterólogo (ZW); y que se ha documentado ampliamente en las hembras de los anfibios (Schmid et al. 1991, Ayling y Griffin 2002, Smith y Voss 2009). Asumiendo con ello, que las hembras son aquellas que tiene como determinante genético el sexo heterogamético (ZW) y los machos el sexo homogamético (ZZ) (Schmid et al. 1991, Ayling y Griffin 2002, Smith y Voss 2009).
Evidencias recientes, sugieren que los cambios en el uso de suelo de vegetación original a una condición de uso agrícola, suburbano y urbano han favorecido de forma directa, con incrementos de acuerdo con el grado de desarrollo urbano, la liberación continua de disruptores endocrinos (pesticidas agrícolas, estronas, fitoestrógenos, entre otros) que han afectado las poblaciones silvestres de anfibios (Kloas 2002, Smits et al. 2014, Lambert et al. 2015). Por ejemplo, desbalanceando y modulando la proporción de sexos natural de la rana R. clamitans que en principio está genéticamente determinada (hembras ZW vs. Machos ZZ); pero promoviendo que los machos genotípicos (o genéticamente determinados a ser machos) cambien el sexo genéticamente determinado (ZZ) durante la metamorfosis hacia el de hembras (feminización o reversión sexual) fenotípicas (Lambert et al. 2015).
En Tabasco, se ha reportado la presencia de contaminantes ambientales como hidrocarburos y metales pesados en los ecosistemas acuáticos y terrestres de la región, (Villanueva y Botello 1992, Fiedler et al. 2009, De la Cruz-Pons et al. 2012, Ramos-Herrera et al. 2012) entre otros compuestos de origen urbano aún no identificados, debido a la carencia de estudios. Sin embargo, los componentes xenobióticos junto con los hidrocarburos y metales pesados, han sido señalados como responsables del origen de los microcromosomas tipo “B” o microfragmentos de cromatina, cuyo origen son la fragmentación de los cromosomas somáticos que están presentes de modo atípico en el genoma de algunas especies acuáticas de Tabasco como: Petenia splendida (Günther 1862), Atractosteus tropicus (Gill 1863), Smilisca baudinii (Duméril y Bibron 1841), Kinosternon leucostomun leucostomum (Duméril y Bibron 1851), Trachemys venusta venusta (Gray 1856) y Staurotypus triporcatus (Wiegmann 1828) (Arias-Rodriguez et al. 2007a, 2008, 2009b, Hernández-Guzmán et al. 2011, 2014).
El espécimen macho recolectado en la localidad de La Lima, se colectó en un hábitat perturbado por desechos y componentes de las aguas residuales de la zona residencial. En este sentido, considerando el concepto y la importancia de los xenobióticos como sustancias extrañas o ajenas al organismo, que tienen su origen en todos aquellos productos de origen natural, industrial o artificial, como los fármacos, aditivos, contaminantes ambientales entre otros (Bender y Murray 2016) y los efectos en los ecosistemas naturales y los organismos que allí habitan como ha sido ampliamente documentado (Kloas 2002, Arias-Rodriguez et al. 2007b, 2008, 2009b, Hernández-Guzmán et al. 2011, 2014, Smits et al. 2014, Lambert et al. 2015). Se puede considerar que las variaciones en el par 11 de cromosomas que integran los dos cariotipos del sapo costero I. valliceps observadas en este estudio, corresponden a una hembra genética o ZW que probablemente por influencia de disruptores endocrinos y genéticos (xenobióticos), modificó los mecanismos que conducen a determinar el sexo genético normal durante los primeros estadios de desarrollo embrionario (o reversión sexual) hacia la de macho fenotípico. El hallazgo no es una sorpresa, si consideramos la hipótesis documentada por Arias-Rodriguez et al. (2007a, 2008, 2009b) y Hernández-Guzmán et al. (2014) sobre la presencia de microcromosomas “B” en P. splendida, A. tropicus, S. baudinii, K. l. leucostomum, T. v. venusta y S. triporcatus, pues ambos procesos (microcromosomas “B” vs. reversión sexual) tienen señalamientos de un origen basado en los efectos de disruptores ambientales de origen antropogénico.
Si bien, los estudios citogenéticos, como el detallado en el presente reporte, no son del todo concluyentes, siguen abriendo ventanas de oportunidades ya que son valiosos porque contribuyen con la descripción de información sobre la genética básica, la composición cromosómica de las especies. Lo que permite avanzar en la comprensión de su evolución y las relaciones taxonómicas de la amplia biodiversidad mexicana. Se confirmo que el cariotipo mitótico del sapo costero I. valliceps está conformado por 22 cromosomas, como ha sido documentado en otras especies de sapos en la familia Bufonidae. Existe variación en la clasificación cromosómica, por la presencia de cromosomas de tipo birrámeos y monorrámeos, una característica única en la familia Bufonidae. También se identificaron caracteres cariológicos que concuerdan con la anatomía de los cromosomas heteromórficos o sexuales. Lo anterior, evidencia de la importancia de continuar con nuevas investigaciones que permitan monitorear desde la perspectiva citogenética, la composición cromosómica y cariotípica de otras poblaciones de I. valliceps, así como de otras especies de anfibios nativos, que permitan revelar caracteres citogenéticos hasta ahora desconocidos y que no han sido descritos.











 text new page (beta)
text new page (beta)



