La presencia de arsénico (As) en suelos y aguas de riego representa una amenaza crítica para la agricultura sostenible, la calidad de los cultivos y la salud pública. Regiones como México, India, Bangladesh y Chile han reportado concentraciones elevadas de As dentro del suministro de la seguridad alimentaria (Bhattacharya et al., 2010; Ruiz- Huerta et al., 2017). Además, el As es altamente tóxico y móvil en medios agrícolas. Por ello, organismos como la Organización Mundial de la Salud (OMS) y la Organización de las Naciones Unidas para la Agricultura y la Alimentación (FAO) han establecido límites permisibles en aguas, suelos y alimentos para reducir los riesgos asociados.
En México, las normas NOM-127-SSA-2021 y NOM-147-SEMARNAT/SSA1-2004 regulan la presencia de As en agua potable y suelos agrícolas, estableciendo valores máximos entre 0.025 mg L-1 en agua y 22 mg kg-1 en suelos (Secretaría de Salud, 2022; SEMARTAT, 2007). Si bien existen métodos tradicionales de remoción como la coagulación, filtración y el intercambio iónico, presentan limitaciones en eficiencia y costos (Kumar et al., 2019).
Ante este escenario, la nanotecnología ha surgido como una alternativa prometedora, en especial mediante el uso de nanomateriales inmovilizados, que ofrecen mayor selectividad, estabilidad y eficiencia en la adsorción de As. Por lo que, este articulo presenta una revisión crítica del uso de nanomateriales inmovilizados en la remediación del suelo y aguas de riego contaminados con As, incluyendo estudios de caso, mecanismos de acción, comparaciones tecnológicas y su evaluación ambiental.
Desarrollo
Impacto del arsénico en la agricultura
El arsénico en suelos agrícolas compromete la salud del ecosistema y la productividad de cultivos (Ruíz-Huerta et al., 2017). En regiones mexicanas como la Comarca Lagunera, el uso de agua contaminada con As ha demostrado alterar el pH, reducir la disponibilidad de nutrientes esenciales y afectar la microbiota edáfica, disminuyendo la calidad de los cultivos y aumentando su toxicidad por bioacumulación (Osuna-Martínez et al., 2021).
Fuentes de arsénico en sistemas agrícolas
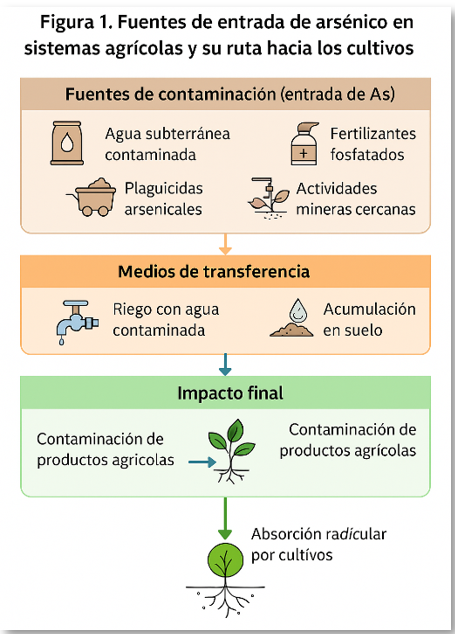
El As tiene orígenes tanto natural como antropogénico. En su forma natural, se libera por la erosión de minerales arsenicales (arsenopirita), la actividad volcánica y la disolución de minerales en acuíferos ricos en As. Por otro lado, las fuentes antropogénicas incluyen el uso de pesticidas arsenicales, fertilizantes contaminados, riego con aguas subterráneas contaminadas, actividad minera y desechos industriales (Jiménez et al., 2023). La Figura 1 resume estas fuentes.
Efectos del As en la fertilidad del suelo
El As interfiere directamente con la dinámica del suelo agrícola, tales como: Microbiota: Inhibe bacterias y hongos beneficiosos como Rhizobium y Mycorrhizae afectando ciclos de nitrógeno y fosforo, y reduce la biodiversidad microbiana. pH del suelo: en suelos ácidos, el As posee mayor movilidad y biodisponibilidad; en suelos alcalinos puede formar complejos que inmovilizan nutrientes. Nutrientes esenciales: Compite con el fósforo y disminuye la disponibilidad de hierro (Fe), zinc (Zn) y manganeso (Mn), alterando procesos metabólicos, tales como la fotosíntesis y síntesis de proteínas (Singh y Srivastava, 2020; Beniwal et al., 2023).
Contaminación de cultivos y seguridad alimentaria
El As se bioacumula en cultivos comestibles, afectando su valor nutricional y generando riesgos toxicológicos en seres vivos. Su absorción depende de las características fisiológicas del cultivo. El Cuadro 1 detalla los cultivos más afectados y sus riesgos asociados, incluyendo arroz, trigo, maíz y hortalizas.
Cuadro 1 Cultivos más afectados por la absorción de As.
| Cultivo | Descripción | Daños o repercusiones específicas del As en el cultivo | Efectos en la salud | Referencia |
|---|---|---|---|---|
| Arroz (Oryza sativa L.) | Cultivo altamente susceptible al As debido a su crecimiento en suelos inundados, donde el As+3 es más soluble y biodisponible. | Alteración en el metabolismo del silicio, estrés oxidativo, inhibición del crecimiento radicular y menor rendimiento de grano. | Exposición prolongada puede causar cáncer de piel, pulmón y vejiga; además de afectar el sistema nervioso y cardiovascular. | Mitra et al. (2017); FAO (2022) |
| Trigo (Triricum spp.) | Absorbe As en menor medida que el arroz, pero puede acumularlo en los granos y reducir la calidad nutricional. | Reducción en la germinación, menor biomasa aérea y radicular, interferencia en el metabolismo del fósforo. | Puede afectar la biodisponibilidad de hierro y zinc, aumentando el riesgo de anemia y deficiencias nutricionales. | Bhattacharya et al. (2010) |
| Maíz (Zea mays L.) | Cultivo base de la alimentación en México, absorbe As del suelo y agua de riego, con acumulación en raíces, hojas y granos. | Daño en tejidos vasculares, reducción de clorofila, menor crecimiento foliar y acumulación de As en granos. | El consumo prolongado puede generar alteraciones metabólicas, menor desarrollo en niños y problemas hepáticos y renales. | Huerta y Hernández (2012) |
| Hortalizas de raíz (zanahoria, papa, betabel) | Crecen en contacto directo con suelos contaminados, lo que facilita la absorción de As en sus tejidos. | Afección en la calidad del tubérculo, deformaciones morfológicas, acumulación de As en tejidos comestibles. | Causa toxicidad crónica, afectando el sistema digestivo y la absorción de nutrientes esenciales | Upadhyay et al. (2019) |
| Hortalizas de hoja (espinaca, lechuga, acelga) | Absorben As a través del agua de riego, acumulándolo en hojas y reduciendo su calidad nutricional. | Clorosis, necrosis marginal, estrés hídrico incluido y disminución del contenido de proteínas y antioxidantes. | La acumulación en hojas puede provocar intoxicaciones leves a moderadas, afectando el sistema nervioso y hepático. | Laizu (2008) |
Impacto en la calidad nutricional de los alimentos
Más allá de su toxicidad, el As deteriora la calidad nutricional de los alimentos al alterar el metabolismo vegetal.
Absorción de nutrientes
Compite con el fósforo y reduce la disponibilidad de Fe, Zn y Mn, afectando el crecimiento y contenido nutricional (Beniwal et al., 2023).
Composición química
Afecta la síntesis de proteínas, azucares y antioxidantes, lo que deteriora el valor energético, sabor y calidad del alimento (Huerta y Hernández, 2012; Ruíz-Huerta et al., 2017; Upadhyay et al., 2019; Beniwal et al., 2023).
Disponibilidad en humanos
Reduce la absorción intestinal de minerales, elevando el riesgo de anemia, inmunodeficiencias y enfermedades óseas (Camacho et al., 2011; Singh y Srivastava, 2020).
Casos documentados y cultivos afectados en el mundo
Estudios en Bangladesh, India, Argentina, México y otros países, muestran que el As presente en suelos y aguas de riego ha causado afectaciones severas a cultivos y salud pública. El Cuadro 2 sintetiza estos casos, mostrando su distribución geográfica, cultivos involucrados y consecuencias sanitarias como hidroarsenicismo, cánceres y deficiencias nutricionales (Bhattacharya et al., 2010; Alarcón Herrera et al., 2020).
Cuadro 2 Impacto del As en cultivos agrícolas.
| País | Situación | Cultivos afectados | Impacto en la salud | Referencia |
|---|---|---|---|---|
| Bangladesh/India | Contaminación de agua subterránea con As (agua potable y cultivos) | Arroz | Cáncer (CA) de piel, pulmón y vejiga, enfermedades cardiovasculares (CV) y diabetes | Bhattacharya et al. (2010); Mitra et al. (2017) |
| Argentina/México | Alta concentración de As en el agua de riego | Maíz y hortalizas | Hidroarsenicismo crónico (HC), CA de vejiga, riñón y pulmón; 4 millones de personas expuestas | , (2008); Huerta y Hernández, (2012) |
| Chile | Contaminación por As (minería) en agua y suelo | Hortalizas y frutas | Aumento regional en tasas de CA y enfermedades CV | Upadhyay et al. (2019) |
| México | Altos niveles de As en agua en zonas agrícolas | Maíz y frijol | HC, riesgo elevado de CA: comunidades rurales afectadas. | Huerta y Hernández, (2012); Alarcón-Herrera et al. (2020) |
| Estados Unidos de América | Presencia de As en pozos, en regiones agrícolas. | Arroz | Riesgo de CA y CV por consumo de arroz contaminado: miles expuestos. | Meharg et al. (2009); USGS (2018) |
El As en sistemas agrícolas no solo compromete el rendimiento de los cultivos, sino que también disminuye su valor nutricional, pone en riesgo la salud pública y limita la seguridad alimentaria en zonas rurales.
Remoción de As en agua de riego mediante nanomateriales inmovilizados
El uso de nanomateriales inmovilizados ha surgido como una estrategia innovadora en la remediación agrícola, ofreciendo soluciones eficientes y sostenibles para remover As en suelos y aguas de riego. Su integración en matrices sólidas mejora la estabilidad, facilita su recuperación y permite una aplicación controlada en campo.
Nanopartículas de hierro cero Valente
Las nanopartículas (Nps) de hierro cero Valente (nZVI), se han usado para la descontaminación de aguas tanto de metales pesados como de compuestos orgánicos clorados, debido a su alta reactividad y capacidad de adsorción. La inmovilización de estas Nps en matrices sólidas, como polímeros o soportes inorgánicos mejora su estabilidad y facilita su aplicación en entornos agrícolas.
Hallazgos como los de Qu et al. (2019) demostró que las nZVI inmovilizadas en una matriz de quitosano fueron efectivas en la reducción de cromo hexavalente (Cr (VI)) en suelos contaminados, logrando una disminución significativa de la concentración de Cr(VI) en un periodo corto (Qu et al., 2019). A la par, en China, la aplicación de nZVI inmovilizadas en suelos agrícolas contaminados con As resultó en una reducción del 70% de la concentración de As disponible, mejorando la calidad del suelo y la seguridad de los cultivos.
Nanoarcillas
Las nanoarcillas, como la montmorillonita, bentonita y otras arcillas esmecitícas, se han usado para la remediación de suelos, debido a su alta superficie específica y capacidad de intercambio catiónico propiedades aptas para adsorber contaminantes y mejorar las propiedades físicas del suelo. Su inmovilización en matrices orgánicas o inorgánicas permite una aplicación más controlada y eficiente (Almasri et al., 2018; Baigorria et al., 2021).
En este sentido, la incorporación de nanoarcillas en suelos contaminados con pesticidas organoclorados mostró una reducción del 85% en la concentración de estos compuestos, además de mejorar la retención de agua y la estructura del suelo. Además, en España, la aplicación de nanoarcillas inmovilizadas en suelos vitivinícolas contaminados con cobre llevó a una disminución del 60% en la concentración de cobre disponible, promoviendo la recuperación de la microbiota del suelo y la salud de las vides.
Óxidos metálicos
Los nanocompuestos de óxidos metálicos, como el óxido de zinc (ZnO) y el óxido de magnesio (MgO), poseen propiedades antimicrobianas y de adsorción de contaminantes. Su inmovilización en matrices poliméricas o cerámicas permite su uso en la remediación de suelos y aguas agrícolas (Gao et al., 2021). La aplicación de nanocompuestos de ZnO inmovilizados en una matriz de alginato mostró eficacia en la remoción de bacterias patógenas y la adsorción de metales pesados en el agua de riego (Gao et al., 2021).
En México, la utilización de filtros cerámicos impregnados con nanocompuestos de óxidos metálicos permitió la purificación de agua de riego con problemas de calidad de agua. En regiones como Coahuila y Durango, la implementación de tecnologías de remediación del agua de riego ha demostrado resultados positivos. El uso óxidos de hierro, como Fe3O4 o Fe2O3, inmovilizados en sistemas de filtración ha permitido reducir significativamente los niveles de As en el agua para el riego de cultivos de maíz y trigo (Morales et al., 2012).
Por ejemplo, en Guanajuato, México, el uso de zeolitas naturales ha ayudado a mejorar la calidad del agua de riego en zonas afectadas por la contaminación con distintos metales pesados, este método ha permitido a los agricultores reducir los niveles de metales pesados en cultivos, garantizando así una mayor seguridad alimentaria (Armienta et al., 2020).
Las Nps de TiO2 inmovilizadas son conocidas por sus propiedades fotocatalíticas, utilizadas para la degradación de contaminantes orgánicos en agua y suelo (Yu et al., 2013). La inmovilización de Nps TiO2 en soportes sólidos evita su dispersión en el medio ambiente y facilita su recuperación. Un estudio reportó que TiO2 inmovilizado en esferas de sílice fue efectivo en la degradación de pesticidas en el agua de riego, logrando una remoción del 90% de los contaminantes bajo irradiación solar (Yu et al., 2013).
Mecanismos de adsorción y eficiencia de nanomateriales
La remoción de As en suelos y agua de riego mediante los nanomateriales ocurre a través de diversos mecanismos fisicoquímicos que dependen de la composición, estructura y funcionalización de los materiales. La interacción entre el As y los nanomateriales determina su eficiencia en la adsorción, influenciadas como el pH, la concentración de As, la competencia con otros iones y la estabilidad del nanomaterial en el medio agrícola. Los principales mecanismos de adsorción de As por nanomateriales incluyen.
Intercambio iónico
En el que implica la sustitución de iones arsenicales en la superficie del nanomaterial (eg. óxidos de hierro funcionalizados), común en zeolitas modificadas y nanoarcillas.
Quimisorción
Es la formación de enlaces covalentes estables o coordinados fuertes, especialmente en nZVI (Fe0) y algunos óxidos metálicos como Fe3O4 y MnO2. Las nZVI actúan principalmente por reducción de As+3 a formas insolubles y quimisorción sobre óxidos de hierro formados in situ.
Adsorción electrostática
Atrae especies arsenicales con carga opuesta, depende del pH, común en nanocompuestos funcionalizados con grupos amino, como nanoarcillas con modificaciones orgánicas y nanopartículas dopadas con biopolímeros. En el caso de las nanoarcillas como la montmorillonita, retiene As+5 mediante intercambio iónico con aniones como fosfato o sulfato.
Fotocatálisis
En el caso de las NPs de TiO2 inmovilizado, oxida As+3 a As+5 y favorece su posterior adsorción en la superficie activa, degradando compuestos orgánicos asociados lo que facilita la adsorción del As por oxidación asistida por luz.
Atrapamiento físico
En matrices porosas, como soportes cerámicos o poliméricos, que aumentan la retención del As por difusión y retención en canales internos.
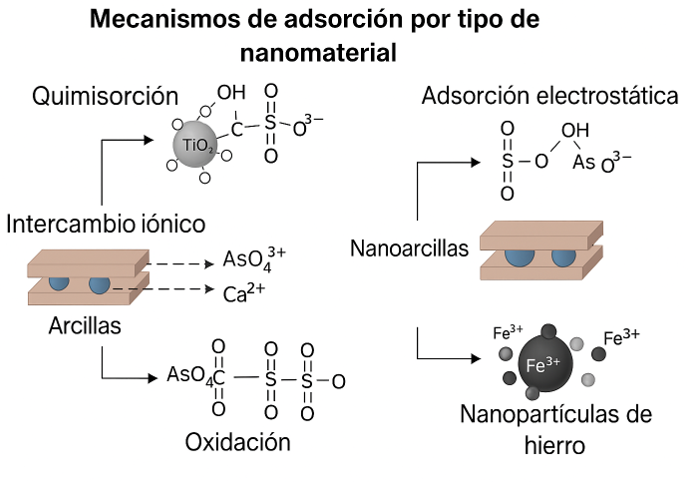
La Figura 2 es una representación esquemática de los principales mecanismos fisicoquímicos de adsorción involucrados en la remoción de As mediante nanomateriales inmovilizados: quimisorción en NPs de TiO2, adsorción electrostática en nanoarcillas, intercambio iónico en arcillas y procesos de oxidación en presencia de NPs de Fe. Las estructuras reflejan interacciones a nivel molecular típicas de cada sistema.
Estos mecanismos en conjunto permiten que los nanomateriales inmovilizados superen las limitaciones técnicas de los métodos tradicionales, la eficiencia depende del tipo de nanomaterial, la especie arsenical (As+3 o As+5), pH, competencia iónica o condiciones del medio. A diferencia de métodos como la coagulación, intercambio iónico o fitorremediación, los nanomateriales inmovilizados presentan mayor eficiencia (aproximadamente del 95%), menor generación de residuos y un potencial de reutilización y regeneración. En el Cuadro 3 se presentaron algunos materiales que superan las limitaciones técnicas y ambientales de tecnologías tradicionales.
Cuadro 3 Capacidad de adsorción de As en nanomateriales inmovilizados.
| Nanomaterial | Capacidad de adsorción (mg As g-1) | Mecanismo de adsorción | Condiciones óptimas (pH, temperatura, etc.) | Referencia |
|---|---|---|---|---|
| Nps de hierro cero Valente (nZVI) | 40-70 | Quimisorción e intercambio iónico | pH 6-8, condiciones aeróbicas | Kang et al. (2019); Qu et al. (2019) |
| Óxidos de manganeso dopados | 30-60 | Oxidación de As+3 y adsorción electrostática | pH 4-7, temperatura moderada | Xie et al. (2022) |
| Nanocompuestos de carbono | 25-55 | Adsorción electrostática y quimisorción | pH 6-9, presencia de materia orgánica | Toor et al. (2015); Gautam et al. (2021) |
| NPs de TiO2 inmovilizadoras | 15-40 | fotocatálisis y adsorción superficial | pH 5-7, irradiación solar moderada | Yu et al. (2013). |
| Nanoarcillas (montmorillonita) | 10-35 | Intercambio catiónico y adsorción por superficie cargada | pH 4-6 humedad moderada | Almasri et al. (2018);Baigorria et al. (2021) |
| Zeolitas naturales modificadas | 20-50 | Intercambio iónico y atrapamiento en canales cristalinos | pH 6-8 condiciones de campo | Morales et al. (2012); Armienta et al. (2020) |
Estudios de caso México
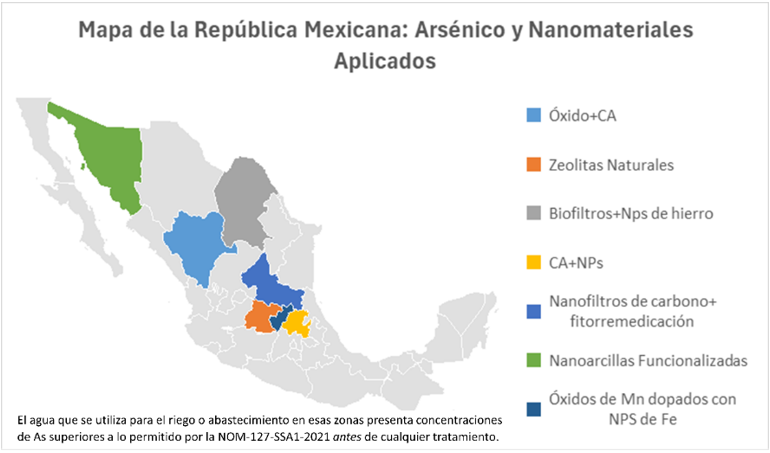
Diversos nanomateriales se han utilizado de manera efectiva para remover metales pesados del agua y suelos en distintas regiones del país. En Durango, se han empleado Nps de óxidos y filtros de carbón activado, con resultados eficientes en la adsorción de As y Pb, reduciendo su solubilidad (García y Bonilla, 2015; Zhao et al., 2020). En Guanajuato, los filtros de zeolita natural han demostrado poseer una alta capacidad para atrapar As y Hg en sus poros (Sridhar y Adeyemo, 2009; Morales et al., 2012).
Así mismo, en Coahuila, se han desarrollado biofiltros combinados con Nps de hierro para remover As y Cd mediante procesos biológicos asistidos por microorganismos (Finnegan y Chen, 2012; Wang et al., 2022). En Hidalgo, el uso de carbón activado con Nps ha mostrado alta eficiencia para remover Pb y Hg, mejorando las propiedades adsorbentes del sistema (Lui et al., 2021; García y Pérez, 2021).
Al mismo tiempo, en San Luis Potosí ha reportado buenos resultados en sistemas de fitorremediación con nanofiltros de carbono, que permiten la retención de As y Pb en combinación con plantas que absorben contaminantes (López y Martínez, 2020; Zhao et al., 2020). En Sonora, las nanoarcillas funcionalizadas con grupos aminos han demostrado gran capacidad para reducir la disponibilidad de As y Pb en suelos agrícolas (Martínez et al., 2020).
Finalmente, en Querétaro, los óxidos de manganeso dopados con Nps de hierro han sido eficaces en la estabilización de As y Cd en suelos contaminados (Figura 3) (Ramírez et al., 2021). Estas aplicaciones no solo han demostrado eficiencia técnica, sino que han contribuido a mejorar la salud ambiental y la calidad de vida en comunidades rurales expuestas a altos niveles de As. En varios casos, se ha observado una reducción en afecciones asociadas al consumo de agua contaminada y un aumento en la confianza de los agricultores hacia el uso seguro del recurso hídrico para sus cultivos.
Comparación con métodos tradicionales en la remoción de arsénico
Históricamente, el As en sistemas agrícolas ha sido tratado mediante métodos convencionales como la coagulación química, filtración con carbón activado, intercambio iónico y fitorremediación. Sin embargo, estos enfoques presentan limitaciones significativas: baja eficiencia a bajas concentraciones, y dificultad para escalar en campo.
En contraste, los nanomateriales inmovilizados ofrecen ventajas clave: mayor eficiencia de adsorción (hasta 95%), bajo impacto ambiental, y posiblemente de regeneración. Inmovilizados en soportes como biopolímeros, zeolitas o bichar, mejoran la estabilidad, reducen lixiviación y facilitan su recuperación. El Cuadro 4 presentó una comparación entre métodos tradicionales y nanomateriales inmovilizados considerando eficiencia, costo y sostenibilidad.
Cuadro 4 Comparación de métodos tradiciones vs nanomateriales inmovilizados.
| Método | Eficiencia (%) | Costo en dólares ($ m-3 tratado) | Limitaciones | Impacto ambiental | Referencia |
|---|---|---|---|---|---|
| Coagulación con sales de hierro | 50-70 | 1.5-3 | Genera lodos tóxicos | Moderado (manejo de residuos) | WHO (2022); Smith et al. (2019) |
| Filtración con carbón activado | 30-50 | 0.5-1.2 | Menos efectivo en agua con materia orgánica | Bajo | Meharg et al. 2017); Zhao et al. (2018); FAO (2022) |
| Intercambio iónico | 60-80 | 2-4 | Requiere regeneración de resinas | Generación de residuos químicos | Kim y Benjamin (2004) |
| Fitorremediación | 20-40 | 0.3-1 | Proceso lento | Beneficioso (absorción de biomasa) | Atabaki et al. (2020);Alka et al. (2021) |
| Nanomateriales inmovilizados | 70-95 | 2.5-4.5 | Requiere optimización en campo | Bajo (puede regenerarse y reutilizarse). | Yu et al. (2013);Qu et al. (2019); Vaddi et al. (2024) |
Evaluación ambiental de los nanomateriales inmovilizados
A pesar de su eficiencia, el uso de nanomateriales requiere una evaluación integral para asegurar su compatibilidad con el entorno agrícola y considerar los siguientes subtemas.
Biodegradabilidad
Los nanomateriales basados en biopolímeros como quitosano o celulosa son preferibles, ya que se degradan naturalmente sin dejar residuos persistentes. En cambio, las nanopartículas metálicas pueden acumularse y alterar la estructura del suelo a largo plazo.
Toxicidad a la microbiota
Algunas nanopartículas (eg. plata. Óxidos de Zn o Ti) tienen propiedades antimicrobianas que pueden reducir poblaciones benéficas del suelo, como bacterias fijadoras de nitrógeno o micorrizas. Se recomienda usar soportes naturales para minimizar su toxicidad.
Riesgo de lixiviación
Nanomateriales no estabilizados pueden migrar hacia cuerpos de agua cercanos. Su inmovilización en matrices solidas reduce este riesgo, manteniendo el material en el sitio de aplicación y evitando la contaminación secundaria.
Riesgos ecológicos
Aunque los nanomateriales inmovilizados presentan técnicas, también implican riesgos ecológicos que deben ser considerados antes de su aplicación a gran escala. Uno de los principales es la alteración del microbiota del suelo, ya que algunos nanomateriales, como los óxidos de zinc y plata, tienen propiedades antimicrobianas que pueden reducir poblaciones de microorganismos benéficos, como bacterias fijadoras de nitrógeno o micorrizas.
Además, si no están adecuadamente estabilizados, los nanomateriales pueden migrar en el ambiente, acumularse en zonas sensibles como cuerpos de agua o raíces de plantas no objetivo y modificar procesos edáficos esenciales. Esta movilidad y persistencia ambiental podría generar efectos ecotóxicos indirectos sobre la cadena trófica.
Estrategias de mitigación
Para minimizar estos riesgos, se recomienda priorizar el uso de matrices biocompatibles o biodegradables, como quitosano, celulosa o alginato, que reduzcan la toxicidad y mejoren la retención del nanomaterial en el sitio de aplicación. Asimismo, deben establecerse protocolos de monitoreo ambiental pos-aplicación, que incluyan bioensayos en microorganismos del suelo, análisis de lixiviados y evaluación de cambios en propiedades fisicoquímicas del suelo.
Finalmente, es esencial que el uso de nanomateriales en sistemas agrícolas esté regulado mediante marcos normativos, que aseguren una aplicación segura, sustentable y socialmente aceptable, especialmente en regiones con alta vulnerabilidad ambiental.
Conclusiones
Los nanomateriales inmovilizados representan una tecnología innovadora y eficaz para la remoción de As en diversas matrices de agua y suelos, con ventajas destacadas sobre los métodos tradicionales en términos de eficiencia, estabilidad, selectividad y sostenibilidad ambiental. Sin embargo, su aplicación a gran escala aún enfrenta retos relacionados con los costos de producción, la optimización según tipo de suelo o agua y la evaluación de su impacto ecológico.
Además, aspectos como la biodegradabilidad, la interacción con la microbiota del suelo y el riesgo de lixiviación deben ser cuidadosamente analizados para asegurar un uso seguro y sostenible. Estos materiales tienen el potencial de transformar las estrategias de remediación en la agricultura, pero su implementación debe ir acompañada de marcos regulatorios, estudios ambientales y estrategias socioeconómicas que garanticen su adopción responsable y efectiva a largo plazo.











 text in
text in