Introducción
La leucemia linfoblástica aguda (LLA) es un tipo de cáncer que se origina en las células precursoras de linfocitos, que ocasiona la proliferación maligna y oligoclonal de progenitores linfoides inmaduros conocidos como blastos. Su incidencia alcanza un pico entre los 3 y 5 años1. El diagnóstico de LLA se basa en la evaluación clínica, pruebas de laboratorio y requiere al menos un 25% de blastos en el estudio de aspirado de médula ósea para el diagnóstico2. La asignación de riesgo, ya sea bajo-estándar o alto, depende de la edad al diagnóstico, el recuento leucocitario (> 50,000/mm3), compromiso del sistema nervioso central, alteraciones citogenéticas y respuesta al tratamiento3.
El tratamiento médico de la LLA en niños y adultos se realiza mediante terapias combinadas que incluyen inmunoterapia, terapia dirigida y, en algunos casos, trasplante de células progenitoras hematopoyéticas. La quimioterapia es la base de tratamiento y se divide en varias fases: inducción, consolidación, intensificación y mantenimiento4.
En las últimas décadas, la supervivencia de los pacientes pediátricos con LLA ha mejorado y se reportan tasas a largo plazo que superan el 80% en muchos casos5. Sin embargo, algunos pacientes pueden experimentar recaídas o no responder al tratamiento, lo que representa un desafío en el manejo de la enfermedad. Los estudios actuales se centran en identificar nuevos blancos terapéuticos, mejorar la eficacia y disminuir la toxicidad de los tratamientos y desarrollar enfoques personalizados según las características de cada paciente6.
El estado nutricional es un determinante potencialmente modificable que puede influir en la tolerancia terapéutica, la farmacocinética y farmacodinamia de los medicamentos antineoplásicos, la competencia inmunitaria y el riesgo de infecciones. Una nutrición adecuada se asocia a menor toxicidad de los medicamentos y menos complicaciones, mientras que los estados de malnutrición pueden exacerbar eventos adversos y comprometer el sistema inmunitario para combatir la enfermedad7,8.
Es importante considerar que la propia enfermedad puede alterar el estado nutricional. Esto debido a la actividad metabólica elevada de las células cancerosas, generando un aumento en las necesidades calóricas y nutricionales de los pacientes pediátricos con LLA9,10. Además, los efectos secundarios del tratamiento pueden provocar náuseas, vómitos, diarrea y alteraciones del apetito, lo que agrava el riesgo de desnutrición. En algunos casos, el cáncer y su tratamiento pueden provocar malabsorción de nutrientes, lo que también contribuye a la desnutrición11.
Por otro lado, aunque la obesidad en la población pediátrica general es un problema de salud creciente8, en pacientes oncológicos pediátricos se ha reportado como un estado nutricional predominante en fases de tratamiento y vigilancia12,13. Las consecuencias clínicas abarcan desde alteraciones en la farmacocinética y la farmacodinamia de los medicamentos contra el cáncer. Asimismo, la obesidad y el sobrepeso en pacientes pediátricos con cáncer se vinculan con menor supervivencia, mayor riesgo de recaída y complicaciones metabólicas en la vida adulta14,15.
La evidencia internacional sobre la relación entre estado nutricional y desenlaces en LLA es heterogénea por diferencias en definiciones (peso/edad, índice de masa corporal [IMC], Z-score del IMC [Z-IMC], puntuaciones compuestas), momentos de medición y ajuste por confusores biológicos. Aun así, múltiples cohortes han vinculado la desnutrición con mayor mortalidad relacionada con el tratamiento, más infecciones y peor supervivencia global. Por ejemplo, Ghafoor et al., en Pakistán, reportaron peor respuesta terapéutica y mayor mortalidad en niños desnutridos16. En contraste, Rodríguez-Gonzales et al., en una cohorte colombiana, no encontraron una relación directa entre la desnutrición y el pronóstico en pacientes con LLA. En su análisis multivariante, el tipo de cáncer fue el factor determinante de la mortalidad. Este hallazgo podría estar relacionado con las diferentes definiciones y mediciones del estado nutricional17.
Por último, en un estudio llevado a cabo por Núñez-Enríquez et al. se examinó si el sobrepeso y la obesidad son predictores de mortalidad temprana y recaída en niños mexicanos con LLA18. Sus hallazgos mostraron que el sobrepeso y la obesidad al momento del diagnóstico fueron predictores de mortalidad temprana, pero no se encontraron asociaciones entre sobrepeso y obesidad con la recaída temprana.
A pesar de la creciente evidencia que sugiere una relación entre el estado nutricional y los desenlaces en pacientes con LLA, la evidencia es heterogénea, por lo que es necesario investigar a fondo el estado de nutrición en este grupo de pacientes, ya que es un factor modificable que podría influir en mejorar las tasas de supervivencia y calidad de vida en niños con LLA.
Por tanto, el objetivo del presente estudio fue evaluar el estado nutricional mediante el Z-IMC en las fases de diagnóstico, inducción y vigilancia, así como su impacto sobre las tasas de mortalidad en pacientes con LLA.
Método
Diseño de estudio
Se realizó un estudio de tipo cohorte retrospectiva utilizando registros hospitalarios de pacientes con diagnóstico de LLA atendidos en el Hospital Infantil de México Federico Gómez (HIMFG). El muestreo fue no probabilístico por conveniencia, basado en casos consecutivos registrados entre 2015 y 2020. Se incluyeron pacientes de entre 2 y 18 años atendidos en los servicios de hematología u oncología, con diagnóstico de LLA confirmado mediante citometría de flujo y aspirado de médula ósea. Se excluyeron aquellos con registros hospitalarios incompletos o no disponibles para consulta, así como pacientes cuyo estado de mortalidad era desconocido al momento del seguimiento. Los datos se ingresaron en una base de datos electrónica anonimizada. El estudio siguió los principios de la Declaración de Helsinki para la investigación clínica y se adhirió a las guías STROBE (Strengthening the Reporting of Observational studies in Epidemiology) para la presentación de estudios observacionales.
Variables de estudio
Se recolectaron datos sociodemográficos, fecha de diagnóstico, etapa de tratamiento de la LLA, así como variables antropométricas y bioquímicas. Entre las variables antropométricas se capturaron el peso y la talla al diagnóstico, al final de la inducción y en la última consulta. Las variables bioquímicas incluyeron albúmina, hemoglobina, hematocrito, electrolitos (sodio y potasio), función renal (medida por nitrógeno ureico en sangre [BUN] y creatinina), ácido úrico, así como pruebas de coagulación (tiempo de protrombina, tiempo parcial de tromboplastina y razón normalizada internacional [INR]), en las diferentes etapas del tratamiento. La principal variable de exposición fue la clasificación del estado nutricional, definido por el Z-IMC según los estándares de la Organización Mundial de la Salud (OMS). Los pacientes fueron estratificados en normopeso (Z-IMC 1.0 a 2.0), sobrepeso/obesidad (Z-IMC ≥ 2.0) y desnutrición (Z-IMC ≤ 1.0) en las diversas etapas del tratamiento. El desenlace primario fue la mortalidad por cualquier causa, estratificada al diagnóstico, al final de la inducción a la remisión o al inicio de la fase de vigilancia.
Análisis estadístico
Para la descripción de los datos continuos, se utilizó la media (± desviación estándar) o la mediana (rango intercuartil [RIQ]), dependiendo de su distribución, evaluada mediante la prueba de normalidad de Anderson-Darling. Las variables categóricas se presentaron como frecuencias absolutas con sus respectivos porcentajes relativos. Se muestran los porcentajes relativos en relación con los datos disponibles en cada tabla y figura. Para analizar la supervivencia de los pacientes, se ajustaron curvas de Kaplan-Meier, estratificadas según la clasificación del estado nutricional. La comparación entre las curvas de supervivencia se realizó utilizando la prueba de log-rank. La asociación entre el estado nutricional y la mortalidad por cualquier causa se evaluó mediante un modelo de regresión de Cox. Los resultados se expresaron en términos de hazard ratio (HR), donde un HR > 1 indica un mayor riesgo de mortalidad asociado con un incremento en la variable independiente. Se utilizó el programa R Studio (Version 2023.06.1) para todos los análisis estadísticos. Se consideró un valor de p < 0.05 como el punto de corte para definir la significancia estadística.
Resultados
Se obtuvieron 108 expedientes completos y evaluables. De estos, 14 fueron eliminados del estudio: seis pacientes por tener una edad menor a 2 años al momento del diagnóstico y ocho debido a que no se pudo verificar el estado de mortalidad, lo que dejó una muestra final de 94 pacientes. Dentro de la muestra analizada, el 84% (n = 79) estaban vivos, mientras que el 16% (n = 15) habían fallecido.
La tabla 1 presenta las características descriptivas de la muestra de estudio de acuerdo con el total de la muestra y los valores disponibles recolectados de cada característica sociodemográfica. La distribución por sexo fue 1:1.8, un 35% (n = 33) de mujeres y un 65% (n = 61) de hombres, con una mediana de edad de 6 años (RIQ: 3.5-10) años. La mayor proporción de los niños (39%, n = 37) tenían entre 2 y 5 años, seguido por el 35% (n = 33) entre 6 y 10 años, el 19% (n = 18) entre 11 y 15 años, y una menor proporción, del 6.4% (n = 6), que eran mayores de 16 años. En términos de lugar de residencia, la mayoría (84%, n = 79) provenía del área conformada por la Ciudad de México, Edo. de México, Puebla y Morelos, en contraste con el 16% (n = 15) que residía fuera de esta área. Respecto al riesgo basal, el 53.2% (n = 50) de los pacientes se clasificaron como riesgo alto al diagnóstico y un 32.9% (n = 31) como riesgo estándar.
Tabla 1 Características generales de la muestra total y estratificada por pacientes vivos y fallecidos durante el seguimiento entre el 2015 a 2020 en el Hospital Infantil de México Federico Gómez
| Características | Total de la muestra (n = 94) | Vivo (n = 79) | Fallecido (n = 15) | p |
|---|---|---|---|---|
| Sociodemográficas | ||||
| Sexo, n (%) | ||||
| Femenino | 33 (35%) | 27 (34%) | 6 (40%) | 0.7 |
| Masculino | 61 (65%) | 52 (66%) | 9 (60%) | |
| Edad (años) | 6.0 (3.5-10.0) | 6.0 (3.5-10.1) | 5.5 (3.4-8.4) | 0.6 |
| Grupos de edad, n (%) | ||||
| 2-5 | 37 (39%) | 30 (38%) | 7 (47%) | 0.9 |
| 6-10 | 33 (35%) | 28 (35%) | 5 (33%) | |
| 11-15 | 18 (19%) | 15 (19%) | 3 (20%) | |
| ≥ 16 | 6 (6.4%) | 6 (7.6%) | 0 (0%) | |
| Servicio tratante, n (%) | ||||
| Hematología | 7 (7.5%) | 7 (9.0%) | 0 (0%) | 0.6 |
| Oncología | 86 (92%) | 71 (91%) | 15 (100%) | |
| Dato perdido | 1 (0.1%) | 1 (1.3%) | 0 (0%) | |
| Residencia, n (%) | ||||
| Área metropolitana | 79 (84%) | 67 (85%) | 12 (80%) | 0.7 |
| Fuera de área metropolitana | 15 (16%) | 12 (15%) | 3 (20%) | |
| Evaluación al diagnóstico | ||||
| Riesgo basal, n (%) | ||||
| Estándar | 31 (32.9%) | 27 (34.2%) | 4 (26.6%) | 0.3 |
| Alto | 50 (53.2%) | 42 (53.1%) | 8 (53.4%) | |
| Dato perdido | 13 (13.8%) | 10 (12.6%) | 4 (26.6%) | |
| Equimosis, n (%) | 17 (18%) | 15 (19%) | 2 (13%) | > 0.9 |
| Epistaxis, n (%) | 9 (9.6%) | 8 (10%) | 1 (6.7%) | > 0.9 |
| Hepatomegalia, n (%) | 22 (23%) | 18 (23%) | 4 (27%) | 0.7 |
| Esplenomegalia, n (%) | 19 (20%) | 16 (20%) | 3 (20%) | > 0.9 |
| Adenomegalia, n (%) | 31 (33%) | 27 (34%) | 4 (27%) | 0.8 |
*Las variables categóricas se presentan mediante su frecuencia y porcentaje, y se someten a comparación estadística utilizando la prueba de chi cuadrado. Por otro lado, las variables continuas se presentan en mediana y rango intercuartílico, y se contrastan mediante la prueba no paramétrica de U de Mann-Whitney.
Los resultados de laboratorio al diagnóstico indicaron una mediana de hemoglobina de 7.40 g/dl (RIQ: 5.20-10.25) y hematocrito del 22% (RIQ: 15-29). En cuanto a los electrolitos, los niveles de sodio mostraron una mediana de 137 mEq/l (RIQ: 136-140), y el potasio tuvo una mediana de 4.00 mEq/l (RIQ: 3.70-4.13). La función renal, medida por BUN y creatinina, tuvo medianas de 16.1 mg/dl (RIQ: 10.0-20.6) y 0.60 mg/dl (RIQ: 0.50-0.71), respectivamente. Los niveles de ácido úrico se situaron en una mediana de 5.2 mg/dl (RIQ: 4.2-6.7).
En cuanto a las pruebas de coagulación, estas revelaron una mediana de tiempo de protrombina de 12.40 s (RIQ: 11.50-14.00) y un tiempo parcial de tromboplastina con una mediana de 32 s (RIQ: 21-33). El INR tuvo una mediana de 1.09 (RIQ: 0.99-1.23).
Se compararon las características descriptivas de la muestra de estudio estratificadas según el estado de mortalidad (Tabla 1). El sexo no mostró diferencias significativas entre los grupos, con un 34% (n = 27) de mujeres y un 66% (n = 52) de hombres en el grupo de vivos, y un 40% (n = 6) de mujeres y un 60% (n = 9) de hombres en el grupo de fallecidos (p = 0.7). Así mismo, la mediana de edad fue similar entre los grupos, con 6 años (RIQ: 3.5-10.1) para los vivos y 5.5 años (RIQ: 3.4-8.4) para los fallecidos (p = 0.6). En ambos grupos, la mayoría de los niños provenían del área metropolitana, 85% (n = 67) en los vivos y 80% (n = 12) en los fallecidos, sin diferencias estadísticamente significativas (p = 0.7). No se observaron diferencias significativas en el riesgo al diagnóstico, con un 53.1% (n = 42) de los vivos y un 53.4% (n = 8) de los fallecidos clasificados como alto riesgo (p = 0.3).
En la tabla 2 se comparan los resultados de laboratorio al diagnóstico, al final de la inducción y a la última consulta. Se observó que entre ninguno de los laboratorios registrados hubo diferencias estadísticamente significativas, tanto al diagnóstico y al final de la inducción. No obstante, se observó una tendencia a la significancia estadística en los niveles de hematocrito (mediana vivos 39.3 [RIQ: 38.2-42.1] vs. mediana fallecidos 36.8 [RIQ: 28.9-38.7]; p = 0.063), proteínas totales (mediana vivos 7.3 [RIQ: 6.42-7.40] vs. mediana fallecidos 6.25 [RIQ: 5.83-6.65]; p = 0.087) y globulinas (mediana vivos 3.10 [RIQ: 2.85-3.50] vs. mediana fallecidos 2.40 [RIQ: 2.40-2.90]; p = 0.067) a la última consulta entre ambos grupos.
Tabla 2 Características bioquímicas en las diferentes etapas del tratamiento y su comparación de acuerdo con el estatus de mortalidad*
| Al diagnóstico | Al final de la inducción | A la última consulta | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Características | n | Vivo, n = 79 | Fallecido, n = 15 | p | n | Vivo, n = 76 | Fallecido, n = 14 | p | n | Vivo, n = 79 | Fallecido, n = 13 | p | |
| Hemoglobina (g/dl) | 55 | 7.10 (5.20-10.40) | 7.80 (6.60-9.93) | 0.8 | 32 | 9.45 (8.73-10.68) | 10.00 (9.85-10.15) | 0.7 | 58 | 13.10 (12.83-13.88) | 12.40 (11.50-13.08) | 0.15 | |
| Hematocrito (%) | 52 | 21 (15-29) | 24 (23-31) | 0.4 | 32 | 27.9 (25.4-32.0) | 30.4 (30.1-30.6) | 0.6 | 58 | 39.3 (38.2-42.1) | 36.8 (28.9-38.7) | 0.063 | |
| Sodio (mEq/l) | 43 | 137 (136-138) | 138 (137-141) | 0.4 | 30 | 141 (139-143) | 140 (140-141) | 0.7 | 23 | 141 (138-142) | 137 (136-140) | 0.10 | |
| Potasio (mEq/l) | 44 | 4.00 (3.70-4.10) | 4.00 (3.75-4.25) | 0.8 | 31 | 3.80 (3.60-4.20) | 3.80 (3.80-3.80) | > 0.9 | 23 | 3.90 (3.80-4.20) | 3.85 (3.80-4.10) | 0.7 | |
| Calcio (mEq/l) | 41 | 9.00 (8.70-9.30) | 8.70 (8.35-9.15) | 0.4 | 28 | 9.30 (9.05-9.45) | 9.50 (9.50-9.50) | 0.4 | 23 | 9.20 (8.65-9.30) | 9.10 (8.50-9.30) | 0.8 | |
| BUN (mg/dl) | 35 | 16.2 (10.4-20.6) | 11.1 (10.0-21.0) | > 0.9 | 30 | 6.9 (6.0-10.5) | 6.0 (6.0-6.0) | 0.6 | 26 | 12.0 (10.1-13.5) | 11.5 (7.1-16.2) | > 0.9 | |
| Creatinina (mg/dl) | 45 | 0.58 (0.46-0.71) | 0.66 (0.57-0.71) | 0.4 | 30 | 0.40 (0.28-0.64) | 0.34 (0.32-0.36) | 0.5 | 26 | 0.47 (0.33-0.59) | 0.42 (0.32-0.46) | 0.4 | |
| Ácido úrico (mg/dl) | 40 | 5.2 (4.3-6.6) | 5.9 (4.1-6.8) | > 0.9 | 24 | 3.55 (2.55-4.40) | 3.15 (3.08-3.23) | 0.8 | 22 | 4.30 (3.05-5.45) | 3.50 (2.10-3.65) | 0.10 | |
| Albúmina (g/dl) | 35 | 3.50 (3.30-3.70) | 3.65 (3.43-3.80) | 0.4 | 28 | 3.85 (3.70-4.08) | 3.80 (3.70-3.90) | 0.8 | 19 | 3.60 (3.60-4.30) | 3.65 (2.55-3.78) | 0.3 | |
| Proteínas totales (g/dl) | 31 | 7.50 (6.50-7.80) | 7.15 (6.63-7.53) | 0.4 | 25 | 6.90 (6.60-7.20) | 6.75 (6.73-6.78) | 0.3 | 14 | 7.30 (6.43-7.40) | 6.35 (5.83-6.65) | 0.087 | |
| Globulinas (g/dl) | 32 | 3.85 (3.23-4.10) | 3.45 (3.08-3.75) | 0.2 | 27 | 3.00 (2.60-3.40) | 2.95 (2.88-3.03) | > 0.9 | 16 | 3.10 (2.85-3.50) | 2.40 (2.40-2.90) | 0.067 | |
| Bilirrubina total (mg/dl) | 37 | 0.48 (0.31-0.67) | 0.36 (0.29-0.48) | 0.4 | 30 | 0.57 (0.30-0.78) | 0.27 (0.19-0.34) | 0.15 | 23 | 0.61 (0.46-0.80) | 0.41 (0.29-0.95) | 0.7 | |
| Bilirrubina directa (mg/dl) | 37 | 0.12 (0.10-0.13) | 0.09 (0.08-0.14) | 0.3 | 30 | 0.15 (0.09-0.19) | 0.08 (0.07-0.09) | 0.2 | 23 | 0.14 (0.10-0.23) | 0.11 (0.09-0.22) | 0.8 | |
| Bilirrubina indirecta (mg/dl) | 37 | 0.38 (0.22-0.48) | 0.30 (0.22-0.34) | 0.3 | 29 | 0.46 (0.23-0.65) | 0.18 (0.12-0.24) | 0.2 | 23 | 0.48 (0.34-0.80) | 0.29 (0.22-0.74) | 0.6 | |
| AST (mg/dl) | 38 | 39 (26-79) | 44 (27-103) | 0.6 | 32 | 38 (29-52) | 49 (48-50) | 0.4 | 23 | 30 (21-51) | 23 (15-34) | 0.2 | |
| ALT (mg/dl) | 38 | 24 (19-70) | 23 (16-54) | 0.6 | 32 | 53 (35-134) | 104 (83-125) | 0.4 | 23 | 61 (19-93) | 52 (27-71) | 0.8 | |
| Deshidrogenasa láctica (U/l) | 39 | 530 (405-1,239) | 549 (403-1,632) | 0.9 | 12 | 287 (215-367) | 255 (255-255) | 0.8 | 12 | 225 (198-265) | 256 (226-327) | 0.3 | |
| TP (s) | 31 | 12.25 (11.48-14.15) | 12.70 (12.55-12.90) | 0.6 | 6 | 12 (11-13) | NA (NA-NA) | 14 | 12.85 (12.10-13.18) | 12.65 (11.73-14.25) | > 0.9 | ||
| TPT (s) | 32 | 32 (23-33) | 20 (17-30) | 0.5 | 6 | 26 (24-38) | NA (NA-NA) | 15 | 27.4 (24.6-28.6) | 25.8 (22.8-29.3) | > 0.9 | ||
| INR | 31 | 1.08 (0.99-1.25) | 1.10 (1.09-1.12) | 0.7 | 5 | 0.92 (0.92-1.07) | NA (NA-NA) | 14 | 1.12 (1.05-1.14) | 1.11 (1.01-1.26) | 0.8 | ||
*Las variables continuas se presentan en mediana y rango intercuartílico, y se contrastan mediante la prueba no paramétrica de U de Mann-Whitney.
ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; BUN: nitrógeno ureico en sangre; INR: razón normalizada internacional; NA: no disponible; TP: tiempo de protrombina; TPT: tiempo parcial de tromboplastina.
Con respecto a la evaluación nutricional de la muestra al diagnóstico, a la inducción y a la vigilancia evaluada mediante el Z-IMC se encontró que las medianas al diagnóstico del IMC reportado fueron de -0.14 (RIQ: -0.66 a 0.71; n = 47), en la inducción de 0.27 (RIQ: -0.21 a 1.09; n = 43) y en la vigilancia de 1.06 (RIQ: -0.22 a 1.79; n = 91).
En la figura 1 se muestra la distribución porcentual del estado nutricional en cada etapa del tratamiento. Al diagnóstico, de 40 pacientes que estaban vivos y en los que se obtuvo este dato, un 75% (n = 30) se clasificaron como normopeso, un 10% (n = 4) como desnutridos y un 15% (n = 6) como sobrepeso-obesidad. En contraste, de siete pacientes que fallecieron al seguimiento y que se obtuvo el IMC al diagnóstico, el 28.6% (n = 2) tuvieron normopeso, el 42.9% (n = 3) en desnutrición y el 28.6% (n = 2) en sobrepeso-obesidad, con una tendencia a la significancia estadística (p = 0.088). Durante la inducción, de 40 pacientes que estaban vivos y en los que se obtuvo este dato, un 57.5% (n = 23) se clasificaron como normopeso, un 15% (n = 6) como desnutridos y un 27.5% (n = 11) como sobrepeso-obesidad. En contraste, de tres pacientes que fallecieron al seguimiento y que se obtuvo el IMC a la inducción, el 33% (n = 1) tuvieron normopeso, el 33% (n = 1) desnutrición y el 33% (n = 1) sobrepeso-obesidad, sin diferencias significativas (p = 0.158). En la fase de vigilancia, de 76 pacientes que estaban vivos y en los que se obtuvo este dato, el 27.6% (n = 21) de los vivos se clasificaron como normopeso, el 15.8% (n = 12) como desnutridos y un 56.6% (n = 43) como sobrepeso-obesidad. En contraste, de 15 pacientes que fallecieron al seguimiento y que se obtuvo el IMC a la inducción, el 26.7% (n = 4) de los fallecidos fueron clasificados como normopeso, el 13.3% (n = 2) como desnutridos y el 60% (n = 9) con sobrepeso-obesidad, sin diferencias significativas (p = 0.88).
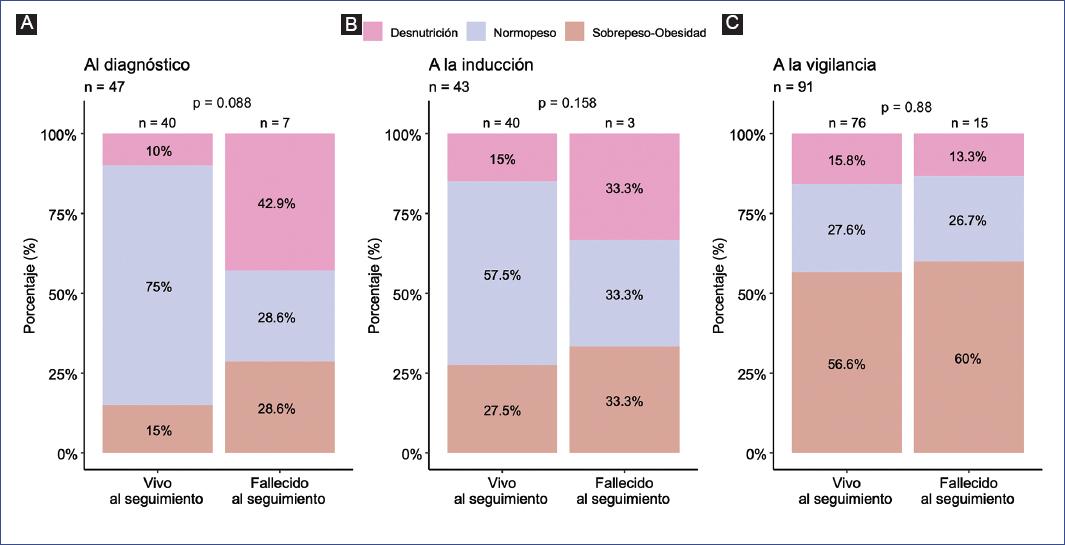
Figura 1 (A-C) Evaluación del estado nutricional en pacientes pediátricos con leucemia linfoblástica aguda en diferentes etapas del tratamiento. Los porcentajes relativos se estimaron en función de los datos disponibles en cada momento de la evaluación.
Con respecto a la supervivencia asociada al estado nutricional al diagnóstico, la figura 2 muestra la curva de Kaplan-Meier que ilustra la probabilidad de supervivencia de pacientes pediátricos, estratificados según su estado nutricional al momento del diagnóstico. Se observa que los pacientes con normopeso presentaron una mayor probabilidad de supervivencia en comparación con los pacientes clasificados con sobrepeso y obesidad, así el grupo de desnutrición presentó la menor supervivencia desde momento del diagnóstico de la LLA, con diferencias estadísticamente significativas (log-rank-test, p = 0.045).
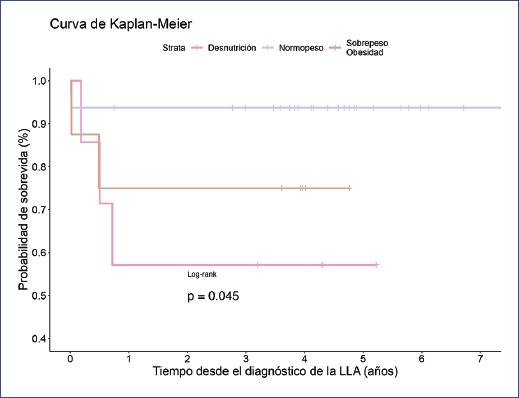
Figura 2 Curva de Kaplan-Meier de la supervivencia en pacientes pediátricos con LLA según el estado nutricional al diagnóstico. LLA: leucemia linfoblástica aguda.
Se calcularon las tasas de mortalidad por cada 100 años-persona estratificadas según el estado nutricio (Fig. 3). Los pacientes clasificados en desnutrición presentaron una tasa de mortalidad estimada de 16.3 (IC 95%: 3.4-47.6) por cada 100 años-persona. Por otra parte, los pacientes con sobrepeso y obesidad tuvieron una tasa de mortalidad estimada de 8.1 (IC 95%: 1.0-29.2) por cada 100 años-persona. Finalmente, los pacientes clasificados con normopeso tuvieron la menor tasa de mortalidad estimada entre los grupos, siendo esta de 1.6 (IC 95%: 0.2-5.9) por cada 100 años-persona. En el modelo de regresión de Cox (Tabla 3) encontramos que los pacientes con sobrepeso/obesidad y desnutrición al diagnóstico tuvieron 4.3 veces (IC 95%: 0.60-30.55; p = 0.150) y 7.16 veces (IC 95%: 1.19-42.9; p = 0.031) mayor riesgo de mortalidad, respectivamente. Este riesgo para mortalidad en los pacientes con desnutrición (HR: 12.5; IC 95%: 1.25-126; p = 0.032) siguió presente en el modelo ajustado por edad, sexo y el riesgo asignado por el oncólogo.
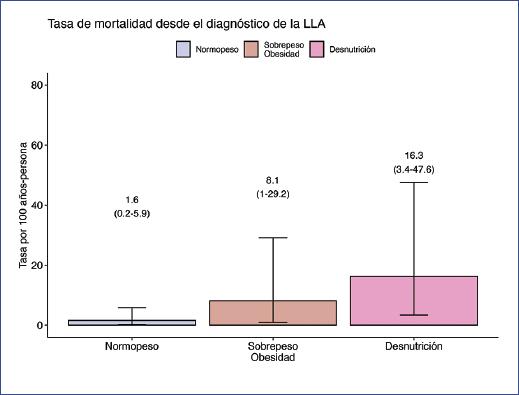
Figura 3 Tasas de mortalidad ajustadas por estado nutricional en pacientes pediátricos con LLA desde el diagnóstico. LLA: leucemia linfoblástica aguda; RTM: razón de tasa de mortalidad.
Tabla 3 Modelos de regresión de Cox para evaluar el riesgo de mortalidad asociado a las categorías nutricionales*
| Característica | Modelo no ajustado | Modelo ajustado* | ||||
|---|---|---|---|---|---|---|
| HR | IC 95% | p | HR | IC 95% | p | |
| Cuatro categorías | ||||||
| Normopeso | - | - | 0.150 | - | - | |
| Sobrepeso y obesidad | 4.30 | 0.60-30.5 | 0.031 | 4.95 | 0.20-122 | 0.300 |
| Desnutrición | 7.16 | 1.19-42.9 | 12.5 | 1.25-126 | 0.032 | |
*Modelo ajustado por las siguientes variables: edad, sexo y riesgo asignado por el oncólogo (alto riesgo/riesgo estándar). HR: razón de riesgo; IC 95%: intervalo de confianza del 95%.
Discusión
Dentro de los principales hallazgos de este trabajo se resalta la importancia de la desnutrición al momento del diagnóstico de LLA como factor de riesgo para mortalidad, debido a que, a lo largo de las distintas fases de tratamiento, no se encontraron diferencias significativas en la supervivencia entre los otros estados nutricionales evaluados. En pacientes desnutridos se observaron mayores tasas de mortalidad en comparación con aquellos con normopeso, sobrepeso y obesidad.
Estos resultados concuerdan con los de Lobato et al., quienes identificaron que la desnutrición al momento del diagnóstico, por sí sola y sin interactuar con otras variables, puede constituir un factor pronóstico significativo en los desenlaces a largo plazo del tratamiento de LLA. Ellos reportaron un riesgo hasta 1.8 veces mayor para el grupo de los desnutridos (IC: 1.72-1.88; p < 0.01) y una supervivencia global a los 5 años de 26% y del 59% en niños sin desnutrición (p < 0.001)19.
En un estudio reciente realizado en población mexicana, con seguimiento retrospectivo de 3 años, se examinó la asociación entre el estado nutricional al diagnóstico y la recaída o mortalidad en LLA pediátrica. Además de los indicadores antropométricos convencionales, los autores incorporaron mediciones de pliegues cutáneos y circunferencias (p. ej., circunferencia media del brazo), y obtuvieron resultados concordantes con los nuestros: la desnutrición se asoció con una supervivencia significativamente menor (76 vs. 63%; p = 0.049). Asimismo, la talla baja para la edad y un pliegue tricipital con puntaje Z < -2 se relacionaron con mayor riesgo de mortalidad (HR: 6.214; IC 95%: 1.372-28.154 y HR: 2.91; IC 95%: 1.27-6.68, respectivamente)20.
El riesgo asignado al diagnóstico de la LLA es un factor importante por considerar para el pronóstico. En nuestro estudio encontramos una mayor proporción de pacientes clasificados como alto riesgo y que fallecieron (67%, n = 8), en comparación con los de bajo riesgo. Aunque nuestros hallazgos no lograron la significancia estadística, al comparar en otros estudios nacionales multicéntricos, como el realizado por Martín-Trejo et al., donde se observó un riesgo mayor de mortalidad en el grupo con desnutrición de alto riesgo, pero con respecto a la mortalidad no encontraron asociación en la fase de inducción. No obstante, su tiempo de seguimiento fue únicamente un año posterior al inicio del tratamiento21.
Los resultados del presente trabajo están respaldados por la fisiopatología que vincula la desnutrición con una mayor mortalidad en pacientes con LLA22,23. Se ha evidenciado que los estados de malnutrición pueden comprometer la función inmunitaria, disminuyendo la capacidad del cuerpo para tolerar y responder al tratamiento quimioterapéutico24,25. Sin embargo, también generan un aumento de riesgo de presentar infecciones graves durante el tratamiento y, por ende, riesgo de mortalidad; si bien no estuvo dentro de nuestros objetivos relacionar el riesgo de infecciones con malnutrición. En un estudio realizado por Sonowal et al. encontraron que los niños varones con desnutrición aguda tuvieron un riesgo de infección casi seis veces mayor que las niñas (odds ratio [OR]: 5.95; IC 95%: 1.29-26.43; p = 0.03). De manera similar, los pacientes con niveles de albúmina sérica < 3.5 g/dl tuvieron un riesgo de infección cuatro veces mayor en comparación con los pacientes con niveles normales de albúmina sérica (OR: 4.2; IC 95%: 1.02-1.81; p = 0.02)26. Así mismo, nuestros resultados únicamente resaltan una tendencia a la significancia de los valores de albúmina y globulinas entre los pacientes vivos y fallecidos a la última consulta.
Aunque nuestro estudio no identificó asociaciones estadísticamente significativas entre el sobrepeso/obesidad y la mortalidad, se observó un aumento en la proporción de pacientes vivos con sobrepeso/obesidad desde la inducción hasta la fase de vigilancia (15, 27.5 y 56.6%). Esto subraya el riesgo a largo plazo de morbilidades cardiometabólicas y la necesidad de implementar intervenciones nutricionales en esta población27.
Finalmente, podemos identificar que, dentro de la malnutrición, el estado de desnutrición al diagnóstico de la LLA puede conducir al paciente pediátrico a un peor pronóstico y a una menor tasa de sobrevida. Dentro de los protocolos actuales de seguimiento, se requiere la implementación de intervenciones tempranas, tamizajes en consultas hospitalarias y protocolos estandarizados, en donde se logre la identificación temprana de pacientes en riesgo de todo el espectro de malnutrición (desnutrición, sobrepeso y obesidad) al diagnóstico y durante el tratamiento de la LLA. Estas intervenciones también tendrían un impacto indirecto en mejorar la respuesta al tratamiento, mejorar la calidad de vida de los pacientes pediátricos con LLA y aumentar la tasa de supervivencia de estos pacientes28. Tales protocolos deben considerar las variaciones individuales en el metabolismo y las necesidades calóricas, además de las preferencias alimentarias y el acceso a alimentos, para ser verdaderamente estrategias costo-efectivas. La meta final es minimizar el impacto de la malnutrición en esta población tanto a corto como a largo plazo.
Limitaciones y fortalezas
Reconocemos limitaciones importantes del estudio. En estudios retrospectivos como este, la precisión de los resultados puede ser baja, ya que normalmente depende de la exactitud de los datos que se encuentran en el expediente clínico, y aunque un estudio retrospectivo puede servir para identificar asociaciones, un estudio retrospectivo por sí solo no puede establecer una relación de causalidad. En segundo lugar, debido al tamaño de muestra, se clasificó a las categorías nutricionales únicamente con tres estratos de riesgo (desnutrición, sobrepeso-obesidad y normopeso), por lo que se requieren más estudios con seguimiento prospectivo donde se utilice el marco de trabajo de la OMS, en el que se consideran cinco categorías de riesgo nutricional (desnutrición, riesgo de desnutrición, normopeso, sobrepeso y obesidad). Si bien los resultados del presente trabajo concuerdan con la evidencia previamente publicada en estudios con mayor tamaño de muestra, donde se observa una asociación entre la desnutrición al diagnóstico y peores resultados en el tratamiento de la LLA, esto da a conocer un área de oportunidad para realizar más estudios específicamente desarrollados en centros de referencia para poder generar estudios prospectivos más controlados y donde se recaben mayores métricas antropométricas, clínicas y nutricionales para evaluar de forma más integral la asociación que existe entre la desnutrición y la mortalidad en pacientes con LLA.
Conclusiones
En conclusión, los hallazgos de este estudio sustentan que la valoración nutricional al diagnóstico de los pacientes pediátricos con LLA necesita un abordaje multidisciplinario que considere todos los valores antropométricos y bioquímicos que implicados en la valoración del estado nutricional integral. Con esto, y un seguimiento nutricional adecuado, se podría mejorar el pronóstico de supervivencia en pacientes con LLA dentro de un contexto hospitalario.











 text new page (beta)
text new page (beta)


