Introducción
El soporte vital extracorpóreo conocido como oxigenación por membrana extracorpórea (ECMO, extracorporeal membrane oxygenation) es una forma modificada de circulación exógena para respaldar temporalmente la función cardiopulmonar, donde la sangre venosa se drena del paciente y se hace avanzar hasta un pulmón de membrana para el intercambio de gases y, posteriormente, la sangre oxigenada retorna al paciente a través de una vena de mayor calibre. Este sistema se clasifica como ECMO venovenoso (ECMO-VV), y cuando el retorno es por un vaso arterial se denomina ECMO venoarterial (ECMO-VA)1,2.
Desde 1990, el uso de ECMO ha ido en aumento en la población pediátrica, con más de 55,000 pacientes en la actualidad3, siendo los neonatos la población con mayor índice de uso de esta terapia2,4; sin embargo, su uso e indicaciones son en casos muy específicos, particularmente en niños operados por una cardiopatía congénita cuando no es posible el destete de la circulación extracorpórea en el quirófano. Con el paso del tiempo se han ido ampliando las indicaciones para el uso de esta terapia, incluyendo pacientes con choque cardiogénico, que requieren soporte inotrópico masivo, escenarios de paro cardiaco extrahospitalario, miocarditis, neumonía y síndrome de insuficiencia respiratoria aguda5. Asimismo, es importante considerar el riesgo-beneficio al momento de optar por ECMO, contemplado los costos, el efecto y la supervivencia a la unidad de cuidados intensivos pediátricos (UCIP)4.
La inmovilización prolongada induce a pérdida de masa ósea y muscular, incluso en ausencia de enfermedad crítica pediátrica, y si a esto se le suma la estancia en la UCIP con uso de ECMO, la atrofia muscular aumenta, la pérdida de fuerza es mayor y, por consiguiente, se incrementa la morbimortalidad, por lo que estos pacientes requieren no solo un correcto inicio de la terapia médica-nutricional, sino también una adecuada rehabilitación nutricional y fisioterapéutica tras la UCIP6, debido a que el uso de ECMO pediátrica induce un aumento en el catabolismo muscular y un incremento del riesgo de desarrollar desnutrición. Además, es necesario considerar las complicaciones propias del uso de esta terapia en conjunto con el uso de algunos fármacos7, ya que se carece de evidencia para estandarizar las dosis de ciertos medicamentos en población pediátrica con esta terapia8.
Por lo tanto, es importante examinar el papel de la nutrición como un elemento crucial en los pacientes de UCIP, considerando que la prevalencia de desnutrición en estos pacientes va desde el 18% hasta el 45%, lo cual aumenta los costos y la mortalidad hospitalaria, al igual que en los pacientes con ECMO, puesto que el bajo peso en esta población es considerado un predictor independiente de mortalidad hospitalaria9.
Evaluación nutricional en pacientes con ECMO
El estado de nutrición en condiciones críticas se ha identificado como un elemento que contribuye significativamente a los resultados clínicos10. La desnutrición puede asociarse con un mayor riesgo de mortalidad en los pacientes en la UCIP9,11,12 debido a que el bajo peso representa un mayor riesgo de mortalidad12, y en los niños con ECMO que tienen un peso inferior al recomendado este riesgo aumenta9,13.
La desnutrición también se considera un predictor de mayor requerimiento de ventilación mecánica9,14 y prolongados tiempos de estancia en la UCIP9. Asimismo, no existen datos sobre el impacto del estado nutricional en el pronóstico de los pacientes pediátricos con ECMO9.
Estos pacientes tienen un alto riesgo de efectos adversos y deterioro nutricional debido a la condición crítica y los impedimentos para el suministro de nutrientes15. Existe mayor riesgo de desnutrición en comparación con los adultos por presentar menos grasa y masa muscular, además de mayores requerimientos energéticos en reposo. Si la desnutrición es prolongada, puede comprometer el crecimiento y el desarrollo óptimos16. Debido a la gravedad de los pacientes sometidos a ECMO, y en consideración de su estado premórbido, es difícil alcanzar una ganancia de peso adecuada, considerando que el aporte de nutrientes puede estar limitado17. En neonatos se han observado pérdidas de peso de hasta el 15% de su masa corporal magra durante el uso de ECMO por 7 días17. Además, posiblemente los pacientes pediátricos en condiciones graves ya presenten un grado de desnutrición al ingreso, lo que puede empeorar el pronóstico médico si a esto se le suma una nutrición intrahospitalaria inadecuada14.
Por lo anterior, la evaluación nutricional es un elemento muy importante para la detección de riesgos16, considerando el impacto del estado nutricional sobre el pronóstico de los niños gravemente enfermos. De acuerdo con estudios observacionales, tanto la desnutrición como la obesidad se asocian con resultados clínicos adversos18. A pesar de conocer su importancia, en la práctica diaria es difícil realizar una evaluación de forma integral, lo que puede deberse a falta de información y de capacitación16.
Se recomienda que los pacientes en la UCIP se sometan a una evaluación nutricional detallada al ingreso hospitalario19 y 48 horas posterior a la admisión, reevaluando el estado nutricional al menos semanalmente durante la estancia hospitalaria18.
Una evaluación nutricional completa comprende la revisión de los registros médicos a través de la historia clínica, medidas antropométricas, datos bioquímicos, reporte de consumo dietético, datos nutricionales, entrevista y exploración física orientada. Esta última ayuda a identificar la existencia de desgaste muscular o pérdida de grasa subcutánea, así como la presencia de edema, y además permite corroborar la información recabada durante la revisión del historial clínico16.
Dentro de las prácticas para la evaluación nutricional de los pacientes pediátricos en condición crítica, con el objetivo de identificar desnutrición o riesgo de deterioro nutricional, se sugiere documentar el peso y la altura al ingreso hospitalario10. La circunferencia media del brazo también puede emplearse para la evaluación, siendo un parámetro relativamente estable y buen indicador del estado nutricional; si es ≤ 12.5 cm sugiere desnutrición, mientras que ≥ 13.5 cm es normal (sensibilidad en hombres del 94.4% y en mujeres del 88.9%, con una especificidad del 83% en ambos sexos para el diagnóstico de desnutrición)16. Este indicador, además, se ha correlacionado con el índice de masa corporal (IMC) en pacientes mayores de 5 años20. Por otro lado, desde el nacimiento y hasta los 5 años de edad, el perímetro cefálico puede ser de utilidad para evaluar el crecimiento cuando no se tiene precisión en la longitud, utilizando el puntaje Z y las tablas de perímetro cefálico para la edad en niños y niñas de la Organización Mundial de la Salud (OMS)16. Las medidas que se obtienen pueden ser comparadas con curvas de crecimiento y se determinan puntajes Z para poder establecer tendencias16, ya que estos permiten identificar qué tan atípica es la medición20. También se pueden considerar puntuaciones Z del IMC para la edad; en los menores de 2 años, se debe considerar el peso para la longitud o el peso para la edad si no se dispone de la altura exacta18. La evidencia sugiere el seguimiento de los cambios en las curvas de crecimiento16 al momento del alta, ya que los gráficos ayudan a que las tendencias del mismo puedan observarse a lo largo del tiempo y de esta manera se identifiquen problemas para su atención oportuna20. Es importante tomar en consideración que, por las condiciones críticas de los pacientes, pueden existir barreras para la precisión de las mediciones16.
Faltan consensos para la evaluación del estado nutricional y marcadores precisos del estado nutricio en el paciente crítico. No obstante, se han considerado algunos elementos, como son la velocidad de crecimiento, la cronicidad y el estado funcional, y algunas otras herramientas de evaluación de riesgos nutricionales y biomarcadores, ya que las mediciones antropométricas, por sí solas, dificultan la detección de riesgos19.
La evaluación integral y precisa de los pacientes contribuye a proporcionar una terapia nutricional individualizada. Mediante esta evaluación se pueden identificar condiciones de desnutrición19. La implementación de tamizajes de riesgo nutricional facilita que los recursos se destinen a pacientes con un alto riesgo para que puedan beneficiarse de una evaluación y una intervención tempranas18. Estos se realizan de manera rápida y sencilla, y permiten identificar de manera confiable a las personas que están en riesgo nutricional21,22. Actualmente no existen herramientas de tamizaje que estén validadas en enfermedades críticas pediátricas con ECMO, a diferencia de un mayor uso de estos cribados nutricionales en adultos19,21,22.
Sin embargo, algunos estudios han considerado al tamizaje PNRS (Paediatric Yorkhill Malnutrition Score) como el más adecuado para la práctica clínica, debido a sus altas sensibilidad y especificidad en comparación con la valoración global subjetiva22. Por otra parte, la herramienta de tamizaje pediátrica PNST (Pediatric Nutrition Screening Tool), validada de manera inicial en pacientes hospitalizados, es muy breve y se enfoca en la pérdida de peso reciente, así como en la reducción de la ingesta calórica20. Se ha considerado la herramienta STRONGKids como una de las más confiables en el entorno clínico para identificar a niños en riesgo nutricional. Se recomienda su implementación en las primeras 24 horas de ingreso en pacientes entre 1 mes y 18 años de edad23. Esto muestra que no existe una herramienta de detección de riesgo superior a otra, y deberán considerarse los entornos donde se aplicarán, así como el diagnóstico médico y su reproducibilidad22. La tabla 1 muestra el consenso para el diagnóstico de desnutrición pediátrica de la Academy of Nutrition and Dietetics (AND) y la American Society for Parenteral and Enteral Nutrition (ASPEN).
Tabla 1 Consenso para el diagnóstico de desnutrición pediátrica y sus indicadores primarios, según la Academy of Nutrition and Dietetics (AND) y la American Society for Parenteral and Enteral Nutrition (ASPEN)
| Indicador | Desnutrición leve | Desnutrición moderada | Desnutrición grave |
|---|---|---|---|
| Puntuación Z del peso para la talla | −1 a −1.9 | −2 a −2.9 | −3 o más |
| Puntuación Z del IMC para la edad | −1 a −1.9 | −2 a −2.9 | −3 o más |
| Puntuación Z de longitud/talla para la edad | NA | NA | −3 |
| Circunferencia media del brazo | Mayor o igual que −1 a−1,9 puntuación Z | Mayor o igual que −2 a−2.9 puntuación Z | Mayor o igual que −3 puntuación Z |
| Velocidad de ganancia de peso (pacientes < 2 años) | < 75%* de la norma† para el aumento de peso esperado | < 50%* de la norma† para el aumento de peso esperado | < 25%* de la norma† para el aumento de peso esperado |
| Pérdida de peso (pacientes 2-20 años) | 5% del peso corporal habitual | 7.5% del peso corporal habitual | 10% del peso corporal habitual |
| Desaceleración en el peso para la puntuación Z de longitud/talla | Disminución de 1 puntuación Z | Disminución de 2 puntuación Z | Disminución de 3 puntuación Z |
| Ingesta inadecuada de nutrimentos | 51-75% del VCT estimado | 26-50% del VCT estimado | ≤ 25% del VCT estimado |
| Cronicidad‡ | Aguda: < 3 meses de duración Relacionada con enfermedad |
Crónica: 3 meses o más de duración Relacionada con consumo dietético, entorno social o económico |
|
*Guo S et al.24
†World Health Organization. Data for patients < 2 years old. Disponible en: http://www.who.int/childgrowth/standards/w_velocity/en/index.html.25
‡Independientemente del grado de desnutrición.
IMC: índice de masa corporal; NA: no aplica; VCT; valor calórico total.
Adaptada de Bouma S et al26,Becker et al.20 y Mehta et al.27
Requerimientos calórico-proteicos en pacientes con ECMO
La desnutrición pediátrica en la UCIP se asocia con un incremento en la morbimortalidad hospitalaria, debido al estado hipermetabólico y catabólico con el que cursa el paciente, sumando a esto el uso de terapias con alto desgaste energético y muscular, como es el caso de la ECMO. Por lo anterior, es imperativo que el clínico aporte la energía y las proteínas necesarias en infantes críticamente enfermos con ECMO para mejorar no solo el curso de la enfermedad, disminuyendo la mortalidad, sino también para disminuir los riesgos asociados a la desnutrición28.
Existe una creciente necesidad de estandarizar por medio de guías de práctica clínica las kilocalorías y las proteínas que se van a proporcionar al paciente pediátrico con ECMO; sin embargo, dada la naturaleza de la enfermedad crítica, se pueden seguir las recomendaciones generales para pacientes pediátricos críticamente enfermos en cuanto a requerimientos calórico-proteicos se refiere29.
Para estimar el gasto energético total del infante, el método de referencia es la calorimetría indirecta. Sin embargo, si esta no se encuentra disponible, se pueden estimar las necesidades calóricas por medio de fórmulas predictivas, como las ecuaciones de peso-talla, el peso de Schofield o bien las ecuaciones recomendadas por la OMS para estimar el gasto de energía. Se debe tener precaución al momento de agregar los factores de estrés que incrementan el requerimiento, ya que su uso sistemático puede resultar en una sobrealimentación involuntaria17,18,30. La tabla 2 muestra las ecuaciones de predicción de gasto energético mencionadas.
Tabla 2 Ecuaciones de predicción del gasto energético en pacientes pediátricos
| Fórmula | Sexo | Edad (años) | Ecuación de predicción |
|---|---|---|---|
| Schofield con peso | Hombres | 3-10 | (22.706 × P) + 504.3 |
| 10-18 | (17.686 × P) + 658.2 | ||
| Mujeres | 3-10 | (16.97 × P) + (161.8 × E) + 371.2 | |
| 10-18 | (8.365 × P) + (465 × E) + 200 | ||
| Schofield con peso y estatura | Hombres | 3-10 | (20.315 × P) + 485.9 |
| 10-18 | (13.384 × P) + 692.6 | ||
| Mujeres | 3-10 | (16.97 × P) + (161.8 × E) + 371.2 | |
| 10-18 | (8.365 × P) + (465 × E) + 200 | ||
| FAO/OMS | Hombres | 3-10 | (22.7 × P) + 495 |
| 10-18 | (17.5 × P) + 651 | ||
| Mujeres | 3-10 | (22.5 × P) + 499 | |
| 10-18 | (12.2 × P) + 746 |
P; peso (kg), E; estatura (cm).
Adaptada de Bouma S et al26, Becker et al.20y Mehta et al.27
Es recomendable administrar gradualmente los requerimientos calóricos, iniciando con un 25% del gasto energético total el día 1 y siguiendo con un aumento paulatino a diario del 25% para alcanzar el 100% en el día 4, o bien durante la primera semana de estancia en la UCIP. Si esto no es posible, al menos dos tercios de los requerimientos deben alcanzarse para el final de la primera semana, ya que si se acumula un déficit de energía durante la fase crítica aumenta el riesgo de resultados clínicamente desfavorables18,30.
Los pacientes recién nacidos y los pediátricos que reciben ECMO tienen mayores requerimientos de proteínas debido al estado hipercatabólico, siendo necesario compensar las pérdidas con un aporte adecuado, pues se ha observado que un suministro inadecuado de proteínas aumenta significativamente la mortalidad en la UCIP en general11. La ASPEN recomienda al menos 1.5 g/kg al día de proteínas en pacientes pediátricos críticamente enfermos; en recién nacidos y pacientes con ECMO, se pueden aportar incluso 3 g/kg al día para compensar las pérdidas catabólicas17,18. En la tabla 3 se muestran las recomendaciones generales para el soporte nutricional en recién nacidos con ECMO17,31.
Tabla 3 Recomendaciones generales de terapia médica-nutricional en pacientes recién nacidos sometidos a oxigenación por membrana extracorpórea (ECMO)
| Recomendaciones de la guía clínica en ECMO | |
|---|---|
| Inicio del soporte nutricional | Iniciarlo dentro de las primeras 24-48 horas, de manera óptima y segura |
| Valor calórico total | Mismas recomendaciones que en el paciente crítico pediátrico. Calorimetría indirecta o estimación con fórmulas predictivas |
| Proteínas | 1.5-3.0 g/kg al día |
| Ruta | Nutrición enteral como primera opción cuando se alcance la estabilidad hemodinámica y no haya contraindicación para uso del tracto gastrointestinal |
Por otro lado, en pacientes pediátricos con ECMO que requieren terapia de reemplazo renal aumentan las pérdidas de micronutrimentos como tiamina, piridoxina, ácido fólico, ácido ascórbico y oligoelementos, especialmente selenio, condicionando una deficiencia de estos y un incremento en el requerimiento, causando una respuesta negativa del organismo al estrés oxidativo y comprometiendo el sistema inmunitario, por lo que se recomienda la administración de la ingesta diaria recomendada de cada uno de los micronutrimentos (vitaminas y oligoelementos)32. Un estudio retrospectivo de un solo centro evaluó 78 pacientes pediátricos con ECMO y halló que en esta población ocurren con frecuencia anomalías del calcio, con esta terapia en particular, lo cual se ha asociado a peores resultados clínicos, mayor duración de la ECMO y más días de estancia en la UCIP33.
Continúa habiendo escasez de datos sobre los requerimientos calóricos y proteicos estandarizados para esta población, aunado a una limitada información sobre la homeostasis y el manejo de los micronutrimentos en pacientes pediátricos con ECMO, por lo que sigue siendo un área clave para futuras investigaciones.
Rutas de entrega nutricional en pacientes pediátricos con ECMO
Nutrición enteral
Es necesaria la implementación de un soporte nutricional óptimo en los pacientes pediátricos críticamente enfermos para mejorar el desenlace clínico10. Debido a que el uso de ECMO ha crecido de manera considerable en los últimos 15 años34, debe ser provista una nutrición adecuada a los pacientes pediátricos que estén bajo esta terapia, ya que se emplea para brindar soporte vital ante diversas enfermedades que progresan a insuficiencia cardiorrespiratoria. Esta condición incrementa el estado catabólico, con una alta demanda de requerimientos energéticos y proteicos13, representando además una carga nutricional y metabólica considerable, pues implementar este soporte no proporciona ningún tipo de reposo metabólico17.
Las pautas para la entrega óptima del soporte nutricional no están claras10. La práctica nutricia es variada en las UCIP, debido a la baja evidencia para guiar las recomendaciones hacia una atención óptima19.
El soporte nutricio en pacientes con ECMO deberá estar fundamentado en una comprensión de los cambios metabólicos, el uso de reservas metabólicas y los requerimientos nutrimentales17, así como la ruta de elección, la forma de administración y el alcance de los objetivos calóricos establecidos; todo esto influye en el pronóstico clínico. Se estima que cerca del 25% de los niños en las UCIP pueden desarrollar un déficit calórico significativo y un incremento del riesgo de deterioro nutricional13.
Se ha propuesto la nutrición enteral (NE) como la vía preferible para alimentar, siendo el acceso preferido sobre la nutrición parenteral (NP) en condiciones críticas, cuando se mantiene la funcionalidad del tracto gastrointestinal y el paciente se encuentra clínicamente estable17. En estudios observacionales en UCIP se ha reportado mejoría con el uso de NE6,18, la cual está significativamente asociada con una disminución de la mortalidad6.
El soporte nutricional enteral debe iniciarse rápidamente en los recién nacidos tratados con ECMO. Las recomendaciones actuales para pacientes pediátricos en estado crítico establecen el inicio de la NE durante las primeras 24-48 h tras el ingreso hospitalario28,35. Los neonatos tienen reservas nutricionales limitadas y requieren un adecuado soporte para garantizar su crecimiento17. En este tipo de pacientes con ECMO clínicamente estables debe iniciarse la NE, mostrando buena tolerancia a la leche materna o la fórmula estándar, aun bajo condiciones de disfunción intestinal relacionadas con enfermedad crítica. Una mejor tolerancia de la NE podría asociarse con una menor estancia hospitalaria17.
Sin embargo, la NE puede retrasarse debido al riesgo considerado de enterocolitis necrosante, isquemia intestinal y hemorragia intestinal, especialmente en pacientes con uso de fármacos vasoactivos36. También existe evidencia reportada de un incremento en la permeabilidad intestinal de los neonatos con ECMO en comparación con los bebés sanos, sin que se hayan presentado complicaciones35.
Los niños con ECMO que reciben infusiones vasoactivas pueden tener dificultades para el inicio de la NE debido a una circulación esplácnica reducida13. Además, se tienen otras preocupaciones para el soporte, como es el riesgo de isquemia intestinal o de traslocación bacteriana17. En 2015, de acuerdo con los datos reportados por una encuesta, el 84.2% de los pacientes con ECMO recibieron soporte nutricional enteral, aunque la administración fue variable y dependió del tipo de ECMO, de las enfermedades subyacentes y del tratamiento con vasopresores13.
Los estudios han demostrado la seguridad del uso de NE, incluso con altas dosis de vasopresores (> 1 μg/kg/min). Esto ha permitido que se recomiende y promueva como soporte nutricional en pacientes con ECMO35; no obstante, siempre es necesaria una evaluación rigurosa y valorar el riesgo-beneficio.
Asimismo, en las UCIP existen algunos otros factores que interfieren en la administración de nutrimentos por vía enteral. La tabla 4 muestra las principales barreras que retrasan el inicio de la NE o que llevan a su suspensión, además de algunas recomendaciones19,31,32. Se ha propuesto que al menos dos tercios de la meta de nutrientes sean provistos en la primera semana de ingreso a la UCIP, lo cual se ha asociado con mejores resultados clínicos18.
Tabla 4 Barreras y recomendaciones para el inicio de nutrición enteral en pacientes pediátricos críticamente enfermos
| Barreras | Recomendaciones |
|---|---|
| Intolerancia percibida a la alimentación por inestabilidad hemodinámica o uso de terapia vasopresora | Reevaluación nutricional a las 48 h |
| Ayuno prolongado por los procedimientos | Considerar uso de NP complementaria en caso de alto riesgo nutricional |
| Riesgo de lesión isquémica intestinal | NP total y reevaluación a las 48 h |
| Disminución de la perfusión intestinal | NP total y reevaluación a las 48 h |
| Presencia de hernia diafragmática congénita | Considerar uso de NE mediante sonda PEG |
NE: nutrición enteral; NP: nutrición parenteral; PEG: gastrostomía endoscópica percutánea.
Cuando la NE es insuficiente por sí sola para cubrir las demandas energéticas, se complementa con NP32; sin embargo, se ha observado que la NE administrada en el día 5 de ECMO se ha asociado con una mayor supervivencia en comparación con el soporte parenteral exclusivo37.
Referente al sitio de administración de la NE, falta evidencia sobre la mejor elección en población pediátrica17, pero se sugiere que la vía gástrica es la opción preferida. Los sitios pospilóricos deben considerarse en pacientes que no toleren la alimentación gástrica o con alto riesgo de broncoaspiración, considerando además que con frecuencia no logra cubrir el objetivo de energía debido a las interrupciones en la administración o la intolerancia alimenticia durante la fase aguda; esto puede permitir que se alcancen objetivos de energía más altos en comparación con la vía gástrica19. En cuanto al método de infusión, continuo o intermitente, la evidencia aún no es sólida para dictar recomendaciones específicas; no obstante, el uso de infusión continua se ha asociado con menor intolerancia gástrica18.
La NE, aunque sea en volúmenes tróficos, iniciada de forma temprana, normalmente es bien tolerada, evaluando las condiciones clínicas13. Incluso se han observado respuestas hormonales intestinales normales después de la administración de pequeños volúmenes de NE en pacientes con ECMO31. Una vez que existe una adecuada tolerancia, se sugiere el avance gradual del aporte de nutrientes18. Los aumentos rápidos en el suministro de energía deben evaluarse sopesando el riesgo de desequilibrio hidroelectrolítico, ya que puede desencadenar un síndrome de realimentación38.
Nutrición parenteral
El uso de NE es la primera opción para el aporte de energía y proteínas, pero en ocasiones no es factible porque el tracto gastrointestinal no es viable o existe una tolerancia baja a la NE, con un aporte menor del 60% del gasto energético total después de 7-10 días. En estas condiciones se puede escalar al uso de NP complementaria o total29; no obstante, no se recomienda su uso dentro de las primeras 24 horas de ingreso a la UCIP18.
Una encuesta de centros de ECMO neonatales y pediátricos reportó que, si bien la NE es la ruta de preferencia para nutrir al paciente, en ocasiones las barreras más comunes para su inicio son el aumento en el uso de fármacos vasoactivos y un diagnóstico subyacente de paro cardiorrespiratorio o trasplante hematológico39. Por esta razón, en estos casos particulares se debe valorar el inicio de la NP40; todo depende del contexto clínico del paciente y del riesgo-beneficio que suponga el empleo de estas terapias1.
La evidencia en cuanto al uso de NP en estos pacientes es limitada, debido a las condiciones clínicas de los niños con ECMO. Sin embargo, el uso de NP complementaria a la NE de manera temprana (dentro de la primera semana de ingreso a la UCIP) puede llegar a ser útil para prevenir los déficits acumulativos de energía y proteínas que no se logran alcanzar por intolerancias digestivas a la vía enteral. El uso de NP complementaria pudiera asociarse con el logro del objetivo de entrega calórica y proteica durante la primera semana de estancia en la UCIP con ECMO13.
En general se ha optado únicamente por la administración de aminoácidos de manera parenteral, con frecuencia una solución que apunta hasta 3 g/kg de peso al día; cada solución debe dosificarse según el contexto clínico del paciente, su peso y sus antecedentes médicos31.
Por otro lado, la NP total proporciona una cantidad mayor y completa de calorías y proteínas, dado que se administran por medio de un catéter central o periférico, dependiendo del paciente y de la osmolaridad de las fórmulas parenterales; sin embargo, el uso de accesos vasculares extra aumenta el riesgo de infecciones asociadas a catéteres36.
En cuanto al uso de multivitamínicos y elementos traza en la NP, se recomienda administrar la ingesta diaria recomendada de cada uno, con excepción de los pacientes en quienes se identifiquen deficiencias séricas de algún micronutrimento en específico, en los que será necesario considerar la administración terapéutica del micronutrimento faltante (vitamina C en presencia de escorbuto, tiamina si existe insuficiencia cardiaca congestiva, niacina para la pelagra, etc.)36-41.
Propuesta de un algoritmo
A partir de las evidencias expuestas respecto a las consideraciones nutricionales, los requerimientos, el inicio de la alimentación y la ruta de administración de nutrimentos, en la figura 1 se propone un algoritmo para la terapia médica-nutricional en esta población tan vulnerable tratada con ECMO, adaptado de Hofheinz et al.40, Toh et al.32 y Farr et al.35.
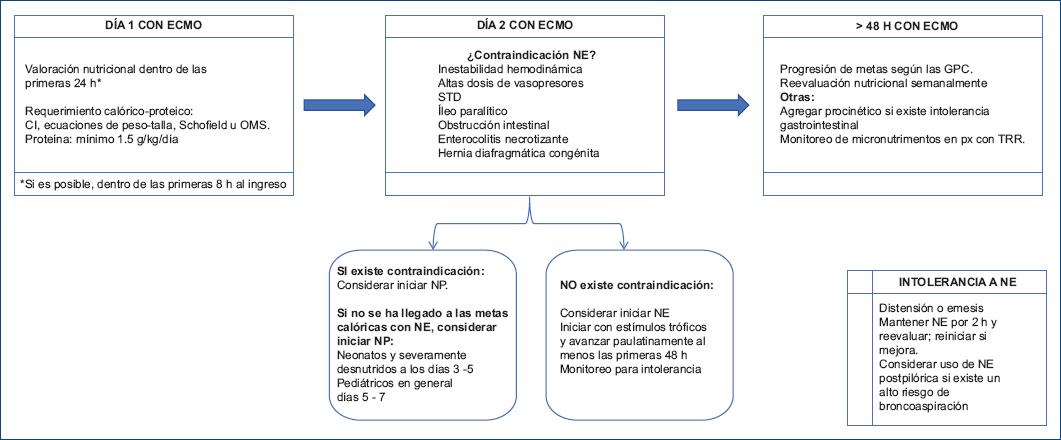
Figura 1 Algoritmo propuesto para la terapia médica-nutricional en pacientes pediátricos con terapia de oxigenación por membrana extracorpórea (ECMO). CI: calorimetría indirecta; GPC; guías de práctica clínica; NE: nutrición enteral; NP: nutrición parenteral; OMS: Organización Mundial de la Salud; RCT: requerimiento calórico total.
Conclusiones
Los pacientes pediátricos críticamente enfermos que reciben terapia de ECMO tienen unos requerimientos nutricionales específicos, así como un incremento en el riesgo de desnutrición intrahospitalaria. Es imperativa una correcta evaluación nutricional en esta gama de pacientes para identificar aquellos que se beneficiarían de un soporte nutricional prematuro, y si bien reconocemos la escasez de evidencia sólida en el campo de la nutrición en ECMO pediátrica, nuestra revisión de la literatura sugiere la seguridad de la NE temprana de bajo volumen y la necesidad de una evaluación precisa de los requerimientos nutricionales, disminuyendo así la morbimortalidad pediátrica.











 text new page (beta)
text new page (beta)


