Introducción
La atresia pulmonar con septum ventricular íntegro (AP-SVI) es una cardiopatía congénita poco frecuente que se caracteriza por atresia pulmonar, ya sea membranosa o muscular, con un espectro morfológico muy amplio con diversos grados de hipoplasia de la válvula tricúspide, del ventrículo derecho (VD) y en algunos casos con anomalías en la circulación coronaria; como sinusoides, fístulas, estenosis o atresia1,2. Debido a esta heterogeneidad, los pacientes con AP-SVI se someten a una variedad de enfoques terapéuticos: reparación biventricular, cirugía 1 y ½ ventricular, cirugía univentricular o el trasplante cardiaco3.
Algunos de los pacientes no presentan fistulas ventrículo-coronarias ni sinusoides intramiocárdicos, consideramos que el mejor término para englobar ambas alteraciones es el de conexiones ventrículo-coronarias (CVC). En contraparte otros pacientes sí presentan CVC, pero solo algunos de estos últimos tendrán circulación coronaria dependiente del ventrículo derecho (CCVDD), esta situación se reporta del 3 al 34%1,4; en los EE.UU. se reporta menos frecuente, siendo del 3 al 20% de los casos con AP-SVI. Esta situación es primordial, ya que el pronóstico de los pacientes con CCVDD generalmente es fatal y se relaciona principalmente con atresia de alguno de los ostium coronarios3.
Está descrito que las CVC están presentes en el 30 al 60% de los casos1, pero solo algunos de estos tendrán CCVDD; la cual se refiere a la perfusión del miocardio ventricular exclusivamente abastecida por el VD con dependencia de esta en las conexiones fistulizadas del VD asociadas a obstrucción significativa de la arteria coronaria principal; así, la perfusión del miocardio ventricular es exclusivamente abastecida por el VD1,2.
Los criterios para definir la CCVDD son variables de centro a centro. Por ejemplo: existe una definición del grupo de Boston y otra por grupo de Houston, sin embargo en cada centro se realizan modificaciones basadas en los hallazgos angiográficos. Los reportes de la CCVDD son principalmente de los EE.UU. y de Europa, pero se desconoce la situación en Latinoamérica.
Específicamente en el grupo de pacientes con CCVDD las opciones de tratamiento se limitan prácticamente al trasplante cardiaco, ya que es extremadamente raro que un paciente con atresia de los ostium coronarios pueda tener una larga sobrevida con cirugía de Fontan3.
Existen reportes donde pacientes con este tipo de circulación coronaria son llevados a fisiología univentricular, pero esta opción de tratamiento sigue siendo muy controversial. Por lo que el objetivo de este manuscrito es compartir tres casos con AP-SVI y CCVDD, su desenlace y las reflexiones que nos aportan estos casos.
Material y método
Se realizó un estudio transversal, descriptivo, observacional, de los pacientes con AP-SVI y CCVDD en el periodo de estudio de julio del 2016 a diciembre del 2022. Se identificaron 27 pacientes con diagnóstico de AP-SVI, confirmándose CCVDD en tres pacientes (12.5%), ninguno de ellos con atresia de los ostium coronarios. En todos los casos se realizó valoración clínica, así como electrocardiograma (EKG), telerradiografía de tórax, además de ecocardiograma transtorácico (ECOTT) y posteriormente cateterismo cardiaco con la finalidad de evaluar la circulación coronaria, y en tres pacientes se confirmó CCVDD.
El ECOTT confirmó el diagnóstico de AP-SVI; se adquirieron imágenes en modo bidimensional, modo M y Doppler pulsado y continuo. El diagnóstico de CCVDD se confirmó angiográficamente. Con seguimiento posterior en la consulta externa de cardiología pediátrica en aquellos pacientes que sobrevivieron después del cateterismo.
Presentación de los casos
Caso 1
Paciente de sexo femenino de dos meses de edad, peso 3,335 g, talla 49 cm. Cianosis desde el nacimiento, hospitalizada a los 13 días por desaturación que mejoraba parcialmente con oxígeno. ECOTT: AP-SVI, motivo de referencia a nuestra institución. Exploración física: cianosis ++, saturación de oxígeno (SaO2) 77%, soplo continuo en foco pulmonar grado III/IV. Se confirma el diagnóstico de AP-SVI además de CVC, comunicación interauricular (CIA) restrictiva y conducto arterioso permeable (CAP) con extremo pulmonar de 2.5 mm. Se realizó cateterismo cardiaco donde se observó un VD tripartita con CVC y estenosis crítica en el tercio proximal de la descendente anterior (DA) con flujo retrógrado en sístole (Figs. 1 y 2). Se catalogó como CCVDC y el plan terapéutico paliativo fue: atrioseptostomía con balón más colocación de un stent coronario no medicado de 4 x 16 mm en el conducto arterioso. A las 8 horas del procedimiento presentó deterioro hemodinámico progresivo, acidosis metabólica, se inició apoyo inotrópico, el EKG demostró infarto extenso del ventrículo izquierdo (VI) (Figs. 3 y 4). ECOTT con hipomotilidad grave del VI y del septum interventricular, evolucionó con choque cardiogénico refractario, bradicardia grave y asistolia, se realizaron maniobras avanzadas de reanimación sin respuesta. No se autorizó estudio post mortem.
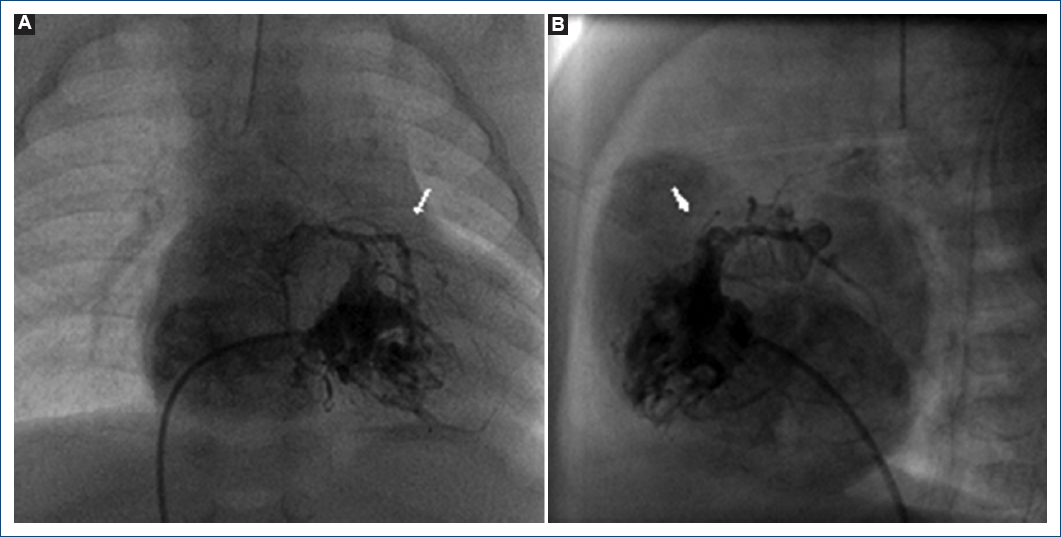
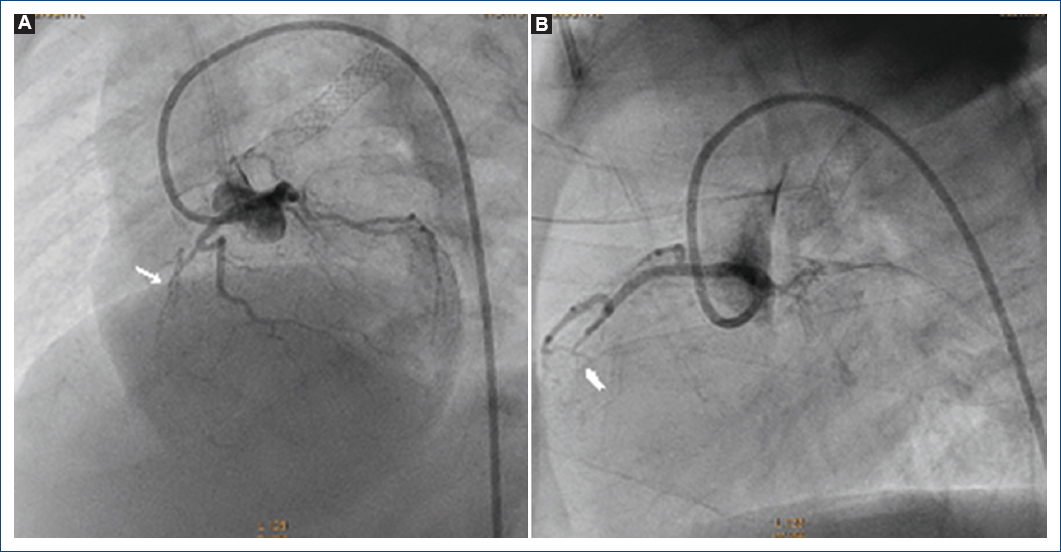
Figura 1 Ventriculografía derecha. Se observa atresia pulmonar con septum ventricular íntegro con conexiones ventrículo-coronarias, estenosis grave en el tercio proximal de la descendente anterior (flecha). A: proyección postero-anterior. B: proyección lateral izquierda.
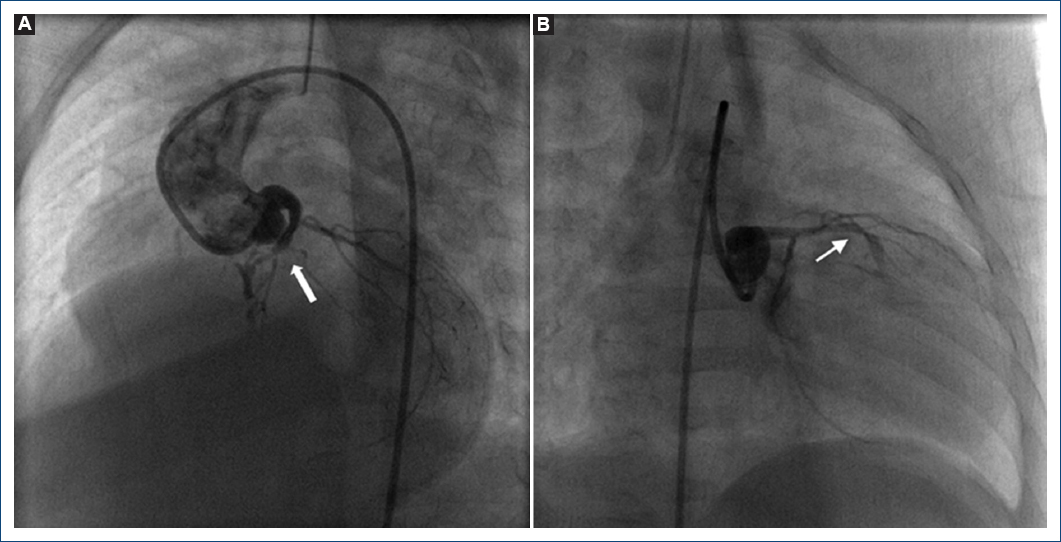
Figura 2 Coronariografía izquierda. Se observa dilatación del tronco coronario izquierdo y estenosis crítica en el tercio proximal de la descendente anterior y las conexiones ventrículo-coronarias (flecha). A: proyección cuatro cámaras. B: proyección oblicua anterior derecha.
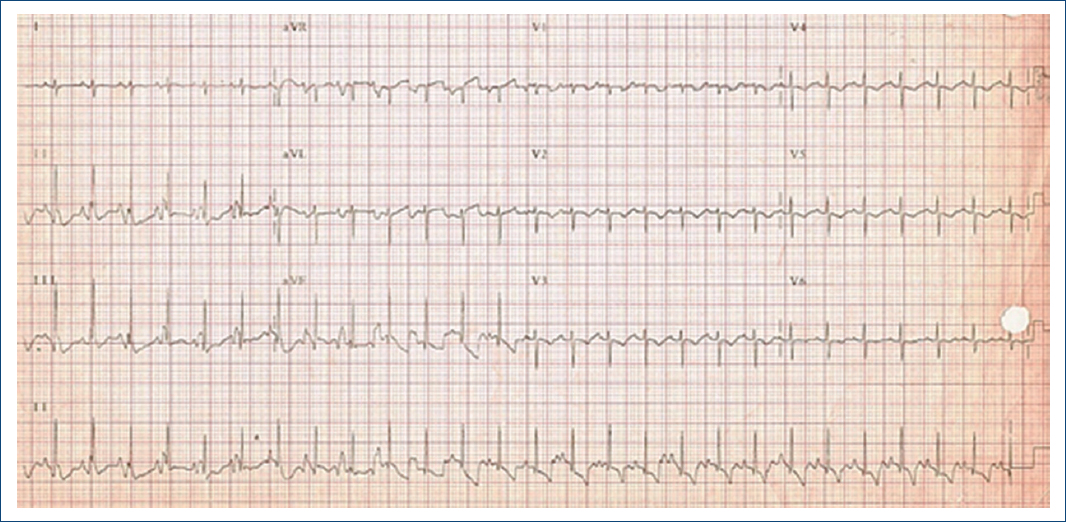
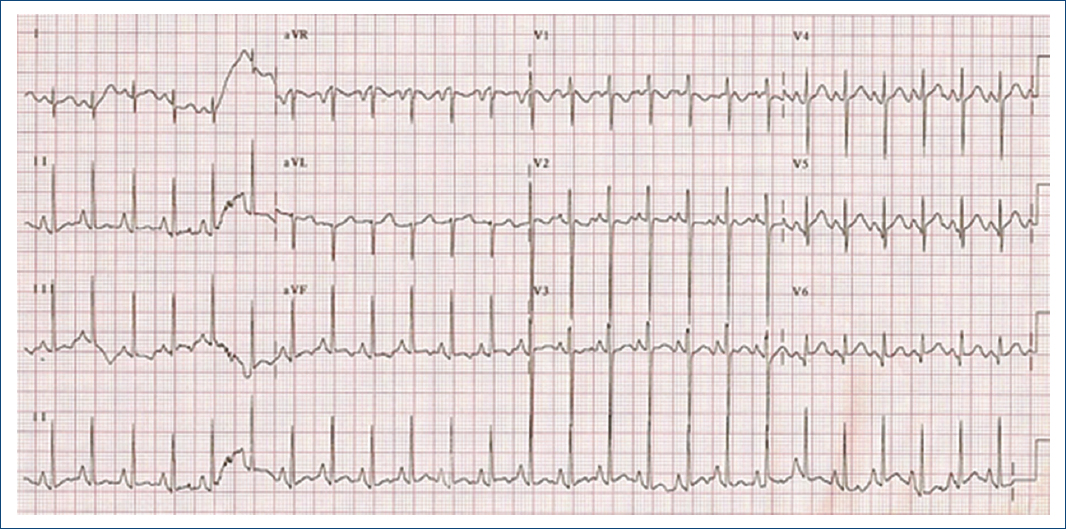
Figura 3 Electrocardiograma precateterismo: ritmo sinusal. FVM 160 lpm, ÂQRS +90°, onda P 0.5 mV, PR 120ms, QRS 40 ms, Qtc 332 Fridericia, crecimiento atrial derecho, ondas T negativas asimétricas en cara inferior, sin lesión ni infarto.
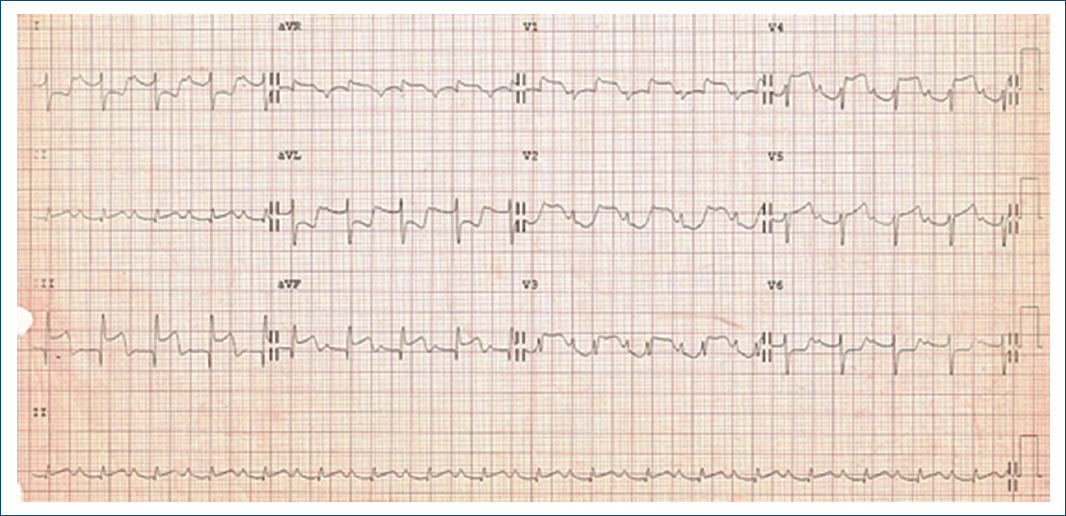
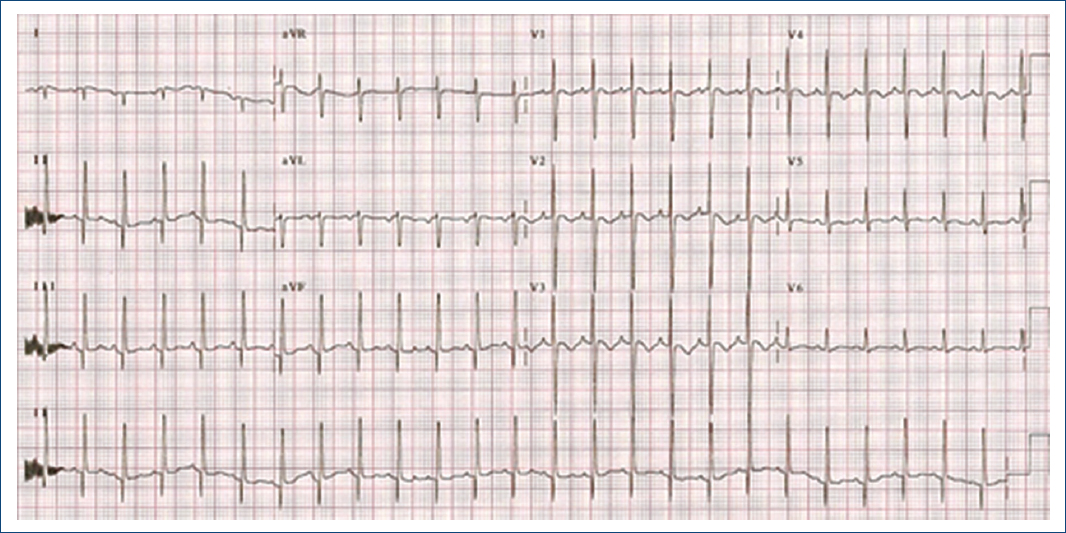
Figura 4 EKG 8 horas poscateterismo: ritmo sinusal, FVM 115 lpm, ÂQRS +160°, onda P 0.3 mV, PR 240 ms, QRS 80 ms, Qtc 345 Fridericia. Bloqueo auriculoventricular de primer grado, con supradesnivel del segmento S-T DIII, AVF, AVR, V1-V5. E infradesnivel en DI, AVL y V6 (infarto extenso de la porción antero-septal, lateral e inferior del ventrículo izquierdo).
Caso 2
Paciente de sexo femenino de tres meses de edad, peso 4.0 kg, talla 54 cm. Cianosis desde el tercer día de vida, referida por sospecha de cardiopatía congénita. A la exploración física con cianosis ++, soplo continuo infraclavicular izquierdo II/IV. ECOTT: AP-SVI, VD hipoplásico, válvula tricúspide pequeña, ramas pulmonares confluentes de buen calibre, CIA de derecha a izquierda con gradiente máximo de 3 mmHg, CAP con estenosis a su llegada a la arteria pulmonar. Cateterismo cardiaco: presenta crisis de hipoxia y se coloca un stent coronario no medicado 4 x 16 mm en el conducto arterioso, con lo que mejora su saturación; se confirmó CCVDD de manera inadvertida al cruzar la válvula tricúspide y generar insuficiencia tricuspídea moderada (Fig. 5), en este momento presentó bradicardia, infradesnivel en el segmento S-T. Se logra realizar una ventriculografía derecha confirmándose la AP-SVI y las CVC, se retira el catéter y paulatinamente se logra estabilidad hemodinámica en aproximadamente 15 minutos, se realiza coronariografía izquierda que demuestra atresia de la DA en su tercio medio (Fig. 6), se decide no realizar septotomía atrial, evoluciona de manera favorable con EKG sin datos de lesión ni de infarto (Fig. 7) y se egresa a las 48 horas. Diecinueve meses después presenta de manera súbita irritabilidad por unos segundos, presenta pérdida del estado de alerta y fallece en domicilio. No se realiza estudio post mortem.
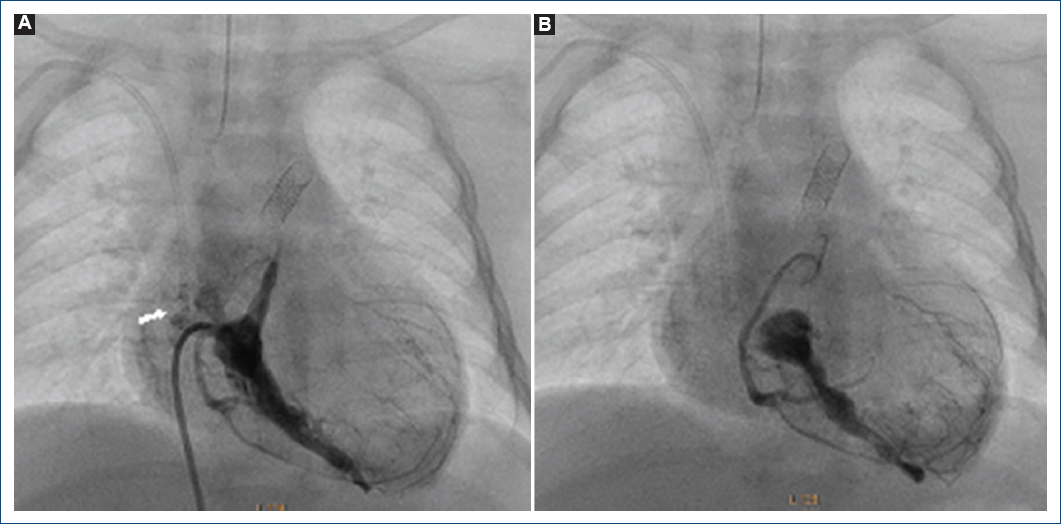
Figura 5 Ventriculografía derecha proyección postero-anterior. A: se observa atresia pulmonar con septum ventricular íntegro con conexiones ventrículo-coronarias con insuficiencia tricuspídea generada por el catéter angiográfico (flecha). B: al retirar el catéter angiográfico desparece la insuficiencia tricuspídea.
Caso 3
Paciente de sexo masculino de cuatro días de vida, peso 2,630 g, talla 48 cm. Cianosis desde el nacimiento, motivo de envío. Exploración física: SaO2 48%, cianosis ++++, sin soplos a su ingreso. Se inició alprostadil. ECOTT: AP-SVI, VD hipoplásico, ramas pulmonares confluentes, CIA amplia, CAP con estenosis y probables CVC. Cateterismo cardiaco: coronariografía izquierda con estenosis en el tronco coronario izquierdo y atresia en el tercio medio de la DA (Fig. 8), además de estenosis de la descendente posterior (Fig. 9A), ventriculografía derecha que confirma AP-SVI y CVC (Fig. 9B), CAP vertical. Se coloca un stent coronario no medicado 4 x 20 mm en el conducto arterioso, evoluciona de manera favorable y se extuba a las 48 horas. Su EKG sin datos de lesión o infarto (Fig. 10). Se egresa a los seis días posterior al cateterismo. A la edad de cinco meses ingresa a urgencias por cuadro de diarrea aguda con deshidratación, presenta de manera súbita irritabilidad, bajo gasto, se documenta taquicardia ventricular-fibrilación ventricular sin respuesta a maniobras avanzadas de reanimación. No se logra obtener estudio post mortem.
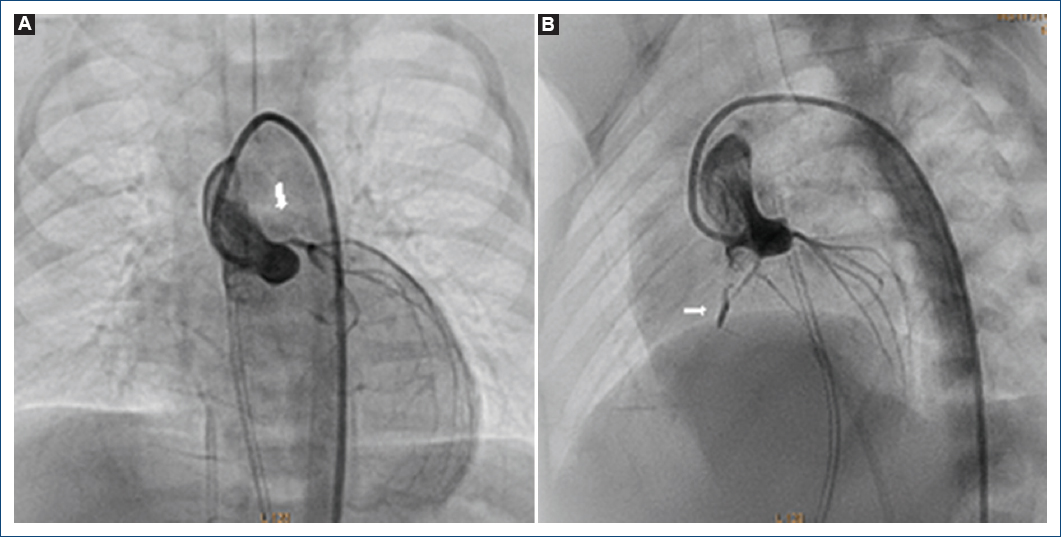
Figura 8 Coronariografía izquierda. A: proyección frontal: se observa el tronco coronario izquierdo con estenosis en su origen (flecha). B: proyección cuatro cámaras; flujo anterógrado de la circunfleja y atresia entre el tercio proximal y medio de la descendente anterior (flecha).
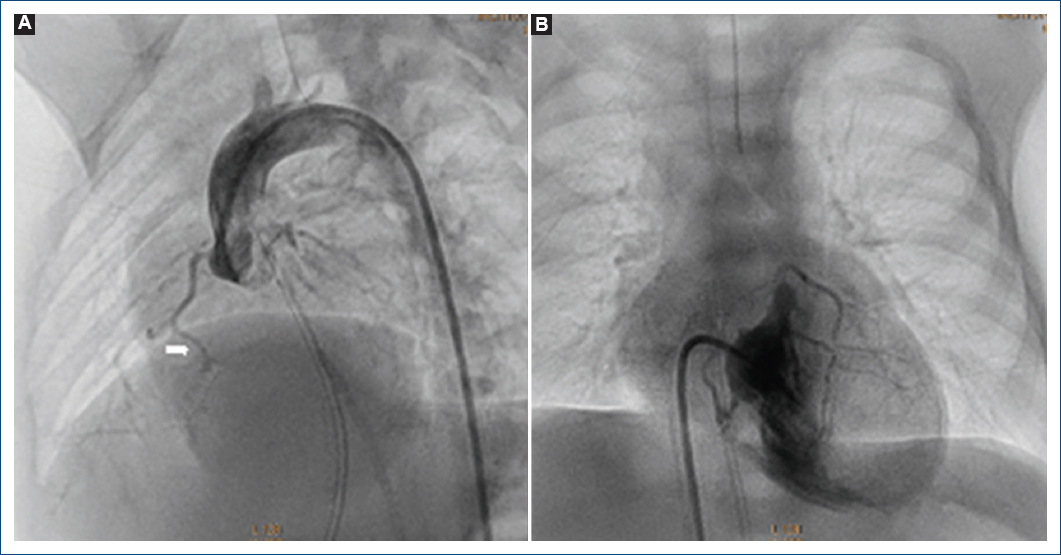
Figura 9 A: coronariografía derecha, se observa estenosis grave en la descendente posterior (flecha). B: ventriculografía derecha proyección postero-anterior, se observa atresia pulmonar con septum ventricular íntegro con conexiones ventrículo-coronarias con flujo retrógrado a la coronaria derecha y a la descendente anterior.
Discusión
Las estrategias de manejo de los pacientes con AP SVI ha cambiado a lo largo de los años, en la década de los 80 existía una tendencia a descomprimir todos los pacientes con AP-SVI, independientemente del tamaño de la válvula tricúspide, de la anatomía del VD y la anatomía coronaria, como consecuencia, aquellos pacientes con CCVDD tenían un desenlace fatal posterior a la descompresión del VD con mortalidad del 100%, esto secundario a isquemia miocárdica irreversible5. En los últimos años se han buscado diferentes métodos diagnósticos que permitan delimitar de forma precisa la anatomía coronaria y con mayor precisión el diagnóstico de la CCVDD con la finalidad de establecer la mejor conducta terapéutica que seguir, ya que estos pacientes tienen alto riesgo de sufrir isquemia progresiva irreversible que conduzca a la muerte independientemente de cualquier tratamiento establecido, siendo su única opción real el trasplante cardiaco1,3. Consideramos que muchos pacientes que se sometieron a cirugía univentricular y supuesta CCVDD realmente no lo son y fueron erróneamente catalogados como portadores de CCVDD.
Debido a la naturaleza heterogénea de esta patología y de las anomalías coronarias asociadas, el tratamiento puede resultar complicado y a pesar de las estrategias de tratamiento que van desde la reparación biventricular mediante descompresión del VD hasta la paliación univentricular o el trasplante cardiaco, la mortalidad global de estos pacientes oscila entre el 20 y el 42%1,3. Sin embargo, posterior a la primera etapa en aquellos pacientes que alcanzan la reparación definitiva (biventricular, 1 ½ ventricular o univentricular) la sobrevida es muy aceptable siempre y cuando no exista CCVDD3.
De acuerdo con un estudio de cohorte multicéntrico3, actualmente el tratamiento con descompresión del VD en aquellos pacientes que no tienen CCVDD ofrece un mejor pronóstico, disminuyendo la morbimortalidad comparada con aquellos pacientes que son sometidos a paliación univentricular. Esta estrategia se muestra promisoria para los casos limítrofes en los que no existen contraindicaciones coronarias para la descompresión del VD. Se han encontrado altas tasas de mortalidad temprana con la forma más grave de enfermedad coronaria (atresia), además los pacientes con enfermedad coronaria menos severa (fístulas ± estenosis pero sin atresia) tuvieron una mortalidad similar a aquellos sin anomalías coronarias conocidas, tanto en el periodo neonatal como después de la reparación definitiva3.
El gran reto de esta patología es la variabilidad interoperador que existe en la interpretación de los estudios angiográficos, incluso se ha desarrollado una escala o score basado en un puntaje tratando de detectar a los pacientes con CCVDD6. En Japón se reportó una descompresión transitoria transquirúrgica por Iwai et al.7, confirmando la CCVDD en un paciente previo a la derivación cavo-pulmonar. Lo anterior hace difícil establecer la mejor conducta terapéutica para cada paciente, por lo que pensamos que con el método angiográfico se está sobreestimando a muchos pacientes con CVC y muchos de estos realmente no tienen CCVDD, en contraparte algunos pacientes sin atresia de los ostium coronarios pueden ser realmente CCVDD (como los tres casos presentados), pero existe el riesgo de que cuando se les ofrece descompresión del VD, es entonces cuando el equipo cardiovascular se percata de la CCVDD, como han reportado otros autores, que presentan este tipo de errores de interpretación del estudio angiográfico2, por tal motivo en el Departamento de Hemodinámica del Instituto Nacional de Pediatría de México se diseñó una maniobra de descompresión transitoria percutánea que podría evaluar de forma objetiva aquellos casos donde exista duda de la existencia de la CCVDD (Fig. 11). Maniobra de descompresión transitoria.
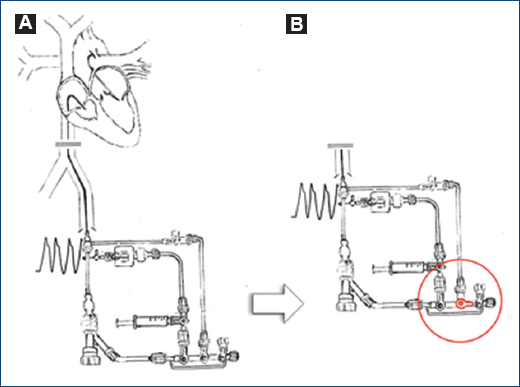
Figura 11 Maniobra de descompresión transitoria del ventrículo derecho. A: previo a la descompresión. B: descompresión del ventrículo derecho, la segunda llave se gira 90° en sentido horario, se permite el flujo libre del ventrículo derecho hasta la vena cava inferior con registro simultáneo de presiones.
La técnica o maniobra propuesta consiste en introducir un catéter multipropósito (diagnóstico) o un catéter guía Judkins derecho en la cavidad ventricular derecha sobre una guía de angioplastia coronaria 0.014”, este catéter se conectará en su parte distal a un circuito de puertos o llaves. como por ejemplo un manifold de tres puertos (válvulas o vías), en donde el primer puerto o vía (proximal) se conectará a un registro de presiones invasivas y el segundo puerto se conectará a la vía lateral de introductor arterial colocado en la vena femoral (se recomienda al menos 2 Fr mayor al tamaño del catéter utilizado), siendo el objetivo producir insuficiencia tricuspídea que mimetice una descompresión transitoria del VD, la tercera vía podrá utilizarse para administrar medio de contraste o puede permanecer cerrado. De manera inicial se realizará registro de presiones comparando la presión del VD y del VI o la aorta (Ao), manteniendo el segundo puerto cerrado (Fig. 11A), posteriormente se abrirá este segundo puerto (Fig. 11B) para que el flujo del VD fluya por el catéter-circuito de llaves o puertos y finalmente llegar libremente a la vena cava inferior. Se registrarán las curvas de presión de forma simultánea (VD y VI o Ao) y se realizará monitoreo hemodinámico, además de registro de EKG. La prueba o maniobra de descompresión transitoria se interpretará como negativa si no hay descompensación hemodinámica, ni datos de isquemia, lesión o infarto. En contraparte, será positiva si el paciente presenta deterioro hemodinámico con hipotensión, bradicardia, isquemia, lesión o infarto.
La maniobra será muy útil para el pronóstico de los pacientes con «verdadera» CCVDD, ya que la mejor conducta en esta situación sería referir tempranamente a estos pacientes a un centro con trasplante cardiaco, o en su defecto, en caso de no ser posible el trasplante, informar del mal pronóstico para la vida a los familiares a corto, mediano o largo plazo y evitar realizar procedimientos quirúrgicos o intervencionistas (p. ej., septostomía atrial) que no tendrán ningún beneficio para el paciente o que incluso pudieran ser deletéreos para la fisiología de los pacientes con CCVDD.
En aquellos casos donde se haya confirmado la CCVDD y exista un defecto interatrial restrictivo habrá que valorar muy bien si se realiza septostomía atrial, ya que se ha descrito que este procedimiento es un factor de riesgo de muerte en este tipo de pacientes5, tal como pudo observarse en nuestro primer caso, que posterior al cateterismo presentó isquemia-lesión e infarto que lo llevó a la muerte.
En aquellos casos donde se ha confirmado la no CCVDD, dependerá del tamaño del anillo tricuspídeo, de las características anatómicas del VD, así como de la experiencia de cada centro, si se ofrece o no descompresión del VD, siendo el objetivo ideal un procedimiento biventricular o 1 y ½ ventricular o en su defecto un procedimiento univentricular, pero con la seguridad de que no habrá eventos súbitos de descompensación o muerte relacionados con la anatomía de la circulación coronaria1,3,5,8.
Así mismo, pensamos que el diagnóstico de CCVDD actualmente está sobreestimado, ya que no existe un método objetivo y reproducible para poder confirmar o descartar la CCVDD en aquellos pacientes sin atresia de los ostium coronarios cuando el estudio angiográfico no es concluyente, sobre todo en los sitios de estenosis de las coronarias principales. El hecho de sobreestimar la presencia de CCVDD puede privar a muchos casos (sin CCVDD) de la posibilidad de descompresión del VD, ya que en muchos casos solo por la presencia de CVC son sometidos a una fisiología univentricular.
Consideramos que en algunos casos muy raros puede existir «codependencia» de la circulación coronaria, donde el VD perfunde el miocardio exclusivamente del VD (esta situación puede observase en la atresia del ostium coronario derecho o atresia en algún segmento de la coronaria derecha proximal), pero el VI tiene perfusión miocárdica por flujo anterógrado a partir de la coronaria izquierda, por lo que estos casos en particular, a pesar de tener dependencia de la circulación coronaria para el VD hacia el miocardio exclusivamente de este mismo ventrículo, no deberían catalogarse como CCVDD «estrictamente» y el término propuesto es el de «codependencia», que sería más apropiado para esta muy rara situación.
Por último, la maniobra de descompresión transitoria no sería recomendable cuando exista obstrucción proximal en el territorio de la coronaria izquierda (como los tres casos presentados), sin embargo puede ser muy útil cuando exista obstrucción proximal de la coronaria derecha y no haya ramas perfundiendo el VI, así mismo también sería útil cuando exista controversia o duda en el estudio angiográfico, ya que de esta precisión diagnóstica en la anatomía coronaria se determinará el procedimiento que ofrecer en cada caso en particular.
En resumen, pensamos que actualmente muchos de estos pacientes con CVC realmente no tienen CCVDD y se les quita la oportunidad de tener la posibilidad de descompresión del VD y por lo tanto de una fisiología biventricular o al menos 1 y ½ ventricular. Así mismo, consideramos que la realización de una paliación univertricular en los pacientes con «verdadera o real» CCVDD es una conducta terapéutica inadecuada, ya que el desenlace posterior a la derivación cavo-pulmonar total será fatal en algún momento de la evolución. Así mismo, la certeza de CCVDD nos deberá hacer valorar la necesidad de realizar una septostomía atrial, ya que en estos pacientes el procedimiento percutáneo para incrementar de tamaño el defecto interatrial es un factor de riesgo para presentar deterioro hemodinámico y muerte en este tipo de casos9.
Al momento de este manuscrito no se ha realizado en ningún paciente la maniobra de descompresión transitoria vía percutánea del VD, lo cual es una limitante de nuestro estudio.
Conclusiones
En muchos casos con AP-SVI el estudio angiográfico podrá ser suficiente para determinar la circulación coronaria de manera fidedigna. Sin embargo, dada la dificultad en algunos casos con CVC de determinar al 100% la no CCVDD, se requiere (aparte del estudio angiográfico) un método o maniobra objetiva, reproducible, así como transitoria y reversible que permita en aquellos pacientes con CVC pero sin CCVDD estar completamente seguros de esta situación, con el objetivo de que se les pueda ofrecer descompresión del VD (ya sea por vía quirúrgica, percutánea o híbrida), siempre y cuando las características del VD y la válvula tricúspide lo permitan.
En contraparte, en aquellos pacientes con «verdadera» CCVDD lo ideal sería ser referidos tempranamente a trasplante cardiaco, ya que consideramos que la fisiología univentricular no es una opción viable en esta situación, en caso de no ser posible el trasplante cardiaco entonces se podría ofrecer una fistula sistémico-pulmonar o un stent ductal, pero con el conocimiento de que el pronóstico será fatal en algún momento de la evolución.
La amplia gama de definiciones de la CCVDD solo refleja que se requiere mayor investigación y conocimiento sobre la fisiología de la circulación coronaria en la AP-SVI. La maniobra propuesta podría ayudar en establecer un diagnóstico preciso de la circulación coronaria en los pacientes con CVC en el contexto de AP-SVI cuando exista duda o controversia en el estudio angiográfico.











 text new page (beta)
text new page (beta)