Introducción
La actividad humana ha causado que las emisiones de CO2 se emitan en grandes cantidades a la atmósfera y afecte seriamente al medio ambiente y la calidad de vida de las personas. Se estima que sin el CO2 y el vapor de agua en la atmósfera, la temperatura promedio en la superficie de la Tierra sería con valores bajo cero, ya que estos gases absorben parte de la radiación infrarroja que va de regreso al espacio después de rebotar en la superficie terrestre (Abdullah et al., 2022). De esta forma, si no se disminuyen drásticamente las emisiones de carbono, habrá un daño irreparable al planeta, pero ¿Qué pasaría si hubiera una manera de capturar carbono de la fuente y atraparlo en algún lugar permanentemente?
La captura de CO2 consiste, de manera general, en la separación del dióxido de carbono del resto de gases que se originan durante la combustión en centrales térmicas, refinerías de petróleo, fabricación de cemento e industria siderúrgica, fundamentalmente. Una vez separado, se transporta e inyecta en formaciones geológicas profundas, donde permanecerá confinado de forma segura por un tiempo indefinido. De esta manera se reduce la cantidad de CO2 emitida a la atmósfera (López et al., 2013).
Acorde a lo que menciona Cuellar et al. (2015) el proceso de transformar CO2 consiste en la conversión química que ocurre con los adsorbentes alcalinos. La transformación de CO2 en carbonatos de calcio y magnesio estables e insolubles en agua es un enfoque sostenible para el almacenamiento permanente de CO2 (Shan et al., 2018). A su vez, la adsorción es un proceso de separación en el que se transfiere un material conocido como adsorbato, de un fluido ya sea líquido o gaseoso a una fase sólida denominada adsorbente (Adamson, 1996). En este proceso, el material adsorbente se trata de un sólido poroso para concentrar al adsorbato en su superficie (Beruto & Botter, 2000).
Varios adsorbentes alcalinos se han propuesto para captura y mineralización del CO2 a través de la carbonatación gas-sólido tales como óxidos metálicos simples (por ejemplo, CaO, MgO), hidróxidos (por ejemplo, Ca(OH)2, Mg(OH)2 y Na(OH) 2 (Reddy et al., 2011). Estas nanopartículas consisten en partículas de metales comunes con tamaños inferiores a los micrones, es decir, de escala nanométrica (Gislason et al., 2014). El hidróxido de calcio se puede utilizar como reactivo (Vance et al., 2015), la carbonatación mineral implica la reacción de CO2 con óxidos metálicos tales como magnesio y óxido de calcio para formar carbonatos (Cuellar et al., 2015). Los hidróxidos y óxidos de calcio y de magnesio son minerales de silicato, que son relativamente abundantes en todo el mundo, son una materia prima atractiva para la mineralización del CO2 (Styring & North, 2015). En este sentido, el material denominado SBA-15 (Santa Bárbara Amorfo No. 15), que fue desarrollado por primera vez por Stucky et al., (1994), posee una alta área superficial y una estructura hexagonal de poros uniformes (honeycomb-like), y que además, puede ser preparado en un amplio rango de tamaños de poro (4.6 nm a 30 nm) y espesores de pared de poro (3.1 nm a 6.4 nm) (que se logra variando la temperatura (35 ºC a 140 ºC) y tiempo de reacción (11 h a 72 h) durante su síntesis); ofrece propiedades texturales adecuadas para incorporar en su superficie nanopartículas de hidróxidos y óxidos metálicos, generando una alta dispersión de éstos y en consecuencia, se podrían generar adsorbentes más activos para la reacción de carbonatación.
En este trabajo se buscan desarrollar materiales adsorbentes de CO2 con base en sílices mesoporosas del tipo SBA-15 de talla corta y decorada con nanopartículas de los hidróxidos y óxidos metálicos de calcio y magnesio, para la captura y conversión de CO2.
Materiales y métodos
Preparación de materiales
Síntesis del material de sílice mesoporoso ordenado SBA-15c
El material de sílice mesoporoso SBA-15 corta se preparó mediante el proceso Sol-Gel (Zarazua et al., 2017), donde se utiliza un surfactante neutro como agente director de la meso-estructura, el Pluronic P123.
El P123 se disuelve en una solución de ácido clorhídrico y agua desionizada con agitación constante a 35°C. Una vez completamente disuelto el P123, se inicia el proceso Sol-Gel mediante la adición del precursor de la sílice (Hernández et al., 2013) el TEOS. La reacción se realizó por 24 horas y con agitación constante.
Transcurrido este tiempo se efectúa el proceso de madurado, colocando el gel obtenido en un recipiente de polipropileno, se tapa y se coloca en la mufla durante 24 horas a una temperatura de 80°C sin agitación.
Al terminar se deja enfriar y se recupera el sólido por filtración (Styring & North, 2015). Se seca a temperatura ambiente y posteriormente a 110°C por 18 h a una rapidez de calentamiento de 2°C/min.
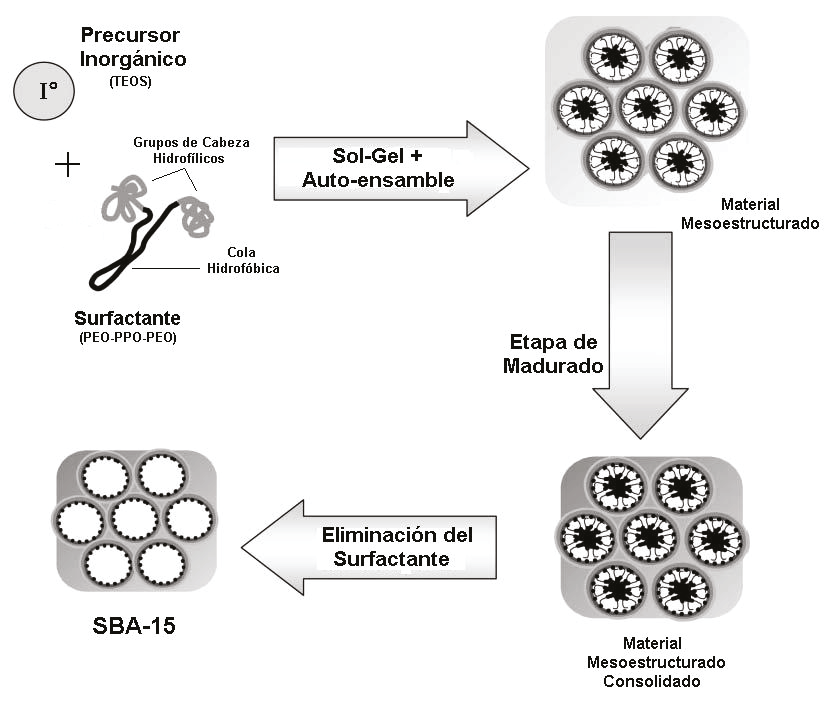
Finalmente, se calcina a 550°C por 4 h a una rapidez de calentamiento de 1°C/min. De esta manera se logrará eliminar la base orgánica dando como producto solo la estructura mesoporosa de sílice (Vance et al., 2015). El proceso se describe en la siguiente Figura 1.
Incorporación de las nanopartículas de Ca(OH)2 y de Mg(OH)2 en la SBA-15c
Para la incorporación de las nanopartículas de hidróxido de calcio (Ca(OH)2) e hidróxido de magnesio (Mg(OH)2) en la superficie de la sílice mesoporosa de talla corta SBA-15c se empleó el método de impregnación por llenado de poro (mojado incipiente) (Feliczak et al., 2016). Se utilizaron como fuente los hidróxidos de calcio y magnesio, soluciones acuosas de acetato de calcio (II) dihidratado Ca(OH)2·2H2O (Sigma-Aldrich) y acetato de magnesio (II) dihidratado Mg(OH)2·2H2O (Sigma-Aldrich). Se variaron las cantidades (5, 10 y 15 % en peso) de Ca(OH)2 y de Mg(OH)2 y de (5, 10 y 15 % en peso) de CaO y de MgO que se depositaron en la SBA-15c. Posteriormente, las muestras impregnadas se secaron a una temperatura de 110ºC por 18h.
Caracterización de materiales
Determinación de las propiedades texturales, morfológicas, estructurales y electrónicas de los materiales adsorbentes:
Isotermas de adsorción-desorción de N2 a 77 K
Las propiedades texturales de las sílices mesoporosas SBA-15 y NH2-SBA-15 se determinaron mediante las isotermas de adsorción-desorción de N2 a 77 K en un equipo Autosorb iQ2, de la marca Quanthachrome.
Previo al análisis, la muestra se desgasifico a 150°C a vacío durante 5 h, para asegurar una superficie seca, limpia y libre de especies débilmente adsorbidas.
Difracción de Rayos-X (DRX) a ángulos bajos y convencionales
Mediante la difracción de rayos-X (DRX) a bajos ángulos (0-5° en 2θ), se verificaron el orden en el arreglo de los poros de la SBA-15C y de la NH2-SBA-15C (Tanev & Pinnavaia, 1995).
Microscopía Electrónica de Barrido (SEM)
Con el microscopio electrónico de barrido HITACHI SU8200 se tomaron las imágenes de las muestras de la SBA-15C y de la NH2-SBA-15C, con las cuales se determinaron principalmente la morfología y el tamaño de las partículas (Chang, 2017b).
Las muestras en forma de pastilla se colocarán en los portamuestras y se recubrirán con carbón.
Espectroscopía de infrarrojo con transformada de Fourier (FT-IR)
La presencia de los grupos amino en la superficie de la sílice mesoporosa SBA-15c, así como la interacción de la molécula de CO2 con los grupos de amino, se analizaron por medio de la respuesta vibracional de sus enlaces moleculares, a través de los análisis por espectroscopía de infrarrojo (Beck et al., 2008). Los espectros de vibración de IR de las muestras en polvo, se medirán en un espectrofotómetro Bruker Vector 33, en el rango de 400 a 4000 cm-1, con una resolución de 2 cm-1.
Espectroscopía micro Raman
Los espectros vibrónicos de los enlaces moleculares debido a la presencia de los grupos amino en las muestras de NH2-SBA-C y como caracterización complementaria a los espectros de FT-IR, se realizó la espectroscopía micro Raman, utilizando un microespectrómetro modelo Labram-Dior (López et al., 2013).
Análisis Termogravimétrico (TGA)
El análisis termogravimétrico TGA/DTG permitirá evaluar la estabilidad térmica de los grupos funcionales amino en el interior de los poros de los materiales mesoporosos (Montes et al., 2012). Este estudio se realizará en un equipo Q500 TGA y Q2000 DSC de TA Instruments, en un rango de temperatura de 25 °C a 600° C.
Reacción decarbonatación
La reacción de carbonatación bajo condiciones no-isotérmicas se efectuó en un analizador termogravimétrico TGA/DTG, en un equipo Q500 TGA de TA Instruments, en un rango de temperatura de 25°C a 800°C. Con una rapidez de calentamiento de 10°C/min y un flujo de 50 mL/min de 100 % de CO2 gas.
Determinación del tipo de interacción entre las nanopartículas de hidróxido y óxido de calcio y magnesio.
Espectroscopía fotoelectrónica de rayos-X (XPS)
La técnica XPS permite identificar las especies en una muestra, su estado de oxidación y su entorno químico. Debido a que cada átomo tiene un factor de respuesta característico, la señal de XPS se puede utilizar en la determinación cuantitativa de especies químicas en la superficie (Zhao et al., 1998).
Para verificar la adsorción de las moléculas de CO2 en los adsorbentes se realizó la espectroscopia fotoelectrónica de rayos X (XPS).
Resultados y discusión
Calorimetría diferencial de barrido (DSC)
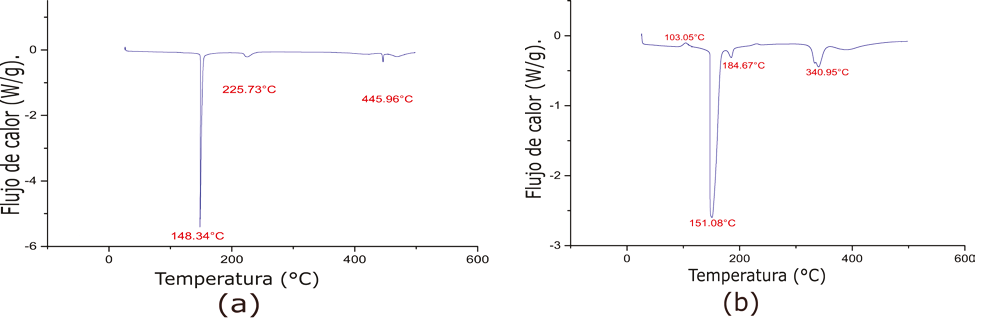
Los precursores del Ca y Mg impregnados en la SBA-15c, y que se les dio un tratamiento térmico de 110°C, determinaron con mayor precisión a qué temperatura se obtienen los hidróxidos y óxidos de calcio y magnesio, de acuerdo con lo reportado en la literatura (Figura 2).
Fluorescencia de Rayos X. FRX
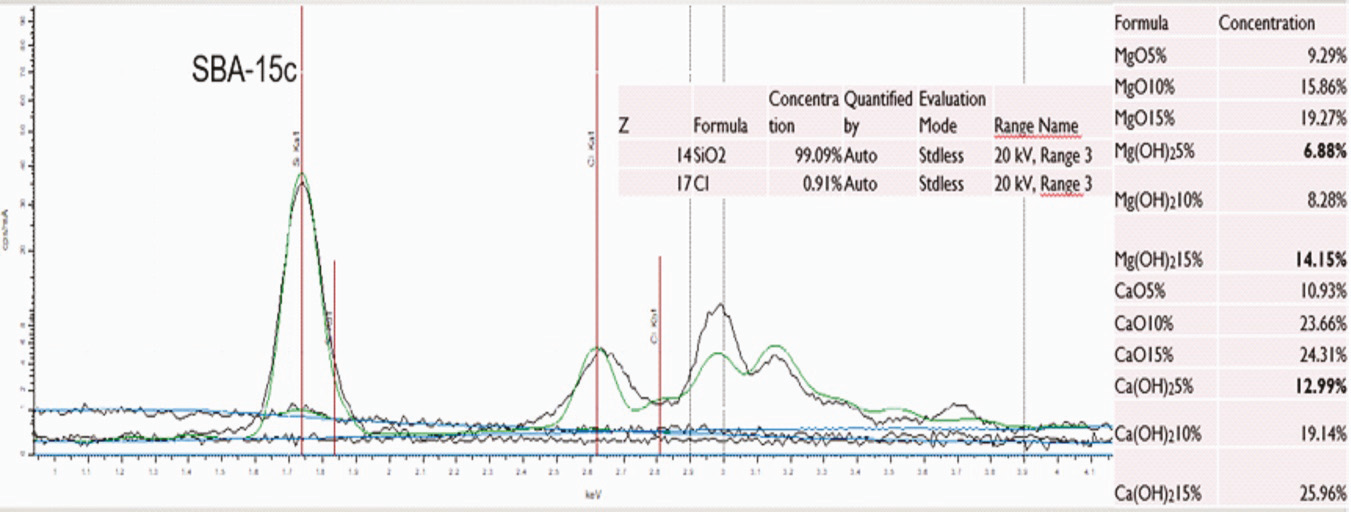
La sílice mesoporosa pura (SBA-15c) y los diferentes resultados se mostraron respecto con la proporción equivalente de cada uno de los precursores, empezando por los óxidos de magnesio, de 5 %, 10 % y 15 %, los hidróxidos de magnesio, de 5 %, 10 % y 15 %, óxidos de calcio, de 5 %, 10 % y 15 % y los hidróxidos de calcio, de 5 %, 10 % y 15 %, los cuales se encuentran en una proporción adecuada (Figura 3).
Espectroscopia micro-Raman
Al igual que en la reflectancia difusa UV-VIS, el estudio en micro-Raman nos confirma la presencia de los hidróxidos y óxidos de calcio y de magnesio. Se muestran las cargas (números de onda) (Figura 5).
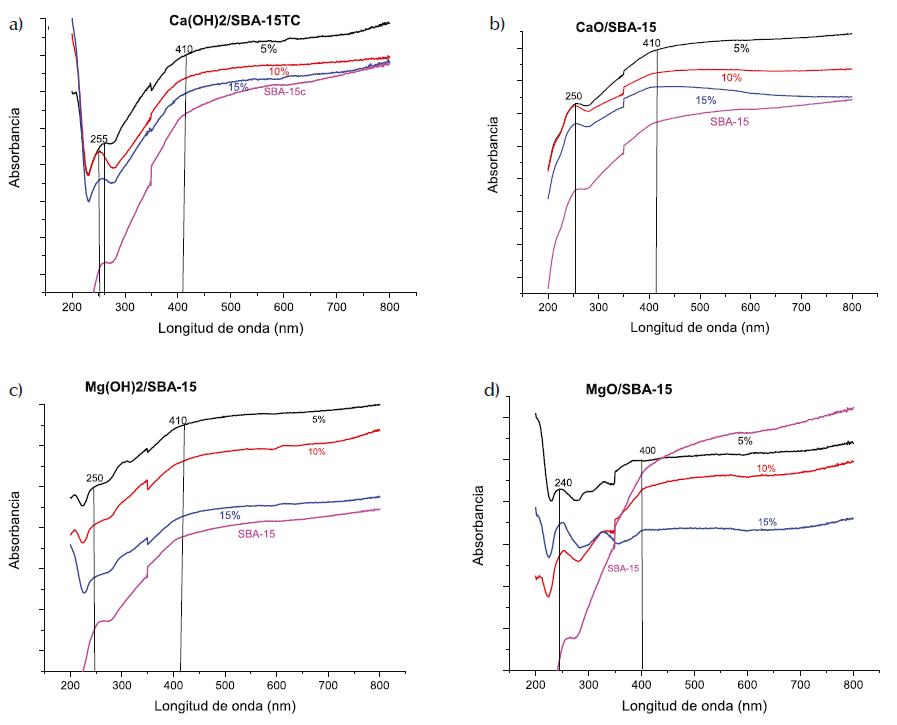
Figura 4 a) Dos bandas de absorción con alta intensidad centradas en aproximandamente 255 y 360 nm, característicos del Ca2+ unido al OH-, en los bordes y esquinas de los cristalitos del Ca(OH)2, b) Dos bandas de absorción con alta intensidad, aproximadamente en 250 y 350 nm, característicos del Ca2+ unido al O2-, en los bordes y esquinas de los cristalitos de CaO, c) Dos bandas de absorción con alta intensidad, aproximadamente en 250 y 330 nm, característicos del Mg2+ unido al OH-, en los bordes y esquinas de los cristalitos de Mg(OH)2, d) Dos bandas de absorción con alta intensidad, aproximadamente en 250 y 330 nm, característicos del Mg2+ unido al O2-, en los bordes y esquinas de los cristalitos de MgO. Estas bandas indican la presencia de los hidróxidos y óxidos de calcio y de magnesio
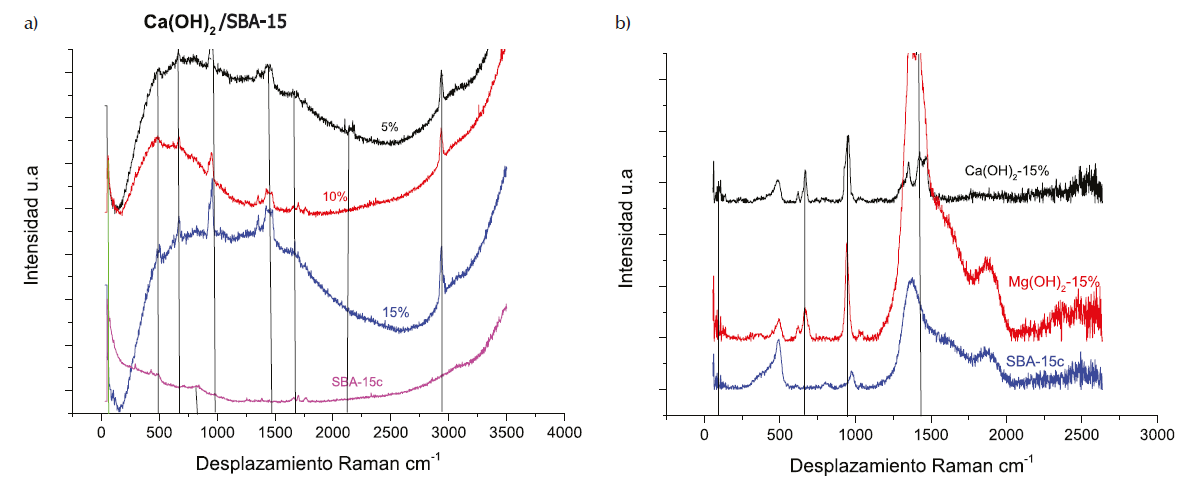
Figura 5 En la figura de la izquierda, en los espectros se observan picos en las posiciones de 80 cm-1, 500 cm-1, 700 cm-1, 1000 cm-1, 1500 cm-1, 1700 cm-1 y 3000 cm-1 aproximadamente, asignados a los modos de vibración, respectivamente. Estos modos ópticos son característicos de la estructura hexagonal. En la figura de la derecha, en estos espectros se observan picos en las posiciones de 80 cm-1, 500 cm-1, 700 cm-1, 1000 cm-1, 1500 cm-1, 1700 cm-1 y 1900 cm-1 aproximadamente, asignados a los modos de vibración, respectivamente
Difracción de Rayos X (DRX)
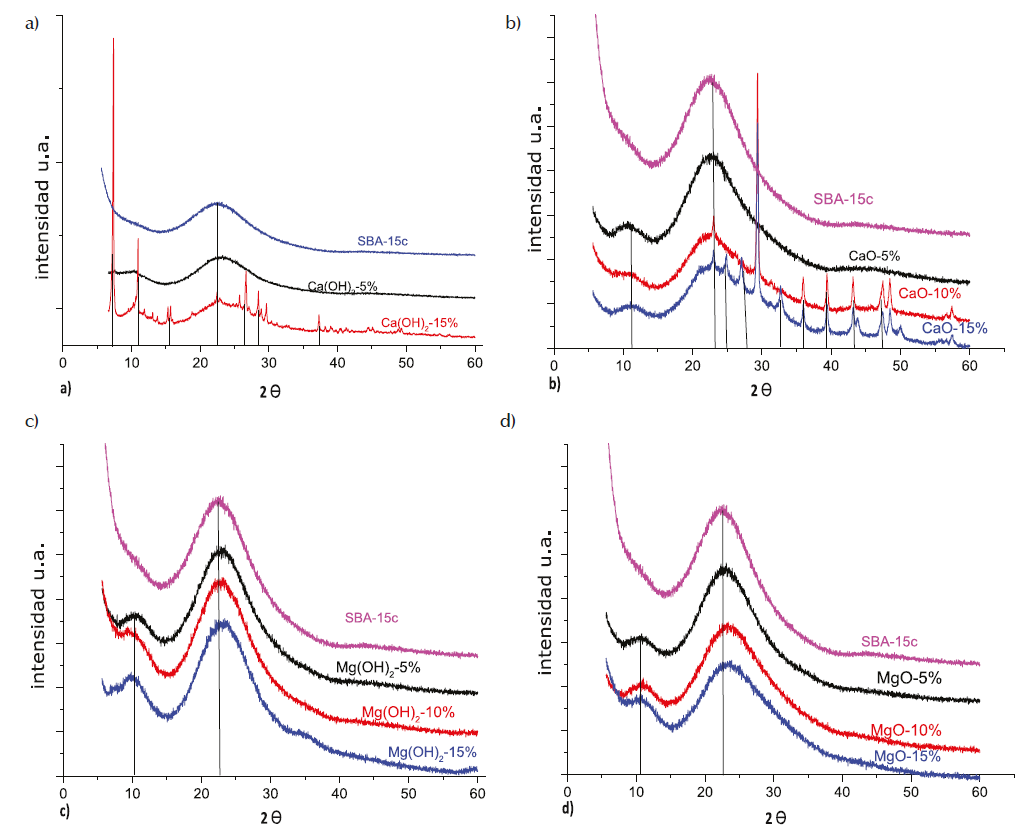
Se puede observar en las imágenes de los incisos a y b (Figura 7), que las reflexiones que se presentan son más, pero más cortas, mientras en la imagen del inciso c se ve una reflexión pronunciada distinta a la de la sílice mesoporosa pura, lo que indica la existencia del Mg(OH)2, impregnado, lo mismo sucede en el inciso d con el MgO, por lo que en todas las muestras analizadas se impregnaron con éxito los hidróxidos y óxidos de calcio y magnesio.
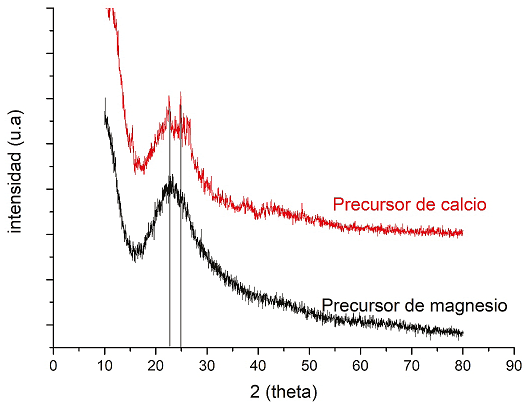
Figura 6 La reflexión intensa, pero muy amplia, centrada en 24° en 2θ corresponde a la sílice amorfa y sobre ella se ven algunas reflexiones características para el CaO y apenas para el MgO, puesto que estos óxidos están soportados en la superficie de la SBA-15c se ven más reflexiones, pero son débiles y amplias, lo cual significa que el CaO soportado en la SBA-15c es amorfa o está tan dispersa que está en tamaño de nanopartículas muy pequeñas de 5 nm o menos, no se puede determinar adecuadamente porque el haz de electrones puede ser más grueso. El MgO no tiene reflexiones bien definidas, se encuentran altamente dispersos en la SBA-15c y es bueno, porque entre más dispersas estén las nanopartículas de óxidos e hidróxidos, se tendrá una mayor cantidad de sitios activos para la adsorción. Se secó a 110°c. En el precursor de calcio se presenta una reflexión aproximadamente en 23° y 25° en 2 theta, característico de una sílice amorfa
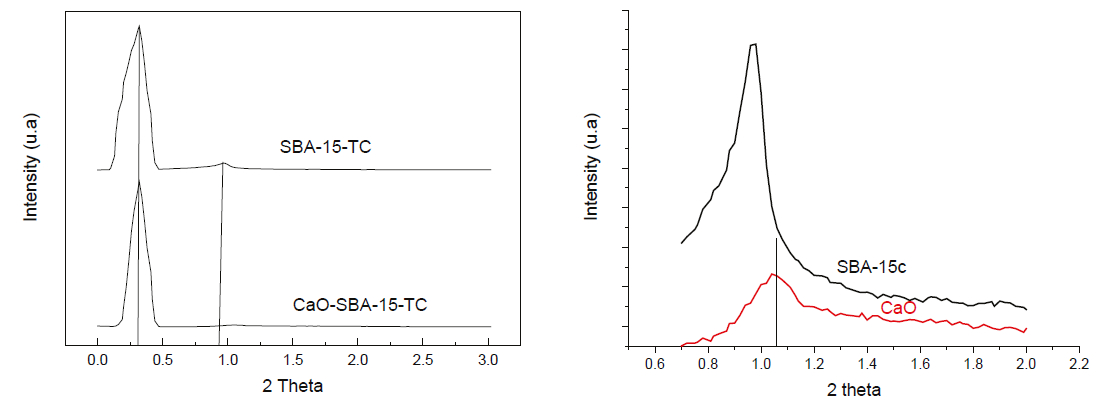
Difracción de Rayos X a bajos ángulos
En la Figura 8 del lado izquierdo, se puede ver el valor de 2 theta entre 0.3 y 0.9, que es característico de una estructura hexagonal del material mesoporoso SBA-15c, del lado derecho se analizó el mismo material, pero acortando el valor de 2 theta desde 0.6 y hasta 2.2, para saber realmente lo que estaba sucediendo, se puede ver la reflexión del CaO, que se encuentra presente en la sílice mesoporosa SBA-15c.
SEM
Aún con la impregnación de los hidróxidos y óxidos de calcio y magnesio se conserva la estructura de la SBA-15c. En todas las imágenes se observan partículas a simple vista que no se ven en la SBA-15c, lo cual comparándolo con los otros métodos que se llevaron a cabo nos dice que existe la presencia del calcio y magnesio, estos se encuentran en la superficie externa. En la figura d, se puede ver que existe mayor área superficial por lo que es muy probable que los CaO, se encuentren impregnados en la superficie interna de los poros (Figura 9).
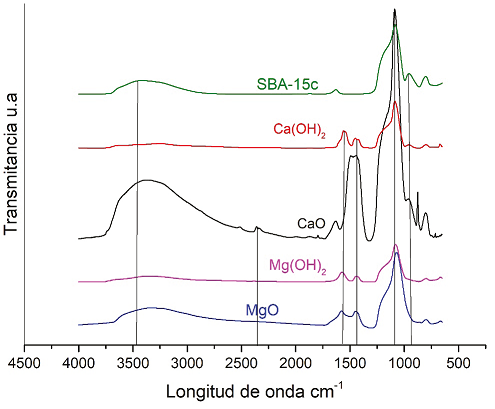
Espectroscopía de Infrarrojo
Las siguientes bandas mostradas en la Figura 10 indican:
750-800 cm-1, se asigna a la vibración del enlace Si-O-Si, grupo siloxano.
950 cm-1 grupo silanol Si-OH.
1100 cm-1 grupo siloxano Si-O-Si.
1600 cm-1 agua adsorbida en el material.
2300 cm-1 interacción entre CaO y Si.
3500 cm-1 grupo silanol Si-OH.
Se confirma con el análisis de Micro Raman que entre mayor porcentaje serán de mayor tamaño los números de onda.
Isotermas de MgO y CaO/ Distribución de tamaño de poros de MgO y CaO
Las propiedades texturales de los materiales mesoporosos se estudiaron mediante las isotermas de adsorción-desorción N2 a 77 K. Las distribuciones de tamaño de poro se calcularon a partir de la isoterma de adsorción, utilizando el modelo Barrett-Joyner-Halenda.
Las isotermas de adsorción-desorción N2 de los materiales se presentan en la Figura 11, del lado izquierdo. Todas las muestras mesoporosas de MgO/SBA-15c y CaO/SBA-15c, así como la SBA-15c pura, exhiben isotermas de adsorción del tipo IV con áreas de histéresis tipo H1 según la clasificación IUPAC. Estas isotermas son características de materiales mesoporosos con una disposición hexagonal de poros.
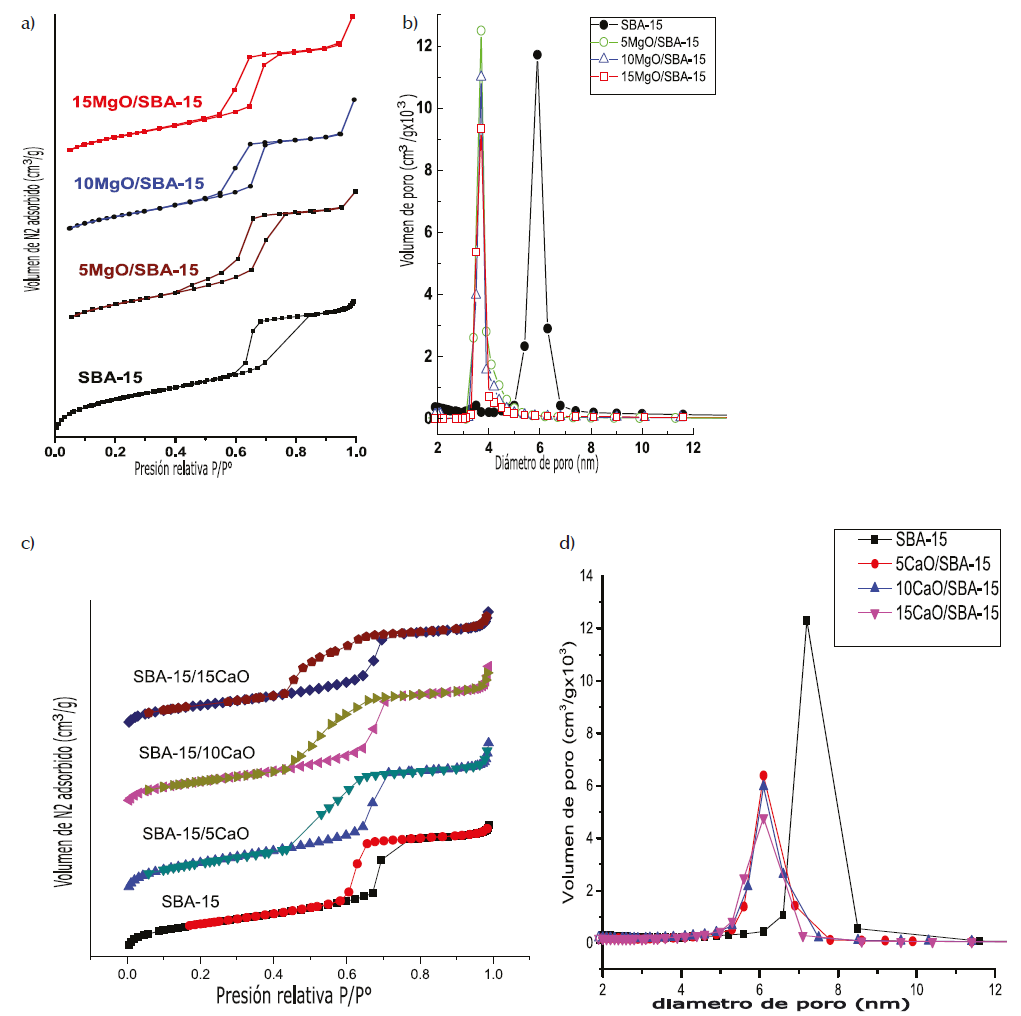
Figura 11 Isotermas de MgO y de CaO del lado izquierdo/distribución de tamaño de poros de MgO y de CaO del lado derecho
La muestra SBA-15c presenta el área de histéresis en un rango bien definido a altas presiones relativas (0.61 <P/P0 <0.8) que representa el llenado espontáneo de los mesoporos debido a la condensación capilar, indicando la presencia de mesoporos uniformes. Las sílices mesoporosas modificadas de MgO y CaO muestran áreas de histéresis a intervalos de presiones relativas más bajas (0.4 <P/P0 <0.7) debido a una disminución en el tamaño de los mesoporos por la presencia de pequeñas partículas de MgO y CaO dispersas dentro de los poros de SBA-15c.
Todas las isotermas presentadas son similares a las reportadas en la literatura para la sílice mesoporosa SBA-15c. Como se ve en la Figura 11, del lado izquierdo, las isotermas de adsorción-desorción de N2 de las matrices mesoporosas (MgO)X/SBA-15 y (CaO)x/SBA-15c son similares, lo que indica que la mesoestructura del material SBA-15c se mantuvo tras la incorporación de MgO.y de CaO.
En cuanto a la distribución del tamaño de poro que se muestra en la misma figura, del lado derecho cabe señalar que todas las matrices mesoporosas muestran una distribución uniforme y estrecha del tamaño de poro. Parece haber un cambio de diámetro de poro a un diámetro más pequeño tras un aumento de la carga de MgO y de CaO. Simultáneamente, el volumen total de N2 disminuyó con el aumento de la carga de MgO y de CaO en las matrices mesoporosas. Como era de esperar, la carga de magnesio y del calico en la matriz de sílice disminuye el área superficial y el volumen de poro del soporte SBA-15 (Tabla 1).
Tabla 1 Propiedades texturales de los materiales mesoporosos de SBA-15, de MgO/SBA-15c y de CaO/SBA-15c
| Muestra | MgO y CaO
(wt.%) |
SBET
(m2/g) |
Vtotal
(m3/g) |
Dp
(nm) |
| SBA-15 | 0.0 | 932 | 1.05 | 5.9 |
| 5%MgO/SBA-15c | 9.29 | 659 | 0.83 | 5.0 |
| 10%MgO/SBA-15c | 15.86 | 505 | 0.69 | 5.0 |
| 15%MgO/SBA-15c | 19.27 | 507 | 0.52 | 4.1 |
| 5%CaO/SBA-15c | 10.93 | 584 | 0.694 | 5.1 |
| 10%CaO/SBA-15c | 23.66 | 575 | 0.683 | 4.9 |
| 15%CaO/SBA-15c | 24.31 | 506 | 0.581 | 4.0 |
Nota: Área superficial específica BET (SBET), volumen total de poros (Vtotal) y diámetro de poro (Dp)
Al aumentar la carga de Mg y de CaO, hay un cambio de diámetro a más pequeño y el volumen total también disminuye.
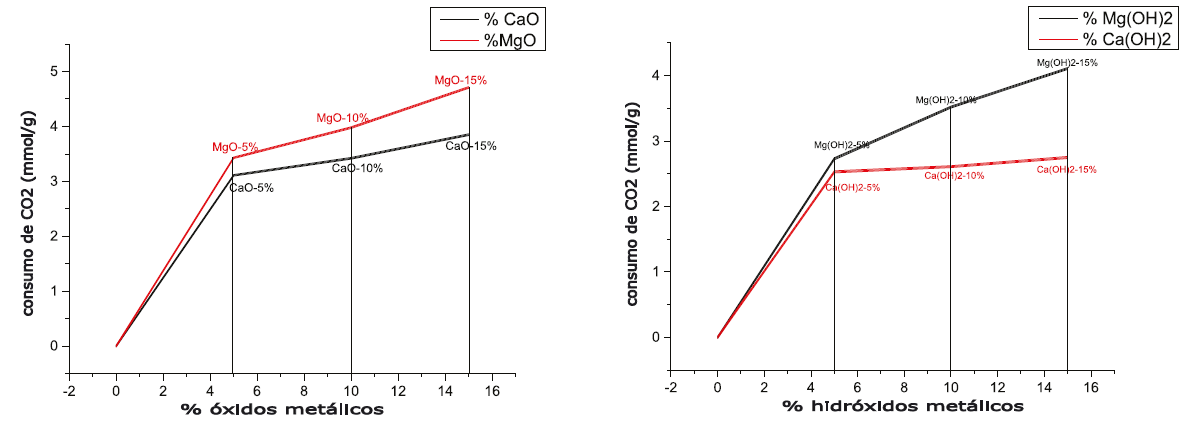
Adsorción de CO2. TGA
De acuerdo con el estudio realizado se puede ver que entre mayor sea el porcentaje de impregnación de los óxidos e hidróxidos de calcio y magnesio, su adsorbancia aumenta, pero el material que mayor adsorción de CO2 presenta es el magnesio (Figura 12).
Conclusiones
Se preparó de manera exitosa el material de sílice mesoporoso SBA-15c mediante el proceso Sol-Gel con un surfactante neutro como agente director de la meso-estructura, el Pluronic P123.
Los resultados de DRX, Micro Raman y FTIR, indicaron la presencia de las nanopartículas de los óxidos e hidróxidos de calcio y de magnesio en la SBA-15c.
Los resultados de SBET (distribución del diámetro de poro) indicaron que las nanopartículas de óxido de magnesio se encuentran dispersas en la superficie interna de los poros de la SBA-15c.
Los resultados de DRX, indicaron una alta dispersión de los hidróxidos y óxidos de magnesio en la SBA-15c, generando una mayor densidad de sitios activos para la adsorción de CO2 y por lo tanto un mayor consumo de CO2.
Entre mayor sea el porcentaje de impregnación de los óxidos de calcio y magnesio, mayor consumo de CO2 se obtendrá.
De acuerdo con los estudios realizados se puede ver que el material que se encuentra soportado en la sílice mesoporosa del tipo SBA-15c con mayor adsorción de CO2 es el magnesio, y el cual va en aumento mientras mayor sea la proporción de la impregnación, para el 15 % de MgO, 4.5 mmol/g y 4.1 mmol/g para 15 % de Mg(OH)2.
Declaración de interés en competencia
Los autores declaran que no tienen intereses financieros en competencia ni relaciones personales conocidas que pudieran haber influido en el trabajo informado en este documento.











 text new page (beta)
text new page (beta)