Introducción
La producción mundial de hongos comestibles ha aumentado significativamente de 1978 al 2022, se registró poco más de 48 millones de toneladas en este último año, el principal productor fue China con 45 millones de toneladas, seguido de Japón con 469, 491 t, y en tercer lugar Estados Unidos con 318,600 t (FAOSTAT, 2023). De las especies más comercializadas, se encuentran Agaricus bisporus (Champiñón de París), Lentinula edodes (Shiitake), Pleurotus ostreatus (hongo ostra), Auricularia (oreja de judas) y Flammulina (seta de aguja de oro) (Briceño y Morales, 2019). El cultivo de hongos comestibles es una alternativa para aprovechar los residuos lignocelulósicos que se encuentran disponibles por ser una abundante materia prima existente (Díaz- Muñoz et al., 2019). Para la producción del género Pleurotus, se utilizan diversos residuos agrícolas y agroindustriales, como las pajas, entre las cuales se pueden encontrar las de trigo, de arroz, de cebada, de soya, de frijol, de sésamo; rastrojos maíz, de tomate, sorgo, de jamaica, de quinua, pulpa de café, de limón, de cardamomo; bagazos de caña, de cebada, yuca, y remolacha azucarera, así mismo, de árboles forestales como el aserrín, viruta de cedro, viruta de pino, astillas de eucalipto, otros como la hierba de india, malezas y especies arbustivas del bosque (Piña-Guzmán et al., 2016). No obstante, la elección del sustrato está ligada a la disponibilidad de residuos agrícolas presentes en una región.
Sin embargo, para utilizar los sustratos en el cultivo del hongo, es necesario proporcionarles un tratamiento previo, se puede aplicar calor para disminuir la flora microbiana nociva que se encuentra presente en ellos y así evitar que los microorganismos compitan por espacio y nutrientes con el micelio a cultivar. De esta manera, la pasteurización es un método cuyo propósito es preparar el substrato para un eficaz desarrollo del hongo al eliminar microorganismos patógenos y se puede aplicar de dos formas: pasteurización con vapor y pasteurización por inmersión en agua caliente (Chen et al., 2021; Gaitán-Hernández et al., 2006; Grassi & Restelli, 2019).
La pasteurización con vapor consiste en colocar el substrato en un área cerrada, puede ser un cuarto pequeño o un recipiente metálico, se aplica vapor generado por una caldera eléctrica, ya sea de diesel o gasolina, por medio de tubos de cobre o mangueras resistentes al calor. La temperatura debe alcanzar entre 70-80 °C, además, el substrato debe mantenerse de 2 a 4 h a esta temperatura. Esta técnica ha sido utilizada por diversos autores como Fernández et al. (2020), Filippi et al. (2019), Garzón-Gómez & Cuervo-Andrade (2008), entre otros.
Por otro lado, Chanchao et al. (2023) desinfectaron a una temperatura de 121 °C durante 30 min el aserrín y harina de arroz utilizados como sustrato para el cultivo de Volvariella volvacea. Así mismo, Ye et al. (2023), para las bolsas con carrizo (Phragmites autrales) utilizaron la misma temperatura (121 °C), no obstante, el tiempo fue de 2 h en la autoclave, para el cultivo de P. ostreatus y P. eryngii (Yin et al., 2025), utilizaron la misma temperatura al pasteurizar, sin embargo, el tiempo fue de 3 h con los sustratos de aserrín, paja de trigo y salvado de trigo para el cultivo de Shiitake, ostra y reishi.
La desinfección por inmersión en agua caliente consiste en sumergir el sustrato en agua (75-80 °C) durante 1 h. Autores como Cruz-Moreno (2019), Díaz Muñoz et al. (2019), Fernández-Uribe (2014) y Romero-Arenas et al. (2018) por mencionar algunos, han utilizado esta técnica, la cual ha sido efectiva para la producción.
Otro método para desinfectar los sustratos fue el utilizado por Cruz et al. (2010) quienes sumergieron el sustrato en agua a temperatura ambiente durante un periodo de tiempo 24-30 h, en una solución de agua y CaO, para posteriormente escurrirlo durante 12 horas en época de verano y 24 horas en época de invierno. Lograron cosechas de entre 0.270 g a 1.59 kg de hongo fresco en sustratos de olote de maíz y pulpa de café, solos y combinados a distintas proporciones.
Por lo anterior, el objetivo de esta investigación fue evaluar dos métodos de desinfección de rastrojo de maíz y de paja de sorgo utilizados como sustratos para la producción de Pleurotus ostreatus de manera rústica.
Materiales y métodos
Este experimento se realizó dentro de las instalaciones del Colegio de Postgraduados Campus Campeche ubicado en la Carretera Haltunchén - Edzná, km. 17.5 Sihochac, Champotón, Campeche, el cual se ubica entre los paralelos 17°49’ y 20°51 N, 89°06’ y 92° 27’ O, en el municipio de Champotón en el Estado de Campeche. La fase de pasteurización de los sustratos se realizó en el campo experimental, la fase de siembra y producción se realizó en el laboratorio de Fitopatología del campus con una temperatura controlada de 23 °C.
El rastrojo de maíz y la paja de sorgo se obtuvieron mediante donación de algunos productores que se dedican a la producción de estos cultivos en la región, en cuanto al micelio con la cepa de P. ostreatus utilizado para la siembra fue adquirido de manera comercial.
Desinfección del sustrato
Se utilizaron dos tipos de residuos agrícolas: rastrojo de maíz (M) y paja de sorgo (S), los cuales se picaron con una picadora de forraje con criba de 5 cm, para posteriormente colocarlos en una arpilla para su desinfección, esto se realizó de manera rústica como se menciona a continuación.
Se utilizaron dos métodos de desinfección de los sustratos: 1) inmersión en agua caliente e 2) inmersión en agua a temperatura ambiente. En los tratamientos con aplicación térmica, se utilizaron dos recipientes de aluminio con una capacidad de 200 litros aproximadamente; los cuales se llenaron con agua potable hasta aproximadamente – del recipiente y se colocaron en una fogata encendida con leña. Una vez que el agua alcanzó los 90 ºC (cuya temperatura fue medida con un termómetro de mercurio) a uno de los recipientes se le vertió 400 g de óxido de calcio (CaO) (evita que se modifique el pH) y 400 g de sulfato cálcico hidratado (CaSO4 2H2O) (evita que se pierdan los nutrientes), posteriormente el agua se agitó hasta homogeneizar los ingredientes añadidos; al segundo contenedor solo se añadió 400 ml de hipoclorito de sodio comercial (NaClO) al 10%, de igual manera se homogeneizó la mezcla (Gaitán-Hernández et al., 2006; Pineda-Insuati et al., 2016).
Para los tratamientos en inmersión en agua a temperatura ambiente, se utilizaron dos recipientes de plástico con capacidad de 200 litros aproximadamente, los cuales se llenaron con agua potable hasta –, a uno de los recipientes se le añadió la misma cantidad de NaClO y de CaSO4 2H2O antes mencionado (400 g) y al segundo recipiente la misma cantidad de NaClO (400 ml). El agua de los recipientes fue agitada de manera manual para mezclar completamente los ingredientes añadidos, una vez mezclados todos los ingredientes dentro del recipiente, las arpillas se sumergieron y se dejaron reposar a temperatura ambiente durante 24 h siguiendo la metodología realizada por Cruz et al. (2010).
Inoculación del sustrato
Una vez que los sustratos fueron desinfectados, para el caso de los tratamientos con aplicación térmica, se dejaron enfriar hasta alcanzar una temperatura de 30 º C aproximadamente, según Gaitán-Hernández et al. (2006), y en el caso de los tratamientos de inmersión a temperatura ambiente, el sustrato solo se escurrió, para que ambos sustratos alcanzaran un porcentaje de humedad aproximada del 30%. Posteriormente se procedió a la siembra, para ello se colocaron 4 kg de sustrato en peso húmedo en bolsas de polietileno y se inoculó con 150 g de micelio de P. ostreatus, se colocó una capa alterna al sustrato y el micelio hasta llegar a tres cuartas partes de la bolsa, con el propósito de una mejor invasión micelial (Flores-Montes de Oca, 2012; Gaitán-Hernández et al., 2006; Pineda-Insuati et al., 2016), al final, se selló con un amarre de la misma bolsa. Los tratamientos evaluados se enlistan en la Tabla 1:
Tabla 1 Tratamientos evaluados en la desinfección de los sustratos para la producción de P. ostreatus.Table 1. Treatments evaluated in the disinfection of substrates for the production of P. ostreatus.
| Clave | Descripción |
|---|---|
| T1M | Rastrojo de maíz + agua + CaO (400 g) + CaSO4 2H2O (400 g) + aplicación térmica |
| T2M | Rastrojo de maíz+ agua + CaO (400 g) + CaSO4 2H2O (400 g) +sin aplicación térmica |
| T3M | Rastrojo de maíz + inmersión en agua con NaClO (400 ml) + aplicación térmica |
| T4M | Rastrojo de maíz + inmersión en agua con NaClO (400 ml) +sin aplicación térmica |
| T5S | Paja de sorgo + agua + CaO (400 g) + CaSO4 2H2O (400 g) + aplicación térmica |
| T6S | Paja de sorgo +agua + CaO (400 g) + CaSO4 2H2O (400 g) + sin aplicación térmica |
| T7S | Paja de sorgo + inmersión en agua con NaClO (400 ml) + aplicación térmica |
| T8S | Paja de sorgo + inmersión en agua con NaClO (400 ml) + sin aplicación térmica |
Por cada tratamiento se hicieron cinco repeticiones, con un total de 40 unidades para todo el diseño experimental.
Fase de incubación
Las bolsas inoculadas fueron colocadas en un estante de metal, el cual se cubrió con una tela color negra para proporcionar oscuridad. Se mantuvo una temperatura ambiente de 26 °C en el área durante toda la fase de incubación y producción mediante un aire acondicionado. Una vez que las bolsas fueron invadidas completamente por el micelio, se les proporcionó iluminación, por lo que se retiró la tela negra que cubría el estante donde se depositaron las bolsas (Flores-Montes de Oca, 2012; Gaitán-Hernández et al., 2006; Pineda-Insuati et al., 2016).
Fase de fructificación
Durante esta fase se brindó iluminación y aireación a las bolsas para inducir a la emergencia de los primordios, para este caso se abrieron las ventanas del área. Una vez que los primordios emergieron, se realizó un corte a la bolsa en forma triangular para cada uno de ellos y así proporcionarles mejor aireación, se procuró no levantar el corte de la bolsa completamente; en casos donde los primordios estuvieron muy cerca uno del otro, se eligió sólo uno, de esta manera, para no competir por el espacio y nutrientes, lo que les ayudó a tener un mejor desarrollo (Flores-Montes de Oca, 2012; Gaitán-Hernández et al., 2006; Pineda-Insuati et al., 2016).
Cosecha
Una vez que los carpóforos alcanzaron su madurez, se procedió a la cosecha, esto ocurrió aproximadamente entre los cinco a los siete días a partir de la aparición de cada primordio. La cosecha se realizó cuidadosamente con la ayuda de una navaja para realizar el corte; realizar la cosecha de esta manera, ayuda a que broten primordios nuevamente en el mismo sitio, a diferencia de cuando se hace de forma manual (girando el pie del hongo con la mano), esto se comprobó al realizar el corte con una navaja y también de forma manual durante experimentos previos.
Las variables evaluadas fueron: % de contaminación de las bolsas por tratamiento (manejándose como el 100% = 5 repeticiones o bolsas), número de primordios (mediante el conteo de cada carpóforo), peso de los carpóforos (g) (con una báscula digital), diámetro del píleo (cm), la longitud y diámetro del estípite (cm) fueron medidos con un vernier digital, los datos fueron recopilados durante dos cosechas realizadas (Flores-Montes de Oca, 2012; Gaitán-Hernández et al., 2006; Pineda-Insuati et al., 2016).
Análisis de datos
Los datos fueron analizados mediante el paquete estadístico InfoStat/E. Se realizó análisis de varianza (ANOVA), posteriormente se aplicó la prueba de comparaciones múltiples de Tukey (P≤0.05) para determinar las diferencias entre los tratamientos evaluados, además se realizó la correlación de Spearman con el paquete estadístico Statística V. 7.0.
Resultados
Eficiencia del tipo de esterilización de los sustratos
Se detectó que no existe correlación entre los métodos de desinfección del sustrato utilizado para cada tratamiento y las variables evaluadas, derivado de los resultados obtenidos con la prueba de Spearman (P≤0.05), no obstante, se encontró que los hongos con el mayor diámetro del píleo están correlacionados con la variable peso (rs=0.53), es decir, a mayor tamaño de los carpóforos, mayor es el peso de ellos. Así mismo, el peso se correlaciona con el número total de carpóforos cosechados (rs=0.58), la longitud y diámetro del estípite también poseen buena correlación con el tamaño del píleo (rs=0.59; rs=0.67). Por ende, a mayor diámetro y longitud del estípite, diámetro del sombrero y número total de carpóforos, mayor es el peso de éstos.
Así mismo, el mejor método para desinfectar los sustratos utilizados en este trabajo fue el de inmersión en agua caliente + CaO + CaSO4 2H2O, esto debido a que los tratamientos que incluían esta forma de desinfección no presentaron contaminación (T1M y T3M) y en algunos casos (T5S y T7S) presentaron menor porcentaje de contaminación del total de las bolsas por tratamiento. Por el contrario, todas las bolsas de los tratamientos T4M, T6S y T8S se contaminaron por otro tipo de hongos no comestibles, del género Trichoderma spp; a estos tratamientos no se les proporcionó aplicación térmica, por lo que las bolsas dañadas se desecharon completamente para evitar contaminación al resto de ellas. Sin embargo, de los tratamientos sin aplicación térmica, se encontró que el tratamiento T2M fue una excepción, debido a que el 57% de sus repeticiones no se contaminó y se lograron cosechar los cuerpos fructíferos (Figura 1).
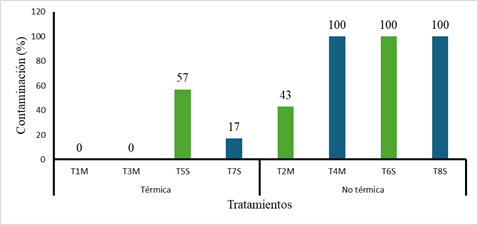
Figura 1 Bolsas de P. ostreatus contaminadas (%) en los diferentes tratamientos realizados. T1M: Rastrojo de maíz + CaO (400 g) + CaSO4 2H2O (400 g) + aplicación térmica. T2M: Rastrojo de maíz + CaO (400 g) + CaSO4 2H2O (400 g) + sin aplicación térmica. T3M: Rastrojo de maíz + NaClO (400 ml) + aplicación térmica. T4M: Rastrojo de maíz + NaClO (400 ml) + sin aplicación térmica. T5S: Paja de sorgo + CaO (400 g) + CaSO4 2H2O (400 g) + aplicación térmica. T6S: Paja de sorgo + CaO (400 g) + CaSO4 2H2O (400 g) + sin aplicación térmica. T7S: Paja de sorgo + NaClO (400 ml) + aplicación térmica. T8S: Paja de sorgo + NaClO (400 ml) + sin aplicación térmica.
Primordios obtenidos por tratamiento
Debido a la presencia de tratamientos completamente contaminados, los cuales se desecharon, sólo se logró la producción de carpóforos en los tratamientos T1M, T2M, T3M, T5S y T7S. Es importante destacar que los tratamientos con mayor cantidad de primordios fueron T3M y T1M, con 65 y 48 unidades, respectivamente, lo que resultó en un promedio de 8.13 y 6.7 primordios por tratamiento (Tabla 2). No obstante, no todos los primordios llegaron a desarrollarse, debido a que aquellos que se encontraban muy próximos entre sí fueron reducidos, eligiéndose sólo uno de ellos.
Tabla 2 Comparación de medias de Tukey sobre las variables evaluadas.Table 2. Comparison of Tukey means on the variables evaluated.
| Tratamientos | Diámetro del estípite (cm) |
Peso de las setas (g) |
Longitud del estípite (cm) |
Diámetro del sombrero (cm) |
Número de primordios emergidos |
Número total de hongos |
|---|---|---|---|---|---|---|
| T1M | 0.94±0.90a | 51.62±84.94a | 3.19±1.50a | 6.14±1.50a | 6.67±11.40a | 15.09±13.60a |
| T2M | 0.81±0.90a | 41.9±84.94a | 3.82±1.50a | 3.82±1.50a | 3.40±11.40 a | 14.39±13.60a |
| T3M | 0.88±0.90a | 85.25±84.94a | 3.36±1.50a | 3.36±1.50a | 8.13±11.40 a | 18.64±13.60a |
| T5S | 0.94±0.90a | 35.17±84.94a | 3.37±1.50a | 3.37±1.50a | 2±11.40 a | 12.37±13.60a |
| T7S | 1±0.90a | 87.33±84.94a | 3.94±1.50a | 3.94±1.50a | 2.83±11.40 a | 23.4±13.60a |
Peso (g) de los carpóforos
De acuerdo con los resultados de la comparación de medias de Tukey sobre la variable peso (g) de los carpóforos cosechados, no se encontraron diferencias significativas entre los tratamientos (P=0.22), no obstante, se obtuvo mayor peso en T7S y T3M con 87.33 y 85.25 g en promedio, respectivamente, a diferencia del tratamiento 5S con menor peso (35.17 g en promedio), es decir, en T7S y T3M se obtuvo más del doble que en el tratamiento 5S (Tabla 2).
Longitud de estípite de los carpóforos
Respecto a la variable longitud de estípite, no se observaron diferencias significativas entre los tratamientos evaluados (P=0.43). Sin embargo, el tratamiento T7S presentó el valor más alto, con un promedio de 3.94 cm, seguido de T2M, T5S, T3M y T1M, con 3.82, 3.37, 3.36 y 3.19 cm, respectivamente (Tabla 2).
Diámetro del píleo de los carpóforos
Por otro lado, no se observaron diferencias significativas en el diámetro del píleo entre los tratamientos (P>0.52) (Tabla 2). El diámetro mínimo registrado fue de 2.4 cm y el máximo de 14.19 cm, con promedios de 10.61 cm en T3M, 7.83 cm en T2M, 6.94 cm en T5S, 6.84 cm en T7S y 6.43 cm en T1M.
Diámetro del estípite
En cuanto al diámetro del estípite de los carpóforos, no se encontraron diferencias significativas entre los tratamientos (P>0.97). Sin embargo, el tratamiento T7S presentó el mayor diámetro del estípite, con un promedio de 1 cm, mientras que el tratamiento T2M tuvo el diámetro más pequeño, con un promedio de 0.81 cm (Tabla 2).
Total de carpóforos obtenidos de las dos cosechas realizadas
Respecto al número de carpóforos obtenidos por tratamiento, la comparación de medias de Tukey no reveló diferencias significativas entre ellos (P=0.15). No obstante, el mayor número de carpóforos se observó en T7S, con un promedio de 23.4, seguido de T3M y T1M en segundo y tercer lugar, con 18.64 y 15.09, respectivamente. En cuarto y quinto lugar se ubicaron T2M, con un promedio de 14.39, y T5S, con 13.37 carpóforos (Tabla 2).
Discusión
Respecto a la desinfección de los sustratos, se observó que el método por inmersión en agua caliente es el más viable para evitar la contaminación en la producción de P. ostreatus (Cruz-Moreno, 2019; Díaz-Muñoz et al., 2019; Fernández-Uribe, 2014; Guzmán-Mejía et al., 2019 y Romero-Arenas et al., 2018).
Con este método se reduce la producción de hasta un 20% comparado con otros métodos como la utilización de vapor, uso de químicos e incluso cuando no se proporciona ningún tratamiento al sustrato (Jaramillo y Albertó, 2013).
La importancia de realizar una buena desinfección de los sustratos radica también en la presencia de azúcares solubles que no se eliminan por lixiviación en ellos, lo que provoca un incremento importante en la temperatura dentro de él durante la fase de incubación, factor que contribuye a un rápido desarrollo de hongos y mohos antagonistas para Pleurotus spp, principalmente Mucor, Trichoderma y Trichurus. Para ello, es necesario remojar la paja por periodos de 60 h, para inducir a un lixiviado de la mayoría de los componentes solubles, azúcares entre ellos (Sánchez-Vázquez et al., 2007).
El número de primordios obtenidos en el presente trabajo es menor al obtenido por Michel-Aceves et al. (2015) con un promedio de 17.2 primordios, también con paja de sorgo como sustrato; aunque estos autores añadieron algunos compuestos químicos y biológicos (Agromil plus, sulfato de cobre, extracto de primordios de las variedades BCL, BGAT y BSMA, metabolitos de Trichoderma y pasta de sorgo, ajenos a la presente investigación) para favorecer el desarrollo de P. ostreatus. Así mismo, Acevedo-Cárdenas (2017) obtuvieron 94.80 primordios en promedio, sólo en la primera cosecha. Sin embargo, ellos utilizaron mezclas de diversos sustratos entre ellos 57% rastrojo de maíz, 30% de aserrín, 10% de residuos de pan, 1% de calcio y 2% de azúcar; colocaron 3 kg de sustrato por cada bolsa y realizaron 10 réplicas por cada tratamiento evaluado. Los resultados de estas investigaciones proporcionan información importante sobre usar aditivos nutrimentales que pueden ayudar al crecimiento y desarrollo de carpóforos en la producción P. ostreatus.
Respecto al peso de los carpóforos obtenido en esta investigación, es bajo comparado con lo reportado por Caicedo Ruiz et al. (2024), quienes obtuvieron 154 y 153.4 g en la primera y segunda cosecha en cultivo de P. pulmonarius sobre cáscara de cacahuate como sustrato. Por su parte, Acevedo-Cárdenas (2017) cosecharon 269.50 gramos en promedio, utilizando mezclas de sustratos y otros aditivos nutrimentales, los cuales no fueron considerados en esta investigación. Cuando se compara la producción de carpóforos en esta investigación, con otras donde utilizan otros sustratos, la cantidad obtenida en este trabajo es menor, ejemplo de ello es lo que reportan Morán-Arellanos et al. (2020) al haber obtenido 187.37 g en promedio en rastrojo de frijol, 93.75 g en cascarilla de Huaxin y 178 g en paja de trigo, no obstante, se observó que el rastrojo de maíz y el rastrojo de sorgo es más productivo que el rastrojo de pulpa de calabaza con 35 g y en fruto de pixoi sólo con 10 g, sólo con cuatro repeticiones por tratamiento, además de haber colocado 200 g de sustrato en peso seco por cada bolsa.
Por otro lado, Roblero-Mejía et al. (2021) señalaron haber obtenido un mínimo de 64.9 g y un máximo de 147.8 g de peso promedio de hongos cosechados por bolsa, en cuyos tratamientos utilizaron como sustratos al olote de maíz, pasto pangola y pulpa de café, todos ellos mezclados en diferentes proporciones y de manera individual. Asimismo, el peso promedio obtenido por Fufa et al. (2021) fue de los 101.11 a 253.07 g con rastrojo de olote de maíz, paja de mijo africano (Eleusina coracana) y residuos de bambú, solos y en combinación, en bolsas con 500 g de sustrato. La explicación puede deberse a que el rastrojo de maíz contiene alto contenido de celulosa y hemicelulosa (40-25 y 17%, respectivamente) (Fuentes et al., 2001).
La longitud del estípite de los carpóforos obtenida es similar a los valores reportados por Dedousi et al. (2024), los cuales se encontraron entre un rango de 3.18 a 3.91 cm en promedio, al utilizar paja de trigo, paja de cebada y avena, combinados con sustrato reutilizado del cultivo de P. ostreatus junto con residuos de setas (estípites/setas deformes), en bolsas con 1 kg de sustrato y cinco repeticiones por tratamiento. Por su parte, Melanouri et al. (2022) obtuvieron entre 2.1 a 3.7 cm en promedio de longitud para la cepa 144 de P. ostreatus y entre 2.7 a 3.3 cm para la cepa 150, con los mismos sustratos que evaluaron Dedousi et al. (2024) pero en esta ocasión cada sustrato por separado. A su vez, Subedi et al. (2023) señalaron entre 3.05 a 3.44 cm de la longitud de estípite en producción de P. ostreatus utilizando paja de arroz, y jacinto de agua (Eichhornia crassipes) como sustratos, combinados y en distintas proporciones. Caicedo Ruiz et al. (2024) mencionan que la longitud del estípite se encuentra relacionada con la concentración de nitrógeno y proteínas contenidas en el sustrato.
Los datos sobre el diámetro del píleo de los carpóforos obtenidos en el presente trabajo son más elevados de acuerdo con López-Rodríguez et al. (2008), al obtener promedios para el diámetro del píleo de 5.77 cm en sustrato de aserrín; 5.53 cm con olote de maíz; 5.47 cm con cáscara de arveja y 5.81 cm con capacho de uchuva (Physalis peruviana). Por su parte, Fufa et al. (2021) obtuvieron entre 2.95 a 4.58 cm en promedio del diámetro de píleo de los cuerpos fructíferos, al utilizar el olote de maíz, paja de mijo africano (Eleusine coracana) y residuos de bambú, solos y combinados como sustratos.
Así mismo, Romero et al. (2010) registraron de entre 4.7 a 8.5 cm para el diámetro del píleo de setas crecidas con residuos de plátano y de 5.1 a 10.2 cm en paja de trigo. Por su parte, Dedousi et al. (2024) reportaron de entre 3.55 a 5.89 cm de diámetro en sustrato de paja de trigo, paja de cebada y avena, combinados con sustrato gastado del cultivo de P. ostreatus junto con residuos de setas (estípites/setas deformes). No obstante, se han reportado resultados más bajos, siendo de entre 4.63 a 5.21 cm de diámetro al utilizar como sustratos a la paja de arroz y jacinto de agua (Eichhornia crassipes) (Subedi et al., 2023).
El diámetro del estípite es similar al obtenido por Dedousi et al. (2024) entre 0.80 a 1.16 cm en promedio, producidos con sustratos de paja de trigo, paja de cebada y avena, residuo de café, combinados con sustrato reciclado del cultivo de P. ostreatus junto con residuos de setas (estípites/setas deformes). Esta medida está relacionada con la concentración de nitrógeno que contenga el sustrato (Caicedo Ruiz et al., 2024). Por lo que se infiere que los sustratos utilizados pudieran tener una baja concentración de nitrógeno.
Finalmente, el valor total de carpóforos cosechados es similar al valor obtenido por Dedousi et al. (2024) de 17-32 carpóforos en promedio con los sustratos evaluados en P. ostreatus. Así mismo, Subedi et al. (2023) obtuvieron entre 16.50-34.50 carpóforos en promedio, en sustratos de paja de arroz y jacinto de agua (Eichhornia crassipes) en distintas combinaciones. El rastrojo de maíz es ampliamente recomendable para la producción de P. ostreatus debido a que contiene grandes cantidades de celulosa, proteína en un 4.90%, Fibra en un 72.45%, entre otros (Fuentes et al., 2001).
Conclusión
Se demostró que el mejor método para desinfectar el sustrato para la producción de P. ostreatus es el de inmersión en agua proporcionando aplicación térmica, además de la adición de CaO y CaSO4 2H2O para evitar la modificación del pH y la pérdida de los nutrientes del sustrato. De esta manera se asegura mayor inocuidad y menos probabilidad de contaminación.
Se recomienda utilizar tanto a la paja de sorgo como al rastrojo de maíz para la producción de P. ostreatus, debido a que con el primero se obtuvo mayor producción de carpóforos (23.4), mayor peso en promedio (87.33 g) y mayor longitud del estípite (3.94 cm). Así mismo, el mayor diámetro de los carpóforos se obtuvo con el sustrato rastrojo de maíz (6.14 cm) a diferencia de T7S con 3.94 cm en promedio.
Así mismo, al producir P. ostreatus de manera rústica y a pequeña escala, se pueden utilizar como sustratos residuos agrícolas disponibles y desinfectarse a través de inmersión con agua y NaClO (opción 1) o bien añadir CaO y CaSO4 2H2O (opción 2) más aplicación térmica.











 text new page (beta)
text new page (beta)



