Introducción
Identificar las características anatómicas de las plantas resulta una herramienta básica para la investigación y la enseñanza en diferentes disciplinas de la botánica. Cada uno de los órganos de la planta (raíz, tallo, hoja y flor) está formado por diferentes tejidos, que derivan todos, por medio de la proliferación y la diferenciación celular (Apóstolo, 2021). Los tejidos pueden estar conformados por un solo tipo de células formando un tejido simple o por varios tipos celulares formando tejidos complejos (Valencia, 2014). De acuerdo con la clasificación propuesta por el botánico alemán Sachs, en el siglo XIX, los tejidos maduros se pueden agrupar en tres sistemas de acuerdo con su función y continuidad en el cuerpo vegetal: sistema fundamental, sistema de protección y sistema vascular, también se pueden usar otras clasificaciones basándose en el origen, la función o diferenciación morfológica (Megías et al., 2020). Por ejemplo, los tejidos meristemáticos que pueden considerarse tejidos embrionarios que persisten en la planta durante toda su vida y son responsables del crecimiento permanente de la planta. Los tejidos meristemáticos primarios dan origen a otros tejidos y están relacionados con el crecimiento de las plantas, posibilitan el crecimiento en longitud y los meristemos secundarios permiten el crecimiento en espesor de las plantas dicotiledóneas leñosas y gimnospermas (Chuncho, 2019). Posteriormente aparecen los tejidos diferenciados o adultos, cuyas células han alcanzado diversos grados de maduración. Se incluyen aquí a la epidermis, tejidos mecánicos o de sostén, tejidos conductores, y el parénquima (Lavalle y Mengascini, 1998).
Para la determinación de caracteres anatómicos el estudio de los tejidos vegetales tiene un valor significativo en diferentes áreas por ejemplo, la industria alimentaria, la medicina , la paleontología, la industria del papel y la académica; esto comprueba que los análisis anatómicos son necesarios para realizar estudios interdisciplinarios para lo cual se han utilizado diversas técnicas de estudio como: inclusiones en parafina, disociados, así como, técnicas de tinción y diafanización (Apóstolo, 2021).
La diafanización es la obtención de material transparente (clarificación) a partir de una técnica que aclara el tejido blando para equilibrar el índice de refracción de la luz en un organismo preservándolo, además de despigmentar las estructuras, dependiendo de su composición y función (Sandoval et al., 2017). Esta técnica es comúnmente empleada en estudios de morfofisiología vegetal para resaltar principalmente la vascularización de las hojas y formar una imagen tridimensional del tejido.
Es importante recalcar que, la técnica de diafanización en las plantas facilita la observación de tejido vascular, células epidérmicas, y utilizando la safranina como colorante, permite observar la pared celular. Este pigmento es el más utilizado en la tinción vegetal ya que presenta afinidad por las paredes secundarias lignificadas, mientras que para teñir paredes no lignificadas (paredes celulares primarias) es común usar el cristal violeta o verde rápido.
A su vez, las plantas presentan pigmentos naturales como la clorofila, antocianinas y carotenos, los cuales facilitan la observación directa con el microscopio óptico, las paredes celulares también favorecen en la delimitación celular y la identificación de algunos tejidos con ciertas características morfológicas. De acuerdo con (Armiñana R. J. y Breijo G. F., 2006), en las técnicas de histología vegetal se pueden emplear tinciones, en las cuales la coloración se produce simplemente por inmersión en el colorante, como la tinción con Safranina, o se pueden utilizar colorantes metacromáticos, como el Violeta de Cresilo el cual tiñe de manera diferencial distintas estructuras, por ejemplo, tiñe color rojo violáceo paredes primarias no lignificadas y de color verde azulado las paredes secundarias lignificadas. Además, se puede recurrir a las combinaciones de colorantes, de forma sucesiva o simultánea, no obstante, en ocasiones las laminillas no alcanzan la calidad o nitidez necesaria por lo que se tendrían que combinar con alguna otra técnica como la diafanización.
En el caso de la técnica de clarificación 5-5-5 (Arambarri, 2018), los reactivos utilizados son Hidróxido de sodio (NaOH) al 5%, Hipoclorito de sodio (NaClO) al 5 % y 50% e Hidrato de cloral (C2H3Cl3O2) al 5%, en el caso de este último reactivo debido a su condición de sustancia regulada por ser un compuesto con propiedades sedantes, hipnóticas y anticonvulsivas es difícil de obtener y con costo aproximado de $950.00 MXN por lo que, se optó por hacer una modificación a la técnica original de diafanización, reduciendo el costo y evitando el uso de hidrato cloral cuya manipulación de este reactivo puede representar un factor de riesgo para los estudiantes, en caso de que ellos preparen las muestras.
Lo anteriormente mencionado deja en evidencia la relevancia que tendría el estandarizar la técnica de diafanización en los tejidos vegetales por lo que, este estudio tuvo como objetivo estandarizar la técnica de diafanización 5,5,5 en las especies de Adiantum pedantum L. (Pteridaceae) y Nephrolepis exaltata (L.) Schott (Nephrolepidaceae) y Pyracantha koidzumii Hayata Rehder (Rosaceae) (https://tropicos.org/home).
Materiales y métodos
Materiales biológicos empleados
Se obtuvieron muestras de material fresco recolectado en el Jardín Botánico de Iztacala (JABIZ) de la FES Iztacala en el mes de marzo de 2024, considerando un total de 10 muestras por género. Aunque inicialmente se analizaron flores, hojas, tallos y frutos de siete géneros, los datos sobre las especies completas no fueron detallados en los análisis comparativos previos. En este estudio, las especies que fueron evaluadas a profundidad fueron (Adiantum pedantum L. (Pteridaceae) y Nephrolepis exaltata (L.) Schott (Nephrolepidaceae) y una Spermatophyta Pyracantha koidzumii Hayata Rehder (Rosaceae).
Después del proceso de diafanización, las preparaciones se observaron en un Microscopio óptico compuesto binocular “Motic” en el Laboratorio de Microscopía de la FES- Iztacala.
Diafanización vegetal
Se tomó como referencia la técnica de clarificación 5-5-5 (Arambarri, 2018) misma que consiste en la diafanización de tejido vegetal usando [NaClO 5%], [NaOH 5%] y (C2H3Cl3O2) al 5%, con un promedio de decoloración de 5 días en dicha solución.
La estandarización consistió en someter de inmediato el material vegetal a las soluciones clarificantes sin utilizar el hipoclorito de sodio al 50% y el hidrato cloral.
Tinción y montaje
En la técnica de clarificación 5,5,5, se utiliza Safranina al 1%, Safranina a saturación en alcohol 80% y Fucsina básica 0,5%. Para este estudio se optó por utilizar como colorante control la solución de safranina (S) y se probó con otros colorantes acuosos que suelen ser utilizados en diferentes técnicas histológicas como, azul de toluidina (AT), azul de metileno (AM), gelatina cristal-violeta (GV) o solo violeta de genciana (V), también se hicieron las combinaciones de azul de toluidina y violeta de genciana (TV) y Azul de Toluidina-gelatina safranina (ST). Como pruebas adicionales se utilizó la Fucsina básica (F) y la tinta china (TC).
Para el montaje de las muestras se utilizó gelatina-glicerina y se le agregaron los colorantes safranina y cristal violeta, las gelatinas se colocaron en baño María durante 10 minutos hasta que estuvieran en estado líquido, posteriormente se tomó cada una de las muestras y se colocó sobre el portaobjetos nuevo y limpio, adicionando una gota de la gelatina y finalmente se colocó el cubreobjetos limpio y seco en ángulo de 45° y se dejó caer suavemente.
Resultados
Con el método anteriormente descrito se logró una buena diafanización en las hojas de Adiantum pedantum, Nephrolepis exaltata y Pyracantha koidzumii. En el proceso de diafanización las muestras fueron colocadas en una solución de [NaClO 5%] e [NaOH 5%] por 5 días tal como se menciona en la técnica original omitiendo el paso de colocar el material en hidrato de cloral al 5%. Considerando los tiempos propuestos por Arambarri en el 2018 la técnica de diafanización podría completarse en un tiempo de 25 a 30 días dependiendo la especie. Sin embargo, como se observa en la Tabla 1, con las modificaciones sugeridas la diafanización podría efectuarse en un tiempo promedio de 7 días logrando una reducción al menos del 77% del tiempo y al evitar el uso de hidrato cloral se puede reducir entre 15- 20% del costo.
Tabla 1 Comparación de la técnica de clarificación 5-5-5 (Arambarri, 2018) y las modificaciones realizadas.Table 1. Comparison and modification of the 5-5-5 clarification technique (Arambarri, 2018).
| Técnica de clarificación 5-5-5 | Modificación | |
|---|---|---|
| Tratamiento previo | Material en fresco se fija 15 días en etanol al 50% o en FAA | El material fresco no se fijó en etanol, se sometió de inmediato al tratamiento clarificante. |
| Aclaramiento | Material en solución 1:1 de NaOH al 5% y NaClO al 5%, conservándolo a temperatura ambiente. El tiempo de decoloración, de acuerdo al material es altamente variable desde horas a 15 días, siendo el promedio 4 a 5 días. | Material en solución 1:1 de NaOH al 5% y NaClO al 5%. Tiempo de decoloración de 2-7 días. |
| Retirar y lavar en cajas petri con agua corriente o agua destilada. | -Retirar y lavar con agua corriente 30 segundos. | |
| Colocar material en solución hipoclorito de sodio al 50% unos segundos o minutos. | -Colocar las muestras en etanol [80%] durante 5 días. | |
| Retirar y lavar con agua destilada 3-5 veces. | ||
| Una vez lavado el material se coloca en solución de hidrato cloral al 5% mínimo 24 horas. | ||
| En caso de obtener una total decoloración en la mezcla inicial de NaOH (5%) + NaClO (5%), se saltará el paso de la decoloración con hipoclorito de sodio (50%) y continuará con el lavado y sumersión en hidrato de cloral (C2H3Cl3O2) al 5%, para su clarificación. El material puede permanecer varios días (nunca menos de un día). | ||
| Tiempo total | 25- 30 días dependiendo de la especie | 7 días |
Tabla 2 Procedimiento de tinción y montaje de las hojas diafanizadas.Table 2. Staining and assembly procedure of the diaphanized leaves.
| Colorantes | Técnica de clarificación 5,5,5 | Modificación |
|---|---|---|
| -Safranina al 1% -Azul de Toluidina -Azul de Metileno -Cristal violeta 0.5% -Fucsina básica 0,5% -Tinta china -Gelatina cristal-violeta -Azul de Toluidina-violeta de genciana -Azul de Toluidina-gelatina safranina |
Para la coloración con safranina se puede seguir la técnica indicada por Dizeo de Strittmatter (1973), el material se somete a etanol al 70% por 10 minutos, posteriormente se sumerge el material en solución saturada de safranina en etanol al 80%. Montaje en directo en gelatina-safranina y gelatina-fucsina | La mitad de las muestras se sometieron directamente a los colorantes, y la otra mitad se colocó en etanol por 5 días y posteriormente se enjuagaron en agua corriente durante 30 segundos después de realizar el proceso de tinción. |
Dentro de las pruebas se observó que las hojas de Adiantum pedantum, Nephrolepis exaltata y Pyracantha koidzumii, mostraron resultados favorables ya que se observó un mejor contraste pudiendo identificar fácilmente el tejido vascular, en el caso de Nephrolepis exaltata se observaron los esporangios, soros y las células epidérmicas. El proceso de clarificación fue de dos a 7 días, diafanizando rápidamente las hojas de las tres especies.
Inicialmente las pinnas de Nephrolepis exaltata estuvieron 5 días en solución de [NaClO 5%] e [NaOH 5%], sin embargo, la manipulación no fue sencilla, por lo que fue necesario reducir el tiempo de exposición en un rango de 24 a 48 horas.
Como se mencionó anteriormente para poder realizar las tinciones, se enjuagó el material con agua corriente por 30 segundos, la mitad de las muestras se sometieron directamente a los colorantes, y la otra mitad fue colocada en etanol por 5 días y un enjuague de 30 segundos para después realizar el proceso de tinción.
Como primeros resultados se notó que la fucsina no se impregnó en las muestras, la fucsina básica se utiliza como colorante de contraste y corresponde al reactivo denominado Violeta Ácido (C20N3H17O9S3Na2), la función específica de contraste se explica por la presencia tanto de los anillos como del grupo NH2 es un colorante básico que se utiliza en histología vegetal para resaltar ciertas estructuras y componentes con cargas negativas,
Por otro lado, el AM, así como el AT resultaron efectivos con tiempos de 10, 20 y 30 minutos, las mejores tinciones fueron las que se sumergieron en los colorantes 30 minutos después de estar en etanol [80%] por 5 días. La S y la tinta china sobresaturó el tejido de todas las muestras dejando residuos en la preparación al momento del montaje e impidiendo la observación de estructuras vegetales nítidas, por lo que se descartaron. El uso de gelatina-glicerina, cristal violeta y safranina (GV, GS), ya sea solas o en las combinaciones de azul de toluidina-violeta de genciana y azul de toluidina - gelatina-glicerina- safranina (TV o TS) tuvieron resultados favorables, ya que, se lograron observar diferentes estructuras celulares.
De todas las preparaciones que se realizaron en ensayos previos no se lograron buenos resultados con flores y tallos. Sin embargo, los resultados fueron satisfactorios para las hojas de Adiantum pedantum, Nephrolepis exaltata y Pyracantha koidzumii teñidas con AT, AM, GS, GV, TV y TS, descartando los colorantes que no se impregnaron o dejaron residuos en las muestras, ya que impedían la identificación de estructuras vegetales.
Al usar el AT, TS, AM y GV en las pinnas del helecho se pudo observar el tejido vascular y los soros, tal como se observa en la Figura 1.
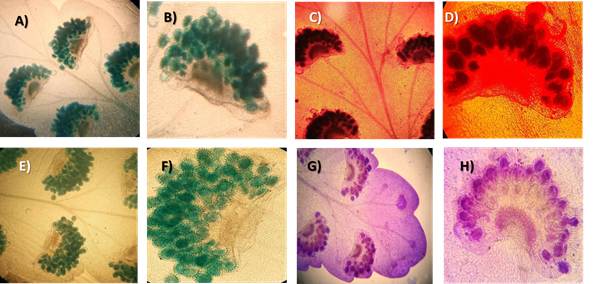
Figura 1 Pinna de Nephrolepis exaltata (L.), se aprecia la pinna con esporangios a diferentes aumentos 4x (A, C, E, G) y (10x (B, D, F, H), resaltando la venación y los soros. A) Soros AT (30 min), B) Soros AT (30 min), C) Soros ST (30 min), D) Soros ST (30 min), E) Soros AM (30 min), F) Soros, AM (30 min), G) Pinna, GV (0 min), H) Soro GV (30 min).Figure 1. Pinna de Nephrolepis exaltata (L.), the pinna with sporangia can be seen at different magnifications 4x (A, C, E, G) and (10x (B, D, F, H)., highlighting the venation and sori. A) Soros AT (30 min), B) Soros AT (30 min), C) Soros ST (30 min), D) Soros ST (30 min), E) Soros AM (30 min), F) Soros, AM (30 min), G) Pinna, GV (0 min), H) Soro GV (30 min).
En las preparaciones de AT, GV y TV se potencia el contraste de estructuras pues permite diferenciar el tejido vascular y los soros con más claridad. Sin embargo, al usar TS se pierde la claridad en la diferenciación de las estructuras.
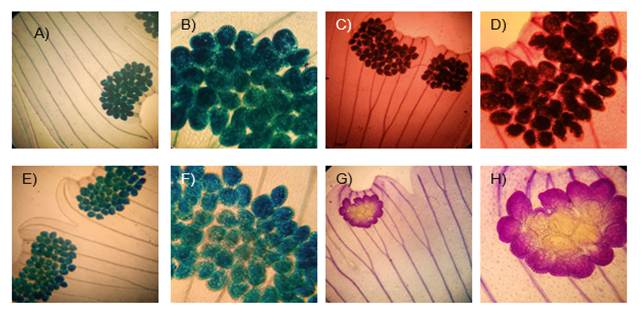
Figura 2 Pinna de Adiantum pedantum L. se aprecia la pinna con esporangios marginales en diferentes aumentos 4x (A, C, E, G) y (10x (B, D, F, H). A) Soros AT (30 min), B) Esporangio, AT (30 min), C) Soros ST (30 min) D) Esporangio ST (30 min) E) Soros AM (30min), F) Esporangio AM (30min), G) Pinna GV, H) Esporangio, GV.
Cuando se utiliza únicamente GV se tiñen con mayor intensidad las paredes celulares, pero se pierden detalles de la pinna del helecho, en el caso de ST se tiñen bien las paredes celulares, sin embargo, el color rojo se impregna de tal forma que impide ver con claridad la diafanización del tejido tanto en los helechos como en Pyracantha koidzumii.
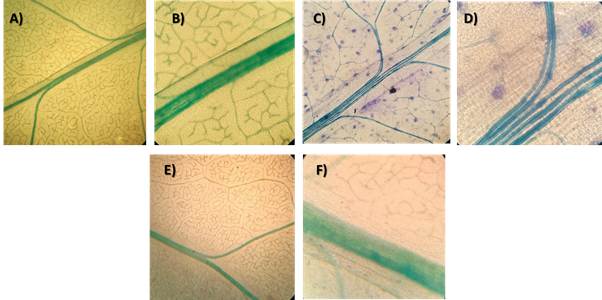
En la Figura 3 la tinción con AM en Pyracantha koidzumii presenta una coloración más clara en comparación con AT y TV, el AM tiñó con claridad las venaciones de la hoja, sin embargo, 30 minutos no fue suficiente para que se impregnará el colorante por lo que no se observaron con nitidez las paredes celulares.
Discusión
El método de Arambarri (2018) describe cuatro etapas, que son el tratamiento previo, la clarificación, la tinción y el montaje. El método propuesto en este artículo consta de cinco procesos en dos etapas omitiendo la fijación en alcohol y comenzando el proceso de aclaración vegetal en las soluciones clarificantes NaOH al 5% y NaClO al 5% (1:1), se excluyeron las fases de introducir el material en hipoclorito de sodio al 50%, retirar y lavar de 3 a 5 veces, y colocar el material en solución de hidrato cloral al 5%.
Arambarri indica que el tratamiento previo es importante, considerando que el trabajo con material fresco generalmente es más difícil que hacerlo con material herborizado, sin embargo, depende del órgano y su composición química. En la técnica original se menciona que debe de permanecer el material fresco por lo menos 15 días en etanol [50%] antes de comenzar la clarificación. En la modificación que se realizó, los materiales fueron colocados de inmediato en la solución clarificante con un tiempo menor a los 5 días indicados por Arambarri para posteriormente ser fijados en etanol [80%] por 5 días.
En la técnica 5-5-5 Arambarri (2018) utiliza safranina líquida al 1% con agua destilada y etanol al 80%, este método se aplicó en las muestras, pero en cuanto se sumergieron en la safranina el tejido se sobresaturó, por lo que se optó por utilizar gelatina-safranina para montar y teñir, sin embargo, se perdió la transparencia y nitidez de las estructuras vegetales.
Se usó fucsina básica como una alternativa más en las tinciones, pero al someter las muestras en esta solución no se tiñó la muestra, contrario a lo realizado por Arambarri, quién utilizó gelatina con fucsina básica, el cual es un colorante catiónico, esta característica le confiere afinidad por las estructuras celulares y los componentes ácidos de los tejidos. Por lo tanto, se utiliza ampliamente en técnicas de tinción para resaltar y visualizar estructuras como los núcleos celulares, considerando que permite una tinción selectiva de ciertos componentes celulares, las muestras vertidas en este colorante no se pigmentaron por lo que también fue descartado.
Se observó que las pinnas de helechos pueden ser un modelo adecuado para la diafanización por su resistencia a la solución clarificante, un fácil manejo a la tinción y montaje, además al teñirlas con AM y AT, solos o con una doble tinción genera un contraste de color lo que permite ver con claridad el tejido vascular, estomas y soros. Estas observaciones concuerdan con las de Tejero, et al., 2010, quién por medio de la diafanización de las hojas pudo identificar patrones de venación en Polypodium plesiosorum sensu Moran (Polypodiaceae) junto con la posición de los soros usando hidróxido de sodio al 2% en lugar de l%, con la modificación propuestas en este trabajo la estructura de los esporangios y esporas se observan más nítidamente, lo que implica una buena alternativa para la identificación taxonómica de dichas estructuras.
Los métodos de aclaración en en las hojas son utilizados principalmente para observar la arquitectura foliar y caracteres específicos que ayudan a diferenciar los taxones, tal como lo reportan Rodríguez y Romero en 2007 en donde observaron los patrones de venación, areolas y estomas en hojas de diez especies de encinos, en esta investigación seleccionaron hojas que sometieron a un proceso de aclaramiento, para lo cual se sumergieron en una solución de hidróxido de sodio (NaOH) a 5% y se dejaron hervir durante 10 minutos, después se lavaron en agua corriente y se colocaron en una solución caliente de hipoclorito de sodio (NaClO) a 30% hasta que quedaron blancas, enseguida se lavaron con agua corriente. Para realizar la tinción, las hojas aclaradas se colocaron en safranina alcohólica a 1% durante 45 minutos. Después se hicieron cambios graduales de alcohol, a 60%, 70%, 80% y 96%, de 15 minutos cada uno; posteriormente se colocaron en xilol hasta lograr su aclaramiento.
Por otro lado, Hernández y colaboradores en 2021, estudiaron las hojas de diez especies de Gouania (Rhamnaceae) para México con el propósito de identificar aspectos morfológicos y anatómicos foliares que pudieran permitir la diferenciación de los taxones. Las hojas completas de cada una de las especies fueron diafanizadas por separado mediante la técnica de Aguirre-Claverán y Arreguín-Sánchez (1988, p. 11) . Las láminas aclaradas permanecieron en cajas de Petri con agua y se tomaron fotografías de este material. Posteriormente una parte de las hojas, fueron teñidas con dos gotas de azul de metileno comercial fish care por un minuto y después se pasaron a otra caja con agua. A la otra parte de las láminas foliares se les añadió dos gotas de safranina por dos minutos y se colocaron en cajas de Petri con agua, como medio de montaje se utilizó una solución de miel de maíz con agua 1:1 y trazas de fenol, para posteriormente tomar fotografías de este material.
Cabe mencionar que en los métodos de montaje se deben de considerar el objetivo del estudio, el origen y características de la muestra, por ejemplo, se pueden obtener preparados frescos en donde el medio de montaje es agua o glicerina-agua y los preparados se descartan posterior a su visualización, en los preparados semipermanentes, como medio de montaje se utiliza glicerina-agua o gelatina-glicerina. Los bordes del cubreobjeto se sellan sobre el portaobjeto con esmalte o un adhesivo, para reducir la deshidratación y el ingreso de contaminantes. Este tipo de preparados duran varios meses o años, dependiendo del cuidado durante la manipulación de la muestra, montaje y sellado y finalmente los preparados permanentes, generalmente la secuencia se organiza como conservación, fijación, deshidratación, inclusión, cortado, pegado, coloración, montaje y observación. El resultado es un preparado que puede utilizarse por décadas (Suárez et. al., 2022).
Es importante destacar que en la FES Iztacala contamos con materiales limitados para la preparación de muestras sobre todo para la enseñanza, por lo cual se utilizaron los materiales con los que se disponía en el laboratorio.
Conclusiones
Se redujeron costos ya que se utilizó para el lavado agua corriente en lugar de agua destilada y se omitió el uso de hipoclorito de sodio al 50% e hidrato cloral.
Las mejores tinciones fueron las que se sumergieron en los colorantes 30 minutos después de estar en etanol [80%] por 5 días.
En hojas diafanizadas de Adiantum pedantum L., Nephrolepis exaltata (L.) Schott (Nephrolepidaceae) y Pyracantha koidzumii Hayata Rehder, se compararon siete tinciones con colorantes simples y dos combinaciones, considerando que los de mayor efectividad fueron cristal violeta, azul de toluidina, azul de metileno, gelatina cristal violeta, azul de toluidina, y la combinación de azul de toluidina-violeta de genciana.
Finalmente es importante destacar que los estudios anatómicos e histológicos del tejido vegetal se relacionan con diferentes intereses científicos, tecnológicos y educativos, por ello la técnica propuesta puede ser útil y de bajo costo para generar colecciones para la docencia e investigación.











 text new page (beta)
text new page (beta)