Introducción
El boque mesófilo de montaña (BMM) es un tipo de vegetación altamente biodiverso con gran cantidad de endemismos por unidad de área (Rzedowsky, 1978). Presenta un dosel compuesto por árboles caducifolios de afinidad holártica, mientras que su sotobosque está conformado por especies tropicales perennifolias de afinidad neotropical (Rosas et al., 2019). Esta vegetación participa en la regulación del clima, la captación, control y purificación de los flujos del agua, la captura de carbono, el control de erosión del suelo y el mantenimiento de la biodiversidad (Williams-Linera et al., 2007). A pesar de todo esto, actualmente el BMM es sumamente vulnerable por su distribución restringida y ha sido severamente perturbado por diversas actividades antropogénicas (Gual-Díaz y Rendón-Correa, 2017).
Las principales amenazas del BMM son la deforestación, la fragmentación, la extracción insostenible de productos forestales no madereros, el cambio climático, el cambio de uso de suelo y los asentamientos humanos irregulares (Sánchez-Ramos y Dirzo, 2014). Todas estas amenazas impactan negativamente su biodiversidad, sus interacciones y los servicios ecosistémicos que provee (Partida-Sedas et al., 2017). En México, este bosque ocupa 1% de la superficie total y más de 50% de su cobertura original fue reemplazada por cultivos anuales, pastizales de uso ganadero y plantaciones de café (Gual-Díaz y RendónCorrea, 2017). Debido a que el BMM se encuentra en amenaza inminente, es necesario diseñar, implementar y evaluar diversas actividades de manejo para su conservación (Williams-Linera et al., 2015; Rosas et al., 2019).
La restauración ecológica sobresale como una actividad de manejo para prevenir y/o revertir la pérdida de la biodiversidad y de los servicios ecosistémicos (Society for Ecological Restoration [SER], 2004). En paisajes de BMM, la restauración puede ser pasiva (sucesión secundaria de un área después de eliminar la fuente de perturbación) o activa (intervención humana como la reforestación, el deshierbe y el aclareo) (Rey et al., 2008; Vaughn, 2010). Además de su implementación, es fundamental analizar y evaluar el papel de dicha actividad de manejo en el mantenimiento o conservación de diversos grupos biológicos en paisajes heterogéneos de BMM (Díaz-Triana et al., 2019; Ríos-Casanova y Godínez-Álvarez, 2023).
Entre la vasta biodiversidad asociada al BMM, los escarabajos coprófagos (Coleoptera: Scarabaeidae: Scarabaeinae) sobresalen como un grupo indicador del estado de perturbación o conservación de los ecosistemas (Gomes et al., 2021; Álvarez et al., 2022). Poseen una estrecha relación con los mamíferos dado que utilizan el componente líquido del estiércol como alimento y el material fibroso como refugio para criar larvas (Rivera et al., 2020). A cambio, ofrecen diversos servicios ecosistémicos como el reciclaje de nutrientes, la degradación de materia orgánica, el enriquecimiento del suelo y actúan como agentes de control biológico de parásitos de vertebrados (Miranda-Flores et al., 2020; Torabian et al., 2024).
El monitoreo de la diversidad de los ensambles de los escarabajos coprófagos puede utilizarse para predecir cambios ambientales derivados de las actividades de manejo en mosaicos de paisaje de BMM. Esto es posible porque las diversidades alfa y beta de estos ensambles cambian significativamente en función del tipo de hábitat dentro un mismo paisaje (Derhé et al., 2016); aumentando inclusive, la abundancia, riqueza y diversidad en función de la complejidad estructural del hábitat, mientras que la similitud composicional disminuye en ese mismo sentido (Álvarez et al., 2022). Estos cambios han sido atribuidos principalmente a las características del hábitat como la capa de hojarasca en suelo, la altura y cobertura del dosel y la densidad de árboles y arbustos (Bogoni et al., 2016). Sin embargo, se ha registrado un incremento de la diversidad de escarabajos en paisajes de BMM con áreas en sucesión secundaria (Deloya et al., 2007), sin identificar, hasta el momento, las actividades de manejo que modulan dichos incrementos. Dado este contexto, es necesario analizar la diversidad de los ensambles de los escarabajos coprófagos en mosaicos heterogéneos de paisajes de BMM compuestos por hábitats estructuralmente contrastantes con diferentes actividades de manejo y/o historias naturales.
Objetivos
Analizar la respuesta de la diversidad de escarabajos coprófagos (Coleoptera: Scarabaeidae: Scarabaeinae) a las trampas instaladas en cuatro sitios con diferentes historias naturales dentro de un paisaje de bosque mesófilo de montaña de Huatusco, Veracruz, México, considerando como parámetros los cambios en la riqueza de especies, la distribución de la abundancia de especies, la similitud composicional de los ensambles y la contribución de la diversidad alfa y beta a la diversidad regional de escarabajos coprófagos.
Materiales y métodos
Área de estudio
El estudio se realizó en el rancho “Las Bellotas de Chicalaba”, ubicado en la Reserva ecológica de bosque de niebla, municipio de Huatusco Veracruz, México (Fig. 1). El tipo de clima en el área de estudio es cálido subhúmedo (Fuentes et al., 2014), con una precipitación de 655 mm a 2821 mm anuales y una temperatura media anual de 17.1 °C. Además de suelos vertisol y regosol predominantes (Instituto Nacional de Ecología y Cambio climático [INECC]-Fondo Golfo de México [FGM], 2017). Actualmente cuenta con aproximadamente 10000 ha de BMM, pero solo 30% está cubierto por bosque primario. Dichos fragmentos de bosque están inmersos en un paisaje compuesto por cultivos agrícolas, sistemas agroforestales, pastizales de uso ganadero y vegetación secundaria (Gual-Díaz y RendónCorrea, 2017).
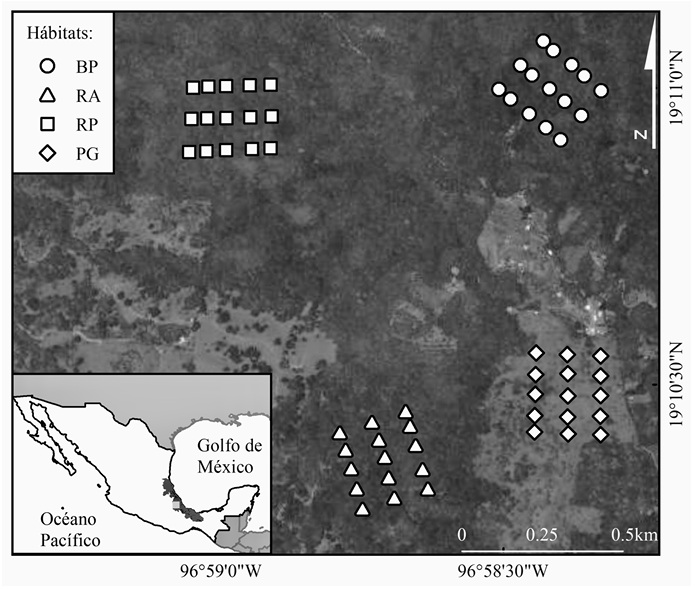
Los hábitats muestreados son bosque primario (BP), vegetación secundaria donde se implementó restauración activa (RA), vegetación con 18 años de sucesión secundaria (RP) y pastizal de uso ganadero (PG).
Figura 1 Localización del área de estudio en un paisaje de bosque mesófilo de montaña en Huatusco, Veracruz, México.
El sitio de estudio es un predio privado de aproximadamente 135 ha, que desde 2005 está en proceso de sucesión secundaria. Antes del año de exclusión, se utilizó como pastizal ganadero durante 25 años con una densidad de una cabeza de ganado por hectárea. La mayor parte del área perturbada se destinó a la restauración, en donde se establecieron 50 ha a la restauración activa y 50 ha a la sucesión secundaria natural. En el área destinada a la restauración activa se reintrodujeron especies como Alnus acuminata Kunth (Fagales: Betulaceae) y Quercus xalapensis Humb. & Bonpl. (Fagales: Fagaceae). Mientras que en el área destinada a la sucesión secundaria se permitió que se iniciara naturalmente el proceso de regeneración o colonización por especies (López-Barrera et al., 2016).
Dentro del paisaje de estudio se seleccionaron cuatro tipos de hábitats con diferente complejidad estructural de la vegetación e historias naturales (Fig. 1): i) un fragmento de bosque mesófilo de montaña que, por sus características estructurales, se consideró como bosque primario (BP); ii) un fragmento de vegetación secundaria donde se implementó la estrategia de restauración activa (RA) hace 18 años, iii) un fragmento de vegetación secundaria con 18 años de sucesión secundaria o de restauración pasiva (RP); iv) un pastizal de uso ganadero (PG) que se utiliza activamente todo el año para el pastoreo de ganado.
Diseño de muestreo
La distancia entre habitas varió de 1 km a 4 km, en cada hábitat se establecieron tres transectos de 250 m de longitud, con una separación de 100 m entre sí y ubicados a por lo menos 100 m del borde. Cada transecto incluyó cinco puntos de muestreo separados a 50 m de distancia uno de otro. El muestreo se realizó en la estación seca (mayo) y de lluvias (septiembre) de 2021.
Muestreo de escarabajos coprófagos
En cada punto de muestreo se colocó una trampa de caída, la cual consistió en un recipiente de plástico de 500 ml (11 cm de diámetro y 7.5 cm de alto). Dicha trampa fue enterrada de tal manera que su abertura estuviera al nivel del suelo. En seguida, se le agregaron 250 ml de propilenglicol diluido a 50%. Como cebo se utilizaron 30 g de excremento humano, el cual fue envuelto en una malla de tela con una apertura de 0.5 mm y suspendido por encima y en el centro de la trampa (Larsen y Forsyth, 2005). Finalmente, la trampa fue cubierta con un plato de plástico de 30 cm de diámetro con el fin de evitar el exceso de basura o agua en caso de lluvia.
Los escarabajos recolectados se procesaron y preservaron en etanol a 70%, algunos ejemplares, uno a cinco, se montaron en seco para su identificaron a nivel género o especie con ayuda de claves taxonómicas (Delgado et al. 2000; Vaz-De-Mello et al., 2011) y listados regionales (Deloya et al., 2007; Huerta et al., 2016; Díaz et al., 2020); y en caso de no lograr su identificación, se designaron como morfoespecies. El muestreo se realizó bajo un permiso de recolección de escarabajos (SPARN/DGVS/05006/23) emitido por la Dirección de Vida Silvestre de la Secretaría de Medio Ambiente y Recursos Naturales (Semarnat) de México. Todos los escarabajos de cada morfoespecie fueron depositados en la Colección Entomológica de la Facultad de Ciencias Biológicas y Agropecuarias Región Orizaba-Córdoba en Amatlán de los Reyes, Veracruz, México.
Caracterización del hábitat
En cada hábitat se midieron las siguientes características estructurales (Tabla 1): i) la proporción de suelo cubierto por hojarasca y herbáceas en 1 m2; ii) la densidad de árboles (individuos/ha); iii) densidad de arbustos (individuos/ha); y iv) cobertura del dosel (%) usando un densiómetro esférico y convexo modelo A (Forestry Suppliers, Inc., Jackson, Misisipi); y v) la altura del dosel utilizando un altímetro modelo Haga (Forestry Suppliers, Inc., Jackson, MisSissippi).
Análisis de datos
La abundancia de especies se consideró como el total de individuos de cada especie en cada trampa instalada dentro de cada hábitat de muestreo. La completitud del inventario para cada hábitat se calculó con el estimador de cobertura de la muestra (
La riqueza de especies se estimó para cada hábitat utilizando una técnica de inter y extrapolaciones basadas en el estimador de la cobertura de la muestra utilizando el paquete iNEXT para R (Hsieh et al., 2016). Se consideró 100% de completitud como un nivel confiable de la diversidad para todos los hábitats (Chao y Jost, 2012). Para comparar la riqueza de especies entre los cuatro hábitats, se utilizaron intervalos de confianza a 95% en donde se infirieron diferencias significativas cuando los intervalos de confianza no se superponen (Cumming, 2008).
Para evaluar las diferencias en la dominancia y rareza de las especies y en la uniformidad de los ensambles entre los sitios, la abundancia proporcional de escarabajos se representó mediante curvas de especies de rango-abundancia o curvas de Whittaker (Magurran, 1988). Se graficó la abundancia proporcional de cada especie ordenada de forma decreciente, para mostrar las diferencias en la dominancia y la rareza de las especies en la uniformidad de los ensambles entre los hábitats.
La similitud composicional entre los ensambles de cada hábitat se determinó con el índice de Bray-Curtis. Este índice tiene valores que van de 0 (similitud mínima) a 100 (similitud máxima) y en este estudio se representó visualmente mediante un análisis de escalamiento multidimensional no métrico (NMDS). Se realizó un análisis de similitud (ANOSIM) como prueba estadística de permutación de las diferencias entre los ensambles de cada hábitat (Clarke y Warwick, 2001). Se empleó el método de porcentajes de similitud (SIMPER) para determinar la contribución porcentual de cada una de las especies a la disimilitud entre hábitats. Estos análisis se realizaron en el programa PRIMER versión 6.1.16 (Clarke y Gorley, 2006).
Para cuantificar la contribución de cada ensamble a la diversidad total (o del paisaje), se calculó el número promedio de especies ausentes de cada hábitat (diversidad beta), definido como
Resultados
Caracterización del hábitat
La cobertura del dosel varió de 84.9% (BP) a 12.3% (PG) (Tabla 1). La densidad de árboles varió de 1593 ha-1 (BP) a 133 ha-1 (PG). La cobertura del estrato arbustivo varió de 18 individuos en el RP a cuatro individuos en el PG. En cuanto a la cobertura del estrato herbáceo varió de 97.5% en el PG a 34.1% en el BP. La cobertura de hojarasca varió de 64.4% en el BP a 0.9% en el PG. En general, el BP presentó el mayor número de árboles por hectárea, mayor proporción de cobertura del dosel y hojarasca.
Tabla 1 Características estructurales de cuatro hábitats de muestreo en un paisaje de bosque mesófilo de montaña en Huatusco, Veracruz, México.
| Característica \ hábitat | BP | RA | RP | PG |
| Suelo cubierto por hojarasca (%) | 64.4 ± 5.2a | 50.2 ± 3.6b | 54.9 ± 6.5b | 0.9 ± 1.2c |
| Suelo cubierto por herbáceas (%) | 34.1 ± 6.2a | 48.1 ± 4.1b | 43.2 ± 6.1b | 97.5 ± 2.1c |
| Riqueza de árboles (número de especies) | 21 ± 1.1a | 15 ± 0.8b | 19 ± 1.1a | 2 ± 1.6c |
| Riqueza de arbustos (número de especies) | 15 ± 1.7a | 17 ± 1.6a | 18 ± 1.8a | 4 ± 1.7b |
| Densidad de árboles (ha-1) | 1593 ± 1.8a | 1380 ± 1.5b | 1426 ± 1.4c | 133 ± 1.1d |
| Densidad de arbustos (ha-1) | 3333 ± 5.3a | 1633 ± 4.3b | 3206 ± 7.3c | 200 ± 3.16d |
| Cobertura del dosel (%) | 84.9 ± 1.9a | 71.4 ± 6.1b | 79.5 ± 3.3b | 12.3 ± 9.5c |
BP: bosque primario; RA: vegetación secundaria donde se implementó restauración activa; RP: vegetación con 18 años de sucesión secundaria; y PG: pastizal de uso ganadero. Los promedios ± error estándar y letras minúsculas diferentes en una misma fila indican diferencias significativas (p ≤ 0.05; prueba Kruskal-Wallis; comparación pareada U de Mann-Whitney).
Diversidad alfa
Se alcanzó 100% de completitud en cada uno de los ensambles de los cuatro hábitats muestreados, al igual que en la completitud del inventario de todo el estudio (los cuatro hábitats juntos), recolectándose un total de 1397 individuos pertenecientes a 11 especies, siete tribus y siete géneros, cada tribu representada por un género (Tabla 2). El género Onthophagus presentó el mayor número de especies (3 spp.), seguido por Coprophanaeus y Dichotomius (2 spp. cada uno). Los géneros Copris, Deltochilum, Phanaeus y Scatimus estuvieron representados por una sola especie.
El número de especies observadas varió significativamente de 6 (BP) a 10 (RP) (Fig. 2). El hábitat RP presentó el mayor número de especies, seguida de los hábitats RA y PG, ambos estadísticamente semejantes; y finalmente, el hábitat BP presentó el menor número de especies.
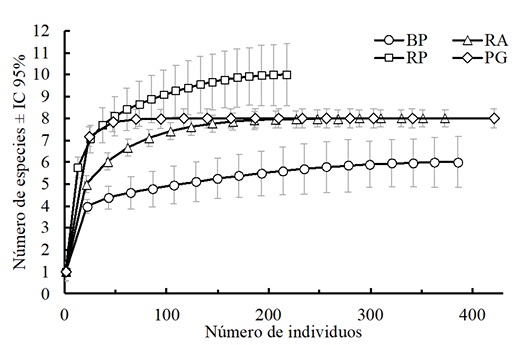
Figura 2 Comparación de la riqueza de especies estimada ± intervalos de confianza (I.C) a 95% entre hábitats de bosque primario (BP), vegetación secundaria donde se implementó restauración activa (RA), vegetación con 18 años de sucesión secundaria (RP) y pastizal de uso ganadero (PG) en un paisaje de bosque mesófilo de montaña en Huatusco, Veracruz, México.
En cuanto a la abundancia proporcional, existió una alta dominancia y baja equidad en BP y una baja dominancia y alta equidad en PG (Fig. 3). Las especies dominantes fueron Deltochilum mexicanum en BP, Dichotomius satanas en RA, Onthophagus taurus en RP y Dichotomius colonicus y Onthophagus taurus en PG.
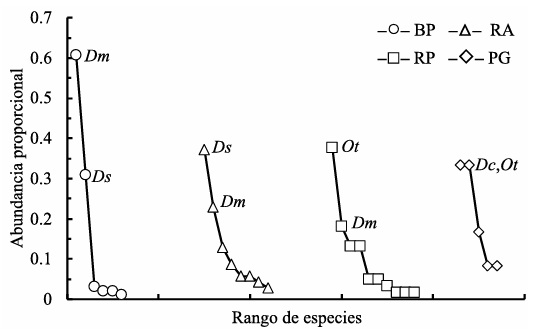
Las especies más abundantes fueron Deltochilum mexicanum (Dm), Dichotomius satanas (Ds) y Onthophagus taurus (Ot).
Figura 3 Curvas de rango-abundancia para las especies de escarabajos coprófagos recolectados en hábitats de bosque primario (BP), vegetación secundaria donde se implementó restauración activa (RA), vegetación con 18 años de sucesión secundaria (RP) y pastizal de uso ganadero (PG) en un paisaje de bosque mesófilo de montaña en Huatusco, Veracruz, México.
Diversidad beta
El ANOSIM indicó un efecto significativo del tipo de hábitat sobre la similitud composicional entre los ensambles de escarabajos coprófagos
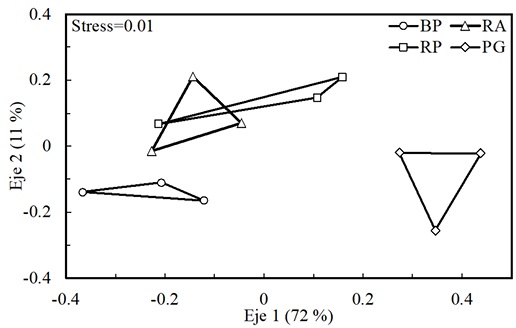
Figura 4 Escalamiento multidimensional no métrico (NMDS) de los ensambles de especies de escarabajos coprófagos asociados a hábitats de bosque primario (BP), vegetación secundaria donde se implementó restauración activa (RA), vegetación con 18 años de sucesión secundaria (RP) y pastizal de uso ganadero (PG) en un paisaje de bosque mesófilo de montaña en Huatusco, Veracruz, México.
Diversidad gamma
La diversidad gamma
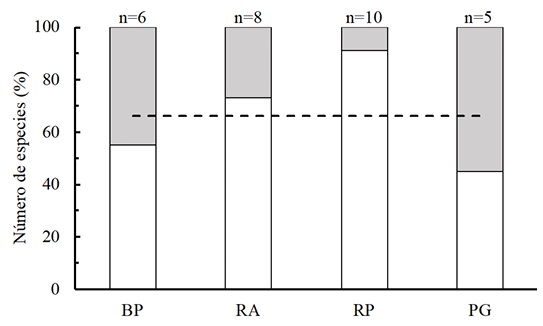
Figura 5 Contribución de la diversidad alfa (barras blancas), alfa promedio (línea punteada) y diversidad beta (barras negras) a la diversidad gamma de los ensambles de especies de escarabajos coprófagos en hábitats de bosque primario (BP), vegetación secundaria donde se implementó restauración activa (RA), vegetación con 18 años de sucesión secundaria (RP) y pastizal de uso ganadero (PG) en un paisaje de bosque mesófilo de montaña en Huatusco, Veracruz, México.
Discusión
El BMM es un ecosistema altamente diverso caracterizado por las condiciones de humedad, nubosidad y altas concentraciones de materia orgánica; en este sentido, las redes tróficas juegan un papel crucial en su biodiversidad asociada y procesos ecológicos. La diversidad de escarabajos coprófagos es de suma importancia dentro de las redes tróficas al reciclar y descomponer estiércol de mamíferos, esta actividad contribuye a la formación de comunidades microbianas del suelo, dispersión de semillas y disponibilidad de recursos para otros niveles tróficos (Almeida et al., 2022; Torabian et al., 2024). En este estudio se registró un total de 11 especies de escarabajos coprófagos que representan aproximadamente 58% de las especies registradas para el paisaje de BMM estudiado (Tabla 2). Otros estudios realizados previamente en la reserva del BMM de Huatusco, Veracruz han encontrado 12 (Deloya et al., 2007) y 13 (Díaz et al., 2020) especies. Todas las especies colectadas en este estudio son compartidas con las informadas por Díaz et al. (2020) debido a la similitud del muestreo y la cercanía con los hábitats estudiados. En comparación con Deloya et al. (2007), solo se compartieron las especies Copris incertus, Coprophanaeus corythus, Deltochilum mexicanum, Dichotomius satanas, Onthophagus rhinolophus y Phanaeus endymion. Esto se debe probablemente a la diferencia de años en los que se realizaron ambos estudios, ya que los cambios espaciales y climáticos pueden provocar el desplazamiento y aparición de nuevas especies (Noriega et al., 2021). La especie más abundante, tanto en este estudio como en los trabajos previos, fue D. mexicanum. Cuya presencia en el paisaje de estudio es indicadora de hábitats conservados por su asociación con bosques primarios (Cancino-López et al., 2014; Giraldo-Mendoza, 2021).
La riqueza de especies fue significativamente mayor en el hábitat RP seguido por PG y RA y menor en BP (Fig. 2). Este resultado es consistente con Díaz et al. (2020), quienes indican que los hábitats expuestos a actividades de manejo, como la restauración, presentan un aumento exponencial de la diversidad. Sugieren también que la composición y estructura del paisaje adyacente juega un rol importante en la aceleración del proceso de sucesión. En otros grupos taxonómicos, que también se consideran bioindicadores, como reptiles, mamíferos, anfibios, aves (Smith et al., 2015) y artrópodos (Cole et al., 2016), se observó una recuperación similar para ambas estrategias. Por lo cual, el patrón de riqueza observado es un indicador de un proceso de sucesión secundaria exitoso, en escarabajos coprófagos y otros grupos bioindicadores. Además, se ha observado que la riqueza de escarabajos coprófagos es indicadora de la abundancia de mamíferos y de árboles en el hábitat (Bogoni et al., 2016; Buse et al., 2021). Estos hallazgos sugieren que los hábitats de vegetación secundaria, y que se encuentran en proceso de regeneración, poseen la capacidad de funcionar como refugios de la biodiversidad en los paisajes de BMM. De hecho, en la última década los estudios que evalúan el funcionamiento y la restauración ecológica de áreas degradadas de BMM han tenido mayor relevancia tanto para México como para Veracruz con un aumento de 100% de estudios (Williams-Linera, 2015).
El hábitat PG presentó la mayor abundancia de especies, mientras que el RP la menor (Tabla 2, Fig. 3). Este resultado es debido al manejo veterinario del ganado, el cual no está basado en el uso de medicamentos o productos formulados a partir de lactonas macrocíclicas (Sands y Wall, 2018). Por ello, el estiércol de vaca disponible es atractivo para que un gran número de individuos de diferentes especies puedan alimentarse, reproducirse y anidar (Bezanson y Floate, 2022). También, es probable que la competencia inter e intraespecífica por tal recurso sea mínima (Hanski y Cambefort, 1991). Contrariamente, en los hábitats RA y RP se observó la menor abundancia, a pesar de que existe una mayor diversidad de mamíferos silvestres (Pérez-Gracida et al., 2023). Tales comunidades de mamíferos estuvieron conformadas en su mayoría por especies carnívoras, herbívoras y frugívoras. Sin embargo, los escarabajos coprófagos generalmente prefieren heces de mamíferos omnívoros debido a que éstas poseen mayor calidad nutricional (Filgueiras et al., 2007). Por esta razón, la disponibilidad y características del estiércol en los hábitats con actividades de restauración no representa un recurso óptimo para mantener una alta abundancia de escarabajos (Costa et al., 2013). Dado este escenario, los escarabajos coprófagos del paisaje de BMM pueden ser señalados como indicadores de actividades de manejo intensivas como la ganadería, ya que estos hábitats les proveen una mayor cantidad y calidad de estiércol.
La composición de los ensambles de los hábitats RA y RP fue similar y únicamente el hábitat RA presentó una composición similar al BP (Fig. 4). Este resultado soporta la hipótesis de que los hábitats de vegetación secundaria en proceso de sucesión secundaria son colonizados por un ensamble de especies proveniente del bosque original (Ríos-Casanova y Godínez-Álvarez, 2023). Sin embargo, cuando existen variaciones en la similitud composicional generalmente son debidas a la complejidad estructural de la vegetación y las actividades de manejo (como la estrategia de restauración) (Davis et al., 2002). Este resultado denota el éxito de la restauración activa en RA, ya que se ha evidenciado la efectividad de esta actividad de manejo en la estructura y composición de especies hasta después de 20 años o 50 años (Bonfil et al., 2021). En el caso de RP, se puede inferir que este hábitat tomó una trayectoria de sucesión divergente, fluctuante y heterogénea como resultado del contexto espacial y climático (Norden et al., 2015). Por lo tanto, la presencia de hábitats sometidos a diferentes actividades de manejo (como la restauración activa o pasiva y la ganadería) enriquecen la diversidad regional de escarabajos coprófagos y probablemente de otros grupos animales como aves (Morrison y Lindell, 2011) y murciélagos (Serna-Lagunes et al., 2024).
Los resultados obtenidos de las biparticiones de la diversidad gamma mostraron que esta depende, en mayor grado, de la diversidad alfa (Fig. 5). Este patrón sugiere una importancia relativa de los filtros ambientales locales sobre la dispersión y colonización de los ensambles a escala regional (da Cunha y Frizzas, 2020; Álvarez et al., 2022). Dichos filtros reflejan tanto diferencias en las características del hábitat como en la calidad y cantidad de recursos ofrecidos, el microclima y la estructura vegetal (Müller y Goßner, 2010). De hecho, los hábitats estudiados poseen diferencias significativas en diferentes características indicadoras de su estructura biofísica (Tabla 1). Por ejemplo, la cobertura del dosel es una característica que regula las condiciones microclimáticas del suelo y reduce la desecación del excremento (Dormont et al., 2012). Estos hallazgos coinciden con Gómez-Cifuentes et al. (2020) y con Guerra-Alonso et al. (2019), quienes postulan que la estructura de la vegetación representa una característica crucial para la riqueza y abundancia local de escarabajos. Finalmente, la complejidad estructural de la vegetación es uno de los principales filtros ambientales en los paisajes de BMM, ya que provee condiciones microclimáticas favorables para la diversidad de escarabajos coprófagos.
Conclusiones
En este trabajo se evidencia que los hábitats que integran un paisaje de bosque mesófilo de montaña cambian la diversidad regional de escarabajos coprófagos. Ciertas actividades de manejo, como la restauración activa y pasiva, son capaces de crear hábitats funcionales como reservorios de la biodiversidad debido al proceso de sucesión secundaria. Tales actividades han demostrado su utilidad en la regeneración de hábitats amenazados como el bosque mesófilo de montaña, permitiendo el reensamblaje de su gran biodiversidad y los servicios ecosistémicos provistos. Finalmente, los distintos hábitats del paisaje de bosque mesófilo de montaña son capaces de albergar diferentes ensambles de especies y por lo tanto su conservación y manejo a escala regional es de suma importancia para los escarabajos y probablemente para otros grupos faunísticos.











 text new page (beta)
text new page (beta)


