Introducción
La biznaga barril de oro Kroenleinia grusonii (Hildm.) J. Lodé (anteriormente Echinocactus grusonii Hildm.) es una cactácea que se encuentra enlistada en la NOM-059-SEMARNAT-2010 en peligro de extinción (SEMARNAT, 2010). La Lista Roja de la IUCN (Unión Internacional para Conservación de la Naturaleza y Recursos Naturales, por sus siglas en inglés) también la coloca como amenazada, debido a que solo se localizan dos subpoblaciones, una en Zacatecas y otra en Querétaro, México (IUCN, 2024). Algunas de las circunstancias que la han llevado a esta situación son la destrucción de su hábitat natural y su colecta ilegal para utilizarlas como fuente de alimento y ornato (Manzo-Rodríguez et al., 2022; Villavicencio-Gutiérrez et al., 2023). Es común introducir las plantas xerófitas para embellecer el paisaje urbano, por requerir baja cantidad de agua (Alanís, 2006). Con el fin de explorar la germinación de semillas de Kroenleinia grusonii, surge la pregunta de si los tratamientos pregerminativos podrían tener influencia en la germinación de las semillas provenientes de las áreas urbanas y así compararlas con lo reportado por otros autores que han estudiado diversos aspectos de K. grusonii en su ambiente natural.
La germinación in vitro es una alternativa viable para la propagación de especies vulnerables, cuando en condiciones naturales las plantas presentan crecimiento lento, bajos porcentajes de germinación (Almeida et al., 2021) o algún tipo de latencia (Rojas-Aréchiga y García-Morales, 2022). Esto es posible ya que permite controlar diversos factores abióticos como la intensidad de luz, temperatura, humedad, entre otros, facilitando la propagación de plantas (Dávila-Sandoval y Galván-Hernández, 2024). Asimismo, la propagación por semilla permite mantener mejores características genéticas en las plantas regeneradas (Rodríguez-Ruiz et al., 2018).
Una de las formas de promover la germinación de las semillas es aplicando diferentes tratamientos pregerminativos como la escarificación química, que ha sido utilizada en numerosas especies de cactáceas (Barrios et al., 2020). Este tipo de escarificación simula el paso de las semillas por el tracto digestivo de herbívoros (Sánchez-Villegas y Rascón-Chu, 2017). Por otro lado, la escarificación mecánica consiste en remover o desgastar la testa para permitir el paso de agua en semillas con testa impermeable y además que el embrión se expanda con facilidad (Robles-Martínez et al., 2016). De esta manera el embrión tiene mayor acceso a la humedad, oxígeno y temperatura promoviendo la germinación (Rodríguez et al., 2019).
De acuerdo con la literatura consultada, se encontraron tres reportes relacionados con la germinación de K. grusonii.En 1994, De la Rosa-Ibarra y García, realizaron escarificación química a las semillas y las colocaron en papel húmedo para promover 68% de germinación. Posteriormente, Manzo-Rodríguez et al. (2022) sembraron semillas en medio de cultivo MS (Murashige y Skoog, 1962) y lograron 20% de germinación. Recientemente, Villavicencio-Gutiérrez et al. (2023) observaron que las semillas de K. grusonii muestran latencia, ya que presentaron 32.5% de germinación, y recomendaron romperla con tratamientos físicos o químicos. Los tratamientos pregerminativos pueden tener un efecto significativo en la germinación y el peso de las semillas, y podrían incidir en la forma de su dispersión que impactaría en el tamaño de sus plántulas (Sosa-Pivatto et al., 2014).
Por tales motivos, la presente investigación tuvo como objetivo comparar la influencia del peso de la semilla en sus variables morfométricas; el efecto de la interacción de los tratamientos pregerminativos y peso de la semilla en la germinación y tamaño de plántulas, así como presentar la descripción morfológica de las plántulas cultivadas in vitro de K. grusonii.
Materiales y Métodos
Variables morfológicas de las semillas
En septiembre 2022 se obtuvieron aproximadamente 300 semillas de cada uno de los 10 frutos maduros obtenidos de dos individuos (30 cm de diámetro y 22 cm de altura) de K. grusonii (Fig. 1). Estas plantas crecen decorando los jardines urbanos de un centro comercial de El Paso, Texas, Estados Unidos de América (31°46'08''N, 106°22'09''O). Según Gold et al. (2004), 500-1000 semillas es un número adecuado de colecta para estudios de germinación.

Figura 1: Plantas adultas de Kroenleinia grusonii (Hildm.) J. Lodé. A. planta 1; B. planta 2. Fotografía: Pedro Osuna Ávila.
Las semillas se extrajeron de los frutos colectados y se almacenaron aleatoriamente en frascos de vidrio a temperatura ambiente y oscuridad durante 14 meses. Los experimentos se realizaron en el Laboratorio de Cultivo de Tejidos Vegetales, ubicado en el Instituto de Ciencias Biomédicas en la Universidad Autónoma de Ciudad Juárez, en Ciudad Juárez, Chihuahua, México.
Para agrupar las semillas, se pesaron 780 semillas una por una en una balanza analítica (Sartorius BP61S® peso máximo 61 g, Goettingen, Alemania). Con esto se obtuvo un intervalo del peso de las semillas, donde el peso mínimo fue 0.2 mg y el máximo 1.3 mg. A partir de estos datos, se formaron tres grupos de semillas según su peso, colocando 260 semillas en cada grupo. En el grupo uno (pequeñas) se situaron las semillas ≤0.5 mg, en el dos (medianas) las semillas 0.6-0.9 mg, y en el tres (grandes) las que pesaban ≥1.0 mg.
Para realizar las medidas morfométricas, se seleccionaron aleatoriamente 50 semillas de cada grupo de peso. Las semillas se observaron a través de un microscopio estereoscópico (SMZ 800, Nikon®, Nikon Corporation, Konan Minato-Ku, Tokio, Japón), con cámara digital (Digital Sight DS-Fi2, Nikon®, Nikon Corporation, Konan Minato-Ku, Tokio, Japón), acoplado al programa computacional NIS-elements (BR, v. 4.30.02, Nikon Corporation, Konan Minato-Ku, Tokio, Japón), con el cual se realizaron y procesaron sus mediciones.
Se midió el ancho (mm) de manera transversal en su límite medio-inferior en la parte más amplia; el largo, según la longitud (mm) de la parte apical-basal y el área (mm2) brindada por el mismo programa (Fig. 2A). Para las mediciones internas de las semillas, se seleccionaron aleatoriamente 10 de cada grupo de peso y se fijaron a un portaobjetos con pegamento instantáneo (Kola Loka®). Después se desgastaron con una lija de agua número 2000 (Fandeli®) hasta que fuera visible el embrión (Cano-Vázquez et al., 2015).
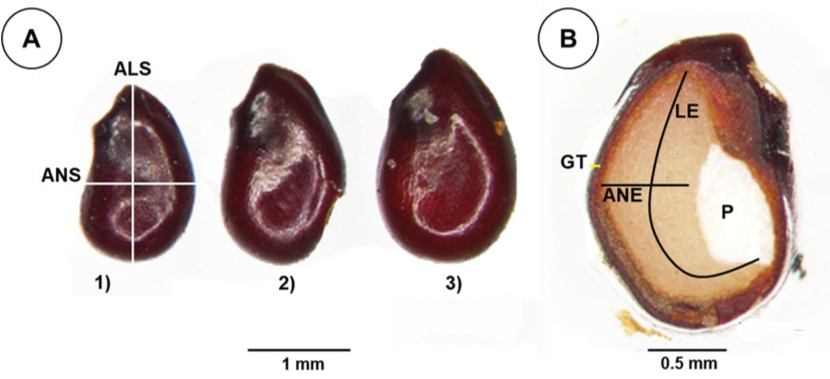
Figura 2: Variables morfológicas de las semillas de Kroenleinia grusonii (Hildm.) J. Lodé. A. semillas de los tres grupos de peso 1) pequeñas, 2) medianas, 3) grandes (2×); ANS=ancho de la semilla, ALS=altura de la semilla; B. semilla escarificada con lija (3×); ANE=ancho del embrión, LE=longitud del embrión, GT=grosor de la testa, P=perispermo. Fotografías: Dolores Adilene García González.
Para medir el largo, ancho del embrión (mm) y grosor de la testa (mm), se usó el programa computacional NIS-elements (BR, v. 4.30.02, Nikon®, SMZ 800, Nikon Corporation, Konan Minato-Ku, Tokio, Japón). El área del embrión dentro de la semilla (mm2) se obtuvo al multiplicar la longitud por el ancho del embrión (Fig. 2B). Las semillas se observaron en un microscopio estereoscópico (SMZ 800, Nikon®, Nikon Corporation, Konan Minato-Ku, Tokio, Japón), con cámara digital (Digital Sight DS-Fi2, Nikon®, Nikon Corporation, Konan Minato-Ku, Tokio, Japón). Estas semillas no fueron utilizadas para los experimentos de germinación. Para calcular el porcentaje que el embrión ocupa dentro de la semilla con respecto al área de las semillas, se dividió el área del embrión entre el área de la semilla y se multiplicó por 100.
Interacción de los tratamientos pregerminativos y peso de la semilla
Se aplicaron cinco tratamientos pregerminativos a las semillas de los tres grupos de peso que consistieron en lo siguiente:
Tratamiento control: se utilizaron semillas intactas y asépticas.
Tratamiento de hidratación: las semillas asépticas se sumergieron durante 24 horas en agua destilada estéril.
Ensayo de escarificación química: las semillas se sumergieron en ácido clorhídrico (HCl) al 30% durante cinco minutos, seguido de un enjuague con agua destilada para remover el exceso de HCl.
Tratamiento con ácido sulfúrico (H2SO4) al 25%: las semillas se sumergieron durante cinco minutos y posteriormente se enjuagaron con abundante agua destilada.
Escarificación mecánica: las semillas asépticas se remojaron por 24 horas en agua destilada estéril; posteriormente, con pinzas y bisturí, 50% de la testa fue removida. Las semillas fueron observadas en un microscopio estereoscópico (BE-S5, Velab®, Ciudad de México, México) en condiciones estériles para facilitar el procedimiento de remoción de la testa sin causar daño al embrión.
A los tres grupos de peso de las semillas se les aplicaron los cinco tratamientos pregerminativos. Para cada grupo de peso y tratamiento se utilizaron 50 semillas (150 semillas por tratamiento), dando un total 750. La unidad experimental fueron frascos Gerber®, en los cuales se colocaron diez semillas con cinco repeticiones para cada grupo de peso por tratamiento.
A todas las semillas se les realizó el mismo procedimiento de asepsia. Este consistió en lavarlas con agua y jabón líquido (Axion®) durante cinco minutos en agitación con un agitador para microplaca (Isotemp®, Fisher Scientific, Pittsburgh, Pennsylvania, EUA) y se enjuagaron con abundante agua de la llave. Posteriormente las semillas se colocaron en una solución de hipoclorito de sodio (Cloralex® 4-6%) al 50% durante 20 minutos y fueron enjuagadas tres veces con agua destilada estéril en una campana de flujo laminar tipo vertical doble (Isaac Lab®, Zapopan, Jalisco, México).
Una vez que las semillas estuvieron asépticas se colocaron en los frascos Gerber® conteniendo 20-25 ml de medio de cultivo MS al 25% de la concentración de macro y micronutrientes, adicionado con 30 g l-1 de azúcar morena como fuente de carbono. El pH del medio de cultivo se ajustó a 5.7±0.1 y se solidificó con 7 g l-1 de agar (tipo I para micropropagación, Caisson Laboratories®). El medio de cultivo se esterilizó en autoclave horizontal de vapor (TE-A22, Terlab®, Tepic, Nayarit, México) por 30 minutos a 121 °C. Los frascos con las semillas se incubaron para su germinación en una cámara bioclimática de cultivo de tejidos vegetales (ubicada en el edificio V del Instituto de Ciencias Biomédicas, Universidad Autónoma de Ciudad Juárez, Ciudad Juárez, Chihuahua, México), con fotoperiodo de 16 horas luz y 8 horas de oscuridad (con intensidad lumínica 111 μmol m-2 s-2 y temperatura de 25±1 °C).
La germinación de las semillas fue monitoreada cada 48 horas durante 30 días. Se consideró como semilla germinada a aquella en la que era visible la emergencia de la radícula a través de la testa. Al concluir el tiempo de germinación se evaluó el efecto que tienen los tratamientos pregerminativos y el peso de la semilla en el tamaño de las plántulas obtenidas. Para determinar el tamaño, se les midió la altura del tallo (mm), diámetro del tallo (mm) y longitud de la raíz (mm). Las mediciones se realizaron con un vernier digital (Truper®, Caldi-6mp, Estado de México, México).
Morfología de plántulas
La descripción morfológica de la etapa juvenil de K. grusonii se realizó a partir de las plántulas obtenidas del tratamiento de escarificación mecánica, debido a que su germinación inició a partir del tercer día de cultivo. Las plántulas de este tratamiento fueron monitoreadas durante 60 días de crecimiento, manteniendo las condiciones asépticas.
Las plántulas fueron observadas a través de un microscopio estereoscópico (SMZ 800, Nikon®, Nikon Corporation, Konan Minato-Ku, Tokio, Japón), conectado a una cámara digital (Digital Sight DS-Fi2, Nikon®, Nikon Corporation, Konan Minato-Ku, Tokio, Japón) y las imágenes obtenidas fueron procesadas con el programa NIS-elements (BR, v. 4.30.02. Nikon®, Nikon Corporation, Konan Minato-Ku, Tokio, Japón), para así obtener con mayor precisión las imágenes digitales de las diferentes estructuras externas de las plántulas de K. grusonii.
Análisis estadísticos
La normalidad de los datos se corroboró con la técnica de Kolmogorov-Smirnov para las variables morfológicas de la semilla. Se realizó la transformación de logaritmo natural (ln) al no presentar normalidad según la variable. Se ejecutó un análisis de correlación de Pearson y cuando resultó significativo se incluyó un análisis de regresión para la obtención del modelo y así expresar la magnitud de la pendiente.
Se realizaron análisis de regresión y correlación entre el peso de las semillas y las variables área de la semilla (longitud × ancho), y grosor de la testa y área del embrión (longitud × ancho). El análisis del efecto de tratamiento pregerminativo y el peso de las semillas en el desarrollo de las plántulas (altura, longitud de raíz y número de raíces) se llevó a cabo con un análisis de varianza (ANOVA) con arreglo factorial en donde el primer factor fue el peso de las semillas con tres niveles, el segundo factor fueron los tratamientos pregerminativos con cinco niveles, y comparación de medias de Tukey (p≤0.05).
El porcentaje de germinación, al tratarse de una variable binomial no paramétrica (germinó sí o no), se analizó con la prueba estadística U de Mann-Whitney para dos muestras independientes, de manera que se compararon cada una de las 15 combinaciones de tratamientos en parejas (p≤0.05). Estos análisis fueron realizados con el programa estadístico SPSS v. 24.0 (IBM, 2017).
Resultados
Variables morfológicas de las semillas
El peso de las semillas presentó una tendencia positiva y correlación lineal positiva (p<0.05) con la longitud de la semilla (r=0.702, F=100.8, p<0.01), mientras que la ecuación de regresión (y= -2.8439+2.0488x) mostró que el peso aumenta en 2.048 mg por cada mm de longitud. La misma tendencia lineal se detectó para el ancho de la semilla (r=0.6458, F=142, p<0.01), donde la ecuación obtenida (y= -2.0174+2.2278x) indica que el peso aumenta en 2.23 mg por cada mm de ancho.
Por ejemplo, las semillas de mayor peso presentaron 1.85±0.01 mm de longitud y 1.31±0.007 mm de ancho (Cuadro 1). Al hacer la correlación entre el peso y el área de la semilla se observó una mejor asociación positiva significativa con efecto logarítmico (r=0.7714 F=142, p<0.01). De esta manera, la ecuación de regresión (y= -0.212+2.047 log x) indica que el peso de la semilla aumenta en 2.05 mg por cada mm2 del área de la semilla, con valores máximos observados en área de 1.80±0.02 mm2 en las semillas grandes (Cuadro 1).
Cuadro 1: Variables morfológicas de semillas de Kroenleinia grusonii (Hildm.) J. Lodé, por grupo de peso. LS=longitud de la semilla, ANS=ancho de la semilla, AS=área de la semilla, AE=área del embrión, LE=longitud del embrión y GT=grosor de la testa. n=50 semillas. Medias ± el error estándar. Letras diferentes significan diferencias significativas (p≤0.05).
| Peso | LS (mm) | ANS (mm) | AS (mm2) | AE (mm2) | LE (mm) | GT (mm) |
| ≤0.5 mg (pequeñas) | 1.65±0.01b | 1.59±0.009b | 1.41±0.01b | 0.95±0.04b | 1.82±0.05b | 0.03±0.002a |
| 0.6-0.9 mg (medianas) | 1.71±0.00b | 1.22±0.01b | 1.56±0.02b | 1.27±0.23a | 2.28±0.12a | 0.05±0.003a |
| ≥1.0 mg (grandes) | 1.85±0.01a | 1.31±0.007a | 1.80±0.02a | 1.77±0.09a | 2.3±0.07a | 0.04 ± 0.003a |
La correlación entre el peso de la semilla y área del embrión (AE) fue significativa (r=0.6022, p<0.01), donde las semillas medianas y grandes presentaron promedios estadísticamente iguales (F=7.86, p=0.0020), siendo mayor en las semillas grandes con 1.77±0.09 mm2 (Cuadro 1). La proporción que ocupa el embrión dentro de la semilla es 67.37% en las semillas pequeñas, en las semillas medianas es 81.41% y en las semillas grandes, 98.33%. Para la longitud del embrión, la correlación lineal es positiva (r=0.7892, F=8.8 p<0.01), donde las semillas más pesadas presentaron el mayor promedio con 2.3±0.07 mm (Cuadro 1).
En cuanto al grosor de la testa y peso de la semilla, no existe correlación entre las variables (F=0.71, p=0.5020). No obstante, las semillas de peso medio fueron las que mostraron una tendencia a presentar mayor grosor con 0.05±0.003 mm (Cuadro 1). En general, los resultados muestran que, a mayor peso de la semilla, mayor será su tamaño.
Interacción de los tratamientos pregerminativos y peso de la semilla
En la interacción de tratamiento pregerminativo y peso de la semilla se encontraron diferencias estadísticamente significativas (p≤0.05). La escarificación mecánica fue el tratamiento que mostró los mejores resultados obteniendo en las semillas medianas 66±0.47% de germinación, seguido de las semillas pequeñas y grandes con 50±0.5% de germinación en ambas (Cuadro 2).
Cuadro 2: Porcentaje de germinación de semillas de Kroenleinia grusonii (Hildm.) J. Lodé, a los 30 días de cultivo in vitro en la interacción grupo de peso y tratamiento pregerminativo. *Grupo 1: ≤0.5 mg (pequeñas), 2: 0.6-0.9 mg (medianas), 3: ≥1.0 mg (grandes). n=50 semillas. Prueba estadística U de Mann-Whitney. Medias ± el error estándar. Letras diferentes representan diferencias significativas (p≤0.05). Esc. Mec.=Escarificación mecánica.
| *Grupo de peso | Tratamiento | % de germinación |
| 1 | Control | 34±0.47 bcd |
| 2 | Control | 38±0.49 bc |
| 3 | Control | 10±0.30 fg |
| 1 | Hidratación | 20±0.48 def |
| 2 | Hidratación | 36±0.48 bcd |
| 3 | Hidratación | 12±0.33 fg |
| 1 | HCl | 22±0.41 cdef |
| 2 | HCl | 30±0.49 bcde |
| 3 | HCl | 06±0.23 g |
| 1 | H2SO4 | 42±0.49 bcdef |
| 2 | H2So4 | 14±0.35 efg |
| 3 | H2SO4 | 24±0.43 bcdef |
| 1 | Esc. Mec. | 50±0.5 ab |
| 2 | Esc. Mec. | 66±0.47 a |
| 3 | Esc. Mec. | 50±0.5 ab |
Aunado a eso es importante señalar que las semillas de este tratamiento iniciaron el proceso de germinación más prontamente, es decir, a partir del cuarto día de incubación in vitro en los tres grupos de peso de semillas. Estos resultados superaron a los obtenidos con el tratamiento control, que, con semillas medianas, obtuvo 38±0.49% de germinación (Cuadro 2), casi la mitad del tratamiento de escarificación mecánica, y las semillas empezaron a germinar hasta el día 12.
Los resultados obtenidos en K. grusonii muestran que las semillas medianas fueron las que presentaron una mejor respuesta de germinación. El porcentaje de germinación más bajo se observó en el tratamiento de HCl en semillas grandes con solo 6±0.23% y germinaron hasta el día 14 (Cuadro 2).
El tamaño de las plántulas se vio afectado por los tratamientos pregerminativos aplicados y el peso de las semillas. En el Cuadro 3, se muestran las mediciones que se realizaron a las plántulas después de 30 días de cultivo in vitro. El tratamiento de H2SO4 en semillas grandes promovió las plántulas con mayor tamaño del tallo con 8.33±0.46 mm de altura (F=8.65, p=<0.0001) y 3.8±0.17 mm de diámetro (F=4.01, p=0.0002). Mientras que las raíces de mayor longitud las promovió el tratamiento de escarificación mecánica (F=3.6, p=0.0006) en semillas grandes con 11.80±1.52 mm.
Cuadro 3: Mediciones de alto y diámetro del tallo, longitud de raíz y número de raíces secundarias en plántulas de Kroenleinia grusonii (Hildm.) J. Lodé, de 30 días de cultivo in vitro. *Grupo 1: ≤0.5 mg (pequeñas), 2: 0.6-0.9 mg (medianas), 3: ≥1.0 mg (grandes). Medias ± el error estándar. Letras diferentes representan diferencias significativas (p≤0.05). Esc. Mec.=Escarificación mecánica.
| *Grupo de peso | Tratamiento | Altura del tallo (mm) | Diámetro del tallo (mm) | Longitud Raíz (mm) | No. raíces secundarias |
| 1 | Control | 5.21±0.39cde | 2.27 0.13±de | 4.36±0.65abc | 2.76±0.66a |
| 2 | Control | 4.96±0.26cde | 2.36±0.13 cde | 4.48±0.82abc | 1.89±0.53ab |
| 3 | Control | 5.08±0.67cde | 2.56±0.42bcde | 3.61±0.40bc | 0.2±0.20ab |
| 1 | Hidratación | 5.45±0.38bcd | 2.58±0.21bcde | 3.97±1.20abc | 0.83±0.63ab |
| 2 | Hidratación | 5.97±0.29bcd | 2.82±0.20abcd | 7.19±1.22abc | 0.64±0.45ab |
| 3 | Hidratación | 6.09±0.29bcd | 2.68±0.36abcd | 3.21±1.18abc | 0.33±3.33ab |
| 1 | HCl | 5.64±0.34 bcd | 2.41±0.24bcde | 4.40±0.76abc | 1.91±0.58ab |
| 2 | HCl | 5.71±0.35bcd | 2.41±0.18bcde | 6.80±1.32abc | 1.47±0.43ab |
| 3 | HCl | 3.54±0.98e | 1.54±0.13e | 0.40±0.32c | 0.00±0.00b |
| 1 | H2SO4 | 7.39±0.31ab | 3.45±0.26ab | 09.58±0.76ab | 2.1±0.32ab |
| 2 | H2SO4 | 4.23±0.3de | 2.23±0.08de | 3.11±0.94bc | 0.33±0.24ab |
| 3 | H2So4 | 8.33±0.46a | 3.8±0.17a | 10.86±1.78ab | 2.33±0.44ab |
| 1 | Esc. Mec. | 6.04±0.28 bcd | 3.28±0.08abcd | 7.48±1.52abc | 1.96±0.36 ab |
| 2 | Esc. Mec. | 6.62±0.2 abc | 3.39±0.12 abc | 8.01±1.11abc | 1.7±0.32 ab |
| 3 | Esc. Mec. | 6.2±0.2 bc | 3.43±1.15 abc | 11.80±1.52 a | 0.83±0.19 ab |
En cuanto al mayor número de raíces secundarias, el tratamiento control promovió 2.76±0.66 raíces por plántula (Cuadro 3). Las plántulas de menor tamaño se obtuvieron a partir de semillas grandes tratadas con HCl, donde la altura del tallo fue 3.54±0.98 mm, el diámetro 1.54±0.13 mm y la longitud de la raíz fue 0.40±0.32 mm, sin la formación de raíces secundarias. Estas variables fueron inferiores a las semillas grandes del tratamiento control, donde la altura del tallo fue 5.08±0.67 mm, diámetro 2.56±0.42 mm y longitud de raíz 3.61±0.40 mm (Cuadro 3).
Morfología de plántulas
Se registraron cambios morfológicos desde el inicio de la germinación de una semilla con escarificación mecánica, hasta una plántula de 60 días de cultivo in vitro. En el día uno la semilla con escarificación mecánica muestra el embrión (E) (Fig. 3A), a la cual se le removió aproximadamente 50% de la testa (T). A los siete días la radícula (Ra) de color blanco es curveada, el hipocótilo (Hc) es suculento de color amarillo pálido y los cotiledones aún se encuentran cubiertos por una porción de la testa (T) (Fig. 3B).

Figura 3: Morfología de las plántulas de Kroenleinia grusonii (Hildm.) J. Lodé. A. semilla escarificada día uno (3×) (E=embrión, T=testa); B. plántula de siete días (1×) (Hc=hipocótilo, T=testa, Ra=radícula); C. plántula de 15 días (1×) (Co=cotiledón, Hc=hipocótilo, Ra= radícula, Rs=raíz secundaria); D. plántula de 21 días (1×) (A=areola, Ec= epicótilo, Co=cotiledón, Es=espina, Ra=radícula, Rs=raíz secuendaria); E. plántula de 30 días (1×) (A=areola, Tb=tubérculo, Ec=epicótilo, Co=cotiledón, Hc=hipocótilo, Rs=raíz secundaria, Ra=radícula); F. plántula de 45 días (1×) (Co=cotiledón, A=areola, Ec=epicótilo, Es=espina, Ra=radícula, Rs=raíz secundaria); G. planta de 60 días (1×) (Co=cotiledón, A=areola, Es=espina, Ra=radícula, Rs=raíz secundaria). Fotografías: Dolores Adilene García González.
Después de 15 días de cultivo, la radícula (Ra) mide 10.2 mm de longitud, empezando a desarrollar raíces secundarias (Rs) en la base del hipocótilo (Hc) el cual presenta una coloración café. El tallo de la plántula mide 7.4 mm de altura y tiene una coloración verde con puntos de color blanco en la superficie, el hipocótilo (Hc) es elongado y los cotiledones (Co) con forma cónica son paralelos y un poco separados entre sí, turgentes y puntiagudos del ápice (Fig. 3C).
A los 21 días, la raíz (Ra) ya muestra raíces secundarias (Rs), los cotiledones (Co) han reducido su tamaño, así como su turgencia debido a la emergencia del epicótilo (Ec) con las primeras areolas (A) con espinas (Es) (Fig. 3D). A los 30 días, la raíz (Ra) alcanza una longitud de 12.4 mm con aproximadamente seis raíces secundarias (Rs); aún mantiene los cotiledones (Co) y se aprecia el alargamiento del epicótilo (Ec) con nueve tubérculos (Tb), una areola (A) en cada uno y de ocho a diez espinas (Es) rectas, transparentes y puntiagudas por areola; la plántula presenta una forma cilíndrica y el tallo mide 7.91 mm de altura (Fig. 3E).
A los 45 días de crecimiento, la raíz primaria (Ra) mide 17.6 mm de longitud y presenta aproximadamente siete raíces secundarias (Rs); los cotiledones (Co) todavía se conservan en la plántula; el epicótilo (Ec) se ha redondeado y presenta 11 areolas (A) con ocho a diez espinas (Es) cada una; el tallo mide 8.64 mm de altura y 4.86 mm de diámetro (Fig. 3F).
A los 60 días la raíz (Ra) mide 18.65 mm de longitud y mantiene el mismo número de raíces secundarias (Rs); la plántula presenta los cotiledones (Co) marchitos, pero aún son visibles; el número de areolas aumenta a 13 y de ocho a diez espinas cada una; el eje epicótilo-hipocótilo tiene 9.28 mm de longitud con 5.06 mm de diámetro (Fig. 3G).
Discusión
Variables morfológicas de las semillas
Las semillas de cactáceas pueden presentar una amplia variación en la forma y tamaño. Específicamente el tamaño puede ser de gran importancia, ya que influye en diversos procesos como la germinación y desarrollo de las plántulas (Sosa-Pivatto et al., 2014). De igual manera, cuando existe variación en el tamaño de las semillas dentro de una misma especie, se puede asegurar una mayor permanencia de sus poblaciones en los ecosistemas (Ayala-Cordero et al., 2004).
Rojas-Aréchiga et al. (2013) realizaron una clasificación de las semillas según su longitud y consideraron a las semillas de K. grusonii como medianas, mientras que las de Echinocactus texensis (Hopffer) Britton & Rose como grandes, con 2.598±0.266 mm de longitud, y pequeñas a las de Mammillaria albilanata Backeb., con 1.32±0.128 mm de longitud. Otras especies presentan semillas muy pequeñas con una longitud promedio de 0.48±0.01 mm en Strombocactus corregidorae S. Arias & E. Sanchez (Camacho-Velázquez et al., 2018).
Las semillas de tamaño grande de K. grusonii fueron las que presentaron mayor área; sin embargo, existen especies con semillas más grandes como Neobuxbaumia scoparia (Poselg.) Backeb., con 2.81 mm2 o más grandes en Neobuxbaumia laui (P.V. Heath) D.R. Hunt, con 9.0±0.02 mm2 (Arroyo-Cosultchi et al., 2007).
No obstante, en especies de Opuntia (L.) Mill. se ha reportado un área hasta diez veces mayor que en K. grusonii. Unos ejemplos son Opuntia polyacantha Haw., con 19.69±mm2 (Núñez-Gastelum et al., 2018), Cylindropuntia imbricata F. M. Knuth in Backeb. & F. M. Knuth, con 14.1±1.3 mm2 y Cylindropuntia spinosior (Engelm) F. M. Knuth, con 13.4±1.5 mm2. Estas diferencias podrían atribuirse a la morfología de las semillas (Reyes-Corral et al., 2022).
Respecto al área del embrión, se han reportado especies que presentan embriones con área hasta tres veces mayor que K. grusonii como Opuntia ficus-indica (L.) Mill., con 6.941 mm2 y Opuntia rastrera F.A.C. Weber, con 5.946 mm2 (González-Cortés et al., 2019). El área de la semilla se relaciona con el tamaño del embrión y a su vez con el porcentaje de germinación, debido a que se pueden obtener porcentajes de germinación mayores en semillas con embriones grandes.
Un ejemplo es el huizache (Vachellia farnesiana (L.) Willd.), en el que el embrión ocupa 72% de la semilla y se obtuvo 100% de germinación (Rivas et al., 2005). En las semillas de K. grusonii se observó que el área que ocupa el embrión en relación con el área de la semilla fue superior a 90% en las semillas grandes. Sin embargo, las semillas medianas donde el embrión ocupa 81.4% del área fueron las que presentaron mejores resultados en el porcentaje de germinación.
Esos resultados podrían deberse a que las semillas grandes requieren de un mayor tiempo de imbibición y en las semillas pequeñas los embriones pueden no estar bien desarrollados (Sánchez-Salas et al., 2006). En cambio, existen otras especies que presentan embriones de menor área con relación al área de la semilla. Por ejemplo, el embrión en Cylindropuntia spinosior ocupa 37.43±3.56% (González-Fernández et al., 2023), mientras que en el chile piquín (Capsicum annuum var. glabriusculum (Dunal) Heiser & Pickersgill) solo abarca 25% del área total de la semilla y el resto se compone por el endospermo (Cano-Vázquez et al., 2015).
El tamaño del embrión puede influir en la cantidad de reservas que las semillas tienen acumuladas en los cotiledones, reflejándose así en el crecimiento y supervivencia de las plántulas (González-Vélez et al., 2020). Un carácter que es relevante en las semillas es el tamaño del embrión y la testa, ya que puede ser de utilidad para la conservación ex situ de las especies (González-Cortés et al., 2019).
El grosor de la testa depende del número de capas de células que la componen y se relaciona con el proceso de absorción de agua (Domínguez-Domínguez et al., 2007). Entre los grupos de peso de las semillas de K. grusonii no se encontraron diferencias significativas en el grosor de la testa, presentando de 0.03 a 0.05 mm, lo cual sugiere que el tamaño de la semilla no afecta en su grosor.
Existen especies en las que, a mayor tamaño de la semilla, mayor es el grosor de la testa. Por ejemplo, Opuntia ficus-indica presenta 0.8 mm de grosor en la testa y sus semillas miden 4.843 mm de longitud. En cambio, las semillas pequeñas de Opuntia microdasys (Lehm.) Pfeiff., con 2.569 mm de longitud, presenta una testa con grosor menor de 0.3821 mm (González-Cortés et al., 2018).
Galussi et al. (2015) encontraron que, a mayor grosor de la testa en semillas de Medicago sativa L., desarrollaban latencia física debido a que aumentaba la permeabilidad, asociada a que las semillas presentan mayor cantidad de sustancias que repelen el agua. Con los datos obtenidos en este estudio y la literatura consultada, se considera que las semillas de K. grusonii presentan una testa delgada, la cual podría no afectar a su permeabilidad.
Interacción de los tratamientos pregerminativos y peso de la semilla
Los tratamientos pregerminativos o el medio de cultivo a utilizar pueden acelerar o retrasar el proceso germinativo (Mascot-Gómez et al., 2019). En este estudio, las semillas de K. grusonii con el tratamiento de escarificación mecánica iniciaron la germinación al cuarto día, a diferencia del tratamiento control (semillas intactas) que fue hasta el día 15. Manzo-Rodríguez et al. (2022) afirmaron que las semillas intactas de K. grusonii colocadas en medio MS al 50% germinaron después de 34 días y en medio MS al 100% fue a los 13 días.
Con la información obtenida se confirma que con la escarificación mecánica la germinación de las semillas de K. grusonii ocurre en menor tiempo. Resultados similares fueron encontrados en Echinocactus parryi Engelm., en la cual la escarificación mecánica incrementó el potencial germinativo promoviendo el inicio de la germinación a partir del segundo día y alcanzando 96% de germinación (García-González et al., 2022). La escarificación mecánica permite eliminar una parte de la cubierta de la semilla sin causar daño al embrión; de esta manera se facilita la absorción de agua y oxígeno favoreciendo la germinación de las semillas (Rodríguez et al., 2019), tal como sucedió en K. grusonii. En el caso de Opuntia engelmannii Salm-Dyck ex Engelm., la escarificación mecánica también logró resultados favorables con 82% de germinación (González-Cortés et al., 2018).
Al realizar escarificación mecánica en las semillas de K. grusonii se obtiene el porcentaje máximo de germinación (66%), a diferencia de la escarificación química con HCl o H2SO4, con las cuales el porcentaje de germinación fue menor. Manzo-Rodríguez et al. (2022) reportaron 40% de germinación en semillas de K. grusonii colectadas en un jardín botánico. Utilizaron el tratamiento de H2SO4 al 100% durante un minuto y sus resultados fueron similares a los obtenidos en la presente investigación en las semillas pequeñas con el tratamiento de H2SO4.
También en Mammillaria mainiae K. Brandegee, al tratar las semillas con HCl, se reduce el porcentaje de germinación al obtener 35% de germinación en comparación con el control que fue de 86.7% (Sánchez-Villegas y Rascón-Chu, 2017). En cambio, en otras especies se obtiene una mejor respuesta al aplicar escarificación química a las semillas como lo que se reporta para Melocactus zehntneri (Britton & Rose) Luetzelb., donde los mejores resultados se lograron al someter a las semillas bajo tratamiento con HCl por 40 minutos con 51% de germinación (Magnani y Cardoso, 2023).
Similarmente, en semillas tratadas durante 1.5 minutos con H2SO4, se obtiene 83% de germinación en Mammillaria sphacelata Mart. (Navarro et al., 2008). Por los resultados encontrados se puede inferir que las semillas de K. grusonii provenientes de jardines urbanos de El Paso, Texas, arrojaron bajos porcentajes de germinación con tratamientos químicos, por lo que se sugiere que sus semillas no sean escarificadas químicamente con estas concentraciones.
Respecto al tratamiento control, los resultados de porcentaje de geminación fueron similares a los reportados por Villavicencio-Gutiérrez et al. (2023), con 32.5% de germinación en semillas K. grusonii colectadas en su hábitat natural. Por tales motivos, se puede asumir que las semillas de jardines urbanos pueden responder de manera similar a semillas provenientes del hábitat natural de K. grusonii. Por lo tanto, se descarta que las semillas de K. grusonii pudieran haber desarrollado pérdida de viabilidad por el tiempo de 14 meses de almacenamiento.
Rojas-Aréchiga y García-Morales (2022) reportaron un aumento de la viabilidad de las semillas de Ferocactus peninsulae (F.A.C. Weber) Britton & Rose, después de cuatro años de almacenamiento. Briseño-Sánchez et al. (2024) confirmaron en otro género de cactáceas que las semillas de Lophophora diffusa (Croizat) Bravo permanecieron viables después de cuatro años de almacenamiento.
Por otra parte, el peso de las semillas se encuentra relacionado con la reserva de nutrientes, aunque también depende de la especie, el tipo de semillas y las condiciones ambientales en la que se desarrollan (González-Vélez et al., 2020). Por lo tanto, se ha considerado que las semillas de mayor tamaño tienden a desarrollar plántulas más grandes (Martino et al., 2021).
Con los resultados observados, las plántulas que se obtuvieron de las semillas grandes (≥1.0 mg) fueron de mayor tamaño, especialmente las del tratamiento de H2SO4. En un estudio realizado por Sosa-Pivatto et al. (2014), se encontró que el peso de la semilla tiene una relación positiva con el tamaño de las plántulas. Por ejemplo, en Gymnocalycium bruchii (Speg.i) Hosseus, con semillas de 1.32 mg, las plántulas alcanzaron 3.64 mm de altura, a diferencia de Gymnocalycium mostii (Gürke) Britton & Rose, en la cual las semillas más pequeñas (0.08 mg) originaron plántulas de menor altura (1.96 mm).
La relación entre el peso de la semilla y el tamaño de la plántula puede ser variante aún en la misma especie como en Gymnocalycium quehlianum (F. Haage ex Quehl) Vaupel ex Hosseus, con semillas en tres grupos de peso (0.14, 0.18 y 0.19 mg), siendo las más pesadas las que desarrollaron plántulas de mayor tamaño (2.57 mm de altura) (Martino et al., 2021), tal como lo observado en K. grusonii. Ortiz-Martínez et al. (2021) explicaron que las plántulas de mayor tamaño almacenan mayor cantidad de humedad y desarrollan raíces más grandes, que pueden asegurar la supervivencia en condiciones ambientales secas.
Morfología de plántulas
El estudio morfológico de las plántulas es de importancia taxonómica, ya que algunas de las estructuras de la etapa juvenil desaparecen en estado adulto (Loza-Cornejo y Terrazas, 2011). Las observaciones realizadas en las plántulas de K. grusonii son una fuente de información que puede contribuir a la identificación de esta especie en etapas juveniles en su hábitat natural.
Es posible detectar diferencias entre las especies de cactáceas en etapas tempranas del desarrollo. Por ejemplo, en Trichocereus candicans (Gillies ex Sam-Dyck) Britton & Rose, al emerger la radícula se acompaña de abundantes pelos radiculares (Cenizo et al., 2013), característica que no fue observada en la radícula de K. grusonii.
En las especies Strombocactus corregidorae, Strombocactus disciformis (DC.) Britton & Rose subsp. disciformis y Strombocactus disciformis subsp. esperanzae Glass & Arias, los cotiledones e hipocótilo se observan de color verde a partir del segundo día y las plántulas son globosas, ya que el hipocótilo es más ancho que los cotiledones y la raíz (Camacho-Velázquez et al., 2018). En cambio, en K. grusonii el color verde de los cotiledones se observó hasta los siete días y sus plántulas son cilíndricas, ya que los cotiledones son paralelos al hipocótilo. En Echinocactus parryi Engelm. se observa que a partir de los 20 días de crecimiento inicia la emergencia del epicótilo junto con las primeras areolas (García-González et al., 2022), de igual forma que en K. grusonii.
A pesar de que las plántulas presenten diferencias morfológicas, la mayoría de las especies de cactáceas muestran una estructura morfológica inicial general, que es una radícula pequeña, hipocótilo suculento y dos cotiledones cónicos (Cenizo et al., 2013).
Los resultados de este estudio podrían ser considerados para la conservación y aprovechamiento de K. grusonii, tanto en su hábitat natural como en los parques y jardines de áreas urbanas. La germinación in vitro bajo condiciones controladas es una opción viable para contribuir en su propagación masiva en el futuro. A partir de las plántulas obtenidas, se podría iniciar su adaptación a condiciones de invernadero o utilizarlas como fuente de explantes para iniciar protocolos de micropropagación.
Conclusiones
El peso de la semilla aumenta conforme aumenta su tamaño. Los tratamientos pregerminativos demuestran que la escarificación mecánica es el mejor tratamiento para acelerar la germinación y promover casi el doble del porcentaje de germinación en comparación con el tratamiento control. De acuerdo con la literatura revisada, se puede mencionar que este estudio reporta la primera descripción de la plántula de K. grusonii durante los primeros 60 días de cultivo in vitro. Esta información podría ser utilizada para la identificación ex situ e in situ en sus etapas de plántula, así como para la conservación y protección de K. grusonii.











 text new page (beta)
text new page (beta)



