Introducción
Echinopsis pachanoi, comúnmente conocido como cactus San Pedro, es una especie nativa de la región andina de América del Sur y ha sido utilizada tradicionalmente por sus propiedades terapéuticas en las culturas indígenas (Engel, Barratt, Ferris, Puljevic y Winstock, 2023; Torres, Zamora, Núñez y González, 2023). Más allá de su importancia cultural, E. pachanoi ha atraído interés en la investigación científica contemporánea por sus posibles aplicaciones farmacológicas y como planta ornamental (Paniagua-Zambrana, Bussmann, Echeverría, 2020; Torres-Toukoumidis, Marín y Hinojosa, 2022). Sin embargo, al igual que todas las plantas, E. pachanoi enfrenta varios tipos de estrés biótico y abiótico en su hábitat natural, lo que hace necesario encontrar mecanismos para mejorar su resistencia y productividad (Li, Hu, Jian, Xie y Yang, 2021; Ruiz-Cruz, 20211).
La rizosfera, del suelo que rodea las raíces de las plantas, es un microambiente dinámico donde ocurren interacciones intrincadas entre las plantas, el suelo y varios microorganismos, incluyendo bacterias del género Pseudomonas (Pathan, Ceccherini, Sunseri y Lupini, 2020; Ling, Wang y Kuzyakov, 2022). Entre estos microorganismos, ciertos consorcios bacterianos han llamado la atención debido a su profundo impacto en la salud de las plantas y la promoción del crecimiento (Santoyo et al., 2021a). Especialmente, la asociación de consorcios bacterianos con la rizosfera de Echinopsis pachanoi representa un punto crucial de investigación, dada la notable adaptabilidad y tolerancia de estos consorcios a entornos extremos, se ha demostrado que estas bacterias pueden inducir la resistencia sistémica adquirida en las plantas, aumentando así su capacidad para tolerar diversos tipos de estrés, como la sequía, la salinidad y la presencia de metales pesados (Behr et al., 2023; Hu et al., 2021).
En este contexto, la presencia y actividad de consorcios bacterianos en la rizosfera de E. pachanoi ofrecen un área de investigación fascinante (Uypan-Farro, García, Carreño, Arellano y Zúñiga, 2021). Estos consorcios, compuestos por diversas especies bacterianas, exhiben relaciones simbióticas o comensales con la planta, influyendo en su crecimiento y desarrollo a través de múltiples mecanismos (Santoyo et al., 2021b). Al colonizar la rizosfera, estas bacterias pueden modular la disponibilidad de nutrientes, mejorar la tolerancia al estrés y estimular la producción de hormonas vegetales, promoviendo así la vigorosidad y productividad general de la planta (Khan, Shahid, Mustafa, Sayyed y Curá, 2021; Kong y Liu, 2022).
Comprender la composición, dinámica y roles funcionales de los consorcios bacterianos asociados con la rizosfera de E. pachanoi tiene una gran importancia tanto para la investigación básica como aplicada (Marín, González y Poupin, 2021). Desde una perspectiva fundamental, elucidar las interacciones entre estas bacterias y el hospedero vegetal contribuye a una comprensión más amplia de las interacciones planta-microorganismo y la dinámica del ecosistema (Aguilar-Paredes, Valdés y Nuti, 2020). Además, desde una perspectiva aplicada, aprovechar el potencial de estos consorcios bacterianos presenta oportunidades para prácticas agrícolas sostenibles, estrategias de biorremediación y el desarrollo de nuevos biofertilizantes y biostimulantes (Gehlot, Pareek y Vivekanand, 2021).
En esta investigación, exploramos el estado actual de los consorcios bacterianos con capacidad promotora del crecimiento en la rizosfera de E. pachanoi. Analizamos el contexto ecológico de la rizosfera, la diversidad y composición de los consorcios bacterianos, sus mecanismos de acción y las implicaciones de estas interacciones para la salud y productividad de la planta. Además, discutimos las posibles aplicaciones de aprovechar estos consorcios bacterianos para fines agrícolas y ambientales, destacando vías para futuras investigaciones e innovaciones en este apasionante campo.
Materiales y Métodos
Zonas de Recolección de Muestras
Para llevar a cabo el estudio se empleó la metodología descrita por Culman, Fulford, Camerata y Steinke (2020), donde se recolectaron 12 muestras de siete zonas diferentes en la región Sierra del Ecuador, incluyendo Cuenca, Girón, Gualaceo, Biblián, Azogues, Otavalo y Cotacachi. Cada muestra se obtuvo específicamente de la rizosfera de plantas adultas de San Pedro (Echinopsis pachanoi), extrayéndose a una profundidad estandarizada de 12 cm. Las muestras, con un peso individual de 1 kg, se rotularon y almacenaron inmediatamente en una hielera para minimizar las alteraciones de sus propiedades debido a factores climáticos.
Aislamiento de Bacterias Rizosféricas
Las muestras fueron procesadas en los laboratorios de Biología y Microbiología ubicados en el Campus Experimental “La María” en los predios de la Universidad Técnica Estatal de Quevedo utilizando la metodología de diluciones seriadas establecida por Patra et al. (2020), empleando como amortiguador el buffer fosfato salino (PBS), compuesto por Cloruro de sodio (NaCl) a una concentración de 137 mM, Fosfato de sodio dibásico anhidro (Na₂HPO₄) a 10 mM, Fosfato de sodio monobásico (NaH₂PO₄) a 1.8 mM y Cloruro de potasio (KCl) a 2.7 mM. Las muestras diluidas se inocularon en placas de agar nutritivo de la marca Difco™ y se incubaron a 28 °C durante un período de 72 horas. Tras la incubación, se seleccionaron colonias con un tamaño superior a 0.5 mm para facilitar su purificación.
Caracterización Bioquímica
Para la caracterización bioquímica, se purificaron las cepas aisladas en tres ocasiones utilizando medio de cultivo agar nutritivo y la técnica de desgaste por estriado en placa. Una vez obtenidas las cepas purificadas, se realizaron diversas pruebas bioquímicas. La tinción de Gram permitió determinar el tipo de pared celular, diferenciando entre bacterias Gram-positivas y Gram-negativas.
También se evaluó la producción de enzimas solubilizadoras de minerales mediante pruebas específicas las cuales son: ureasa, utilizando un medio con urea e indicador de pH para detectar la producción de amoníaco; fosfatasa, observando la liberación de fosfato inorgánico; y solubilización de potasio, identificando la formación de halos claros en el medio. Además, se realizaron pruebas de producción de catalasa, añadiendo peróxido de hidrógeno y observando la formación de burbujas; oxidasa, empleando el reactivo de oxidasa para detectar citocromo c oxidasa por el cambio de color a azul oscuro; proteasa, evaluando la capacidad de hidrolizar proteínas mediante la formación de zonas claras en el medio; y fluorescencia, examinando la producción de compuestos fluorescentes bajo luz UV.
Tolerancia a la Salinidad de los Cultivos Bacterianos
De las cepas previamente purificadas, se hicieron crecer en medio de cultivo LB líquido durante 72 horas en agitación orbital a una temperatura de 28 °C. Transcurrido el tiempo de incubación, se procedió a generar un medio de cultivo LB con adición de cloruro de sodio (NaCl) a concentraciones de 0.5 M y 1.0 M. Posteriormente, se transfirieron 200 microlitros de las cepas desarrolladas, ajustadas a una concentración de 1×1010 UFC mL-1. Estos cultivos se incubaron durante 20 horas, capturando datos de crecimiento a 600 nm en un espectrofotómetro marca HACH modelo DR 3900, en intervalos de 2 horas. Todas las cepas se compararon con un control sin adición de NaCl.
Producción de AIA
Las bacterias se cultivaron en caldo L-triptófano de la marca Merck, aprovechando este medio enriquecido donde el triptófano sirve como precursor del ácido indolacético (AIA). Después de 48 horas de crecimiento, se recolectaron 10 mL de cada cultivo para determinar la cantidad de AIA presente en el medio, utilizando el método colorimétrico de Salkowsky. Para cuantificar la concentración de AIA en los cultivos bacterianos, se construyó una curva de interpolación. Esta curva se basó en soluciones patrón de AIA (Sigma) con concentraciones conocidas de 2.5, 5, 10, 15, 20, 25, 30, 40, 45, 50 y 70 mg L-1. La absorbancia de estas soluciones se midió a 540 nm utilizando un espectrofotómetro GENESYS 180.
Caracterización Molecular
Se realizo la extracción de ADN bacteriano empleando el kit de extracción PureLinkTM Genomic DNA Mini Kit, luego se realizó la caracterización molecular de las cepas siguiendo el protocolo descrito por Karst et al. (2018), donde se utilizaron los partidores universales 8F (5’-AGAGTTTGATCCTGGCTCAG-3’) y 1492R (5’-ACG GCTACCTTGTTACGACTT-3’) que amplifica la subunidad ribosomal 16S de 1500 pb.
Para el protocolo de PCR se empleó una mezcla maestra en hielo, de un volumen de 1 mL más dos muestras adicionales para compensar pérdidas durante la pipeteo; cada reacción de 25 μL contenía agua libre de nucleasas, 2.5 μL de buffer de PCR 10X, 0.5 μL de dNTPs (10 mM cada uno), 0.5 μL de forward primer (10 μM), 0.5 μL de reverse primer (10 μM), 1.5 μL de MgCl2 (25 mM), 0.25 μL de Taq DNA polimerasa (5 U μL-1) y 1-5 μL de ADN template (20-50 ng). Se mezcló bien la mezcla y se alicuotaron 20 μL en cada tubo de PCR, añadiendo 5 μL de ADN a cada tubo y realizando un control negativo sin ADN para verificar la ausencia de contaminación.
Se programó el termociclador con un ciclo de desnaturalización inicial a 95 °C por 5 minutos, seguido de 30-35 ciclos de desnaturalización a 95 °C por 30 segundos, alineación a 55 °C por 30 segundos y extensión a 72 °C por 1 minuto, con una extensión final a 72 °C por 10 minutos y mantenimiento a 4 °C hasta su análisis. Para la verificación del producto de PCR, se preparó un gel de agarosa al 1% en buffer TAE, se cargaron 5 μL del producto de PCR mezclado con 1 μL de buffer de carga y se corrió la electroforesis a 100 V durante 30-40 minutos. Los fragmentos se recuperaron mediante el kit de purificación de bandas GFX PCR DNA, posteriormente los fragmentos recuperados fueron secuenciados mediante la técnica de Sanger.
Inducción del Desarrollo en Plántulas
Para la inducción del desarrollo en plántulas, se emplearon semillas de arroz de la variedad INIAP 16 por su capacidad de crecimiento acelerado y elasticidad en ensayos de estímulo de desarrollo celular. Las semillas se lavaron inicialmente con hipoclorito de sodio al 0.5%, seguido de un triple lavado con agua destilada para eliminar las trazas de cloro. Posteriormente, las semillas fueron sembradas en un sustrato compuesto de tierra negra y perlita en una proporción 2:1.
Transcurridos 4 días desde la siembra, se realizó la primera inoculación de cultivos bacterianos directamente al sustrato, utilizando una concentración de 1×107 UFC mL-1. Esta inoculación inicial fue seguida por dos inoculaciones adicionales, llevadas a cabo a intervalos de 5 días, aplicando 2 mL de la suspensión bacteriana en cada ocasión y manteniendo la misma concentración de la primera inoculación.
Durante el período de evaluación, no se fertilizaron las plantas para evitar interferir con los parámetros microbiológicos resultantes de la inoculación bacteriana en el suelo. Los riegos se realizaron diariamente con agua destilada estéril, la cual se obtuvo del laboratorio de Química y Bioquímica de la UTEQ.
Tolerancia a la Salinidad en Plántulas de Arroz Inoculadas con Bacterias
El ensayo se llevó a cabo empleando semillas de arroz de la variedad INIAP 16, siguiendo el mismo procedimiento de desinfección y siembra empleado en el ensayo de inducción de crecimiento. Las semillas se lavaron con hipoclorito de sodio al 0.5%, seguido de un triple lavado con agua destilada para eliminar las trazas de cloro, y luego se sembraron en un sustrato compuesto de tierra negra y perlita en una proporción 2:1. A los 4 días después de la siembra. Posteriormente, se realizó la primera inoculación bacteriana aplicando una suspensión con una concentración de 1×107 UFC mL-1 directamente al sustrato, y se llevaron a cabo dos inoculaciones adicionales a intervalos de 5 días, aplicando 2 mL de la suspensión bacteriana en cada ocasión. A los 15 días después de la germinación, se modificaron las condiciones del suelo con la adición de NaCl en una concentración de 0.5 M para inducir condiciones de salinidad. El ensayo incluyó un grupo control sin inoculación bacteriana ni adición de NaCl. Las plantas se colocaron en recipientes plásticos herméticos para atrapar los gases liberados durante el proceso de estrés. Después de cuatro días, se extrajeron muestras de aire de los recipientes y se analizaron utilizando un cromatógrafo de gases equipado con un detector de ionización de llama (GC-FID) para cuantificar la producción de etileno.
Resultados y Discusión
Tolerancia a la Salinidad de Cultivos Bacterianos
El estudio Bioquímico (Cuadro 1) permitió la caracterización de diversas cepas bacterianas de distintas zonas, analizando la tinción Gram, la actividad enzimática (catalasa y oxidasa) y la capacidad de solubilización de urea, fosfato y potasio, así como la producción de proteasa y fluoreceína. Las cepas AM-32, VC-31, CA-01, CM-04 y BL-15 fueron Gram positivas, mientras que AM-42, CD-22, VC-01, VC-03, CA-22, CM-09 y BL-51 fueron Gram negativas. Estudios llevados a cabo por Lianou, Nychas y Koutsoumanis (2020), demuestran que las variaciones en la producción enzimática de las cepas se deben a la variabilidad genética y fenotípica inherente a cada cepa. Por otra parte, Amaya-Gómez, Porcel, Mesa y Gómez (2020), menciona que estas diferencias son el resultado de la adaptación a diferentes ambientes y nichos ecológicos, lo que lleva a la diversificación de sus capacidades metabólicas y fisiológicas.
Table 1: Biochemical Characterization of Rhizospheric Bacteria Isolated from E. pachanoi.
| CEPA | ZONA | TINCIÓN GRAM | CAT | OXD | SOLUBILIZACIÓN | PTR | FLC | ||
| URE | FOS | POT | |||||||
| AM-32 | Cuenca | + | + | + | + | + | - | + | - |
| AM-42 | Cuenca | - | + | - | - | - | - | - | + |
| CD-22 | Girón | - | - | - | + | - | - | - | + |
| VC-01 | Girón | - | + | + | - | - | + | - | + |
| VC-31 | Girón | - | - | + | - | + | - | - | + |
| VC-03 | Gualaceo | + | + | - | + | - | - | + | - |
| CA-01 | Biblián | - | + | + | - | - | + | - | + |
| CA-22 | Biblián | - | - | + | - | + | - | + | + |
| CM-09 | Azogues | - | - | + | - | - | - | - | + |
| CM-04 | Otavalo | + | + | - | + | - | - | + | - |
| BL-15 | Cotacachi | - | + | + | - | + | - | - | + |
| BL-51 | Cotacachi | + | + | - | + | + | + | - | - |
Producción enzimática = CAT- Catalasa, OXD- Oxidasa, PTR-Proteasa. Capacidad adaptativa = FLC- fluorescencia. Solubilización = URE-Ureasa, FOS- fosfatasa y POT-degradación de potasio.
Enzymatic Production = CAT - Catalase, OXD - Oxidase, PTR - Protease. Adaptive Capacity = FLC - Fluorescence. Solubilization = URE - Urease, FOS - Phosphatase, and POT - Potassium Degradation.
En las reacciones bioquímicas todas las cepas mostraron actividad positiva de catalasa excepto AM-42 y VC-01, y actividad negativa de oxidasa, excepto AM-32, VC-31, CA-01 y BL-15. las diferencias en la actividad enzimática, como la catalasa y oxidasa, indican variaciones en las rutas metabólicas y en la capacidad de las bacterias para manejar el estrés oxidativo. En la investigación ejecutada por Sharma et al. (2022) demuestran que las diferencias en la actividad enzimática, como la catalasa y oxidasa, indican variaciones en las rutas metabólicas y en la capacidad de las bacterias para manejar el estrés oxidativo.
En las pruebas de solubilización todas las cepas, excepto CA-22 y BL-51, solubilizan urea; todas solubilizaron fosfato; y solo AM-42, CD-22, VC-01, VC-03, CA-22 y CM-09 no solubilizan potasio. Las cepas AM-32, AM-42, VC-03, CA-22, CM-04 y BL-15 produjeron proteasa, mientras que AM-32, CD-22, VC-01 y VC-03 no producen fluoreceína esto se relaciona con la variabilidad significativa en las capacidades de las cepas, destacando su potencial uso agrícola según sus propiedades individuales. Jana, Islam, Hore y Mandal (2023) en su estudio expresa que la capacidad de solubilización de urea, fosfato y potasio, así como la producción de proteasa y fluoreceína, se relacionan con la eficiencia en la utilización de nutrientes y la interacción con el entorno.
Caracterización Molecular
La identificación molecular de las cepas bacterianas, mostrada en la (Cuadro 2), se llevó a cabo mediante la consulta de sus secuencias en la base de datos NCBI/GenBank. La cepa AM-32 fue identificada como Bacillus megaterium con una cobertura de consulta del 100% y una identidad del 100% (Número de acceso: OQ658362.1).
Table 2: Molecular characterization of strains isolated from the rhizosphere of E. pachanoi.
| CEPA | Identidad (Base de datos NCBI / GenBank) | ||||
| Código | Nomenclatura | Cepa | Cobertura de consulta | Identidad | Numero de acceso |
| - - - - - - % - - - - - - | |||||
| AM-32 | Bacillus megaterium | GSEB2 | 100 | 100 | OQ658362.1 |
| AM-42 | Pseudomona putida | G-16 | 99 | 100 | OP107882.1 |
| CD-22 | Pseudomona veronii | NY11384 | 100 | 100 | CP120883.1 |
| VC-01 | Pseudomona fluorescens | qhj301 | 100 | 100 | MK217783.1 |
| VC-31 | Pseudomona fluorescens | G27 | 100 | 100 | KT767924.1 |
| VC-03 | Bacillus licheniformis | Lichen114 | 100 | 100 | MT279447.1 |
| CA-01 | Pseudomona putida | R43 | 100 | 100 | KC990820.1 |
| CA-22 | Pseudomona putida | N18 | 99 | 99.73 | KT883846.1 |
| CM-09 | Pseudomona corrugata | E11 | 100 | 99.90 | MK774793.1 |
| CM-04 | Bacillus megaterium | 8S6 | 100 | 100 | KM374745.1 |
| BL-15 | Pseudomona chlororaphis | A4 | 100 | 100 | HQ283403.1 |
| BL-51 | Bacillus brevis | C50 | 100 | 99.91 | AF424048.1 |
La cepa AM-42 fue identificada como Pseudomonas putida con una cobertura del 99% y una identidad del 100% (Número de acceso: OP107882.1). La cepa CD-22 fue identificada como Pseudomonas veronii con una cobertura del 100% y una identidad del 100% (Número de acceso: CP120883.1). La cepa VC-01 fue identificada como Pseudomonas fluorescens con una cobertura del 100% y una identidad del 100% (Número de acceso: MK217783.1). Estos resultados concuerdan con los descrito por Korshunova et al. (2021), quien demuestra que las bacterias del género Pseudomonas poseen una notable capacidad para metabolizar una amplia variedad de compuestos orgánicos. Sin embargo, Phale, Mohapatra, Malhotra y Shah (2022), establece que esto les permite aprovechar los exudados radiculares de las plantas, que contienen una mezcla diversa de azúcares, aminoácidos, ácidos orgánicos y otros nutrientes.
La cepa VC-31 fue identificada como Pseudomonas fluorescens con una cobertura del 100% y una identidad del 100% (Número de acceso: KT769424.1). La cepa VC-03 fue identificada como Bacillus licheniformis con una cobertura del 100% y una identidad del 100% (Número de acceso: MT729447.1). La cepa CA-01 fue identificada como Pseudomonas putida con una cobertura del 100% y una identidad del 100% (Número de acceso: KC990820.1), Yasmeen et al. (2021) determinan que las bacterias Pseudomonas spp. son conocidas por su resistencia a condiciones adversas como la sequía, salinidad y presencia de metales pesados.
La cepa CA-22 fue identificada como Pseudomonas putida con una cobertura del 99% y una identidad del 99.73% (Número de acceso: KT883446.1). La cepa CM-09 fue identificada como Pseudomonas corrugata con una cobertura del 100% y una identidad del 99.90% (Número de acceso: MK774793.1). La cepa BL-15 fue identificada como Pseudomonas chlororaphis con una cobertura del 100% y una identidad del 100% (Número de acceso: HQ238403.1) esto concuerda con Yasmeen et al. (2021) quien determino que algunas Pseudomonas. establecen relaciones simbióticas con las plantas, promoviendo su crecimiento mediante la producción de fitohormonas como las auxinas, y ayudando en la solubilización de fosfato y otros nutrientes esenciales.
La cepa CM-04 fue identificada como Bacillus megaterium con una cobertura del 100% y una identidad del 100% (Número de acceso: KM347745.1). Finalmente, la cepa BL-51 fue identificada como Bacillus brevis con una cobertura del 100% y una identidad del 99.91% (Número de acceso: AF424048.1). estudios llevados a cabo por Youssfi et al. (2024) demuestran que las esporas de Bacillus son altamente resistentes a condiciones ambientales adversas, como la sequía y las fluctuaciones de temperatura. Sin embargo, Lahlali et al. (2022) establece que esto permite que las bacterias sobrevivan en el suelo durante periodos desfavorables y colonizar rápidamente las raíces de las plantas cuando las condiciones mejoran. Por su parte, Longoria-Espinoza, Félix-Gastélum y Zamudio-Aguilasocho (2024) aislaron bacterias endófitas de raíces de Zea mays L. y evaluaron in vitro la capacidad promotora de crecimiento vegetal y actividad antagónica contra hongos fitopatógenos. La evaluación metabólica de las bacterias aisladas mostró a Bacillus subtilis con capacidades relevantes para la promoción de crecimiento vegetal con alta producción de hormonas y solubilización de fosfatos.
Tolerancia a Condiciones de Salinidad en Cepas Bacterianas
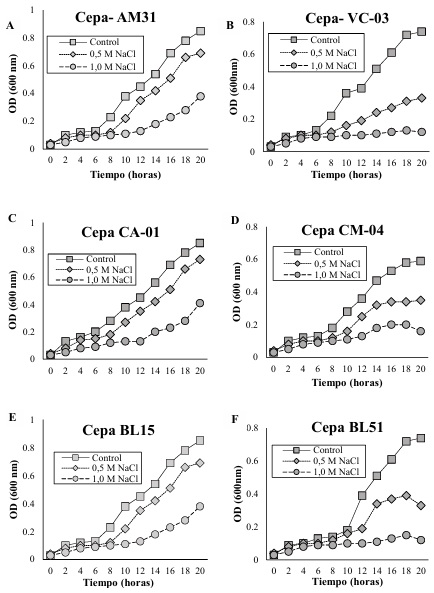
En la cepa AM31 (Figura 1A), evidenció crecimiento constante en la condición de control con una densidad óptica a las 20 horas de 0.85, mientras que en presencia de NaCl 0.5 M, el crecimiento fue menor con 0.69, en concentración de 1.0 M el crecimiento fue reducido con un valor de 0.38 a las 20 horas de evaluación. Este fenómeno se explica según lo estudiado por Sagar et al. (2022) quien determina que las bacterias tolerantes a la salinidad producen y acumulan solutos compatibles (conocidos como osmoprotectores) como glicina-betaína, prolina, trehalosa y ectoína. Sin embargo, Etesami y Glick (2020a) mencionan que estos compuestos no interfieren con las funciones celulares y ayudan a equilibrar el potencial osmótico dentro de la célula sin afectar las proteínas y otros componentes celulares.
Para la cepa VC-03 (Figura 1B), el patrón es similar, con un crecimiento robusto en el control y una disminución en el crecimiento a medida que aumenta la concentración de NaCl. La diferencia en el crecimiento entre las condiciones de 0.5 M y 1.0 M es más marcada en esta cepa con un valor de 0.12 en la concentración más alta a las 20 horas de evaluación. Estos resultados concuerdan con los descritos por Stautz et al. (2021) quienes mencionan que las bacterias ajustan el transporte de iones a través de sus membranas para mantener el equilibrio iónico. Por otra parte, Dahuja et al. (2021) establece que las bacterias también utilizan bombas iónicas y canales específicos para expulsar iones de sodio (Na+) y acumular iones de potasio (K+), que son menos dañinos para las células.
La cepa CA-01 (Figura 1C) evidenció una reducción gradual en presencia de NaCl 0.5 M y una mayor reducción a 1.0 M NaCl con un promedio de 0.41, indicando sensibilidad a la salinidad. En el caso de la cepa CM-04 (Figura 1D), el crecimiento bajo condiciones salinas a 0.5 M NaCl, es moderadamente afectado con un promedio de 0.35, mientras que a 1.0 M NaCl, se observa una inhibición considerable del crecimiento con 0.16. Esto concuerda con Klähn et al. (2021) quien estableció que, en respuesta al estrés salino, las bacterias inducen la expresión de proteínas específicas conocidas como proteínas de choque salino (Salt Stress Proteins, SSPs). Sin embargo, Leandro et al. (2021) menciona que estas proteínas ayudan a estabilizar otras proteínas y estructuras celulares, protegiéndolas del daño causado por altas concentraciones de sal.
Para la cepa BL15 (Figura 1E), el patrón de crecimiento sigue la misma tendencia, con el control mostrando la mayor densidad óptica, y una reducción del crecimiento en las condiciones de 0.5 M con 0.69 y 1.0 M NaCl, con una mayor inhibición a un valor de 0.38. Finalmente, la cepa BL51 (Figura 1F) exhibe un comportamiento similar, donde el crecimiento en la condición de control es el más alto, seguido por una disminución a en la presencia de NaCl a una concentración de 0.5 M con un promedio de 0.33, siendo más pronunciada en la condición de 1.0 M NaCl con un valor de 0.12. en relación a los resultados de Shilev (2020), se menciona que las bacterias modifican la composición de sus membranas celulares para mejorar su resistencia a la salinidad. Sin embargo, Morcillo y Manzanera (2021), establecen que esto incluye cambios en la proporción de ácidos grasos saturados e insaturados, lo que afecta la fluidez de la membrana y su capacidad para funcionar en ambientes salinos.
Todas las cepas bacterianas estudiadas muestran un crecimiento reducido en condiciones de estrés salino, con una inhibición más significativa a una concentración de 1.0 M de NaCl. Indicando que la salinidad afecta negativamente el crecimiento bacteriano sin embargo ciertas cepas toleran las concentraciones de 0.5 M. estos resultados concuerdan con lo descrito por Lipsman, Shlakhter, Rocha y Segev (2024) quienes hacen referencia a que muchas bacterias producen exopolisacáridos (EPS) que forman una matriz extracelular protectora. Por otra parte, Karygianni, Ren, Koo y Thurnheer (2020) mencionan que los EPS pueden ayudar a retener agua y reducir la concentración de sal alrededor de las células bacterianas, creando un microambiente más favorable.
Producción de AIA en Aislados Bacterianos
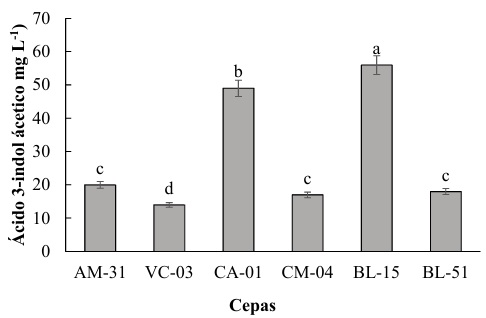
Las cepas en estudio presentaron variaciones significativas en la producción de IAA, destacándose la cepa BL-15 con la mayor producción, alcanzando un promedio de 60 mg L-1 lo que es significativamente más alto que todas las otras cepas, por otra parte, la cepa CA-01 alcanzo una producción de alrededor de 50 mg L-1. En concordancia con el estudio de Oleńska et al. (2020) se establece que al producir AIA, las rizobacterias pueden promover un ambiente más favorable para el establecimiento de una relación simbiótica con la planta huésped. Por lo tanto, Saeed et al. (2021) determina que las plantas, a su vez, pueden proporcionar a las bacterias nutrientes y un ambiente protegido en la rizosfera. Santoyo et al. (2021b) establece que esta relación mutuamente beneficiosa mejora la supervivencia y proliferación de las rizobacterias.
Las cepas AM-31, CM-04 y BL-51 muestran una producción intermedia de IAA, todas rondando los 20-25 mg L-1. En contraste, la cepa VC-03 presenta la menor producción de IAA, con aproximadamente 15 mg L-1. La cepa BL-15 se destaca por su alta capacidad de producción de ácido 3-indol acético, seguida por CA-01. Las cepas AM-31, CM-04 y BL-51 tienen producciones intermedias y comparables, mientras que VC-03 produce la menor cantidad de IAA entre las cepas evaluadas. Este efecto se podría estar relacionado con los descrito por Cavalcante da Silva et al. (2020) quien menciona que el triptófano es un aminoácido que se encuentra en el medio ambiente y puede ser utilizado por las bacterias como sustrato para la síntesis de AIA. Sin embargo, Leontovyčová et al. (2020) determinó que la enzima triptófano aminotransferasa (TAA) cataliza la conversión del triptófano en indol-3-piruvato (IPyA). Por otra parte, Zhang et al. (2022) demuestra que esta reacción implica la transferencia de un grupo amino del triptófano a un aceptador de grupos ceto, que en este caso es el alfa-cetoglutarato, generando IPyA y glutamato (Figura 2).
Inducción del Desarrollo en Plántulas de Arroz
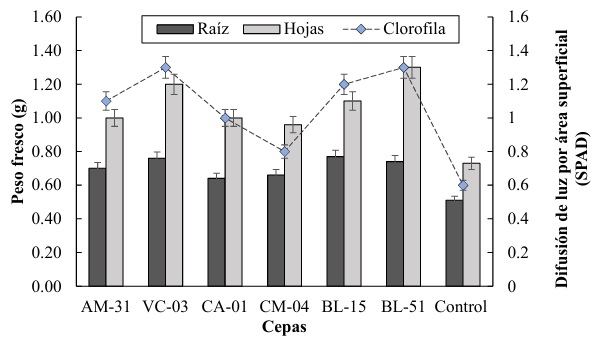
Para la variable de peso fresco de las raíces, se observa que las cepas CM-04 y BL-15 presentan los promedios más altos, con 0.8 g, mientras que la cepa BL-51 obtuvo un valor inferior con un promedio de 0.6 g. mientras que el control muestra un peso fresco de raíz cercano a 0.7 g. estos resultados se relacionan con los descrito por Khatoon et al. (2020) quien establece que las rizobacterias tienen la capacidad de producir ácido indolacético (AIA), una fitohormona que promueve el crecimiento de las raíces. Por otra parte, Li, Hu, Jian, Xie y Yang (2022) determina que el AIA puede estimular la elongación de las células radiculares y aumentar la densidad de los pelos radicales, lo que resulta en un sistema radicular más extenso y voluminoso.
En cuanto al peso fresco de las hojas, la cepa CM-04 destaca con el valor más alto de aproximadamente 1.3 g, seguida de las cepas VC-03 y BL-15 con valores cercanos a 1.2 g. La cepa AM-31 presenta el menor peso fresco de hojas con aproximadamente 1.0 g. El control tiene un valor intermedio de alrededor de 1.1 g. esto coinciden con lo reportado por Khoshru et al. (2020) quien señala que algunas rizobacterias tienen la capacidad de solubilizar nutrientes en el suelo, como el fósforo y el potasio, convirtiéndolos en formas más disponibles para las plantas. Ashfaq, Hassan, Ghazali, y Ahmad (2020) demostraron que estas bacterias solubilizadoras mejoran el suministro de nutrientes esenciales logrando aumentar la tasa fotosintética y la producción de biomasa foliar.
La difusión de luz por área superficial (SPAD) muestra su valor más alto en la cepa CM-04, con un valor de 1.5 SPAD, y su valor más bajo en la cepa CA-01 con de 0.9 SPAD. Mientras tanto el tratamiento control presenta un valor de difusión de luz de aproximadamente 1.2 SPAD. La cepa CM-04 sobresale tanto en peso fresco de hojas como en la difusión de luz (SPAD), sugiriendo una posible mayor eficiencia fotosintética y crecimiento vegetal. Las cepas BL-51 y CA-01 muestran los valores más bajos en varias mediciones, indicando un rendimiento relativamente menor comparado con las otras cepas y el control (Figura 3).
Tolerancia a la Salinidad en Plántulas de Arroz Inoculadas con Bacterias
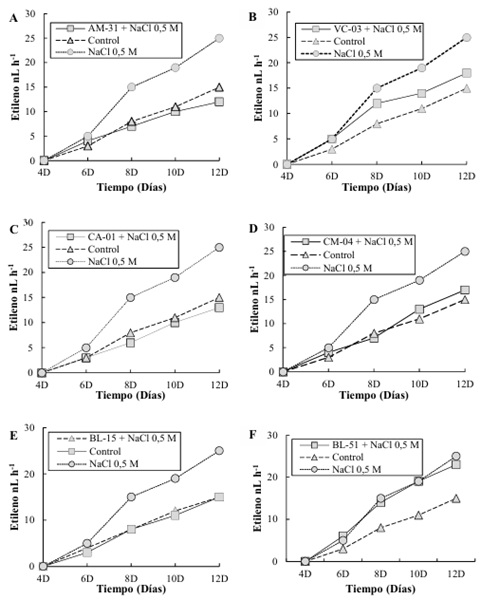
Para la cepa AM-31 (Figura 4A), se observó que la producción de etileno en presencia de NaCl 0.5 M disminuyó hasta alcanza aproximadamente 12 ηL L-1 a los 120 días, superando significativamente al control, que produce alrededor de 15 ηL L-1. La condición de NaCl 0.5 M sin bacterias presenta la producción más baja de etileno, con 25 ηL L-1. esto concuerda con lo descrito por Kumar et al. (2023) quien demuestra que las rizobacterias pueden producir y liberar solutos compatibles (osmoprotectores) como glicina-betaína, prolina y trehalosa. También Ayuso-Calles, Flores y Rivas (2021) señalan que estos compuestos ayudan a las plantas a mantener el equilibrio osmótico y a proteger las estructuras celulares bajo condiciones de alta salinidad.
En la cepa VC-03 (Figura 4B), la producción de etileno bajo NaCl 0.5 M alcanza cerca de 18 ηL L-1 a los 120 días, mientras que el control produce alrededor de 15 ηL L-1. La condición de NaCl 0.5 M sin bacterias muestra un incremento gradual alcanzando aproximadamente 25 ηL L-1. en contraste con la investigación ejecutada por Dar et al. (2021) estas rizobacterias producen exopolisacáridos que mejoran la agregación del suelo y su capacidad de retener agua sin embargo Mandal, Chatterjee y Majumdar (2022) mencionan que esto puede reducir el estrés hídrico en plantas cultivadas en suelos salinos.
Para la cepa CA-01 (Figura 4C), la producción de etileno en presencia de NaCl 0.5 M es menor, llegando a cerca de 13 ηL L-1, en comparación con el control que produce alrededor de 15 ηL L-1. La condición de NaCl 0.5 M sin bacterias sigue un patrón similar a las otras cepas con una producción inferior, alcanzando cerca de 25 ηL L-1. La cepa CM-04 (Figura 4D) muestra una producción de etileno de aproximadamente 17 ηL L-1 bajo NaCl 0.5 M a los 120 días, que es ligeramente mayor que la producción del control (alrededor de 15 ηL L-1). La condición de NaCl 0.5 M sin bacterias produce alrededor de 25 ηL L-1. esto podría estar relacionado con lo descrito por Desoky, Saad, El-Saadony, Merwad y Rady (2020) quienes señalan que las rizobacterias pueden aumentar la producción de enzimas antioxidantes en las plantas, como superóxido dismutasa (SOD), catalasa (CAT) y peroxidasa (POD), que ayudan a neutralizar los radicales libres generados por el estrés salino.
En la cepa BL-15 (Figura 4E), la producción de etileno alcanza cerca de 14 ηL L-1 bajo NaCl 0.5 M a los 120 días, mientras que el control muestra una producción de alrededor de 15 ηL L-1. La condición de NaCl 0.5 M sin bacterias muestra un valor más alto con una producción de 25 ηL L-1. comparado con lo expuesto por Gupta et al. (2021) se demuestra que las rizobacterias promotoras del crecimiento vegetal producen la enzima ACC desaminasa. Por lo tanto, Gamalero, Lingua, y Glick (2023) expresan que esta enzima degrada el ácido 1-aminociclopropano-1-carboxílico (ACC), que es el precursor directo del etileno en las plantas. Por otra parte, Etesami, Noori, Ebadi y Reiahi-Samani (2020b) mencionan que, al reducir los niveles de ACC, estas bacterias disminuyen la síntesis de etileno, mitigando los efectos negativos del estrés en el crecimiento de las plantas.
Finalmente, para la cepa BL-51 (Figura 4F), la producción de etileno bajo NaCl 0.5 M es aproximadamente 17 ηL L-1 a los 120 días, en comparación con el control que produce alrededor de 15 ηL L-1. La condición de NaCl 0.5 M sin bacterias muestra una producción similar a otras cepas, con alrededor de 25 ηL L-1. Oleńska et al. (2020) demostró que además de reducir los niveles de etileno, las rizobacterias pueden producir otras fitohormonas como citoquininas y giberelinas, que contrarrestan los efectos negativos del etileno y promueven el crecimiento vegetal.
Conclusiones
La investigación confirmó que los consorcios bacterianos aislados de la rizosfera de Echinopsis pachanoi compuestos por bacterias del género Bacillus y Pseudomonas, tienen un impacto positivo en el crecimiento de las plantas. Las bacterias promotoras del crecimiento mostraron una capacidad significativa para mejorar la disponibilidad de nutrientes y la producción de hormonas vegetales, contribuyendo así a una mayor vigorosidad y productividad.
Los estudios sobre la producción de etileno en condiciones de estrés salino demostraron que ciertos consorcios bacterianos pueden mejorar la tolerancia de plantas de arroz al estrés abiótico. Las plantas inoculadas con bacterias mostraron niveles de producción de etileno similares a los controles sin salinización, lo que sugiere un mecanismo de adaptación mejorado frente a condiciones adversas.
Declaración de Ética
Este estudio se llevó a cabo siguiendo estrictamente los principios éticos y normas de seguridad aplicables en la investigación científica. Todas las prácticas de manejo y tratamiento de las semillas y plántulas se realizaron conforme a las guías establecidas para minimizar cualquier posible impacto negativo en el medio ambiente. Las inoculaciones bacterianas y la aplicación de soluciones salinas se efectuaron bajo condiciones controladas, asegurando que no se produjera contaminación fuera del ámbito experimental. Además, se garantizó el uso de equipos y procedimientos adecuados para la recolección y análisis de gases, respetando las normativas de bioseguridad y salud ocupacional del laboratorio.











 text new page (beta)
text new page (beta)