Introducción
En México, el cultivo de chile (Capsicum annuum) representa una de las principales actividades hortícolas, con un valor económico estimado en más de 17 mil millones de pesos y un rendimiento promedio de 19 t ha-1. México es el segundo lugar en producción a nivel mundial, solo por detrás de China (SIAP, 2019). Además, México es reconocido como centro de origen y domesticación de esta especie vegetal, cultivándose prácticamente en todo el territorio nacional y abarcando la mayoría de las variedades conocidas (Chew- Madinaveitia et al., 2008).
Diversas enfermedades bacterianas afectan al cultivo de chile, siendo la mancha bacteriana una de las más importantes (Vauterin et al., 2000; Jones et al., 2004; Voloudakis et al., 2005; Sadunishvili et al., 2015). Esta enfermedad es causada principalmente por Xanthomonas euvesicatoria (Xe; Jones et al., 2004). Los métodos de control más empleados incluyen el uso de compuestos a base de cobre y antibióticos agrícolas (Balogh et al., 2003; Iriarte et al., 2012). Sin embargo, el uso prolongado y repetido de estas estrategias ha favorecido la aparición de cepas resistentes (Voloudakis et al., 2005; Carrillo-Fasio et al., 2001; Balogh et al., 2003; Shenge et al., 2014).
El uso de microorganismos benéficos para manejar enfermedades en cultivos es una táctica segura y respetuosa con los agroecosistemas, que ha despertado el interés en el ámbito de la protección de cultivos (Ayaz et al., 2023). Para el control de bacterias fitopatógenas, el uso de virus bacterianos, denominados bacteriófagos o “fagos”, ha demostrado ser una alternativa viable a los tratamientos convencionales (Ravensdale et al., 2007; Balogh et al., 2008; Chae et al., 2014; Rombouts et al., 2016). La fagoterapia vegetal tiene muchos beneficios, entre los que destacan, su alta especificidad con la bacteria huésped, no son tóxicos para células eucariotas, son capaces de infectar bacterias resistentes a antibióticos y pueden utilizarse en cultivos libres de pesticidas (Halawa, 2023). Sin embargo, su aplicación en invernadero y en campo puede llegar a enfrentar algunos desafíos.
Al ser aplicados sobre el follaje de la planta, se enfrentan a condiciones climáticas adversas que pueden comprometer su integridad (Jones et al., 2007). La radiación UV proveniente de la luz solar representa la principal amenaza, aunado a otros factores como la desecación, las fluctuaciones de temperatura, el pH e incluso el lavado causado por las lluvias, pueden reducir rápidamente la persistencia del fago en la superficie foliar (Balogh et al., 2003; Iriarte et al., 2007). Se han propuesto diversos compuestos y formulaciones como alternativa para proteger a los fagos de la radiación ultravioleta (Balogh et al., 2003; Iriarte et al., 2007; Born et al., 2015; Khalil et al., 2016; Wdowiak et al., 2023). Entre ellas, destacan algunos pigmentos vegetales y la combinación de leche descremada en polvo y sacarosa (Born et al. 2015; Balogh et al., 2003).
No obstante, la mayoría de estos estudios se han limitado a condiciones de laboratorio, y son escasas las evaluaciones realizadas en invernadero o campo, a pesar de que estos escenarios son fundamentales para validar la efectividad de las formulaciones bajo condiciones reales (Dy et al., 2018). Por ello, el objetivo del presente trabajo fue determinar la efectividad biológica del bacteriófago lítico ΦXaF18 en una formulación denominada Fagolytic, sobre la mancha bacteriana provocada por Xe en el cultivo de chile bajo condiciones de parcelas comerciales en campo.
Materiales y Métodos
Ensayo en condiciones de cielo abierto con control parcial del ambiente Material vegetal e inoculación Xe. Se utilizaron semillas de chile poblano, variedad Ancho "San Luis", las cuales se sembraron en charolas plásticas utilizando un sustrato estéril compuesto por 37.5 % de arena, 37.5 % de suelo, 12.5 % de turba, 3.5 % de humus y 9 % de agrolita. El trasplante se realizó en vasos de unicel (1 L) (~600 g de sustrato por vaso) después de presentar dos hojas verdaderas y se mantuvieron en condiciones de invernadero. Se realizaron dos fertilizaciones iguales con una dosis total de 70-70-70 (20 y 40 días después de la siembra) con Triple-16 y el riego se administró cada dos días. Después de 35 días de la siembra, las plantas se aclimataron al aire libre en los vasos, donde se realizó el experimento a cielo abierto.
Se inoculó la cepa BV801 de Xe, proveniente de la colección del Laboratorio de Fitopatología de CIATEJ. El inóculo bacteriano se preparó a partir de un cultivo nocturno en medio líquido NYG (0.3 % de extracto de levadura, 0.5 % de peptona, 2.0 % de glicerol), se centrifugó a 10000 rpm durante 15 min y se decantó el sobrenadante, la pastilla se resuspendió en agua destilada estéril. Este proceso se repitió dos veces más. Luego, se ajustó el inóculo a una concentración de 1×108 UFC (unidades formadoras de colonia) mL- 1 (OD600=1.0). La aplicación del inóculo bacteriano en el follaje (1 mL por hoja) se realizó con un aspersor manual, cubriendo completamente ambas caras de todas las hojas de las plantas. Posteriormente, las plantas se mantuvieron en cajas plásticas durante 18 h para asegurar una alta humedad relativa.
Preparación y aplicación de tratamientos. Se utilizó el bacteriófago lítico ΦXaF18 (Ríos-Sandoval et al., 2020). El bacteriófago fue ajustado a una concentración de 1×108 UFP (unidades formadoras de placa) mL-1. La formulación Fagolytic se elaboró conforme a la patente MX412087 (Ibarra-Rivera et al., 2024). La formulación denominada LS consistió en 7.5 % de leche descremada en polvo y 5 % de sacarosa (Balogh et al., 2003). El antibiótico Kasumin® (RSCO-FUNG-0301K-301-052-002; Arysta LifeScience) se aplicó a la dosis recomendada de 2.0 L ha-1. Como control o sin tratamiento se aplicó el medio de cultivo NYG después de que en él creció Xe y se filtró con una membrana de 0.22 µm, esto con el fin de simular el medio en el que se encontró el fago ΦXaF18. La preparación de los distintos tratamientos, a excepción del antibiótico, se realizó 24 h antes de su aplicación preventiva, y se conservaron a 4 °C para su uso posterior. El antibiótico se preparó justo antes de la aplicación. Se aseguro una cobertura total del follaje por ambas caras, inoculando 1 mL por hoja.
Diseño experimental. El experimento se llevó a cabo en invernadero y a cielo abierto en las instalaciones de la unidad Zapopan del CIATEJ (20.701569, -103.474393). Se empleó un diseño completamente al azar con estructura factorial 5 × 3 × 2 (30 tratamientos con seis repeticiones), correspondiente a tres factores: (A) manejo de la enfermedad; con cinco niveles (Fagolytic, formulación LS, fago ΦXaF18 sin formular, antibiótico Kasumin®, sin tratamiento= control); (B) momento de aplicación, con tres niveles (preventiva, simultánea en la cual se aplicó al mismo tiempo Xe y el tratamiento -“curativa”- y combinada: preventiva y simultanea); (C) presencia del inoculo bacteriano de Xe, con dos niveles (con y sin inóculo de Xe). La unidad experimental fue un vaso de unicel con un planta de chile. Las variables de respuesta evaluadas fueron: número de manchas cloróticas por planta, número de hojas con síntomas y número de hojas defoliadas. El ensayo fue establecido en condiciones de cielo abierto, donde se aplicaron tanto el inóculo como los tratamientos. Dado que durante las dos primeras semanas posteriores a la aplicación de los tratamientos no se presentaron condiciones climáticas propicias para el desarrollo de la enfermedad, las plantas fueron trasladadas a un invernadero, donde se completó la evaluación hasta los 30 días posteriores a la inoculación de la bacteria Xe.
Análisis estadístico. Los datos obtenidos se sometieron a un análisis de varianza, ANOVA, (p ≤ 0.05) y prueba de comparación de medias de Tukey (p ≤ 0.05) cuando se cumplió la normalidad y homocedasticidad de datos; en caso de no cumplirse esos requisitos, se realizó una prueba no paramétrica de Kruskal-Wallis (p≤0.05). Los análisis se realizaron utilizando el programa de análisis estadístico Statgraphics Centurion XV (http://www.statgraphics.com/).
Ensayos en condiciones de campo Parcela experimental 1 de un campo comercial de chile en Mascota Jalisco. En noviembre de 2018 se llevaron a cabo dos experimentos independientes en una parcela de cultivo de chile Güero tipo Caribe (Var. Becán, Seminis®) ubicada en el municipio de Mascota, Jalisco (20.544465, -104.806627), proporcionado por un agricultor local. Se seleccionaron dos sitios (A y B) dentro de la parcela con diferentes niveles de severidad de la mancha bacteriana (sintomatología visible). Durante el trascurso de los experimentos, el cultivo se encontró en la etapa fenológica de fructificación. En cada sitio se empleó un diseño experimental de bloques completamente al azar con cuatro tratamientos: (1) Fagolytic, (2) el fago ΦXaF18 sin formular, (3) antibiótico (Kasumin®) y (4) control sin tratamiento (aplicación de solo agua), con cinco repeticiones por tratamiento. La unidad experimental (UE) fue una parcela con 20 plantas ubicadas en un surco de 1 m de longitud por 0.8 m de ancho (10 plantas de cada lado del surco); la parcela útil donde se midieron las variables de respuesta se constituyó de las dos plantas centrales en la UE. Los tratamientos con fagos se aplicaron a una concentración de 1×10⁸ UFP mL⁻¹, y el antibiótico a la dosis recomendada de 2.0 L ha⁻¹. Las aplicaciones se realizaron con una aspersora manual tipo mochila (15 L), equipada con boquilla de cono hueco, aplicando un volumen aproximado de 35 mL por planta para cada tratamiento.
Variables de respuesta evaluadas. La recolección de datos se llevó a cabo antes y después de la aplicación de los tratamientos (22 días después de la aplicación). Se utilizó una escala ordinal de severidad para evaluar la severidad de la mancha bacteriana en las plantas, registrando la sintomatología de la enfermedad en una escala de 0 a 5 (Cuadro 1). Se contó el total de hojas por planta y el número de hojas con síntomas. Para la cuantificación de la concentración del fago ΦXaF18 en el follaje, se seleccionaron aleatoriamente 10 hojas por tratamiento a las 48 h posteriores a la aplicación de los tratamientos. Los datos cuantitativos fueron analizados mediante un análisis de varianza y la prueba de Tukey. Para los datos cualitativos se aplicó la prueba no paramétrica de Kruskal-Wallis; todos los análisis se realizaron a un nivel de significancia del 5 % (p ≤ 0.05). El procesamiento de los análisis estadísticos se hizo con el programa Statgraphics Centurión XV (http://www.statgraphics.com/).
Cuadro 1 Descripción de la escala ordinal de severidad utilizada para evaluar la mancha bacteriana (X. euvesicatoria) en plantas de chile a nivel de parcelas comerciales en campo ubicadas en Mascota, Jalisco.
| Valor cualitativo | Descripción de la severidad de la mancha bacteriana |
|---|---|
| 0 | Planta sana: ausencia de síntomas. |
| 1 | Planta con síntomas ligeros: hasta 10 hojas con lesiones. |
| 2 | Planta con síntomas evidentes: presencia de hasta 20 hojas con lesiones. |
| 3 | Planta con síntomas avanzados: inicio de defoliación y mayoría de hojas con lesiones coalescentes. |
| 4 | Planta con síntomas severos: defoliación del 50 % y lesiones en todas las hojas. |
| 5 | Planta con síntomas terminales: 75 % de afectación por defoliación avanzada. |
Determinación de la concentración del bacteriófago ΦXaF18 en follaje. Las 10 hojas recolectadas en la parcela experimental se guardaron en bolsas plásticas y se mantuvieron refrigeradas a 8 °C hasta su procesamiento en el laboratorio. Luego, se añadieron 100 mL de agua destilada estéril a cada bolsa y se agitaron constantemente a 200 rpm durante 20 min. Después, se transfirió 1 mL de la muestra a tubos de 1.5 mL y se añadieron 400 μL de cloroformo. Se agitó 20 min (200 rpm) y se centrifugaron a 13000 rpm durante 10 min. Por último, se descartó el cloroformo por evaporación y se procedió a determinar la presencia de los bacteriófagos ΦXaF18 mediante la técnica de doble placa en agar suave (Kropinski et al., 2009).
Parcela experimental 2 de un campo comercial de chile en Mascota, Jalisco. Se realizó en noviembre de 2018 en un segundo campo de cultivo de chile Güero tipo Caribe (Var. Becán, Seminis®) ubicado en Mascota, Jalisco (20.576549, -104.867441). Se utilizaron los mismos tratamientos, concentraciones, método de aplicación y número de repeticiones por tratamiento descritos en la parcela experimental 1. La unidad experimental (UE) fue similar a la diseñada para la parcela experimental 1. En este ensayo, la única variable de respuesta evaluada fue la severidad de la enfermedad empleando la escala presentada en el Cuadro 1, por lo cual el análisis estadístico de los datos de esta parcela experimental fue con la prueba no paramétricas de Kruskal-Wallis (p≤0.05).
Resultados
Evaluación de la efectividad de bacteriófagos ΦXaF18 en el control de la mancha bacteriana en chile. Durante el ensayo realizado en las instalaciones de la unidad Zapopan del CIATEJ, la severidad de la enfermedad fue baja, lo que limitó la aparición de síntomas avanzados como lesiones necróticas coalescentes o defoliación. En cuanto al número de hojas con síntomas, se observaron diferencias numéricas entre los tratamientos, siendo Fagolytic el que mostró el menor número promedio de hojas afectadas. Sin embargo, se encontraron diferencias estadísticamente significativas (p ≤ 0.05) al comparar Fagolytic con el tratamiento con el bacteriófago ΦXaF18 sin formular para el número de hojas sintomáticas y manchas cloróticas (Cuadro 2). De manera similar, los tratamientos con Fagolytic y con la formulación LS mostraron un menor grado de severidad, evidenciado por un menor promedio de manchas cloróticas, con diferencias significativas (p ≤ 0.05) en comparación con el tratamiento con el fago ΦXaF18 sin formular y para el control sin tratamiento. Por su parte, el antibiótico Kasumin® no mostró diferencias significativas con el tratamiento control en ambas variables (número de manchas cloróticas o de hojas con síntomas).
Cuadro 2 Efecto de tratamientos biológicos para el manejo de la mancha bacteriana en plantas de chile en condiciones de cielo abierto / invernadero.
| Tratamiento | Síntomas de la mancha bacteriana en plantas de chile | |
|---|---|---|
| Número de hojas con síntomas | Número de manchas cloróticas | |
| Fagolytic | 1.75 a | 4.52 a |
| Formulación LS | 2.36 ab | 5.80 a |
| Antibiótico Kasumin® | 2.41 ab | 8.55 ab |
| Bacteriófago ΦXAF18 sin formular | 2.97 b | 10.55 b |
| Sin tratamiento | 2.58 ab | 11.13 b |
Letras distintas indican diferencias significativas de acuerdo con la prueba de Tukey (p ≤ 0.05).
Finalmente, no se observaron diferencias significativas entre los distintos momentos de aplicación (preventiva, simultánea o combinada), lo cual indica que este factor no influyó de manera significativa en la aparición de síntomas (Cuadro 3). No obstante, como se muestra en la Figura 1, se puede detectar diferencias significativas (p ≤ 0.05) entre los tratamientos evaluados para la variable de las manchas cloróticas. En este sentido, la formulación Fagolytic evidenció una efectividad biológica consistente, independientemente del momento de aplicación, mostrando niveles de severidad estadísticamente similares (p ≤ 0.05) al tratamiento control sin inóculo de la bacteria (Xe). En contraste, el tratamiento con Kasumin® presentó diferencias significativas frente al control, indicando una menor eficacia relativa en el control de la enfermedad. De manera general se puede observar que los tratamientos con fagoterapia vegetal mostraron una tendencia favorable a reducir la incidencia de manchas cloróticas.
Cuadro 3 Efecto del momento de aplicación de los tratamientos para el manejo de la mancha bacteriana en plantas de chile en condiciones de cielo abierto.
| Tratamiento | Síntomas de la mancha bacteriana en plantas de chile | |
|---|---|---|
| Número de hojas con síntomas | Número de manchas cloróticas | |
| Aplicación preventiva | 2.28 a | 7.43 a |
| Aplicación simultánea | 2.30 a | 7.16 a |
| Aplicación preventiva y simultánea | 2.66 a | 9.85 a |
Letras distintas indican diferencias significativas de acuerdo con la prueba de Tukey (p ≤ 0.05).
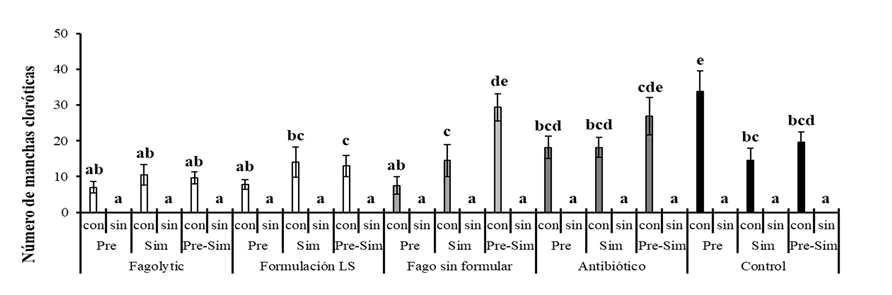
Figura 1 Efecto de los distintos tratamientos en el manejo de la mancha bacteriana en plantas de chile en condiciones de invernadero y cielo abierto. Letras distintas indican diferencias significativas de acuerdo con la prueba de Tukey (p ≤ 0.05). Las barras en cada rectángulo indican ± el error estándar. Con inoculo de Xe (con), sin inoculo de Xe (sin). Pre: Preventiva. Sim: Simultánea. Pre-Sim: Preventiva y Simultánea.
Evaluación de la efectividad de bacteriófagos para el control de la mancha bacteriana en la parcela experimental 1 de Mascota, Jalisco. En la escala ordinal de severidad correspondiente a la recolección de los datos iniciales, se evidenciaron diferentes niveles de severidad entre los dos experimentos (Cuadro 4). En el sitio A, la presión inicial de la enfermedad fue más alta en comparación con el sitio B, lo que se reflejó en síntomas más avanzados, como lesiones necróticas coalescentes y un mayor grado de defoliación en todos los tratamientos. Este nivel de severidad al inicio del ensayo pudo haber influido en la ausencia de diferencias significativas en la evaluación final del índice de severidad (Cuadro 4). No obstante, se observó una tendencia numérica a menor número de hojas con síntomas en el tratamiento Fagolytic comparado con el control sin tratamiento (Cuadro 5). En el sitio B, el tratamiento con antibiótico mostró una efectividad comparable a la de Fagolytic, el cual redujo significativamente el índice de severidad respecto al control (p ≤ 0.05; Cuadro 4), efecto que se ilustra con claridad en la Figura 2. Asimismo, el número de hojas con síntomas fue menor en el tratamiento Fagolytic en comparación con el control, aunque sin alcanzar significancia estadística (Cuadro 5).
Cuadro 4 Evaluación de la severidad de mancha bacteriana en plantas de chile a los 0 y 22 días después de la aplicación de tratamientos para control de la enfermedad en la parcela comercial experimental 1 ubicada en Mascota, Jalisco.
| Tratamiento | Inicio del experimento (0 días) | 22 días | |
|---|---|---|---|
| Sitio A | |||
| Fagolytic | 1.5 a | 2.5 a | |
| Antibiótico Kasumin® | 1.5 a | 2.0 a | |
| Bacteriófago ΦXAF18 sin formular | 1.0 a | 2.0 a | |
| Sin tratamiento | 1.0 a | 2.0 a | |
| Sitio B | |||
| Fagolytic | 1.0 a | 2.0 a | |
| Antibiótico Kasumin® | 1.0 a | 2.0 a | |
| Bacteriófago ΦXAF18 sin formular | 1.0 a | 3.0 ab | |
| Sin tratamiento | 1.0 a | 3.0 b | |
Letras distintas indican diferencias significativas de acuerdo con la prueba de Kruskal-Wallis (p ≤ 0.05) e intervalos de confianza (95 %) de la mediana.
Cuadro 5 Efecto de los tratamientos para el manejo biológico de la mancha bacteriana en plantas de chile en la parcela comercial experimental 1 ubicada en Mascota, Jalisco.
| Valor cualitativo | Descripción de la severidad de la mancha bacteriana |
|---|---|
| 0 | Planta sana: ausencia de síntomas. |
| 1 | Planta con síntomas ligeros: hasta 10 hojas con lesiones. |
| 2 | Planta con síntomas evidentes: presencia de hasta 20 hojas con lesiones. |
| 3 | Planta con síntomas avanzados: inicio de defoliación y mayoría de hojas con lesiones coalescentes. |
| 4 | Planta con síntomas severos: defoliación del 50 % y lesiones en todas las hojas. |
| 5 | Planta con síntomas terminales: 75 % de afectación por defoliación avanzada. |
Letras distintas indican diferencias significativas de acuerdo con la prueba Tukey (p ≤ 0.05).
Respecto a la persistencia foliar del bacteriófago ΦXaF18, en el sitio A se observaron diferencias significativas en la concentración residual entre el tratamiento Fagolytic y el fago no formulado (p ≤ 0.05; Cuadro 6). Fagolytic mantuvo concentraciones más elevadas sobre el follaje hasta 48 h después de su aplicación. En contraste, en el sitio B, aunque se registraron diferencias numéricas entre ambos tratamientos, estas no fueron estadísticamente significativas (Cuadro 6).

Figura 2 Comparación visual de la severidad de la mancha bacteriana en plantas de chile tratadas con Fagolytic (A y C) y el control sin tratamiento (B y D) a los 22 dias después del inicio del experimento, en la parcela experimental comercial 1 ubicada en Mascota, Jalisco.
Cuadro 6 Determinación de la concentración viral en el follaje de plantas de chile en los sitios A y B de la parcela experimental comercial 1, localizada en Mascota Jalisco, después de 48 h de la aplicación del tratamiento con los bacteriófagos ΦXaF18.
| Tratamiento | Concentración del bacteriófago ΦXaF18 (106 UFP / g de tejido foliar) | |
|---|---|---|
| Sitio A | Sitio B | |
| Fagolytic | 0.84 a | 0.62 a |
| Bacteriófago ΦXAF18 sin formular | 0.23 b | 0.32 a |
Letras distintas indican diferencias significativas de acuerdo con la prueba de Tukey (p ≤ 0.05).
Evaluación de la efectividad de bacteriófagos para el control de la mancha bacteriana en la parcela experimental 2 de Mascota, Jalisco. Las plantas en esta parcela presentaron índices bajos de severidad al inicio del experimento en todos los tratamientos. Durante el periodo de evaluación, el desarrollo de la enfermedad se mantuvo con niveles reducidos de severidad y mínima defoliación. Como resultado, no se observaron diferencias significativas entre los tratamientos (Cuadro 7). En contraste, el tratamiento con antibiótico mostró los valores más altos de severidad, presentando diferencias significativas (p ≤ 0.05) en comparación con los tratamientos con la aplicación de los bacteriófagos. El tratamiento con Fagolytic no difirió significativamente del fago ΦXaF18 sin formular, aunque ambos mostraron una disminución en la severidad final con respecto al inicio del ensayo.
Cuadro 7 Evaluación de la severidad de mancha bacteriana en plantas de chile a los 0 y 22 días después de la aplicación de los tratamientos en la parcela experimental comercial 2 localizada en Mascota, Jalisco.
| Tratamiento | Índice de severidad de la enfermedad de la mancha bacteriana en plantas de chile | |
|---|---|---|
| Inicio del experimento (0 días) | 22 días | |
| Fagolytic | 1.5 a | 1.0 a |
| Antibiótico Kasumin® | 1.0 a | 2.0 b |
| Bacteriófago ΦXAF18 sin formular | 1.0 a | 1.0 a |
| Sin tratamiento | 1.0 a | 1.0 ab |
Letras distintas indican diferencias significativas de acuerdo con la prueba de Tukey (p ≤ 0.05).
Discusión
Diversos bioensayos han evidenciado que la aplicación de bacteriófagos en la agricultura puede ser efectiva para el control de enfermedades bacterianas, con el objetivo de reducir progresivamente el uso de antibióticos y posicionarse como una alternativa ecológica. No obstante, una de las principales limitantes para su implementación en campo es la rápida inactivación de las partículas virales en el follaje, principalmente por la exposición a la radiación solar UV, lo que compromete su efectividad.
En este estudio, la formulación Fagolytic incrementó significativamente la eficacia del control biológico de la mancha bacteriana en plantas de chile bajo condiciones de cielo abierto. En comparación con el bacteriófago ΦXaF18 sin formular, Fagolytic redujo la severidad de la enfermedad en un 32 % y el número de manchas cloróticas en un 57 %. Además, Fagolytic mostró una mayor persistencia sobre el follaje hasta 48 h después de la aplicación en condiciones de campo. Este resultado es relevante, ya que diversos estudios han reportado que los bacteriófagos aplicados sin protección pierden su actividad lítica en pocas horas debido a la radiación UV, reduciendo su eficacia a menos de 24 h (Jones et al., 2007; Svircev et al., 2010; Iriarte et al., 2007; Balogh et al., 2003). Esta persistencia representa un beneficio importante para el control sostenido de la enfermedad y puede mejorar la ventana de protección frente a nuevos eventos de infección.
En relación con el momento de aplicación de los tratamientos, no se observaron diferencias significativas entre la aplicación preventiva (24 h antes de la inoculación), la aplicación simultánea o la combinación de ambas. Esto sugiere que la estrategia preventiva, por sí sola, puede ser suficiente para lograr un control efectivo de la enfermedad bajo las condiciones evaluadas. Investigaciones previas han señalado que la aplicación preventiva puede favorecer la cobertura inicial del follaje por los bacteriófagos, permitiendo su establecimiento antes de la llegada del fitopatógeno (Iriarte et al., 2012; Álvarez et al., 2019).
En condiciones de campo comercial, Fagolytic mostró una eficacia comparable al antibiótico Kasumin® en la reducción de síntomas, particularmente en el sitio B de la parcela experimental comercial 1, ubicada en Mascota, Jalisco. Estos resultados coinciden con un estudio previo sobre el control de la mancha bacteriana en tomate (Xe), donde las aplicaciones foliares de fagos formulados lograron niveles de eficacia comparables a los obtenidos con tratamientos convencionales a base de cobre o antibióticos (Obradovic et al., 2004).
En México, la kasugamicina, ingrediente activo del Kasumin® se utiliza ampliamente para el control de la mancha bacteriana en chile y tomate (Vallad et al., 2010). Sin embargo, se ha reportado un rápido desarrollo de resistencia por parte de poblaciones de X. perforans (Vallad et al., 2010). Otro riesgo de gran importancia son los residuos de este antibiótico en frutas, ya que se han asociado con daños a la salud humana. En países como Estados Unidos, se han establecido límites de tolerancia para regular su presencia en algunas frutas (US EPA, 2018).
Por otro lado, el uso de bacteriófagos es seguro para la salud humana y no causa fitotoxicidad (Gasic et al., 2018). En cuanto a la probabilidad de desarrollar resistencia, puede ser evitada con aplicaciones en concentraciones superiores de 108 UFP mL-1 y/o utilizando mezclas o “cocteles” de diferentes bacteriófagos con el mismo espectro de huésped bacterianos (Balogh et al., 2010; Sadunishvili et al., 2015; Wei et al., 2017; Holtappels et al., 2021). Existen además otras tácticas que pueden ser empleadas para evitar la resistencia por parte de la bacteria blanco a un fago específico, como el monitoreo constante (aislamiento) de las cepas bacterianas tratadas con fagos para evaluar cambios sutiles en la susceptibilidad del fago (Balogh et al., 2010; Holtappels et al., 2021).
En la producción de cultivos, el método de aplicación para prácticamente cualquier producto dirigido al follaje se realiza por aspersión y la buena implementación es imprescindible ya que garantiza un amplio espectro de alcance y una adecuada distribución. La formulación Fagolytic permitió una aplicación eficiente mediante aspersión manual con aspersoras tipo mochila, empleadas habitualmente por agricultores de la región de Mascota, Jalisco, sin presentar inconvenientes técnicos.
Conclusiones
El bacteriófago ΦXaF18, formulado como Fagolytic, presentó la menor severidad de mancha bacteriana bajo condiciones de cielo abierto, con promedios de 1.8 hojas con síntomas y 4.5 manchas cloróticas, significativamente inferiores al tratamiento con el fago ΦXaF18 sin formular (3 y 10.6, respectivamente). En campo, Fagolytic redujo significativamente la severidad en el sitio B de la parcela experimental comercial 1 (p ≤ 0.05) y mantuvo mayores concentraciones virales residuales hasta 48 h después de su aplicación. En la parcela experimental 2, los tratamientos con fagos mostraron menor severidad en comparación con el antibiótico, aunque sin diferencias estadísticas en Fagolytti y los otros tratamientos virales. En conjunto, estos resultados confirman el potencial de Fagolytic como alternativa biológica para el manejo de Xathomonas euvesicatoria en plantas de chile.











 text in
text in 


