Introducción
En México, el cultivo del frijol (Phaseolus vulgaris) y de la papa (Solanum tuberosum) cubrieron una superficie de 1,472,462 y 60,102 ha en 2022, respectivamente. La producción de frijol alcanzó 965,371 t con un valor de 16,984 millones de pesos; mientras que de papa se cosecharon 1,878,976 t con un valor de 16,173 millones de pesos (SIAP, 2022). En Sinaloa, en el mismo año se sembraron 58, 925 ha de frijol con un rendimiento de 165,475 t y un valor de la producción de 3,271 millones de pesos. De papa se sembraron 11,975 ha con una producción 403,923 t con un valor de 3, 363 millones de pesos. Las enfermedades fungosas resaltan como factor limitante en ambos cultivos en Sinaloa; por ejemplo, en frijol ocurren pudriciones de raíz (Fusarium spp., Rhizoctonia solani, Pythium spp., Macrophomina phaseolina y Sclerotium rolfsii), el moho blanco (Sclerotinia sclerotiorum), la roya o chahuixtle (Uromyces appendiculatus var. appendiculatus) (RodríguezCota et al., 2022), además de la cenicilla (Erysiphe diffusa) (Félix-Gastélum et al., 2011). En el caso de enfermedades bacterianas sobresalen el tizón común (Xanthomonas axonopodis pv. phaseoli) (Rodríguez-Cota et al., 2022) y el tizón del halo Pseudomaonas syringae pv. phaseolicola (Félix-Gastélum et al., 2016).
Sclerotinia sclerotiorum es un fitopatógeno que ataca a 408 especies pertene-
cientes a 278 géneros y 75 familias; la mayoría de las especies susceptibles se ubican en la subclase Dicotiledonae, del grupo de las angiospermas, aunque también puede atacar varios miembros de la subclase Monocotiledonae (Boland y Hall, 1994; Islam et al., 2021; Jahan et al., 2022) y puede presentarse como endofítico en cereales como arroz (Oryza sativa), trigo (Triticum aestivum), maíz (Zea mays), cebada (Hordeum vulgare) y Avena (Avena sativa) (Tian et al., 2020). Las pérdidas anuales por moho blanco en Estados Unidos de Norteamérica superan los 200 millones de dólares (Bolton et al., 2006). En Sinaloa la enfermedad se ha consignado en berenjena (Cebreros-Sánchez y Sánchez-Castro,1998) y en frijol (RodríguezCota et al., 2022), con pérdidas del 50 %, mientras que en papa pueden alcanzar el 30 %; a pesar de ello, no se han realizado investigación aplicada, orientada al manejo de la enfermedad. En la presente revisión se describen los síntomas del moho blanco en frijol y en papa en el norte de Sinaloa, las características morfológicas del teleomorfo de S. sclerotiorum, su ecología y la epidemiología de la enfermedad, así como las estrategias para su manejo en otras partes del mundo. Se indica además la situación actual del manejo de la enfermedad en Sinaloa y futuras líneas de investigación que se deberán abordar para el control eficiente del moho blanco del frijol y de la papa en esta región.
Síntomas y signos de la enfermedad
Las plantas de frijol y papa infectadas por S. sclerotiorum muestran el típico micelio blanco con aspecto algodonoso, el cual se observa en la superficie del tejido infectado. El micelio produce celulasas y pectinasas e intervienen en el proceso de infección y provocan pudrición de tejidos de la planta (Fernando et al., 2004; Bolton et al., 2006). El micelio también produce ácido oxálico, que tiene efectos tóxicos en el tejido del hospedante (Hegedus y Rimmer, 2005). En campo se observan plantas marchitas, las cuales presentan lesiones acuosas en tallos hojas y vainas; al tejido infectado lo cubre micelio blanquecino; en estados avanzados ocurren aglomeraciones de micelio, las cuales maduran y se transforman en esclerocios negros de diversas formas que varía de 0.5 a 1.7 cm y se encuentran principalmente en la superficie del tejido blanquecino, aunque, también se pueden encontrar en el interior de los tallos (Hooker, 1981).
Características morfológicas del agente causal del moho blanco (S. sclerotiorum) en Sinaloa
El moho blanco del frijol y de la papa ocurre año tras año en Sinaloa y las colonias de S. sclerotiorum aisladas en papa dextrosa agar (PDA) son algodonosas blanquecinas regulares con crecimiento ligeramente elevado y los esclerocios se producen en doble círculo en la caja Petri, en el centro y en el margen de la colonia junto a la pared de la caja Petri (Figura 1A). Aun cuando las colonias del hongo obtenido de papa fueron similares a las de frijol los esclerocios se produjeron de manera dispersa sobre el PDA (Figura 1C). Se han consignado varias especies de Sclerotinia como fitopatógenas, pero en esta región del país, sólo se ha identificado a S. sclerotiorum como agente causal (Mora-Romero et al., 2016). El hongo sobrevive el verano mediante esclerocios de 0.5 a 1.7 cm de longitud, cuando se producen en frijol (Figura 1B) y de 0.3 a 1.0 cm cuando se producen en papa (Figura 1D) los que producen de uno a varios apotecios de color café claro de 0.5 a 0.8 cm de diámetro (Figura 3D). Los apotecios son más frecuentes en lotes de papa, lo que probablemente se debe a los altos niveles de humedad que se generan por los sistemas de riego por aspersión. El himenio de los apotecios presenta ascas de 85.0 a 160.0 µm X 3.0 a 5.5 µm (Figura 3B) y paráfisis hialinas; las ascosporas también son hialinas, unicelulares, ovoides a elípticas de 5 a 7.0 µm (Figura 3C).
Observaciones de campo en Sinaloa indican que en frijol es frecuente el inicio
de la enfermedad en la base del tallo de las plantas (Figura 2 A), por lo que es probable que la infección inicial ocurra mediante la germinación directa de los esclerocios (miceliogénica); de ahí, el síntoma avanza a tallos, foliolos y vainas (Figura 2 B y 2 C) donde se forma micelio algodonoso y blanquecino causando una pudrición suave, donde inicia la formación de esclerocios (Figura 2 D). Esta observación coincide con trabajos previos donde los esclerocios germinan produciendo micelio que causa infección en las plantas (Abawi y Grogan, 1979; Lane et al., 2019).

Figura 1 Crecimiento micelial y esclerocios de Sclerotinia sclerotiorum. A). Crecimiento del hongo obtenida de frijol y esclerocios en doble círculo en caja de Petri con PDA; B). Esclerocios de color café claro producidos en plantas de frijol en campo; C). Crecimiento del hongo obtenido de planta de papa con esclerocios dispersos en caja de Petri con PDA; D). Esclerocios color negro producidos en plantas de papa en campo.
En papa, se han observado esclerocios en el interior de los tallos (Figura 3A) así como apotecios del hongo en la superficie del suelo (Figura 3D) con ascas (Figura 3B) y ocho ascosporas en su interior (Figura 3C); también se han observado inflorescencias infectadas que caen sobre las hojas, y a partir de este punto ocurren los síntomas iniciales de la enfermedad (Figura 3E) la cual avanza e invade el resto de las partes de la planta (Figura 3F). También se han observado tallos sobre el suelo

Figura 2 Síntomas y signos el moho blanco en frijol. A). Síntomas de la enfermedad que inician en la base del tallo de la planta; B). Progreso de síntomas y signos en tallos; C). Síntomas y signos en vainas; D). Tallos blanquecinos invadidos por S. sclerotiorum con aglomeración de micelio y abundantes esclerocios.

Figura 3 Estructuras del teleomorfo de S. sclerotiorum, síntomas y signos del moho blanco. A). Tallo de papa con esclerocios en su interior; B). Fragmento del himenio de un apotecio con ascas, ascosporas y paráfisis; C). Asca con ocho ascosporas en su interior; D). Apotecios producidos por esclerocios en la superficie del suelo; E). Síntoma inicial de moho blanco en hoja de papa a partir de una inflorescencia infectada; F). Pudrición suave de hojas y presencia de micelio sobre tejido infectado; G). Tallo sobre suelo colonizado por el hongo con abundante micelio blanquecino.
con síntomas y signos de la enfermedad (Figura 3G), donde la infección puede originarse a partir de la germinación directa de esclerocios.
Ecología de S. sclerotiorum
S. sclerotiorum es un hongo habitante del suelo y su medio de supervivencia lo constituyen los esclerocios (Sousa-Melo et al., 2019), la capa externa de los esclerocios está integrada por células que contienen melanina (Butler et al. 2009), lo que protege al hongo de la luz ultravioleta, metales tóxicos, enzimas líticas y microorganismos antagónicos (Butler y Day, 1998; Thomma, 2003). En algunos suelos sembrados con frijol se han encontrado promedios de 0.6 a 6.2 esclerocios por kg de suelo (Schwartz y Steadman, 1977). La temperatura del suelo, pH, y la humedad, parecen tener un efecto limitado en la supervivencia de los esclerocios, pero el componente biológico tiene un efecto mayor en la supervivencia de éstos en el suelo (Adams y Ayers,1979). La cantidad de esclerocios en el suelo se puede incrementar en dos formas: a) la producción de esclerocios secundarios y b) la producción de éstos en el hospedante (Adams y Ayers, 1979).
La amplia gama de hospedantes del hongo (Toby et al., 2023), así como los monocultivos susceptibles conduce al incremento de poblaciones de esclerocios en el suelo. Se ha observado que la supervivencia de los esclerocios varía de acuerdo con la profundidad que se encuentran; estudios demostraron que los esclerocios colocados a una profundidad mayor de 10 a 30 cm permanecieron viables por más tiempo que aquellos que permanecieron a 5 cm (Cosic et al., 2012). También se reportó que la viabilidad de los esclerocios de S. sclerotiorum a 0, 5 y10 cm disminuyó con la profundidad (Duncan et al. 2006). Otros trabajos indicaron que los esclerocios de S. sclerotiorum permanecen viables en el suelo por ocho o 10 años años (ColeySimth y Cooke, 1971). Se demostró que 3.2 esclerocios por m2 pueden causar 95 % de incidencia en frijol “kidney” en condiciones de campo (Suzui y Kobayashi (1972). Sin embargo, 0.2 esclerocios por kg de suelo podían causar moho blanco en niveles moderadamente severos en frijol (Schwartz y Steadman, 1977). Por otra parte, las ascosporas constituyen la fuente de inóculo primario pues germinan y colonizan tejido senescente y a partir de éste, el hongo invade diferentes partes de la planta (Hossain et al., 2023).
S. sclerotiorum se disemina de un lote de siembra a otro o de una región a otra en varias maneras: a) en forma de micelio adherido a la superficie de la semilla, b) equipos de labranza (Zubieta-Coronado, 2021), animales o el hombre (Starr et al., 1953). Se ha observado que alrededor del 2 % de los esclerocios ingeridos por borregos, permanecen viables después de pasar por su sistema digestivo, lo que sugiere que este tipo de ganado y otros animales pueden diseminar esclerocios a terrenos libres del patógeno (Brown, 1937). El agua de riego, representa otro medio de diseminación de los esclerocios, donde permanecen viables de 10 a 21 días (Steadman et al., 1975); sin embargo, la diseminación a grandes distancias ocurre a través de semilla infectada por micelio como en girasol (Helianthus annuus) (Young y Morris, 1927), repollo (Brassica oleracea var. capitata), coliflor (Brassica oleracea var. botrytis), col rizada (Brassica oleracea var. sabellica) (Neergaard, 1958.), trébol (Trifolium sp.) (Dillon-Weston et al., 1946), frijol (Starr et al., 1953) y cacahuate (Arachis hypogaea) (Porter y Beute, 1974). El aire como elemento de diseminación de ascosporas también se ha considerado en años recientes (Leyronas, 2019; Reich et al., 2024).
Epidemiología del moho blanco del frijol y de la papa
Las epidemias de moho blanco en frijol y papa inician por ascosporas que se producen en apotecios que se originan a partir de esclerocios (Abawi y Grogan, 1979; Cook et al., 1975; Schwartz y Steadman, 1978; Clarkson, et al., 2003). Aunque en Sinaloa se ha observado daño en tallos de papa sobre el fondo del surco; en plantas de frijol también se presentan daños en la base del tallo, lo que ocurre mediante germinación directa de esclerocios. Así, que la producción de apotecios por los esclerocios en frijol es esencial en el desarrollo de epidemias (Abawi y Grogan, 1979). En cambio, en algunas regiones de Canadá, los esclerocios pueden producir micelio directamente para causar infección debajo del nivel del suelo en girasol, aunque también puede ocurrir infección mediante ascosporas provenientes de apotecios (Hung y Hoes, 1980). Sólo los apotecios que se encuentran en la superficie del suelo a 2.0-3.0 cm de profundidad liberan ascosporas, pues el estípite (pie) de los apotecios no superan los 3.0 cm de longitud y aquellos que se encuentra a profundidades mayores, no afloran sobre la superficie del suelo y no lanzan las ascosporas al aire, pues la intensidad de luz no es suficiente para su formación (Sun y Yang, 2000). El inicio de una epidemia no necesariamente ocurre por ascosporas producidas en un determinado lote, sino que éstas pueden provenir de lotes vecinos, inclusive de algunas arvenses como diente de león (Taraxacum officinale) y trébol (Trifolium spp.) (Cooke et al., 1975). Los primeros apotecios aparecen cuando el cultivo cubre el 100 % de la superficie del suelo y la evaporación disminuye (Abawi y Grogan, 1979).
Se ha observado que la exposición de esclerocios a sequías extremas y altas
temperaturas tienen efecto detrimental en la producción de apotecios por los esclerocios; sin embargo, estos permanecen viables por tres años a una profundidad de 20 a 25 cm en el suelo (Peltier et al., 2012). Hao et al. (2007) demostraron que la germinación carpogénica de los esclerocios ocurrió entre 15 y 20 °C, cuando el potencial mátrico de agua en el suelo fue de -0.03 a 0.07 MPa; pero no se produjeron apotecios a temperatura superiores a 26 °C (Clarkson et al., 2003). Los apotecios producen ascosporas cuya dispersión del punto de origen puede variar de 25 cm (Suzui y Kobayashi, 1972) a varios km (Leyronas et al., 2019) y la temperatura óptima para su germinación sobre flores de frijol con humedad libre es de 21 °C (Shahovesi y del Río-Mendoza, 2020); también se ha establecido que las ascosporas se liberan a 15 °C en luz y oscuridad continua y regímenes de humedad relativa de 90 a 95 % y 65 a 75 % con la liberación de 7.6 x105 ascosporas por apotecio en 20 días. La liberación de ascosporas de S. sclerotiorum en campo se han observado al medio día (Harthill, 1976; Raynal, 1990), lo cual podría estar relacionado con la temperatura que con la luz del día (Clarkson et al., 2003).
Manejo del moho blanco
Para el manejo del moho blanco se ha recurrido a la solarización (Ferraz, 2003; Supriya et al., 2017; Juliatti et al., 2019), rotación de cultivos y control químico (Kurozawa y Pavan, 1997). Debido a los bajos niveles de resistencia de los hospedantes al patógeno, se ha empleado un grupo amplio de fungicidas para el control de la enfermedad; por ejemplo, en Estados Unidos de Norteamérica, Canadá, Australia, China y Europa utilizan boscalid, fluazinam, fluxapyroxad, pyraclostrobin, penthiopyrad, picoxystrobin, prothioconazole y trifloxystrobin, tetraconazole, thiophanato metilo (Matheron y Porchas, 2004; Bradley et al., 2006 y Wang et al., 2015). La efectividad biológica de procymidone y fluazinam se demostró en el control del moho blanco en soya, cuando se aplicaron al inicio de la floración y a los 15 días después de iniciada la misma (Hideki-Sumida et al., 2015). En Sinaloa se usan carbendazim, benomilo, metil-tiofanato y fluazinam, para el control de la enfermedad en frijol y papa (Rodríguez-Cota et al., 2022; Comunicación personal, Ing. Joel González; Pasa, SA de CV, Los Mochis, Sinaloa) en ambos cultivos se logra una eficacia de control del 85 al 90 % cuando se aplican en forma preventiva. Los fungicidas boscalid+pyraclostrobin, carbendazim, fluazinam, fludioxonil+ ciprodinil y procloraz mostraron efectividad in vitro en la inhibición del crecimiento micelial de S. sclerotiorum al igual que los productos biorracionales: ácido salicílico, dióxido de hidrógeno, extracto de semilla de toronja (Ayala-Armenta et al., 2015). No existe evidencia en campo sobre la efectividad biológica de estas sustancias excepto carbendazim y fluazinam (Rodríguez-Cota et al., 2022).
Con relación al control biológico, la actividad de los agentes antagónicos es
afectada por factores abióticos y bióticos como temperatura, tipo de suelo y humedad del mismo, pH, plaguicidas, materia orgánica, microorganismos del suelo, especies de plantas, entre otros, lo que conduce a que este tipo de agentes sean menos eficaces que los fungicidas de síntesis química (Smolińska y Kowalska, 2018). Varias especies de hongos han mostrado un control biológico con la actividad micoparásita contra S. sclerotiorum sobresaliendo Coniothyrium minitans (Huang y Hoes, 1976; McQuilken et al., 1995; Zeng et al., 2012b; Patel et al., 2020). Aspersiones de conidios del hongo en etapa de floración redujeron en 56 % la incidencia de moho blanco en frijol (Huang et al., 2000). Además, la incorporación del hongo micoparásito en la superficie del suelo antes de la siembra de soya redujo la severidad de la enfermedad en 68 % y el número de esclerocios hasta en 95.3 % (Zeng et al., 2012a). La temperatura óptima para el crecimiento del micoparásito fué de 15 a 20 °C y un pH de 4.5 a 5.0 (Zeng et al., 2012b).
Los estudios sobre la eficacia de Trichoderma en el control de S. sclerotiorum en campo son limitados (Knudsen et al., 1991; Zeng et al., 2012a); sin embargo, en frijol Trichoderma asperellum a la dosis 2x1012 conidios por mL redujo el número de apotecios y severidad del moho blanco (Geraldine et al., 2013). T. hamatum redujo la incidencia de la enfermedad en 31 a 57 %, como resultado de la colonización de los esclerocios y la reducción en la producción de apotecios por el patógeno en repollo (Brassica oleracea var. capitata) (Jones et al., 2015). En pepino (Cucumis sativus), T. harzianum T39 redujo la pudrición de tallos y frutos en invernadero (Elad, 2000); mientras que la cepa T22 del mismo antagonista disminuyó el índice de severidad de enfermedad en 38.5 % (Zeng et al., 2012a).
Con relación a bacterias antagonistas, Bacillus cereus y B. subtilis afectaron el crecimiento micelial de S. sclerotiorum y redujeron la incidencia de moho blanco en girasol (Zazzerini, 1987). B. subtilis BY-2 controló la misma enfermedad en colza (Brassica napus) cuando se aplicó en la semilla y en etapa de floración; la incidencia en las parcelas tratadas con la bacteria varió de 8.9 a 11.8, mientras que en las parcelas sin tratamiento la incidencia varió de 18.1-22.9 % (Hu et al., 2014). Con dos aplicaciones de B. cereus SC en intervalos semanales redujeron la pudrición de tallo de canola por S. sclerotiorum en 6.5 a 9.3 % mientras que en las parcelas testigo la incidencia fue de 20.0 a 29.8 % (Kamal et al. 2015). También se demostró la eficacia del tratamiento de la semilla de frijol con Bacillus sp. B19, Bacillus sp. P12 y B. amyloliquefaciens B14 en el control del moho blanco (Sabaté et al., 2018).
Estudios preliminares sobre el control biológico del agente causal del moho blanco del frijol en Sinaloa demostraron el efecto inhibitorio in vitro de Trichoderma harzianum, T. viride y T. atroviride endémicas del norte de Sinaloa, contra S. sclerotiorum obtenido de frijol (Félix-López, 2016). Además, en un experimento en campo, a nivel semi-comercial, aplicaron cepas de Trichoderma a la semilla de frijol al momento de la siembra; una segunda aplicación se realizó en el sistema de riego por gravedad. Se observó una reducción de incidencia y severidad del moho blanco y un incremento de 40 % en el rendimiento con respecto al testigo regional, donde hicieron dos aplicaciones del fungicida fluazinam (Comunicación personal Ing. Fernando Urías; Asociación de Agricultores del Río Sinaloa Poniente, Guasave Sinaloa).
Supervivencia de S. sclerotiorum e incidencia de la enfermedad
Los esclerocios constituyen la estructura de supervivencia del patógeno durante el verano en Sinaloa pues tanto el frijol como la papa se desarrollan durante otoñoinvierno, contrario a otras zonas agrícolas donde sobreviven el invierno, donde los cultivos se desarrollan durante primavera-verano.
Estudios previos indicaron que la germinación carpogénica de los apotecios puede ocurrir entre 5 y 25 °C, cuando el potencial mátrico de agua en el suelo de -0.03 a 0.07 MPa (Hao, et al., 2007). Observaciones de campo en el norte de Sinaloa indican que dichas temperaturas a 2.5 cm de profundidad del suelo ocurren a partir de la primera semana de diciembre (Figura 4). Estas condiciones coinciden con la etapa de floración tanto de frijol como de papa; además, el 100 % de la superficie del suelo se cubre por el follaje de las plantas, lo que reduce la evaporación, principalmente en papa cuyas variedades crecen de manera exuberante y se irrigan por aspersión, lo que origina periodos con follaje mojado hasta por 17 horas diarias en el tercio basal de las planta y humedad permanente en la superficie de suelo cercana a la saturación. Estas variables climáticas y la fenología del cultivo, favorecen la formación de apotecios y la subsecuente liberación de ascosporas, las que penetran e infectan flores senescentes que se desprenden y caen sobre las hojas y tallos de las plantas donde se observan los síntomas iniciales de la enfermedad. También, con frecuencia se observan síntomas y signos de la enfermedad en la base del tallo en plantas de frijol o en tallos de papa sobre el suelo en el fondo del surco; en estos casos la infección primaria podría ocurrir a partir de la germinación directa de los esclerocios (Hossain et al., 2023).
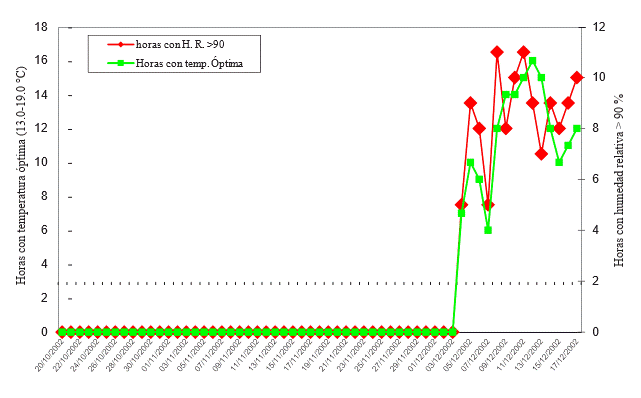
Figura 4 Períodos diarios con temperatura óptima del suelo (2.5 cm de profundidad) para la germinación de esclerocios de S. sclerotiorum y períodos con humedad relativa > 90 % en el norte de Sinaloa del 20 de octubre al 03 de diciembre de 2002.
Aun cuando se ha reportado que la exposición de esclerocios a sequías y temperaturas de30°C no favorecen la producción de apotecios por los esclerocios; éstos permanecen viables y germinan mediante la formación de micelio (Abawi y Grogan; 1979). Estas condiciones climáticas ocurren en lotes de papa que no se siembran en el ciclo primavera-verano en Sinaloa y se someten a laboreo para sembrarse en el ciclo agrícola otoño-invierno. En este caso los esclerocios a 5 cm de profundidad en el suelo se exponen a 40 °C y a bajos niveles de humedad (15 bares) (Sifuentes-Ibarra et al., 2021) en lotes baldíos durante el verano; aunque 50
% de los lotes se siembran con sorgo, donde la temperatura podría ser inferior a los 40 °C.
Manejo del moho blanco del frijol y papa en Sinaloa
En Sinaloa, en años recientes se diseñó un sistema en el que la primera aplicación preventiva de fungicidas sintéticos en frijol y papa se recomienda cuando la temperatura del suelo a 2.5 cm de profundidad varía de 13 a 19 °C. Estas condiciones se presentan durante la primera semana de diciembre en el municipio de Ahome, lo que coincide con el incremento de períodos con humedad relativa ≥ 90
% (Figura 4). En el caso de frijol, estas condiciones se dan cuando se ha aplicado el primer riego de auxilio y el cultivo cubre el 100 % de la superficie del suelo y se ha iniciado la floración con la acumulación de 630 unidades calor en la variedad Noroeste. La primera aplicación de fungicida debe realizarse, a los siete días después de que se registran entre 13 a 19 °C, lo que favorece la formación de apotecios y liberación de ascosporas.
Estos criterios también se aplican para el manejo del moho blanco en papa, donde las condiciones de humedad tanto en el follaje como en el suelo son favorables para la formación de apotecios, la liberación de ascosporas y el progreso de la enfermedad debido al uso de sistemas de riego por aspersión. Al igual que en frijol, en papa, las aplicaciones preventivas de fungicidas se inician a los siete días, después de que ocurra en el suelo a 2.5 cm de profundidad, una variación de 13 a 19
°C y el cultivo presenta las primeras inflorescencias; en esta etapa el suelo se cubre totalmente por el follaje, lo que reduce la evaporación de la humedad suministrada por los sistemas de riego. Los fungicidas; carbendazim, benomilo, metil-tiofanato
y fluazinam se utilizan para el control de la enfermedad cuando se dan estas condiciones (Rodríguez-Cota et al., 2022). Con base en este sistema de manejo de la enfermedad, en frijol se recomiendan dos aplicaciones durante el ciclo del cultivo y en papa se recomiendan hasta tres aplicaciones con intervalos de siete días, principalmente en variedades donde el período de floración es prolongado. Es frecuente la presencia de flores senescentes infectadas a partir de ascosporas, que caen sobre las plantas donde se presentan los síntomas iniciales de la enfermedad. Debido a los niveles de humedad en el suelo también ocurre daño en tallos y hojas senescentes con la consecuente producción de esclerocios que sobreviven hasta por cinco años (Ben-Yephet et al., 1993). En Sinaloa los suelos destinados a monocultivos de papa, muestran incrementos de esclerocios, los que ciclo tras ciclo producen el inóculo primario constituido por las ascosporas.
Líneas futuras de investigación
Aun cuando S. sclerotiorum ataca a cultivos económicamente importantes en Sinaloa, no se han desarrollado estudios sobre su ecología. Estudios sobre el tema, se han realizado principalmente en Estados Unidos de Norteamérica, donde el frijol y la papa se cultivan durante primavera y verano, lo que contrasta con Sinaloa donde lo mismos cultivos se desarrollan durante el ciclo otoño-invierno. Lo anterior indica áreas potenciales de investigación relacionadas con los ciclos y regiones de siembra donde la temperatura y diferentes regímenes de humedad afectan los esclerocios a diferentes profundidades, así como la actividad de microorganismos antagónicos bajo esas condiciones.
En lo relativo al control del moho blanco, tradicionalmente se ha recurrido al uso de fungicidas. Sin embargo, estas moléculas inducen resistencia en el agente causal y contaminan el ambiente. En la búsqueda de estrategias amigables con el ambiente para el control de la enfermedad, se debería determinar la efectividad biológica de especies nativas de Trichoderma. Este enfoque es crucial en la identificación de especies del hongo en la región, la determinación de su efectividad in vitro, las formas de acción del antagonista contra el patógeno bajo estas condiciones como son: micoparasitismo, antibiosis, genes inductores de la resistencia, desactivación de enzimas del patógeno, entre otras. Entre mayor número de modos de acción de especies de Trichoderma, más eficiente y duradero será el control sobre el patógeno, aspectos que no poseen los fungicidas de síntesis química (Infante et al., 2000). Otro punto para atender, es investigar la efectividad biológica de las especies de Trichoderma in planta en condiciones de invernadero y campo donde se incluya la resistencia inducida (Bisen et al., 2016). En campo se debe determinar el efecto de las aplicaciones al tubérculo semilla al momento de la siembra y aplicaciones subsiguientes mediante el sistema de riego por aspersión en cada uno de los riegos durante el crecimiento del cultivo.
La reducción en la viabilidad de los esclerocios de especies de Sclerotinia probablemente se debe a la acción de microorganismos benéficos (Williams y Western, 1965). De ahí la importancia de ensayar la eficacia de especies de Trichoderma aplicadas al momento de la cosecha tanto de frijol como de papa. Así, cuando los terrenos se barbechen, los esclerocios estarían inoculados con especies antagónicas al hongo del moho blanco. También habría que determinar la viabilidad de los esclerocios a diferentes profundidades en el suelo, así como el efecto de la temperatura y humedad en el suelo durante todos los meses del año; paralelamente determinar los niveles de incidencia de Trichoderma en los mismos y capacidad para germinar directamente y mediante la producción de apotecios. Es evidente el amplio estudio de agentes de control biológico, donde se ha acotado investigaciones en condiciones in vitro a hasta invernadero, pero poco se ha encauzado a investigaciones en campo (Córdova-Albores et al., 2021) y menos a investigación referente a este hongo y cultivos en el noroeste de México.
La efectividad del hongo Coniothyrium minitans contra el moho blanco se ha
demostrado en otras partes del mundo (Huang y Hoes, 1980; McQuilk et al., 1995; Zeng et al., 2012b); la eficacia de aplicaciones preventivas contra la germinación de ascosporas de S. sclerotiorum sobre las inflorescencias de frijol y papa se debería determinar en Sinaloa, pues esta etapa fenológica en ambos cultivos ocurre durante el invierno, cuando hay una variación de 5 a 25 °C, lo cual favorece la liberación de ascosporas por el patógeno y la potencial colonización de las mismas por el hongo antagónico (Clarkson et al., 2003 ). Sin embargo, la aplicación de
C. minitans, sobre los residuos de cosecha con esclerocios del patógeno quizá no sea eficaz para reducir la viabilidad de los mismos ya que en verano en Sinaloa se alcanzan hasta 40 °C en la superficie del suelo, lo que contrasta con otras zonas productoras donde el micoparásito se aplica sobre los residuos de cosecha al inicio de otoño donde ocurren temperaturas de alrededor de 20 °C (Zeng et al., 2012b).
En el caso de bacterias antagónicas, se encontró que Bacillus cereus y B. subtilis ejercieron control contra la pudrición del tallo del girasol causado por S. sclerotiorum (Zazzerinim, 1987). Un efecto similar se observó cuando B. subtilis BY-2 se aplicó en tratamiento de semilla o aspersión en la etapa de floración contra la misma enfermedad en colza (Hu et al., 2014). Estos hallazgos conducen hacia la búsqueda de este tipo de bacterias en Sinaloa y, la determinación de su eficacia en el control del moho blanco en frijol y papa.
Para complementar el esquema de manejo del moho blanco se deberían realizar estudios sobre la fenología de las variedades de frijol y de papa en los que se determine la acumulación de unidades calor necesarias para el inicio de floración, pues cuando esta etapa fenológica coincide con condiciones ambientales favorables para la producción de ascosporas, éstas infectan las flores fecundadas y senescentes, las cuales se desprenden y caen sobre las plantas; a partir de ahí se inician los primeros síntomas de la enfermedad. Además, tanto en frijol como en papa, el período de floración es variable, lo que sin duda influye en la presencia de sustrato para la infección por las ascosporas en el desarrollo de la enfermedad. Sin duda, el copilar información sobre este tema contribuirá a una mayor eficacia de los fungicidas y agentes de biocontrol en el manejo de la enfermedad.
Conclusiones
El moho blanco del frijol y la papa constituye una de las enfermedades importantes de estos cultivos en Sinaloa. Aun cuando se han realizado estudios sobre la ecología del agente causal y la epidemiología de la enfermedad en otras partes del mundo, en esta región los estudios sobre estos temas son incipientes. En este sentido, la implementación de un sistema de manejo que integra la temperatura del suelo y la fenología del cultivo ha permitido el uso eficiente de fungicidas en el control de la enfermedad; sin embargo, se abren nuevas líneas de investigación relativas a la fenología de variedades de frijol y de papa, donde se determinen las unidades calor requeridas para el inicio de la etapa de floración en las variedades comerciales; importante en el progreso de epidemias de moho blanco. Además, en el esquema de control se debe investigar la efectividad biológica de especies nativas o locales de Trichoderma en el manejo de la enfermedad in vitro hasta experimentación en parcelas semicomerciales y la subsiguiente transferencia en lotes comerciales.











 text in
text in 


