Introducción
La diabetes mellitus tipo 2 (DMT2) es una enfermedad multifactorial con alta incidencia en el mundo. Aproximadamente 536.6 millones de personas experimentan este padecimiento en el mundo.1 En México, la DMT2 tuvo una prevalencia de 18.3 % y una tasa de mortalidad promedio de 11.95 por cada 100 mil habitantes en 2022, con lo que constituyó la segunda causa de muerte y primera de discapacidad del país.2
Las causas de la DMT2 son alteraciones del metabolismo de la glucosa, alteraciones en la síntesis y secreción de insulina de las células β pancreáticas, elevada secreción de glucagón, insulinorresistencia o la combinación de las anteriores.3 La DMT2 puede desencadenar complicaciones crónicas divididas en dos grupos: macrovasculares y microvasculares. Las primeras se originan por daño a vasos sanguíneos grandes, por ejemplo, aterosclerosis y enfermedades cardiovasculares.4 Las segundas ocurren por daño a vasos sanguíneos pequeños o neurofibrillas como la nefropatía, retinopatía y neuropatía diabética (NfD, RD y NPD, respectivamente)5.
Las variantes en el ADN nuclear y el ADN mitocondrial (ADNmt) se han identificado como factores genéticos de riesgo para el desarrollo de DMT2 en diversas poblaciones del mundo, incluyendo las mexicanas.6,7 Su estudio permitirá un mejor entendimiento de los mecanismos de la enfermedad, y revelará patrones genéticos que expliquen el origen y susceptibilidad en población mexicana. Consecuentemente, el objetivo de la revisión fue identificar las variantes en el ADN nuclear (Tabla 1, Figura 1) y ADNmt (Tabla 2, Figura 2) en pacientes mexicanos con DMT2; las complicaciones microvasculares y los desafíos y perspectivas genéticas se discuten para identificar biomarcadores de pronóstico y prevención.
Tabla 1 Variantes nucleares asociadas a DMT2 y sus complicaciones microvasculares en poblaciones mexicanas
| Variantes asociadas a diabetes mellitus tipo 2 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Gen (símbolo, por sus siglas en inglés) | Función de su proteína | Número rs | Localización | Alelo asociado | RM (IC 95 %), p | n | Población | Área geográfica | Referencia | ||
| Riesgo | Miembro 1 de la subfamilia A del casete de unión de adenosín trifosfato (ABCA1) | Transporta colesterol y fosfolípidos al exterior de las células y participa en la formación de lipoproteínas HDL | rs9282541 | Región codificante | T | 2.29 (1.33-3.92), p = 0.003 | 429 | Maya mexicana | Yucatán, Campeche, Quintana Roo | 27 | |
| Receptor alfa 2 adrenérgico (ADRA2A) | Participa en la secreción ineficiente de insulina | rs553668 | 3' UTR | A | 3.66 (2.33-5.69), p = 1 × 10-4 | 831 | Mestizo-mexicana | CDMX | 14 | ||
| Receptor de angiotensina II tipo 2 (AGTR2) | Regula el ciclo celular, apoptosis y estrés oxidativo, provocando daño en células renales y corazón | rs1914711 | Región intergénica | A | 6.824 (ND), p = 1.448×10-9 | 92 | Maya mexicana | Yucatán | 13 | ||
| Apolipoproteína E (ApoE) | Realiza el transporte de moléculas lipídicas | rs429358 | Región codificante | Genotipo e2e3 | 2.36 (1.28-4.34), p = 0.006 | 617 | Mestizo-mexicana | Guadalajara | 28 | ||
| rs7412 | Genotipo e2 | 2.1 (1.20-3.79), p = 0.009 | |||||||||
| Proteína 1 asociada a la subunidad reguladora CDK5 1 (CDKAL1) | Participa en la modificación postraduccional y plegamiento adecuado de la insulina | rs7756992 | Intrón | C | 2.10 (1.05-4.17), p = 0.034 | 593 | Pima | Sonora | 23 | ||
| Inhibidor 2A de la quinasa dependiente de ciclina (CDKN2A/2B) | Regula el crecimiento celular al inhibir quinasas dependientes de ciclinas | rs10811661 | Región intergénica | C | 2.015 (1.01-4.02), p = 0.04 | 575 | Maya mexicana | Yucatán, Campeche, Quintana Roo | 33 | ||
| Complejo mayor de histocompatibilidad clase I, A (HLA-A) | Participa en el sistema inmunológico y puede generar autoinmunidad | rs72498368 | Intrón | A | 1.36 (ND), p = 0.0002 | 8214 | Mestizo-mexicana | CDMX | 31 | ||
| rs199474578 | Región codificante | A | 1.27 (ND), p = 0.002 | ||||||||
| rs707910 | A | 1.24 (ND), p = 0.002 | |||||||||
| rs2571420 | 2KB río arriba* | G | 1.21 (ND), p = 0.003 | ||||||||
| Grupo de alta movilidad AT-Hook 1 (HMGA1) | Regula la transcripción de genes implicados en la transducción de señales de insulina y el metabolismo de la glucosa | rs146052672 | Intrón | InsC | 1.44 (1.09-1.90), p = 0.011 | 1144 | México-americana | California | 16 | ||
| Proteína 2 de unión al ARNm del factor de crecimiento similar a la insulina 2 (IGF2BP2) | Asociada a la susceptibilidad a la diabetes | rs4402960 | Intrón | T | 1.45 (1.1-2), p = 1.4×10-2 | 2453 | Mestizo-mexicana | CDMX | 10 | ||
| Interleucina 6 (IL-6) | Regula funciones hepáticas y la homeostasis de glucosa, participa en rutas inflamatorias y de respuesta inmune, importantes en el desarrollo de la DMT2 | rs1800795 | Intrón | C | 6.31 (3.29-12.1), p = 0.001 | 412 | Mestizo-mexicana | Morelos | 8 | ||
| rs1800796 | 2KB río arriba* | C | 2.60 (1.40-4.81), p = 0.002 | ||||||||
| rs1800797 | 2KB río arriba* | A | 0.39 (0.23-0.64), p = 0.0002 | ||||||||
| Factor de crecimiento similar a la insulina 2 (IGF2) | Participa en el metabolismo de glucosa y lípidos | rs149483638 | Intrón | T | 1.76 (1.3-2.4), p = 4.2×10-4 | 2453 | Mestizo-mexicana | CDMX | 10 | ||
| Sustrato 1 del receptor de insulina (IRS-1) | Participa en la cascada de señalización de la insulina y susceptibilidad a DMT2 y resistencia a insulina | rs1801278 | Región codificante | A | 2.44 (1.53-3.89), p = 0.0001 | 1465 | Mestizo-mexicana | Guerrero CDMX | 12 | ||
| Miembro 1 de la subfamilia Q de canales de potasio dependientes de voltaje (KCNQ1) | Participa en la secreción de insulina | rs2237897 | Intrón | T | 2.17 (1.7-2.8), p = 5.4×10-9 | 2453 | Mestizo-mexicana | CDMX | 10 | ||
| Lipoproteína lipasa (LPL) | Cataliza la hidrólisis de triglicéridos a partir de lipoproteínas LDL y participa en la progresión de DMT2 y sus comorbilidades | rs285 | Intrón | T | 2.51 (1.60-3.94), p = 0.0001 | 412 | Mestizo-mexicana | Morelos | 9 | ||
| Receptor de melanocortina 4 (MC4R) | Participa en la señalización de la secreción de insulina. | rs79783591 | Región codificante | T | 2.63 (1.62-4.28), p = 9.3×10-5 | 6929 | Mestizo-mexicana | CDMX | 24 | ||
| Subunidad 1 del factor nuclear kappa B (NF-kB) | Participa en inmunidad, inflamación, metabolismo, producción de energía y modula la insulinorresistencia | rs28362491 | 2KB río arriba* | Inserción/deleción | 2.20 (1.36-3.56), p = 0.001 | 412 | Mestizo-mexicana | Morelos | 8 | ||
| Deleción/deleción | 4.32 (2.62-7.13), p = 0.0001 | ||||||||||
| Receptor activado por proliferadores peroxisomales gamma (PPARG) | Activa la transcripción de genes de regulación lipídica y homeostasis de glucosa | rs1801282 | Región codificante | G | 3.620 (1.77-7.43), p = 1 × 10-4 | 831 | Mestizo-mexicana | CDMX | 14 25 | ||
| Subunidad reguladora 3A de la proteína fosfatasa 1 (PPP1R3A) | Participa en la síntesis de glucógeno | rs1799999 | Región codificante | A | 1.625 (1.10-2.38), p = 0.014 | 600 | Maya mexicana | Yucatán | 21 | ||
| Parálogo B de RAD51 (RAD51L1) | Participa en la reparación de ADN de doble cadena durante la recombinación homóloga | rs4902613 | Intrón | G | 2.41 (1.17-4.98), p = 0.01 | 593 | Pima | Sonora | 23 | ||
| rs4899250 | Intrón | T | 2.60 (1.24-5.44), p = 0.01) | ||||||||
| Sirtuina 1 (SIRT1) | Homeostasis de glucosa propiciando la reducción de colesterol, insulina y glucosa al inducir la restricción calórica | rs3758391 | 2KB río arriba* | T | 1.32 (ND), p = 0.031 | 1455 | Mestizo-mexicana | CDMX | 11 | ||
| Miembro 16 de la familia de transportadores de solutos 30 (SLC30A8) | Transporta cinc en células β pancreáticas y promueve la liberación de insulina de las vesículas secretoras | rs3802177 | 3' UTR | A | 1.61 (1.2-2.2), p = 3.6×10-3 | 2453 | Mestizo-mexicana | CDMX | 10 | ||
| Proteína supresora de la señalización de citocinas 3 (SOCS3) | Interactúa con el receptor a insulina y suprime la señalización de la insulina | rs4969168 rs7221341 rs9914220 | 3' UTR, 3' UTR, Intrón | Ca Aa Ta | a1.47 (1.08-2.00), p≤0.05 | 1923 | Indígena mexicanaf | México (Norte, Centro y Sur) | 22 | ||
| Factor de transcripción 7-tipo 2 (TCF7L2) | Regula el metabolismo de lípidos y glucosa | rs7903146 | Intrón | T | 1.87 (1.39-2.52), p = 0.0001 | 2453 | Mestizo-mexicana | CDMX, Guerrero | 10 | ||
| 1.47 (1.2-1.8), p = 9.4×10-5 | 1465 | 11 | |||||||||
| 1.76 (ND), p = 0.001 | 1455 | 12 | |||||||||
| rs12255372 | Intrón | T | 1.74 (1.34-2.26), p = 0.0001 | 1455 | Mestizo-mexicana | CDMX, Guerrero | 12 | ||||
| Factor de necrosis tumoral alfa (TNFα) | Participa en inmunidad, inflamación, metabolismo, producción de energía y modula la resistencia a insulina | rs361525 | Río arriba* | A | 1.57 (1.07-2.29), p = 0.018 | 904 | Mestizo-mexicana | Colima, Jalisco, Michoacán, Nayarit, Morelos | 17 | ||
| 2.25 (1.36-3.72), p = 0.001 | 412 | 18 | |||||||||
| rs1800629 | Río arriba* | A/G | 2.61 (1.45-4.57), p = 0.001 | 412 | Mestizo-mexicana | León, Morelos | 18 | ||||
| 5.80 (1.77-18.98), p = 0.0003 | 230 | 19 | |||||||||
| Protección | Factor de ribosilación ADP similar a la GTPasa 15 (ARL15) | Modula el metabolismo lipídico y de la glucosa | rs4311394 | Intrón | G | 0.318 (ND), p = 0.001 | 92 | Maya mexicana | Yucatán | 13 | |
| Receptor de estrógeno beta (Erβ) | Participa en el metabolismo de glucosa y lípidos | rs1256031 | Intrón | T | 0.596 (0.458-0.776), p = 0.0001 | 1202 | Mestizo-mexicana | CDMX | 29 | ||
| Regulador de la glucoquinasa (GCKR) | Participa en el metabolismo de la glucosa al inhibir a la glucoquinasa y la secreción de lipoproteína de muy baja densidad | rs1260326 rs780094 | Región codificante Región codificante | Tb Tb |
b0.66 (0.52-0.84), p = ≤≤0.01 | 1923 | Indígena mexicanaf | México (Norte, Centro y Sur) | 22 | ||
| Prepropéptido de grelina y obestatina (GHRL) | Regula el apetito y adipogénesis | rs696217 | Región codificante | T | 0.40 (0.23-0.70), p = 0.001 | 284 | Mestizo-mexicana | Jalisco | 30 | ||
| Complejo mayor de histocompatibilidad clase I, A (HLA-A) | Participa en el sistema inmunológico y puede generar autoinmunidad | rs199474485 | Región codificante | G | 0.894 (ND), p = 0.0009 | 8214 | Mestizo-mexicana | CDMX | 31 | ||
| rs45617033 | T | 0759 (ND), p = 0.002 | |||||||||
| rs1136702 | T | 0.906 (ND), p = 0.002 | |||||||||
| rs9260124 | Intrón | T | 0.904 (ND), p = 0.002 | ||||||||
| rs9260145 | G | 0.901 (ND), p = 0.003 | |||||||||
| rs576213756 | Inserción MLA | InsTCTCCAAGACCAA | 0.908 (ND), p = 0.0036 | ||||||||
| rs2735114 | 5' UTR | A | 0.911 (ND), p = 0.00394 | ||||||||
| Complejo mayor de histocompatibilidad clase I, C (HLA-C) | Participa en el sistema inmunológico y puede generar autoinmunidad | rs17408553 | Región codificante | T | 1.11 (ND), p = 0.002 | 8214 | Mestizo-mexicana | CDMX | 31 | ||
| rs2308557 | T | 1.11 (ND), p = 0.002 | |||||||||
| rs1131115 | T | 1.14 (ND), p = 0.002 | |||||||||
| rs2001181 | Intrón | T | 1.14 (ND), p = 0.002 | ||||||||
| rs7383157 | Intrón | G | 1.13 (ND), p = 0.003 | ||||||||
| rs1065711 | 3' UTR | A | 1.14 (ND), p = 0.002 | ||||||||
| Sirtuina 1 (SIRT1) | Participa en la reducción de colesterol, insulina y glucosa | rs7896005 | Intrón | G | 0.560 (0.450-0.690), p = 1 × 10-4 | 831 | Mestizo-mexicana | CDMX | 14 | ||
| Riesgo | Proteína 2 asociada a contactina (CNTNAP2) | Participa en la migración y densidad en el córtex prefrontal medial y la agrupación de canales de potasio | rs731565 | Intrón | T | 1.58 (1.30-1.92), p = 4.06 × 10-6 | 1376 | México-americana | California | 47 | |
| Defensina beta 1 (DEFB1) | Participa en la eliminación de la infección por Escherichia coli uropatógena | rs11362 | 5' UTR | A | 1.875 (1.031-3.409), p = 0.038 | 331 | Mestizo-mexicana | Culiacán | 44 | ||
| Interleucina 10 (IL-10) | Modula la inflamación y la homeostasis celular, y puede reducir la infiltración del tejido renal y el grado de fibrosis intersticial, inhibiendo la proliferación de células mesangiales | rs1800896 rs1800871 rs1800872 | Intrón, 5' UTR, 5' UTR | Ad Td Cd |
Ge Te Ae |
d3.686 (1.691-8.035), p = 0.0007 e4.388 (1.168-16.480), p = 0.022 | 278 | Mestizo-mexicana | Jalisco | 47 | |
| Subunidad 13L del complejo mediador (MED13L) | Coactivador transcripcional para genes transcritos por ARN polimerasa II | rs7975752 | Intrón | G | 1.76 (1.39-2.21), p = 1.67 × 10-6 | 13736 | México-americana | California | 47 | ||
| Factor de crecimiento transformante beta-1 (TGF-β1) | Regulación inmune, angiogénesis, apoptosis, proliferación celular, transición epitelio-mesénquima | rs1982073 | Región codificante | C | 1.818 (1.128-2.930), p = 0.016 | 438 | Mestizo-mexicana | CDMX | 46 | ||
| rs1800471 | C | 4.073 (1.355-12.249), p = 0.008 | |||||||||
| Factor de transcripción 11 de SRY-Box (SOX11) | Participa en el desarrollo embrionario del riñón | rs4849965 | Intrón | C | 1.50 (1.26-1.79), p = 6.18 × 10-6 | 13736 | México-americana | California, Estados Unidos | 47 | ||
| Protección | Defensina beta 1 (DEFB1) | Participa en la eliminación de la infección por Escherichia coli uropatógena | rs1799946 | 5' UTR | T | 0.307 (0.104-0.905), p = 0.026 | 331 | Mestizo-mexicana | Culiacán | 44 | |
| NFE2 similar a factor de transcripción 2 BZIP (NFE2L2) | Participa en procesos del metabolismo antioxidante, lípidos, catabolismo de iones, proteostasis, y en la inhibición de la inflamación | rs35652124 | 5' UTR | A | 0.5 (0.3-0.9), p = 0.04 | 651 | Mestizo-mexicana | Jalisco | 48 | ||
| rs2364723 | Intrón | G | 0.3 (0.1-0.8), p = 0.009 | ||||||||
| Riesgo | Proteína estructural de filamentos granulados 2 (BFSP2) | Codifica la proteína faquinina de los filamentos intermedios específicos del cristalino | rs1197310 | Intrón | T | 2.25 (1.45-3.51), p = 3.35 × 10-4 | 286 | México-americana | Texas | 52 | |
| Contactina 5 (CNTN5) | Aumento de la presión arterial y de la hemoglobina glicosilada | rs10501943 | Intrón | C | 3.04 (1.68-5.52), p = 2.53 × 10-4 | 286 | México-americana | Texas | 52 | ||
| Histamina-N- metiltransferasa (HNMT) | Participa en la degradación de histamina y recluta células inmunes que causan daños en superficies oculares | rs763970 | 500B río abajo* | A | 2.25 (1.44-3.52), p = 4 × 10-4 | 286 | México-americana | Texas | 52 | ||
| Proteína de unión 1 similar a SCY1 (SCYL1BP1) | Estabiliza a p53 acelerando el proceso de senescencia de las células endoteliales | rs6427247 | Río arriba* | G | 2.17 (1.41-3.35), p = 4.56 × 10-4 | 286 | México-americana | Texas | 52 | ||
| Receptor de inmunoglobulina similar a células asesinas (KIR) con dos dominios Ig y cola citoplasmática corta 4 (KIR2DS4) | Regulación de la respuesta inmune | 700 C>T | Región codificante | T | 0.04 (0.001-0.36), p = 0.04 | 60 | Mestizo-mexicana | CDMX | 53 | ||
| Inhibidor de la apoptosis 5 (API5) | Regula negativamente la apoptosis en condiciones de estrés nutricional | rs899036 | Intrón | C | 0.32 (0.17-0.59), p = 2.52 × 10-4 | 286 | México-americana | Texas | 53 | ||
| Repeticiones similares a EGF y dominios 3 similares a discoidina (EDIL3) | Media la respuesta inmune y antiinflamatoria y regula la adhesión, proliferación, migración y angiogénesis de células endoteliales de la retina humana | rs1445754 | Intrón | A | 0.37 (0.22-0.64), p = 3.35 × 10-4 | 286 | México-americana | Texas | 52 | ||
| Formina 1 (FMN1) | Participa en la producción de las uniones adherentes y polimerización de monómeros de actina | rs10519765 | Intrón | A | 0.30 (0.16-0.54), p = 6.21 × 10-5 | 286 | México-americana | Texas | 52 | ||
DMT2: diabetes mellitus tipo 2; IC: intervalo de confianza; MLA: marco de lectura abierto; ND: no disponible; RD: retinopatía diabética; RM: razón de momios;
aHaplotipo CAT;
bHaplotipo TT;
dHaplotipo ATC;
eHaplotipo GTA;
fIndígena mexicano: chinanteco, chuj, huasteco, jakalteko, kanjobal, kaqchikel, mam, maya, mayo, mazateco, mixe, mixteco, mocho, náhuatl, otomí, pame, popoluca de la sierra, seri, tarahumara, tojolobal, totonaco, yaqui, zapoteco; Norte, Centro y Sur de México: Sonora, Chihuahua, Nuevo León, Zacatecas, Oaxaca, Veracruz, Chiapas, Yucatán, CDMX, Morelos, Puebla, San Luis Potosí, Estado de México.
*Con respecto al sitio de inicio de la transcripción.
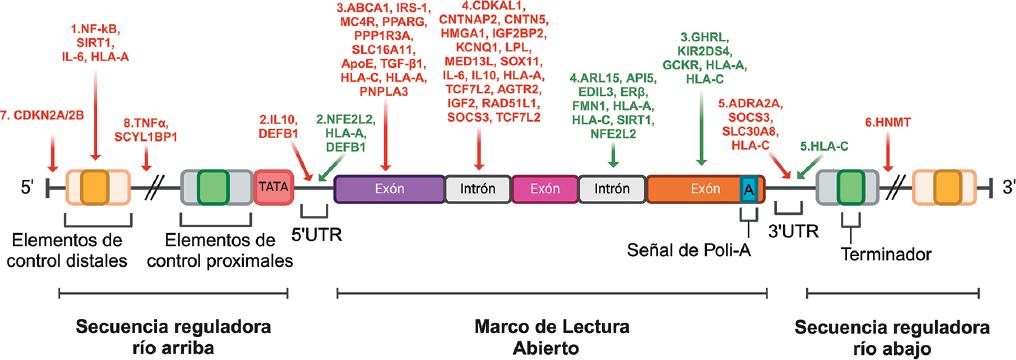
Figura 1 Esquema representativo de la localización de las variantes genéticas del ADN nuclear asociadas al riesgo o protección de la DMT2 y sus complicaciones microvasculares. Las variantes de riesgo (rojo) y de protección (verde) están distribuidas en diferentes regiones de la estructura génica, indicadas por las flechas que señalan las ubicaciones de estas variantes dentro del gen. 1: secuencia río arriba; 2: 5'UTR, región no traducida en el extremo 5'; 3: región codificante (exones); 4: región intrónica (intrones); 5: 3'UTR, región no traducida en el extremo 3'; 6: secuencia río abajo; 7: región intergénica (espacio entre genes); 8: región reguladora. La descripción de cada variante se muestra en detalle en la tabla 1. Elaboración en BioRender.
Tabla 2 Variantes y haplogrupos mitocondriales asociados a DMT2 y sus complicaciones microvasculares
| Región génica | Función | Variante | Complicación | RM (IC 95 %), p | n | Población | País | Referencia |
|---|---|---|---|---|---|---|---|---|
| D-Loop | Regulación de la replicación y transcripción | 315_316insC | DMT2 | 6.13 (3.42-10.97), p = 1.97 × 106 | 1001 | Mestizo- mexicana (CDMX) | México | 7 |
| 16362T>C | 2.17 (1.57-3.00), p = 0.001 | |||||||
| 16519T>C | 1.69 (1.23-2.33), p = 0.006 | |||||||
| 489T>C | 1.45 (1.00-2.11), p = 0.006 | |||||||
| D-Loop | Regulación de la replicación y transcripción | 16189T>C | DMT2 | 2.27 (1.37-3.77), p = 0.002 | 778 | Punjab, Jammu, Kashmir | India | 36 |
| Subunidad central 2 de la NADH oxidorreductasa (ND2) | Transporte de electrones | 5178C>A | DMT2 NfD | 1.49 (1.005-2.197), p < 0.05 | 1894 | Han | China | 37 |
| Subunidad central 3 de la NADH oxidorreductasa (ND3) | Transporte de electrones | 10398G>A | DMT2 | 2.67 (1.77-4.00), p = 0.001 | 236 | Punjab, Jammu, Kashmir | India | 35 |
| Subunidad central 4 de la NADH oxidorreductasa (ND4) | Transporte de electrones | 12026A>G | DMT2 | 5.81 (1.27-26.53), p = 0.01 | 236 | Wuhan | China | 35 |
| Variantes mitocondriales asociadas a la protección contra el desarrollo de DMT2 y sus complicaciones | ||||||||
| D-Loop | Regulación de la replicación y transcripción | 16189T>C | DMT2 | 0.32 (0.14-0.71), p = 0.0045 | 132 | Han | China | 38 |
| D-Loop | Regulación de la replicación y transcripción | 16519T>C | DMT2 | 0.13 (0.05-0.33), p = 0.000 | 132 | Han | China | 38 |
| Subunidad central 1 de la NADH oxidorreductasa (ND1) | Transporte de electrones | 3394T>C | DMT2 | 0.07 (0.01-0.56), p = 0.0015 | 132 | Han | China | 38 |
| Subunidad central 2 de la NADH oxidorreductasa (ND2) | Transporte de electrones | 4491G>A | DMT2 | 0.07 (0.01-0.56), p = 0.0015 | 132 | Han | China | 38 |
| Haplogrupos mitocondriales asociados al riesgo de desarrollar DMT2 y sus complicaciones | ||||||||
| Haplogrupo | Complicación | RM (IC 95 %), p | n | Población | País | Referencia | ||
| U3 | NfD | 3.75 (1.21-11.53), p = 0.04 | 904 | Italiana | Italia | 50 | ||
| H | RD | 2.0 (1.3-3.0), p = 0.0012 | 291 | Estadounidense | Estados Unidos | 39 | ||
| T | RD | 3.60 (1.02-12.68), p = 0 0.046 | 714 | Austriaca | Austria | 40 | ||
| Haplogrupos mitocondriales asociados a la protección contra el desarrollo de DMT2 y sus complicaciones | ||||||||
| N9a | DMT2 | 0.55 (0.40-0.75), p = 0.0002 | 286 | Coreana, japonesa | Corea, Japón | 52 | ||
| Uk | RD | 0.5 (0.3-0.8), p = 0.0049 | 291 | Estadounidense | Estados Unidos | 39 | ||
DMT2: diabetes mellitus tipo 2; IC: intervalo de confianza; NfD: nefropatía diabética; RD: retinopatía diabética; RM: razón de momios.
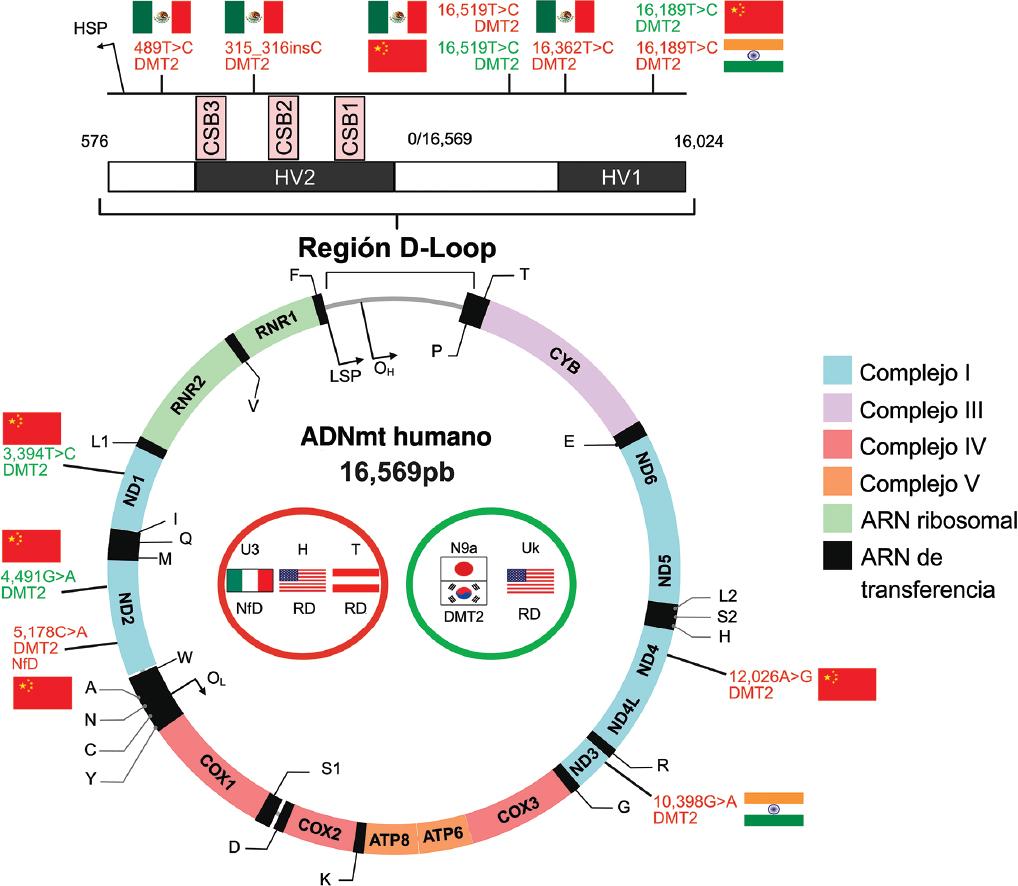
Figura 2 Variantes y haplogrupos del ADNmt humano asociados a DMT2 y sus complicaciones microvasculares. La distribución de las variantes se muestra a escala en el genoma completo del ADNmt; las letras indican que se trata de una variante de riesgo (rojo) o una variante de protección (verde); en los círculos en el centro del genoma del ADNmt se observan los haplogrupos mitocondriales de riesgo (rojo) y protección (verde) asociados a DMT2, NfD o RD; las banderas muestran el país de cada población estudiada. La descripción de cada variante se muestra a detalle en la Tabla 2. DMT2: diabetes mellitus tipo 2; NfD: nefropatía diabética; RD: retinopatía diabética. Elaborado en BioRender.
Variantes genéticas en ADN nuclear asociadas a DMT2
Regulación del metabolismo energético
Las variantes en genes de regulación energética que participan en la alteración de las vías metabólicas (glucosa y lípidos), el estrés oxidativo y la actividad transcripcional, que afectan su expresión y función,6 son de gran importancia en el desarrollo de la DMT2. Las variantes de riesgo que se han identificado en poblaciones mestiza mexicana son rs28362491 en NF-kB,8 que codifica para un factor de transcripción;9 y rs7903146 y rs12255372 en TCF7L2,10-12 involucradas como factor de transcripción de moléculas que participan en las vías metabólicas.9 También se han identificado las variantes de protección rs4311394 en ARL1513 en población maya mexicana, cuya proteína modula los niveles de adiponectina; y rs3758391 y rs7896005 en SIRT1, variantes de riesgo y protección, respectivamente,11,14 aunque la variante rs7896005 fue de riesgo solamente en población indígena pima.15 Se ha descrito que cuando hay restricción calórica, SIRT1 reduce el colesterol, la insulina y la glucosa.9
Regulación del metabolismo de la glucosa
Debido al papel de la glucosa en la fisiopatología de la DMT2, las variantes genéticas que alteran su metabolismo son de gran importancia. En población mestiza mexicana se detectó la variante rs146052672 en HMGA1, identificada también en síndrome metabólico;16 esta variante se asocia a la pérdida de la regulación de la transcripción de genes implicados en la transducción de señales de insulina y el metabolismo de la glucosa.9 La variante de riesgo rs149483638 en IGF210 altera su procesamiento alternativo, disminuyendo la expresión de su isoforma 2, implicada en el metabolismo de la glucosa y los lípidos.9 La variante de riesgo rs4402960 en IGF2BP2,10 cuya proteína regula la expresión de IGF2,9 consecuentemente está implicada en el metabolismo de la glucosa y los lípidos. La proteína de las variantes de riesgo rs1800629 y rs361525 en TGFα17-19 fosforila a los receptores de insulina, disminuyendo la expresión de GLUT4, lo que promueve la insulinorresistencia.9 Estas variantes detectadas en población mestiza mexicana17,19 también se han identificado en poblaciones de Estados Unidos, China e India.20
En otros genes que regulan la homeostasis de la glucosa también se han reportado variantes en población mestiza mexicana, como la de riesgo rs1799999 en el gen PPP1R3A,21 que codifica para la fosfatasa 1 y participa en el metabolismo y en la síntesis de glucógeno;9 y el haplotipo protector TT, conformado por rs1260326 y rs780094 en GCKR,22 cuya proteína inhibe a la glucoquinasa que participa en el metabolismo de la glucosa.9
Regulación del metabolismo de la insulina
Las variantes en las proteínas que regulan la insulina y sus funciones desempeñan un papel clave en el desarrollo de la DMT2. Se detectaron las siguientes variantes de riesgo: rs1801278 en IRS-1,12 que provoca un cambio de glicina por alanina en el residuo 972 de la proteína, asociado a la susceptibilidad a insulinorresistencia y DMT29 en población mestiza mexicana; rs4969168, rs7221341 y rs9914220 en el haplotipo de riesgo CAT en SOCS3 se identificaron en 27 etnias indígenas22 y su proteína suprime la señalización de insulina;9 y rs7756992 en CDKAL1,23 cuya proteína participa en la modificación postraduccional y plegamiento adecuado de la insulina,9 que se identificó en población indígena pima.
Las variantes de riesgo implicadas en diferentes genes de importancia en la secreción de insulina incluyen rs3802177 en SLC30A8,10 cuya proteína promueve la liberación de insulina de las vesículas secretoras de las células β pancreáticas;9 rs2237897 en KCNQ1, que codifica para canales de potasio cuya inhibición estimula la secreción de insulina;10 rs79783591 en MC4R, que codifica para un receptor de melanocortina que señaliza la secreción de insulina, se asoció a DMT2 exclusivamente en pacientes masculinos;24 y rs553668 en ADRA2A,14 cuya proteína es un receptor adrenérgico, se asoció a la secreción ineficiente de insulina.9
Regulación del metabolismo de lípidos
La regulación del metabolismo de lípidos es importante en la patogénesis de la DMT2, ya que es un factor predictivo de la enfermedad, por lo que variantes que alteren estos procesos de regulación son relevantes en la progresión de la enfermedad. En población mestiza mexicana se reportaron las siguientes variantes de riesgo: rs1801282 en PPARG,14,25 que codifica para un receptor nuclear en adipocitos, además de que activa la transcripción de genes de regulación lipídica y homeostasis de glucosa,9 aunque en otras poblaciones tiene un papel protector;26 rs9282541 en ABCA1,27 cuya proteína transporta colesterol y fosfolípidos al exterior de las células y participa en la formación de HDL;9 rs429358 y rs7412 en ApoE,28 cuya lipoproteína realiza el transporte de moléculas lipídicas;9 y rs285 en LPL,8 cuya proteína cataliza la hidrólisis de triglicéridos.9
Variantes de protección en genes cuyas proteínas participan en vías hormonales están implicadas en la regulación del metabolismo de lípidos: la activación de rs1256031 en Erβ29 media funciones del metabolismo de lípidos y glucosa, así como la expresión y traslocación de GLUT4 a la membrana;9 la proteína grelina de rs696217 en GHRL30 regula el apetito y la adipogénesis.9
Alteraciones de los procesos inmunológicos
Con relación a la fisiopatología de la DMT2, la inmunidad participa en procesos como inflamación o daño a los tejidos. En población mestiza mexicana se han identificado las variantes de riesgo rs72498368, rs199474578, rs707910 y rs2571420 en HLA-A; y rs17408553, rs2308557, rs1131115, rs2001181, rs1065711 y rs7383157 en HLA-C; y las variantes de protección rs199474485, rs45617033, rs9260145, rs9260124, rs1136702, rs576213756, rs2735114 en HLA-A.31 Alteraciones en sus proteínas pueden ser causadas por la hiperglucemia, mediada por estrés oxidativo y glicación, provocando que las células T y dendríticas las reconozcan como extrañas.9 También se han identificado las variantes de riesgo rs1800795, rs1800796 y rs1800797 en IL-6,8 cuya proteína regula funciones hepáticas, el desarrollo de insulinorresistencia, la homeostasis de glucosa, además de que participa en rutas inflamatorias y en la respuesta inmune.9 En otras poblaciones, la variante rs1800795 puede ser de riesgo o protección.32
Variantes genéticas de funciones desconocidas en DMT2
Se han detectado variantes de riesgo en genes donde su asociación con los procesos fisiopatológicos en DMT2 no se comprende por completo, entre estas se han descrito rs1914711 en AGTR2,13 que codifica para un receptor de angiotensina II;9 rs10811661 en CDKN2A/2B,33 cuya proteína regula el crecimiento celular al inhibir quinasas dependientes de ciclinas,9 ambas identificadas en población indígena maya de México; y rs4899250 en RAD51L1,23 cuya proteína participa en la reparación del ADN de doble cadena durante la recombinación homóloga9 en población indígena pima.
Variantes genéticas en ADNmt asociadas a DMT2
En la DMT2, la mitocondria participa en la producción de energía en forma de adenosín trifosfato, la fosforilación oxidativa, la oxidación de lípidos y en el proceso de la síntesis y secreción de insulina;34 consecuentemente, las variantes del ADNmt alterarían sus funciones moleculares.35-37 Variantes de riesgo se han identificado en ND2, ND3 y ND4 en diversas poblaciones y de protección en ND1 y ND2.38
En población mestiza mexicana se han reportado las siguientes variantes de riesgo de DMT2: 315_316insC, 489T>C, 16362T>C, y 16519T>C, localizadas en la región hipervariable del ADNmt.7 En población china se identificaron las variantes de protección 16189T>C y 16519T>C en la región hipervariable.38 Asimismo, se identificaron los haplogrupos mitocondriales de riesgo a DMT2 de protección: N9a en poblaciones de Corea y Japón.42 No se han reportado haplogrupos asociados a DMT2 en población mexicana.
Variantes genéticas asociadas a complicaciones microvasculares
NfD, RD y NPD están relacionadas con la hiperglucemia de manera causal,4 donde el componente genético desempeña un papel importante en su aparición y evolución clínica.5
Variantes genéticas asociadas a NfD
La NfD es una de las principales causas de enfermedad renal crónica y terminal en el mundo. Su desarrollo en la DMT2 se debe a la interacción de factores metabólicos, hemodinámicos, inflamatorios y fibróticos, causantes de daño en tejidos y células renales, provocando hiperfiltración y pérdida de la función renal. Los fenotipos de la NfD dificultan el diagnóstico; consecuentemente, las variantes genéticas podrían usarse como biomarcadores.43
Variantes genéticas en el ADN nuclear
En mestizos mexicanos se reportaron las variantes rs11362 y rs1799946 en DEFB1 que confieren riesgo y protección, respectivamente;44 este gen expresado en el túbulo distal y el sistema colector del riñón participa en la eliminación de la infección por Escherichia coli uropatógena;9 las variantes de riesgo rs1800896, rs1800871 y rs1800872 en IL-10,45 cuya proteína modula la inflamación y la homeostasis celular, pueden reducir la infiltración del tejido renal y el grado de fibrosis intersticial, inhibiendo la proliferación de células mesangiales;9 y rs1982073 y rs1800471 en TGFβ1,46 que incrementa su proteína en pacientes con NfD y otras enfermedades renales fibróticas,9 lo que estaría afectando la regulación del sistema inmune.
En mexicoamericanos se identificaron las variantes de riesgo47 rs7975752 en MED13L, cuya proteína es un coactivador transcripcional para genes transcritos por la RNA polimerasa II;9 rs731565 en CNTNAP2, donde la disminución de su proteína altera la migración y densidad en el córtex prefrontal medial y la agrupación de canales de potasio;9 y rs4849965 en SOX11, cuya proteína es un factor de transcripción que participa en el desarrollo embrionario del riñón y sus variantes genéticas incrementan la predisposición a anormalidades congénitas del riñón y el tracto urinario.9
En mestizos mexicanos se han identificado rs35652124 y rs2364723 en NFE2L2,48 cuya proteína regula genes involucrados en procesos del metabolismo antioxidante, lípidos, catabolismo de iones, proteostasis e inhibición de la inflamación;9 por tanto, son variantes de protección a NfD.
Variantes genéticas en el ADNmt
En individuos con DMT2 y NfD, la hiperglucemia altera la energía mitocondrial, induciendo cambios en la cadena de transporte de electrones, aumento de ROS y disminución de adenosín trifosfato. Estas alteraciones incrementan la división mitocondrial, disminuyen los niveles de PGC1α, cambian la morfología mitocondrial y aumentan la apoptosis celular, agravando la NfD.49
La variante de riesgo 5178C>A asociada a DMT2 en población china provoca mayor riesgo de complicaciones renales.37 Asimismo, se ha asociado el haplogrupo mitocondrial U3 al riesgo a NfD en población italiana.50 En población mexicana aún no existen estudios sobre variantes o haplogrupos mitocondriales asociados a NfD.
Variantes genéticas asociadas a RD
La RD se presenta en la tercera parte de las personas con DMT2 y es una de las principales causas de pérdida de visión en personas > 40 años con evolución prolongada de DMT2 e hiperglucemia. Los mecanismos fisiopatológicos que causan la RD son mayor producción de radicales libres, productos de glicosilación avanzada, factores inflamatorios, factores genéticos y epigenéticos.51
Variantes genéticas en el ADN nuclear
Como factores de riesgo para RD, en población mexicoamericana se ha asociado rs2300782 en CAMK4, cuya proteína es una quinasa dependiente de Ca2+/calmodulina asociada a insulinorresistencia, a la inactivación de la señalización de la insulina y la captación de glucosa en células del trofoblasto;9 rs10501943 en CNTN5, cuyo producto participa en el desarrollo del sistema nervioso, el aumento de la presión arterial y de la hemoglobina glicosilada (las alteraciones en esta última sugieren una disminución en el transporte de oxígeno y, por tanto, la disminución de la producción de adenosín trifosfato en las mitocondrias afecta los tejidos oculares);9 rs1197310 en BFSP2, de la cual su proteína, faquinina, forma parte de los filamentos intermedios específicos del cristalino;9 rs763970 en HNMT, cuya proteína participa en la degradación de histamina y recluta células inmunes que causan daños en superficies oculares;9 y rs6427247 en SCYL1BP1,52 cuyo producto es un regulador que al unirse a la proteína Mdm2 promueve su autoubiquitinación y estabiliza a p53, que a su vez acelera el proceso de senescencia de las células endoteliales.9
La variante 700 C>T en KIR2DS4 de protección a RD53 podría conferir protección a los tejidos oculares en población mestiza mexicana; su proteína participa en la regulación de la respuesta inmune; rs10519765 en FMN,52 cuya proteína interactúa con α-catenina en la producción de las uniones adherentes y polimerización de monómeros de actina;9 rs1445754 en EDIL3, cuya proteína, un factor proangiogénico, media la respuesta inmune y antiinflamatoria y regula la adhesión, proliferación, migración y angiogénesis de células endoteliales de la retina humana;9 rs899036 en API, cuya proteína es un regulador negativo de apoptosis en condiciones de estrés nutricional9; y rs599019 en COLEC12,53 cuya proteína participa en la interiorización de la glucosa.9
Variantes genéticas en el ADNmt
Los cambios metabólicos de las células de la retina en condiciones de hiperglucemia pueden provocar disfunción mitocondrial e inducir apoptosis, mitofagia y dinámica mitocondrial de forma adaptativa.54 Hasta el momento, no se han identificado variantes en el ADNmt asociadas a RD, aunque en población caucásica (de Estados Unidos) se ha reportado la asociación de riesgo y protección de los haplogrupos H y Uk, respectivamente;39 y en población caucásica europea se ha identificado el haplogrupo T como de riesgo.40 En poblaciones mexicanas no existen estudios de asociación en el ADNmt.
Variantes genéticas asociadas a NPD
La NPD afecta a 20 % de las personas con DMT2, se caracteriza por el deterioro de la circulación sanguínea hacia los nervios periféricos y es causada por ROS, alteraciones neurovasculares, glicosilación proteica modificada, inmunomodulación, inflamación55 y factores genéticos.
Variantes en el ADN nuclear
En poblaciones no mexicanas se han descrito variantes de riesgo para desarrollar NPD en los genes ACE, MTHFR GPx1, RMI2 y MYBPHL y variantes de protección en CAT, MVB12B y RXRA.56,57 En población mexicana no existen estudios de asociación con variantes nucleares para NPD.
Variantes en el ADNmt
En modelos animales y cultivos celulares se han observado alteraciones en el genoma mitocondrial que contribuyen al desarrollo y evolución de NPD, debido a que el potencial de la membrana mitocondrial se modifica, disminuyendo la actividad de la cadena respiratoria en neuronas sensoriales, donde un aumento en la concentración de glucosa incrementa la apoptosis.58 No se identificaron estudios de asociación del genoma mitocondrial a NPD en la población mexicana u otras poblaciones.
Conclusiones
La fisiopatología de la DMT2 es causada principalmente por secreción insuficiente de insulina en las células β pancreáticas y pérdida de respuesta a la insulina en sus tejidos blanco. En esta revisión se describen variantes genéticas relacionadas con estas funciones, incluyendo las que alteran la expresión de proteínas que participan en la regulación del metabolismo de la glucosa (HMGA1, IGF2, IGF2BP2, TNFα, PPP1R3A y GCKR), variantes genéticas que actúan en la regulación de la señalización de la insulina (IRS-1, SOCS3, CDKAL1 y SLC30A8) y genes que influyen en su secreción (KCNQ1, MC4R y ADRA2A).
También se describen variantes genéticas que alteran la regulación del metabolismo de lípidos (PPARG) y la regulación de lípidos por vías hormonales (Erβ y GHRL), así como variantes genéticas que propician el aumento del transporte y síntesis de moléculas lipídicas (ABCA1, ApoE y LPL). Participan en la progresión de la DMT2 y propician la aparición de complicaciones macrovasculares por la acumulación de moléculas lipídicas, principalmente en arterias, así como en procesos inflamatorios. Se describen variantes genéticas en la DMT2 que participan en la inflamación (IL-6) y en la autoinmunidad (HLA-A y HLA-C). También se describen las variantes genéticas en AGTR2, CDKN2A/2B y RAD51L1, cuya función se desconoce en DMT2.
En relación con la NfD, se identificaron nueve variantes de riesgo y tres de protección en genes que participan en procesos de la respuesta inmune. En RD se identificaron cuatro variantes de riesgo y dos de protección en genes asociados a la estructura, proliferación, y senescencia de las células oculares.
Variantes genéticas asociadas a DMT2 se identificaron en el ADNmt, que podrían relacionarse con la producción de energía y la homeostasis de la glucosa que pueden afectar la función de la mitocondria, la sensibilidad a la insulina y el metabolismo de la glucosa, influyendo en la susceptibilidad a la enfermedad y sus complicaciones. En la región hipervariable que contiene sitios reguladores se encontraron cinco variantes de riesgo y dos de protección (Figura 2), lo que sugiere que estas variantes podrían alterar la regulación de la replicación y la transcripción, afectando al número de copias del ADNmt, aunque se desconoce su función directa en la DMT2. Variantes asociadas a DMT2 también se identificaron en los genes codificantes para subunidades del complejo I de la cadena de transporte de electrones, donde se observaron dos variantes de riesgo y dos de protección. En ND2 se encontró una variante de riesgo asociada a DMT2 y NfD, la cual podría afectar los procesos de producción de energía.
Las variantes determinantes de los haplogrupos mitocondriales de protección N9a para DMT2 y Uk para RD, o los haplogrupos de riesgo U3 para NfD, H y T para RD, pueden estar participando en la regulación del metabolismo de la mitocondria, por lo cual sugerimos realizar estudios con cíbridos mitocondriales para conocer su función.
La alta prevalencia y mortalidad asociadas a estas patologías destacan la importancia de la identificación de los factores genéticos que permitirán el desarrollo de nuevas estrategias preventivas y la identificación de nuevos blancos terapéuticos. Pese a la relevancia clínica de este tema en poblaciones mexicanas, las investigaciones son escasas, lo que representa un área de oportunidad de estudio para comprender las bases genéticas de DMT2, aplicadas a la predisposición, pronóstico y progresión de esta enfermedad y sus complicaciones.











 text new page (beta)
text new page (beta)


