INTRODUCCIÓN
El ligamento periodontal es un tejido conectivo fibroso, compuesto de fibras, células y sustancia intercelular rica en colágeno, alto contenido proteico y polisacáridos. De origen ectomesenquimal. Tiene como funciones: 1) suspender el diente en su alvéolo óseo; 2) suministrar nutrientes al alvéolo y al cemento; 3) proteger los dientes; y 4) mantener la homeostasis de los dientes en su alvéolo por medio de la regeneración continua.1 Esta regeneración del ligamento periodontal (LPD) como un mecanismo fisiológico continuo, dio lugar a la teoría de que este tejido podía contener una subpoblación de células progenitoras.2 En el 2004, Seo y colaboradores3 publicaron que era posible que el LPD humano contuviera una población de células troncales postnatales multipotenciales, con capacidad clonogénica, con alto índice de proliferación y con capacidad de regenerar tejido periodontal.4-6
Se ha demostrado que las células troncales mesenquimales del ligamento periodontal (PDLSCs: periodontal ligament stem cells) son similares a otras células troncales mesenquimales en la expresión de los marcadores: STRO-1, CD146, CD90, CD29, CD44, CD13, CD105 y CD166, así como su capacidad autorregenerativa y multipotencialidad.3,7,8
Varios autores, después de aislar PDLSCs demostraron su capacidad para diferenciarse a linajes de tipo mesodérmico, diferenciándose en células similares a cementoblastos, osteoblastos, condrocitos, adipocitos, miofibroblastos y células formadoras de colágeno,9,10 incluso se ha investigado el potencial de las PDLSCs para dar lugar a células propias del sistema nervioso; así como cemento.11
Actualmente, se han conseguido cultivar PDLSCs a través de diferentes métodos de extracción, demostrando que el LPD es una buena fuente de células troncales para su potencial aplicación en medicina regenerativa; sin embargo, los métodos descritos hasta la fecha tienen algunos problemas técnicos. Por esta razón, se compararon seis métodos (Cuadro I) en un esfuerzo de mejorar el método de aislamiento de células primarias del LPD, ya que ninguno de los métodos reportados es preciso, por ello el objetivo de este trabajo fue presentar un método simplificado altamente reproducible para la extracción de dichas células.
MATERIAL Y MÉTODOS
Obtención y transporte de la muestra
Previo consentimiento informado avalado por el Comité de Bioética de la Facultad de Estudios Superiores Iztacala se obtuvieron 36 premolares sanos, por donación de pacientes de la Clínica de Especialidades Ortodónticas Naucalpan que pertenece a la Facultad de Estudios Superiores Iztacala de la Universidad Nacional Autónoma de México. Con los criterios que a continuación se describen: se incluyeron sólo pacientes sin alteraciones sistémicas, buena salud periodontal, dientes primeros y segundos premolares, tanto maxilares como mandibulares, izquierdos y derechos. Los criterios de exclusión fueron: pacientes con enfermedades sistémicas, pacientes con gingivitis y/o enfermedad periodontal, premolares con presencia de cálculo dental y/o presencia de caries y/o con reacción periapical.
Las muestras fueron trasladas en tres mililitros de medio D-MEM (BioWest) suplementado con 1% de antibiótico (penicillin-streptomycin Gibco® No Cl. 15140-122) a 4 oC.
Las técnicas empleadas se describen detalladamente en el cuadro I, en todas las técnicas para el sembrado, se empleó D-MEM (BioWest) completo (adicionado con L-glutamina, 10% de FBS y 1% de antibiótico) y condiciones estándares de cultivo a 37 oC con presencia del 5% de CO2.
Los subcultivos fueron realizados a una confluencia del 60/80% previo lavado con solución de Hank (Sigma Aldrich) durante 30 segundos. Se agregaron 500 μL de tripsina/EDTA al 0.25%/0.1% (BioWest), durante 1-3 minutos, a una temperatura de 37 oC. Realizando los subcultivos celulares en proporción 1/3.
Ensayo para proliferación celular
Se realizaron sembrados celulares de 500 células en cajas de 24 multipocillos en la cual se sembraron por pocillo. La evaluación de la proliferación celular se realizó a 1, 3, 5, 7 y 14 días después del sembrado, mediante la adición de 50 μL de MTT (Sigma Aldrich), que se incubó durante cuatro horas a 37 oC con una atmósfera de 5% de CO2. Posteriormente se adicionaron 100 μL de dimetilsulfóxido (DMSO, Sigma Aldrich) para realizar la lectura de densidad óptica en un espectrofotómetro a una de longitud de onda de 540 nm.
Evaluación de migración celular
Con las células en confluencia se realizó una lesión a lo largo del cultivo, causando pérdida de continuidad y se monitoreó el cultivo mediante fotografías a las 24, 48 y 72 horas.
Inmunocitofluorescencia Las células fueron fijadas en tampón de fosfato de paraformaldehído al 4% durante 20 min. El bloqueo se realizó en PBS con 3% de albúmina de suero bovino y 0.01% de Tritón-X 100. Las células se tiñeron con los siguientes anticuerpos de conejo antihumano conjugado con Fluor® 647, PE TRITC, FITC y DAPI (Fluoroshield®); RUNX2, osteocalcina, CD73, CD90, CD105 y vimentina (1:250 Santa Cruz); durante 45 minutos; las muestras fueron observadas en el microscopio de fluorescencia Zeiss Axio LAB1.
Diferenciación osteogénica
Se utilizaron 105 células, se sembraron en el pasaje número 3 y se les adicionó medio "StemPro Osteogenesis Differentiation Kit" (Gibco®), que fue sustituido cada 72 horas; durante 14 días.
Tinción con rojo de alizarina
Una vez diferenciadas las células a los 7 y 14 días de cultivo fueron fijadas y teñidas con rojo de alizarina, se les realizaron tres lavados de cinco minutos con PBS Se agregaron 500 μL de rojo de alizarina 0.1% (HYCEL®) y se dejó reposar durante 15 minutos a temperatura ambiente.
RESULTADOS
Obtención de la población celular
La poca especificidad técnica de los artículos encontrados influyó para lograr la obtención de la población celular; los cultivos realizados por triplicado con cada una de las técnicas expuestas, nos condujo a obtener una concentración mínima de células que no llegaban a confluencia, en algún caso después de siete días de cultivo no se obtenían células y en alguno las pocas células obtenidas fueron susceptibles a contaminarse, probablemente por el medio de transporte del diente y los lavados.
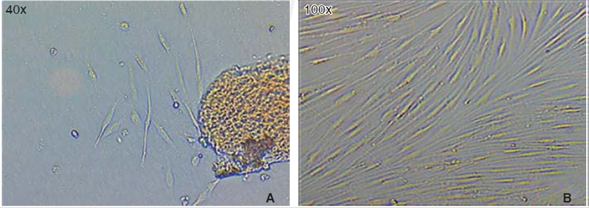
La población celular óptima para el estudio se logró obtener empleando la «técnica estandarizada digestión enzimática y cultivo de explantos». Una vez que se realizó la disección y sembrado del tejido periodontal, en las primeras 72 horas aparecieron células, que luego de 46 horas más mostraron una apariencia fibroblastoide en la periferia de los explantos cultivados llenando el plato de cultivo en un 65 a 70%, luego de esto, los explantos fueron eliminados con los lavados. A los siete días el plato de cultivo se encontraba con las células en confluencia (Figura 1).
Viabilidad y/o proliferación celular
Se realizó la evaluación de la capacidad de autorrenovación de la población celular obtenida mediante el ensayo de metiltiazoltetrazolio (MTT) 3-(4,5-dimetiltiazol-2 il)-2,5-bromuro difeniltetrazolio; la absorbancia medida por espectrofotometría es proporcional a la viabilidad/proliferación de las células.
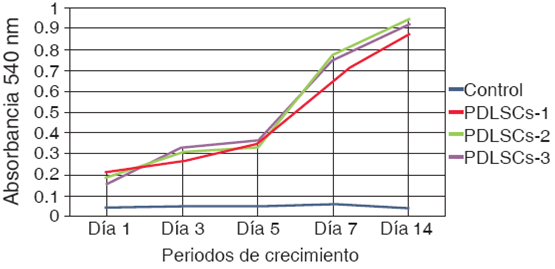
Se sembraron 500 células en cajas de 24 multipocillos se evaluaron a 1, 3, 5, 7 y 14 días; se midió la absorbancia a una longitud de onda de 540 nm; las mediciones obtenidas fueron graficadas. Se obtuvo una gráfica creciente, que corresponde a una concentración de células por la unidad de medida, demostrando así, que las células mantuvieron su proliferación durante 14 días en condiciones estándares de cultivo (Figura 2).
Capacidad de migración celular
La migración de las células hacia el área lesionada se observó a partir de las 12 horas después de realizarla, las células cubrieron entre un 10-20% del área crítica, a las 24 horas aumentó el número de células que cubrieron ya en un 40-60% la superficie del frasco de cultivo, posteriormente a las 48 horas las células se observaron en semiconfluencia y a las 72 horas las células cubrieron por completo el área, esto es observable en las imágenes (Figura 3).
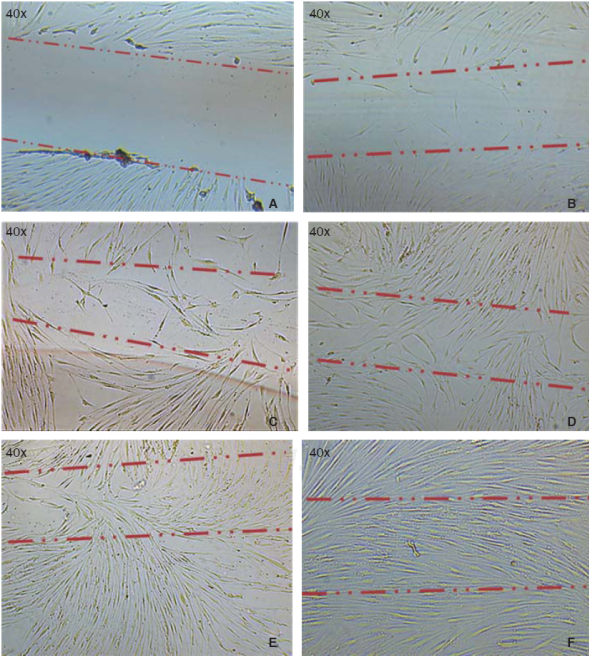
Figura 3 A) Fotografía inmediata, después de realizar la lesión en el cultivo. B) A las 12 horas después de la lesión, se observa migración de un grupo de células recolonizando del 10 al 20% de la lesión. C) A las 24 horas se observa la migración de un grupo de células recolonizando el área dañada en un 40-60%. D) y E) A las 48 horas se observa que las células han cubierto en un 80-90%. F) A las 72 horas después de la lesión, las células llegan a confluencia nuevamente.
Inmunofluorescencia
Los ensayos de inmunofluorescencia fueron realizados en el tercer subcultivo de nuestra población celular, luego de nuestro conteo, se observó expresión positiva de CD90 en más del 80% de las células; expresión positiva a CD73 en un 70%, CD105 en un 60% y vimentina en un 90% de la población (Figura 4).
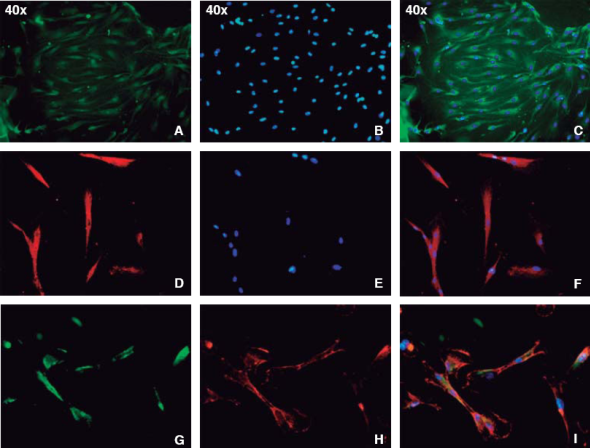
Imagen a color en: www.medigraphic.com/facultadodontologiaunam
Figura 4 Imágenes tomadas con microscopio de fluorescencia a un aumento de 40x. A) Expresión de CD90 (verde), B) DAPI nuclear (azul), y C) Fusión, D) CD73 (rojo), E) DAPI nuclear (azul), y F) Fusión, G) Vimentina (verde), H) CD105 (rojo), y I) Fusión de ambas con DAPI nuclear (azul).
Diferenciación osteogénica
Una vez inducida la diferenciación ósea, las células perdieron su morfología fibroblastoide a los siete días, y adquirieron una morfología prismática, de apariencia cuboide y menos alargada, apareció también mayor cantidad de matriz extracelular y presencia de nódulos de calcificación, que se observaron mediante la tinción de rojo de alizarina el área cultivada y observada es de 9.6 cm² (Figura 5).
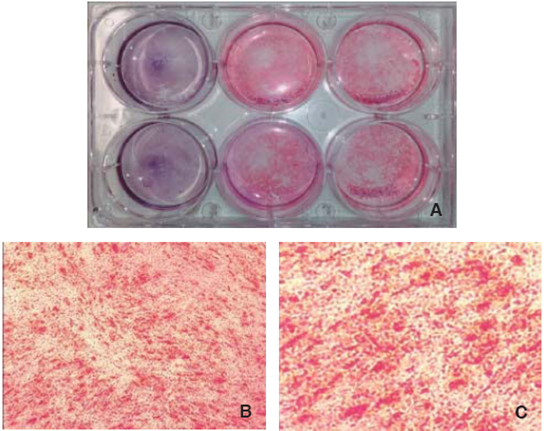
Imagen a color en: www.medigraphic.com/facultadodontologiaun
Figura 5 Tinción con rojo de alizarina. A) Fotografía macroscópica en contraste con hematoxilina de las células control e inducidas a diferenciación a 14 días. Tinción con rojo de alizarina de las células diferenciadas B) 10x y C) 40x.
RUNX2 es un factor de transcripción indispensable para la maduración ósea que fue expresado en nuestra población celular en diferenciación osteogénica a los 14 días, en al menos el 15% de las células.
La osteocalcina es una proteína secretada en la etapa tardía de la diferenciación ósea; es capaz de unirse al calcio para su estabilización; la presencia de esta molécula a los 14 días en un 90% de las células nos indica la regulación de la mineralización (Figura 6).

Imagen a color en: www.medigraphic.com/facultadodontologiaunam
Figura 6 Imágenes tomadas con microscopio de fluorescencia. A) Expresión de RUNX2, 40x (verde), B) DAPI nuclear (azul) 40x y C) Fusión 40x, D) Osteocalcina (verde) 63x, E) DAPI nuclear (azul) 63x, y F) Fusión 63x.
DISCUSIÓN
El ligamento periodontal puede ser considerado como una fuente accesible, ya que los órganos dentales son considerados tejidos de desecho una vez extraídos, y en el caso de los pacientes que están bajo tratamiento de ortodoncia, la extracción es la mejor alternativa de tratamiento.12
Como han demostrado ya, las poblaciones obtenidas del ligamento periodontal tienen la capacidad de regenerar diversos tejidos13-16 y, recientemente se ha publicado información sobre el uso del ligamento periodontal como una fuente de células troncales; sin embargo, hacía falta llegar a un consenso sobre los protocolos usados, ya que éstos pueden ser muy inconsistentes y no permiten poder comparar claramente las poblaciones celulares obtenidas,17 por ello, conocer en profundidad el mecanismo de las técnicas empleadas nos permitió sugerir este «método estandarizado» centrado en mantener la integridad de la muestra, así como evitar su contaminación.18-20 Este método de cultivo requiere de menor experticia en el manejo de los tejidos periodontales, por lo que es de fácil realización y evita posibles contaminaciones de los cultivos.
La capacidad de nuestras células derivadas de PDL para formar grupos de células clonogénicas adherentes de características similares a fibroblastos, se demostró por la formación de alrededor de 1 x 106 células generadas a partir de 1 x 103 células individuales cultivadas a baja densidad en siete días de cultivo. Esta población de células formadoras de colonias, que hemos denominado PDLSCs, mostró una alta tasa de proliferación por MTT, similar a la tasa observada por otros autores.3,8
Así, demostramos que el nuevo método mejoró, o al menos resultó efectivo para extraer una población de células semejantes a células mesenquimales del ligamento periodontal, que mostraron un perfil antigénico positivo a los marcadores de células mesenquimales, CD105, CD90, CD73 y vimentina que nos confirma su origen mesodérmico y estadio mesenquimal permiten reportar su estadio de células troncales mesenquimales.13-15,21
Las PDLSCs mostraron que pueden diferenciarse a la línea osteogénica en un tiempo igual o menor a ocho días, esto quizás se deba a su origen ectomesenquimal en armonía con lo ya mencionado por Cha Y. y cols. que se trata de una población celular que se diferencia22 expresando marcadores osteogénicos como: RUNX2, OCN y la formación de nódulos de mineralización.15











 text in
text in