Introducción
La inmunoterapia ha resurgido con fuerza y gran relevancia en los últimos años en el tratamiento de tumores sólidos. La cirugía, radioterapia y quimioterapia, intervenciones clásicas en el tratamiento del cáncer, se han fortalecido con la llegada de la terapia dirigida y la inmunoterapia.
El cáncer de próstata (CP) constituye uno de los principales cánceres en hombres y representa el segundo lugar en incidencia (1.4 millones nuevos casos), siendo el de mayor prevalencia en el mundo (3,724,658 casos). Este panorama es muy similar para nuestro país (27,096 nuevos casos)1-3.
Tanto la incidencia como la mortalidad del CP se correlacionan con la edad, en general con una edad promedio al momento del diagnóstico de 66 años. La dieta y la actividad física desempeñan un rol importante en el desarrollo y progresión del CP. Los factores dietéticos se asocian principalmente con una dieta abundante en grasas y algunas diferencias étnicas observadas en las tasas de incidencia de CP4-7.
La zona periférica de la próstata, que constituye hasta un 70% de la glándula en adultos jóvenes, y rodea la mayor parte de la zona central extendiéndose caudalmente para rodear parcialmente la porción distal de la uretra, representa el sitio más común para el desarrollo de carcinomas de próstata (70-75%). La zona de transición es una región glandular adicional más pequeña que rodea la uretra prostática, constituye hasta el 5% de la glándula en adultos jóvenes y es el sitio donde se origina principalmente la hiperplasia prostática benigna8.
En comparación con los cánceres de la zona periférica, se ha sugerido que los carcinomas que se originan en la zona de transición tienen un potencial maligno menor, sin embargo otros estudios han sugerido que no existe tal diferencia9,10.
Inflamación crónica en la carcinogénesis del cáncer de próstata
La arquitectura histológica de la próstata sufre constantes cambios relacionados con la edad, que continúan durante toda la vida11. Estos cambios podrían deberse a una alteración de la acción androgénica y a procesos inflamatorios que conducen a un efecto trófico constante en la glándula y a una inflamación crónica.
Existe la posibilidad que este daño epitelial constante durante el proceso de envejecimiento, asociado con la acción androgénica para regular la función de la próstata produzca un efecto tal, que tenga que ver más con una función de reparación crónica de «heridas» por la misma glándula, que con el paso del tiempo pueda favorecer el proceso de oncogénesis12.
La inflamación es una respuesta biológica estrictamente regulada y coordinada cuya finalidad es eliminar estímulos nocivos (patógenos, sustancias irritantes o células dañadas), lo que permite restablecer la homeostasis de los tejidos y órganos.
Por sí misma la inflamación no es sinónimo de infección, ya que existen otros estímulos que pueden desencadenar este proceso. Sin embargo, cuando ocurre un daño o lesión en cualquier parte de nuestro cuerpo, se desencadena una respuesta fisiológica como un mecanismo de defensa para detener o limitar el daño y reparar el tejido, el sistema inmunitario tiene una participación vital en este proceso.
En lo que respecta a la inflamación aguda, se observa una respuesta óptima en tiempos cortos, que favorece la reparación de los tejidos y a la homeostasis una vez que se elimina la causa que dio origen a este proceso. En contraste, la inflamación crónica es un proceso prolongado y sin regulación que ejemplifica el esfuerzo y falla de nuestro organismo para eliminar estímulos nocivos.
El mantenimiento de la integridad de las barreras epiteliales como la epidermis y las mucosas es fundamental, el daño conduce al desarrollo de múltiples patologías, todas ellas tienen como respuesta de inicio la inflamación. El reflujo de orina hacia la próstata o la formación de cuerpos amiláceos pueden alterar el epitelio de la próstata. Esto da origen al establecimiento de un mecanismo de retroalimentación persistente que conduce a un estado inflamatorio crónico13.
El sistema inmunitario está compuesto de múltiples poblaciones celulares, con diferentes proteínas en su membrana celular y citoplasma, las cuales funcionan como sistemas de alarma capaces de reconocer patrones moleculares asociados a daño (DAMP), así como patrones moleculares asociados a patógenos (PAMP), lo que permite iniciar la respuesta inflamatoria e inmunitaria.
Tanto las células epiteliales como las del estroma en la próstata expresan PAMP como TLR 2, 3 y 4, los cuales desencadenan una señalización río abajo que conduce a la secreción de interleucina 1 (IL-1), IL-5, IL-6, IL8 y CXCL10, que favorece el reclutamiento de leucocitos, así como la expresión de CD80, CD86, CD40 y CD134L en células del estroma de la próstata. Todo esto conlleva una posible activación de linfocitos T en el tejido prostático, lo que a su vez contribuye al establecimiento de un proceso inflamatorio crónico si no existe una regulación de este proceso14,15.
En conjunto, la prostatitis causada por agentes infecciosos (bacterias grampositivas y gramnegativas), por el reflujo de orina en los conductos prostáticos, por los cambios hormonales o el estilo de vida, pueden detonar un proceso de inflamación crónica con un potencial riesgo para el desarrollo de CP. Por supuesto, en el proceso de carcinogénesis el eje neuroinmunoendocrino, el estado energético y metabólico de las células, así como el microbioma, tienen un rol determinante en el inicio y desarrollo del tumor.
Desarrollo del cáncer de próstata y respuesta inmunitaria
Los factores que desencadenan el inicio, desarrollo y progresión del CP y el rol del sistema inmunitario en este proceso son bastante complejos. Como en otros tipos de cáncer, el CP se origina a partir de una acumulación de alteraciones genéticas y epigenéticas. Se han descrito fusiones y deleciones en los genes ERG y ETV1, lo que favorece la activación de la vía ETS16, deleciones y mutaciones en el gen APC, así como ampliaciones en el gen AR que favorecen la activación de la vía WNT, los procesos de proliferación, migración y finalmente la progresión del cáncer17.
La edad, la etnia y la historia familiar son factores de riesgo asociados al desarrollo del CP. Sin embargo, aunque importantes, no son determinantes, ya que numerosas líneas de investigación señalan a la inflamación como factor desencadenante de la carcinogénesis prostática y progresión del tumor18. La inflamación podría tener un rol determinante en la próstata, que en conjunto con el eje hormonal (andrógenos-estrógenos), actúen como detonantes carcinogénicos.
Las infecciones, reflujo de la orina, traumas físicos, químicos y dieta pueden conducir a la ruptura de la homeostasis inmunitaria y al desarrollo de un proceso autoinmune en la próstata, con una perpetuación del proceso inflamatorio y conducir a la formación del cáncer19.
Las células del sistema inmunitario presentes en el tracto genitourinario son consideradas parte del sistema inmunológico de las mucosas. En próstata existen células del sistema inmunitario en el compartimento estromal e intraepitelial. La mayor concentración se encuentra en el estroma, donde se localizan células T CD4, macrófagos, mastocitos y células B principalmente, y una pequeña población de células T y δ. En el compartimento intraepitelial se localizan células T CD8, esto sugiere que estas células son la primera línea de defensa contra agentes extraños presentes en el lumen, también se han observado células T reguladoras, células NK, células dendríticas (CD) CD11c y algunos linfocitos B20.
Conforme se envejece, se incrementa el infiltrado inflamatorio. Como sucede en algunos tumores, es probable que un proceso de inmunoedición se lleve a cabo en el epitelio prostático, ya sea como consecuencia de daño de tipo oxidativo y nitrosativo de las propias células prostáticas o células inmunitarias, todo ello en respuesta a un proceso inflamatorio, ya sea de origen infeccioso o no. Esto facilitaría la proliferación de las células epiteliales que podrían adquirir un fenotipo de «célula madre» y con el tiempo sufrir daño en su genoma (metilación, acortamiento de telómeros) incrementando su inestabilidad genética y conduciendo a la activación de factores de transcripción oncogénicos y pérdida de genes supresores de tumores dando lugar a la formación de una neoplasia intraepitelial y la formación del CP.
No se comprende en detalle el por qué y con qué frecuencia se incrementa la población de leucocitos en próstata. Se ha documentado que la mayoría del tejido prostático resecado muestra en mayor o menor medida signos de un proceso inflamatorio. También existen diferencias claras con respecto al infiltrado de células inmunitarias tanto en próstata normal, como en procesos inflamatorios o en CP21,22.
En particular, en la hiperplasia prostática existe un incremento importante de células T en comparación con próstata normal, con una reducción importante del infiltrado de células T en adenocarcinoma23, posiblemente existe una respuesta inicial de tipo celular que posteriormente en cáncer refleja un proceso de evasión e inmunosupresión, por medio de mecanismos mediados por las células tumorales y el microambiente establecido en el sitio del tumor.
En la atrofia inflamatoria proliferativa y en la hiperplasia benigna de la próstata también se ha observado un infiltrado de células T activadas, que, junto con los macrófagos, mastocitos, células B, fibroblastos y células NK secretan MIC-1, IL-6, IL-8, IL-13, IL-17 y factor de crecimiento de fibroblastos-2, que contribuyen a perpetuar el proceso inflamatorio, dando lugar a cambios importantes en la estabilidad genética de las células y posterior desarrollo tumoral. Todo lo anterior sugiere que la inflamación y la respuesta inmunitaria tienen un rol como desencadenantes en las enfermedades prostáticas. En particular en hiperplasia prostática benigna la activación crónica de tipo inflamatorio de las células inmunitarias juega un rol fundamental24,25.
En algunos tipos de cáncer como el colorrectal se puede realizar una puntuación inmunológica de acuerdo con el infiltrado de células inmunitarias y correlacionar con buena o nula respuesta a tratamiento26. El CP se considera un tumor frío27, con poco infiltrado de células inmunitarias. Además, existe una fuerte actividad metabólica supresora28, que junto con la presencia de células T reguladoras en el sitio del tumor12,29-31 contribuye a la creación de un microambiente hostil para las células T efectoras. Otro mecanismo asociado incluye la alteración en la presentación de antígenos a las células T citotóxicas mediante la disminución de la expresión del MHCI32.
Se ha descrito una reducción de células B vírgenes, con una pobre activación de las CD, lo cual afecta la presentación antigénica y favorece el escape a la respuesta inmunitaria21, por otra parte, un alto infiltrado de macrófagos M1 y baja infiltración de mastocitos se relaciona con una supervivencia mayor en pacientes con CP21.
Las células NK de pacientes con CP son capaces de reclutar monocitos induciendo su polarización a macrófagos hacia un fenotipo M233. También se ha observado una baja frecuencia de células NK en el tejido prostático tumoral caracterizadas con un fenotipo inmaduro, nula actividad citotóxica y con abundante secreción de TGFβ134. Concentraciones importantes de IL-6 se han asociado con el inicio, progresión y recurrencia del CP, además esta citocina promueve el crecimiento de células tumorales en modelos in vitro e in vivo35-37.
Un incremento de células supresoras de origen mieloide de la estirpe monocito en sangre periférica de pacientes con CP se correlaciona con otros factores de pronóstico negativo para este cáncer como lactato deshidrogenasa, fosfatasa alcalina, antígeno prostático específico (PSA) y anemia38.
Inmunoterapia en cáncer de próstata
En caso de sospecha de CP, la biopsia de tejido sigue siendo el estándar para el diagnóstico. La identificación y caracterización del tumor y una mejor estratificación del riesgo se pueden hacer con otras herramientas y estudios. De acuerdo con el diagnóstico, diferentes opciones de tratamiento existen desde la vigilancia activa, la cirugía y la radiación siguen siendo los tratamientos curativos para la enfermedad localizada, pero con efectos adversos en aparato urinario.
La terapia de privación androgénica (TPA) sigue siendo el estándar actual de atención para el tratamiento inicial de los pacientes con CP metastásico39. En 2018, la Food and Drug Administration (FDA) aprobó la adición de abiraterona con prednisona a TPA para el CP sensible a la castración (CSPC) recién diagnosticado40. Además, la quimioterapia (docetaxel) añadida a la TPA también es una opción terapéutica para el CSPC metastásico41. Sin embargo, con el tiempo, todos los pacientes con CSPC progresan a un CP resistente a la castración (CRCP). Las terapias aprobadas actualmente para el CRPC metastásico incluyen abiraterona, enzalutamida, radio-223, Sipuleucel-T y quimioterapia que incluye docetaxel y cabazitaxel, la mediana de supervivencia en estudios recientes de fase III oscila entre 12.2 y 21.7 meses42-46. El desarrollo de resistencia a las terapias hormonales y la quimioterapia indica la necesidad de desarrollar nuevos enfoques terapéuticos47, y la inmunoterapia es una alternativa en el tratamiento de CP.
La historia de la inmunoterapia inicia hace unos 3,000 años en el antiguo Egipto y continúa hasta principios del siglo XIX, donde se describe la desaparición de tumores de manera espontánea o posterior a un proceso infeccioso caracterizado por estado febril48. Los primeros intentos con base científica para modular el sistema inmunitario en pacientes con cáncer se pueden atribuir a Fehleise y Busch49,50, ambos observaron de manera independiente una regresión significativa del tumor después de la infección por erisipela, Fehleisen logró identificar adecuadamente la cepa de bacteria responsable de la erisipela (Streptococcus pyogenes).
El avance significativo fue gracias a William Bradley Coley, quien intentó utilizar el sistema inmunitario para tratar el cáncer de hueso; en 1891 observó que algunos pacientes con cáncer entraban en remisión espontánea después de desarrollar erisipela. Coley comenzó a inyectar diferentes mezclas de Streptococcus pyogenes y Serratia marcescens vivos o inactivados en los tumores de sus pacientes51, así comienza la inmunoterapia en cáncer.
La inmunoterapia contra el cáncer puede ser activa o pasiva. La inmunoterapia activa (vacunación e inmunomoduladores) actúa sobre las células cancerosas mediante la activación de células inmunitarias endógenas que reconocen antígenos tumorales o regulando la respuesta inmunitaria contra tumor mediante su acción en diferentes dianas presentes en las células inmunitarias. La presencia de antígenos asociados a tumor entre ellos: el PSA, el antígeno prostático específico de membrana (PSMA), el antígeno prostático de células madre (PSCA) y la fosfatasa de ácido prostático (PAP), mucina-1 (MUC-1) y el antígeno de cáncer de testículo NY-ESO-1, sugieren que el CP podría ser inmunogénico52, esto abre un campo de oportunidad y nuevas perspectivas en la inmunoterapia del CP. Así mismo, la terapia pasiva incluye la terapia adoptiva (células presentadoras de antígeno [APC] o linfocitos T, generalmente). Y la utilización de anticuerpos dirigidos contra diferentes blancos moleculares (Fig. 1).
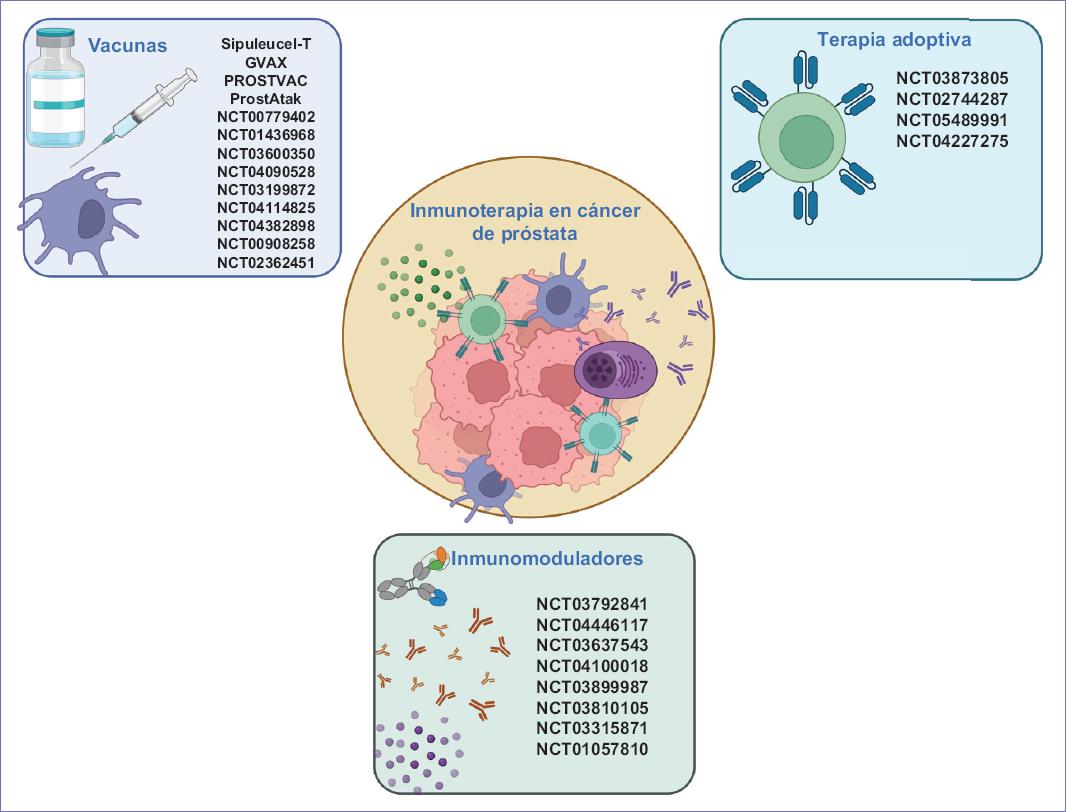
Figura 1 Inmunoterapia en cáncer de próstata. Los datos son extraídos de los estudios evaluados. NCT: National Clinical Trial Identification Number.
Las células T efectoras en pacientes con CRPC responden a los antígenos asociados a tumor (TAA) de próstata53 y datos preclínicos muestran que la respuesta puede ser específica de órgano54. Otro hallazgo interesante en CP es la presencia de linfocitos CD4 + y CD8 + infiltrantes de tumor que se expanden oligoclonalmente, lo que sugiere una estimulación antigénica55.
Las «vacunas» diseñadas para estimular células inmunitarias y destruir células de CP se basan en utilizar TAA específicos. Se pueden clasificar en aquellas que se preparan ex vivo (Sipuleucel-T), las que utilizan vectores (PROSTVAC) y las que emplean células tumorales completas (GVAX).
Sipuleucel-T
La vacuna Sipuleucel-T utiliza el proceso de presentación antigénica, las células mononucleares de sangre periférica del paciente, incluidas las APC, se activan ex vivo con una proteína de fusión recombinante (PAP fusionada con GM-CSF [factor estimulante de colonias de granulocitos y macrófagos]) y las APC se administran al paciente. El mecanismo de acción preciso no se conoce, sin embargo, probablemente las APC estimulan la respuesta inmunitaria mediada por células T contra PAP, antígeno que se expresa de manera importante en las células de CP. Sipuleucel-T es un ejemplo de vacuna de CD personalizada y procesada ex vivo contra el CP56. Esta estrategia ha mostrado que prolonga la supervivencia 4.5 meses en hombres con CRPC57. Por otra parte, NCT00779402 es un estudio multicéntrico fase III doble ciego que tuvo como propósito evaluar el efecto de Sipuleucel-T en pacientes con CP no metastásico posterior a prostatectomía radical. Los pacientes recibían terapia hormonal posterior a la cirugía y después eran aleatorizados a recibir Sipuleucel T o placebo, comparando la incidencia de recurrencia bioquímica. En este escenario, la incidencia de recurrencia no difirió significativamente entre Sipuleucel T y placebo58. Sin embargo, varios estudios clínicos fase II han demostrado seguridad en la combinación de Sipuleucel T con otras estrategias como quimioterapia y terapia hormonal, lo cual podría determinar su uso como adyuvante en futuros estudios de fase III58.
GVAX
GVAX es una vacuna polivalente compuesta de dos células de CP: las células LNCaP dependientes de andrógenos y células PC3 resistentes a andrógenos, estas células son irradiadas y transfectadas con GM-CSF. Esta citocina actúa en el sitio de administración para potenciar la activación de APC e induce un incremento en la capacidad de presentación antigénica sobre células T (CD4+ y CD8+) y células B59.
Los estudios de fase I/II establecieron una buena seguridad para GVAX en CSPC y CRPC mostrando respuestas prometedoras, ya que redujeron los niveles de PSA60, posteriormente se realizaron dos estudios de fase III que incluyeron docetaxel. El ensayo de fase III VITAL-1 comparó directamente GVAX (cada 15 días durante las primeras 26 semanas, luego mensualmente) vs. docetaxel cada tres semanas más prednisona. La población de estudio incluyó hombres con CPRC que no habían recibido quimioterapia previa. Este ensayo se cerró debido a que existían pocas posibilidades de alcanzar el criterio de valoración principal (mejoría de la supervivencia), sin embargo se observaron indicios de la eficacia de la vacuna. La supervivencia media fue de 20.7 meses con GVAX y 21.7 meses con docetaxel/prednisona (p = 0.78). Es de destacar que los eventos adversos de grado 3/4 fueron menos frecuentes con GVAX (8.8 frente a 43%) de los que recibieron docetaxel61,62. Se siguen evaluando tanto GVAX autólogas (específicas del paciente) como las alogénicas (no específicas del paciente) como agentes únicos o en combinación con otras estrategias inmunomoduladoras.
PROSTVAC
Esta vacuna utiliza poxvirus recombinantes que expresan PSA, además de tres moléculas coestimuladoras LFA-3, ICAM-1 y B7.1 (TRICOM) para estimular la respuesta inmunitaria. Con esta vacuna se incitan las respuestas de células T específicas para PSA. A pesar de mostrar un beneficio en la sobrevida global a 8.5 meses, el ensayo de fase II con esta vacuna no demostró beneficio en la supervivencia libre de progresión en el CRPC metastásico que era su principal criterio de valoración63. En consecuencia, el ensayo de fase III, PROSPECT, se realizó para investigar más a fondo estos hallazgos, pero no logró demostrar un beneficio en la sobrevida global64.
ProstAtak
Otra estrategia terapéutica es la utilización de un vector adenoviral que contiene el gen de timidina cinasa del virus del herpes (AdV-tk), esta vacuna se aplica vía intratumoral. Las células tumorales transducidas expresan timidina cinasa, que convierte un profármaco administrado sistémicamente (valciclovir o ganciclovir) en un análogo de nucleótido que es tóxico para las células tumorales. El profármaco activado induce la muerte celular y esto desencadena una muerte celular inmunogénica mediante la liberación en el microambiente de DAMP y TAA, lo cual desencadena la maduración y activación de CD y linfocitos B. En consecuencia se lleva a cabo la presentación y activación de células T y una retroalimentación entre estas células, promoviendo una respuesta inmunitaria contra el tumor59.
En un ensayo de fase I/II65 se encontró que la terapia AdV-tk combinada con radioterapia reducía significativamente la tasa de recurrencia en pacientes con CP, en particular en aquellos con enfermedad de riesgo intermedio-alto. Se ha comenzado con un ensayo controlado aleatorizado de fase III (NCT01436968)58 que pretende evaluar la efectividad de la inmunoterapia ProstAtak en combinación con radioterapia en pacientes con CP localizado de riesgo intermedio-alto. Se espera que ProstAtak pueda mejorar el resultado clínico de los pacientes con CP.
Otra vacuna que se evalúa en CP contiene ADN plasmídico que codifica PAP y podría tener una acción inmunoestimuladora contra tumor. Una vez administrada la vacuna puede estimular la respuesta inmunitaria para generar una respuesta específica de linfocitos T citotóxicos contra células de CP que expresan este antígeno. Se han realizado varios estudios con resultados alentadores66. El NCT03600350 es un estudio fase I/II donde se utiliza la combinación de la vacuna de ADN pTVG-HP junto con nivolumab con el objetivo de mejorar la respuesta contra tumor, se determina la eficacia de esta combinación para disminuir el PSA en suero en pacientes con CP sin castración y no metastásico (estadio clínico D0/M0)58. El NCT04090528 es un ensayo fase II donde se evaluará pTVG-HP (PAP) y pTVG-AR (receptor de andrógenos) solos o combinadas junto con pembrolizumab. El objetivo es determinar la respuesta de células T CD8+ contra tumor tras la administración de estas dos vacunas y el bloqueo de PD-158.
Otra vacuna que se está evaluando en CP consiste en la administración al paciente de RV001, que actúa de manera específica sobre RhoC, una proteína sobreexpresada en las células metastásicas de cáncer; se administra vía subcutánea, el antígeno se encuentra con las CD que lo capturan y procesan, para después realizar la presentación antigénica. Se generan células T CD8+ y CD4+ específicas, estableciéndose una respuesta contra células que sobreexpresan RhoC (células tumorales metastásicas). Esto es importante, ya que RhoC puede potenciar la capacidad metastásica de la célula tumoral (NCT03199872)67. Una ventaja de RV001 es que está dirigida para células cancerosas metastásicas y para las metástasis en formación temprana.
El NCT04114825 es un estudio de fase II en el cual se estudia la respuesta inmunitaria contra tumor en pacientes varones adultos con un diagnóstico histológico anterior de adenocarcinoma de próstata y una recurrencia bioquímica (BCR) dentro de los tres años posteriores a la prostatectomía radical (PR) o RT definitiva y sin metástasis a distancia o recurrencia locorregional58.
Otra estrategia en desarrollo son las vacunas de ARNm. En el ensayo clínico NCT04382898 se evalúa la vacuna W_pro1 que consiste en ARNm dirigido a cinco antígenos expresados en CP de novo y metastásico. Las moléculas de ARN son optimizadas para darles una mayor estabilidad, eficiencia de traducción y presentación en moléculas del complejo mayor de histocompatibilidad (MHC) clase I y II, se administra por vía I.V. Es un ensayo multicéntrico fase I/II donde se evalúa la seguridad, tolerabilidad, inmunogenicidad y eficacia preliminar de la vacuna en monoterapia o en combinación con cemiplinab58.
La TARP (proteína del marco de lectura alternativo del receptor de células T gamma) es un antígeno asociado a tumores expresado en más del 90% de carcinomas de próstata y el 50% de carcinomas de mama68, por lo que representa un potencial blanco terapéutico. En un ensayo piloto con TARP (NCT00908258) en pacientes con CP se realizó la caracterización de las CD utilizadas en la vacuna, los datos muestran que las CD tienen una menor expresión de genes implicados en la tolerancia inmunitaria y son capaces de inducir una fuerte respuesta inmunitaria específica de antígeno69. El NCT02362451 es un estudio de fase II donde se evalúa la efectividad de una vacuna dirigida contra TARP, así como el cambio en los niveles de PSA durante el tratamiento y su efecto en la incidencia de recurrencia entre los participantes58, la ventaja aparente de esta vacuna es que se utiliza la totalidad de la proteína TARP, con la potencial inducción de una respuesta anti-TARP multivalente. Además, los péptidos sintéticos más largos incluyen la generación de mejores respuestas mediadas por linfocitos T CD8 y células B.
Células T
Las células T utilizadas en las terapias de células CAR-T se modifican en el laboratorio para que puedan identificar células cancerosas específicas, para ello se adiciona un receptor artificial (llamado receptor quimérico de antígenos o CAR), que identifica un antígeno especifico en la célula tumoral. En este sentido, las células T modificadas para reconocer específicamente PSCA fueron capaces de lisar células de CP que expresaban PSCA70.
Se están llevando a cabo ensayos clínicos con esta estrategia. El NCT03873805 es un ensayo de fase I que estudia los efectos secundarios y la mejor dosis de células T CAR-PSCA en el tratamiento de pacientes con CP resistente a la castración con metástasis y antígeno PSCA+58. Otro estudio de fase I/II es el NCT02744287, que determina la seguridad, así como la actividad contra tumor de células CAR-T BPX-601 en pacientes con tumores sólidos avanzados (pancreáticos y de próstata) tratados previamente y que expresan niveles altos de PSCA58. Otros estudios realizados sobre otros antígenos son el caso del NCT05489991, estudio de fase I/II que evalúa la dosis y el régimen de células T-CAR PSMA apropiado en pacientes con CP metastásico posterior a linfodepleción, y el NCT04227275 un estudio de fase I en pacientes con CP metastásico resistente a la castración donde células T autólogas son modificadas genéticamente para reconocer PSMA expresado en las células tumorales58.
Inmunoreguladores
La activación de células T mediante el uso de anticuerpos permite bloquear o activar receptores reguladores expresados en estas células, lo cual parece ser suficiente para provocar la regresión de algunos tumores. En este caso los anticuerpos están dirigidos a las células de respuesta inmunitaria, por lo tanto, no son necesariamente específicos de ningún tipo de cáncer. Por supuesto algunos tipos de tumores responden mejor a este tipo de terapia, por lo cual hay que utilizarlos en el contexto terapéutico adecuado. Diversos ensayos clínicos se están realizando para buscar el mejor escenario para su uso individual o combinado, minimizar sus efectos adversos, determinar momento de intervención y duración de la terapia que son aspectos muy importantes que considerar para su eventual éxito.
El NCT03792841 es un estudio para evaluar la seguridad y tolerabilidad de AMG 160 (HLE BiTE®, del inglés half-life extended bispecific T-cell engager) que se une a PSMA expresado en células de CP y a células T, de esta manera se dirige la actividad citotóxica de células T contra células que expresan PSMA (células de cáncer), esto favorece la activación de células T58. Esta terapia se estudia como monoterapia o en combinación con pembrolizumab en pacientes con CP metastásico resistente a la castración (CRPCm).
El NCT04446117 es un estudio de fase III, multicéntrico, aleatorizado, diseñado para evaluar la seguridad y eficacia de cabozantinib que es un inhibidor de la tirosina cinasa c-Met, VEGFR2 y también inhibe AXL y RET, en combinación con atezolizumab, anticuerpo monoclonal dirigido contra PD-L1 vs. una segunda terapia hormonal nueva (NHT) en hombres con CRPCm que han sido tratados previamente con una NHT para su enfermedad de CP58.
El NCT03637543 es un ensayo clínico fase II que estudia la seguridad y eficacia de nivolumab (anticuerpo que bloquea al receptor de muerte programada 1 [PD-1]). Se evalúa si el nivolumab tiene alguna actividad en pacientes que tienen un PSA en aumento después de someterse previamente a una cirugía o radiación y si esta terapia tiene un efecto mayor en una etapa más temprana del curso de la enfermedad, antes de que los pacientes reciban terapias hormonales58.
El NCT04100018, un estudio de fase III, tiene como propósito valorar la seguridad y eficacia de nivolumab con docetaxel en hombres con CP avanzado resistente a la castración con recaída después de la terapia hormonal de segunda generación58.
El NCT03899987 es un ensayo clínico fase II que determina el efecto de la aspirina y el rintatolimod (fármaco inmunomodulador) con o sin interferón-a 2b en el tratamiento de pacientes con CP.
El NCT03810105 es un estudio de fase II donde se analiza si la combinación de olaparib (inhibidor de la enzima poliADP ribosa polimerasa) y durvalumab (anticuerpo monoclonal anti-PD-L1) es mejor que el estándar de atención para el tratamiento de CP no metastásico bioquímicamente recurrente sensible a la castración58. Otro estudio fase II es el NCT03315871, un estudio de inmunoterapia combinada en CP bioquímicamente recidivante.
El NCT01057810 es un estudio de fase III que determinó el efecto del anticuerpo anti-CTLA4 ipilimumab en supervivencia y progresión de la enfermedad de pacientes con CP metastásico que no habían recibido quimioterapia. El grupo tratado con ipilimumab demostró una disminución significativa del riesgo de progresión (hazard ratio [HR]: 0.67), así como una disminución de la quimioterapia (HR: 0.65) comparada con placebo después de 57 meses de seguimiento58.
Conclusiones
La inmunoterapia ha resurgido con nuevo ímpetu, como una herramienta novedosa en la terapia del cáncer. Tiene el potencial para incrementar la respuesta inmunitaria contra el tumor. Diversos ensayos clínicos están evaluando estas interrelaciones entre células inmunitarias y células tumorales que se establecen en el microambiente tumoral y sus efectos sistémicos, lo que permitirá diseñar nuevas estrategias terapéuticas, sus resultados ofrecerán información valiosa para su correcta aplicación por si solos y como adyuvantes en la terapia del CP. Se han dado los primeros pasos para ganar esta ardua batalla contra el cáncer utilizando como punta de lanza la inmunoterapia.











 text new page (beta)
text new page (beta)


