Antecedentes
El incremento en la prevalencia de las enfermedades respiratorias de etiología alérgica, como el asma y la rinitis, ha condicionado el desarrollo de diferentes modalidades terapéuticas que abarcan las siguientes áreas: medidas preventivas, manejo farmacológico y tratamiento etiológico con inmunoterapia específica con alérgenos (ITA). Esta última consiste en la aplicación de dosis gradualmente incrementadas de extractos alergénicos y es considerada como la única medida terapéutica que tiene la capacidad de modificar el curso de la enfermedad alérgica.1,2,3,4,5,6,7,8
La ITA promueve el desarrollo de mecanismos efectores que conllevan hacia la inmunotolerancia, lo que implica cambios en la respuesta específica por parte de los linfocitos T (LcT), B (LcB) y en los umbrales de activación de las células efectoras. Entre los efectos inmediatos observados desde la primera inyección se encuentra la supresión relacionada con la degranulación de mastocitos y basófilos, así como el incremento progresivo de interleucina (IL) 10, acompañado a su vez por disminución en la reacción tardía inducida por el alérgeno. Los aumentos en la producción de IL-10 y la regulación de la respuesta tardía se continúan secuencialmente por la acentuación de los niveles séricos de inmunoglobulina (Ig) G4 entre la sexta y octava semana posterior a la administración de ITA, alcanzando un pico máximo a las 16 semanas junto con la supresión de la respuesta temprana.
Inicialmente se pensó que la función de los anticuerpos IgG era solo bloquear la activación de los mastocitos y basófilos compitiendo con la IgE por los alérgenos. Recientemente se ha propuesto que la IgG4 puede inhibir la presentación de antígenos alergénicos mediada por CD23 a los LcT. La ITA induce un estado de tolerancia alergénica alterando la memoria alérgeno-específica, así como la respuesta de los LcT y B hacia los alérgenos, con la participación de los linfocitos T reguladores (LcTreg) y de la IL-10. Se sabe que la ITA logra inducir el desarrollo y activación de LcTreg CD4+ CD25+ productores de IL-10 con capacidad reguladora, por lo que la estimulación de LcTreg es considerada el evento cardinal de la inmunoterapia. Además, se ha demostrado que se produce un incremento inicial de IgE sérica específica durante los primeros meses del tratamiento procediendo con un descenso subsecuente y gradual de la misma tras su administración de forma prolongada. De este modo, la ITA cumple una importante función en el tratamiento de la patología alérgica modulando al sistema inmunitario, reduciendo la gravedad clínica de la enfermedad, modificando la necesidad de tratamiento farmacológico e, incluso, previniendo nuevas sensibilizaciones.2,9,10,11,12,13
La eficacia clínica de la inmunoterapia subcutánea con alérgenos (ITSC) puede ser valorada con parámetros clínicos mediante el uso de cuestionarios validados, tal es el caso del Control of Allergic Rhinitis and Asthma Test (CARAT) que permite objetivar numéricamente el control de los síntomas de rinitis o asma, habiéndose demostrado confiable y sensible al cambio en el control de los síntomas con el paso del tiempo.14,15 En cuanto a la evaluación de la seguridad de la ITSC, una de las escalas útiles es el método Portnoy, herramienta que valora las reacciones adversas asociadas con la ITA mediante una puntuación del 0 al 6, asignando un valor numérico a las reacciones adversas tanto locales como sistémicas acorde con su gravedad.
Se ha reportado asociación significativa entre la presencia de reacciones adversas locales múltiples, así como de eventos sistémicos previos con el riesgo de cursar con efectos adversos sistémicos tanto en la fase de inducción como en la de mantenimiento, por lo que se sugiere seguimiento estrecho del paciente que manifieste este tipo de reacciones adversas.16,17,18 Tomando en cuenta los distintos antecedentes previamente comentados, la Guía Mexicana de Práctica Clínica de Inmunoterapia 2011 refiere que la duración de la inmunoterapia debe mantenerse el tiempo suficiente para obtener eficacia clínica a largo plazo, aun después de haber interrumpido el tratamiento. Se menciona también que la fase de mantenimiento, determinada por la dosis mensual efectiva de extractos alergénicos que disminuya los síntomas y la necesidad de medicamentos sin reacciones adversas, tiene mayor eficacia a mayores dosis de los alérgenos administrados, con una calidad de evidencia alta.18 Justificamos el desarrollo de la presente investigación, dando seguimiento a los resultados de un reciente estudio publicado sobre la seguridad y eficacia de los efectos clínicos inmediatos presentados durante la fase de inducción del esquema de ITA utilizado en el Hospital Universitario de Puebla, siendo de sumo interés conocer que los efectos clínicos tardíos derivados de los múltiples mecanismos inmunológicos producidos por la administración del tratamiento durante el primer año, se mantienen a lo largo de la fase de mantenimiento, momento en que el paciente se encuentra aplicándose dosis altas de alérgenos y con una menor o nula necesidad de medicamentos.
Métodos
Se realizó un estudio longitudinal, secuencial, analítico, cuasiexperimental y prolectivo. Se incluyeron los pacientes del proyecto de investigación Eficacia y seguridad de inmunoterapia subcutánea para alérgenos inhalables en pacientes con alergia respiratoria del Servicio de Alergia e Inmunología Clínica del Hospital Universitario de Puebla, Puebla, con edades comprendidas entre cuatro y 65 años, de uno y otro sexo, en un periodo de tiempo de 12 meses, con diagnóstico de asma o rinitis alérgica, con evidencia de sensibilización a aeroalérgenos mediante pruebas de punción cutánea o IgE sérica específica y que aceptaron iniciar tratamiento con inmunoterapia subcutánea, utilizando extractos alergénicos mexicanos de Allergomex®, tanto para las pruebas cutáneas como para la ITA.
La evaluación de la eficacia se realizó en términos de la modificación favorable y significativa de la puntuación de control clínico del cuestionario CARAT, mientras que la seguridad se evaluó mediante el cuestionario de reacciones adversas de Portnoy.
Se realizaron las mediciones al inicio del tratamiento con ITA y después bimensualmente hasta completar un año de seguimiento, calculando comparación de promedios por prueba t de Student, considerando al valor de p < 0.05 como estadísticamente significativo.
El presente trabajo estuvo orientado por el Reglamento para Investigación en Seres Humanos, derivado de la Ley General de Salud en Materia de Investigación para la Salud de los Estados Unidos Mexicanos y la Declaración de Helsinki de la Asociación Médica Mundial. El protocolo de investigación fue revisado y autorizado para su ejecución por el Comité de Ética en Investigación del Hospital Universitario de Puebla, y se obtuvo consentimiento informado firmado por parte de todos los pacientes o tutores legales.
Resultados
Se incluyeron 47 pacientes, que constituyeron una muestra suficiente posterior al cálculo de la estimación de una media, ajustada a una proporción máxima de 20 % de pérdidas. Del total de la muestra, 37 (78.7 %) fueron mujeres. La edad promedio fue de 29.8 ± 16.6 años. El 23.4 % (n = 11) de los pacientes presentó diagnóstico de asma y rinitis alérgica, mientras que 76.6 % (n = 36) cursó únicamente con diagnóstico de rinitis alérgica. Los promedios de las puntuaciones del cuestionario CARAT inicial y bimensuales se muestran en la Figura 1; al comparar la puntuación inicial con el de la última medición mediante prueba de t para muestras relacionadas se obtuvo un valor de t de -8.86 y un valor de p < 0.05. Se reportó una incidencia de reacciones adversas locales de 19 % (n = 9), de las cuales todas fueron grado 1 (eritema > 3 cm de diámetro o formación de pápula). Desde el inicio del esquema de la ITA se obtuvo una frecuencia de reacciones adversas locales de 46.6 % (Figura 2). El promedio de estas reacciones adversas al inicio de la ITA fue de 15.25 %, mientras que a los 12 meses de seguimiento fue de 10.6 %. Solo se reportó una reacción adversa sistémica grado 3 (exacerbación de síntomas nasales) y grado 2 (urticaria) en el sexto y doceavo mes, respectivamente.
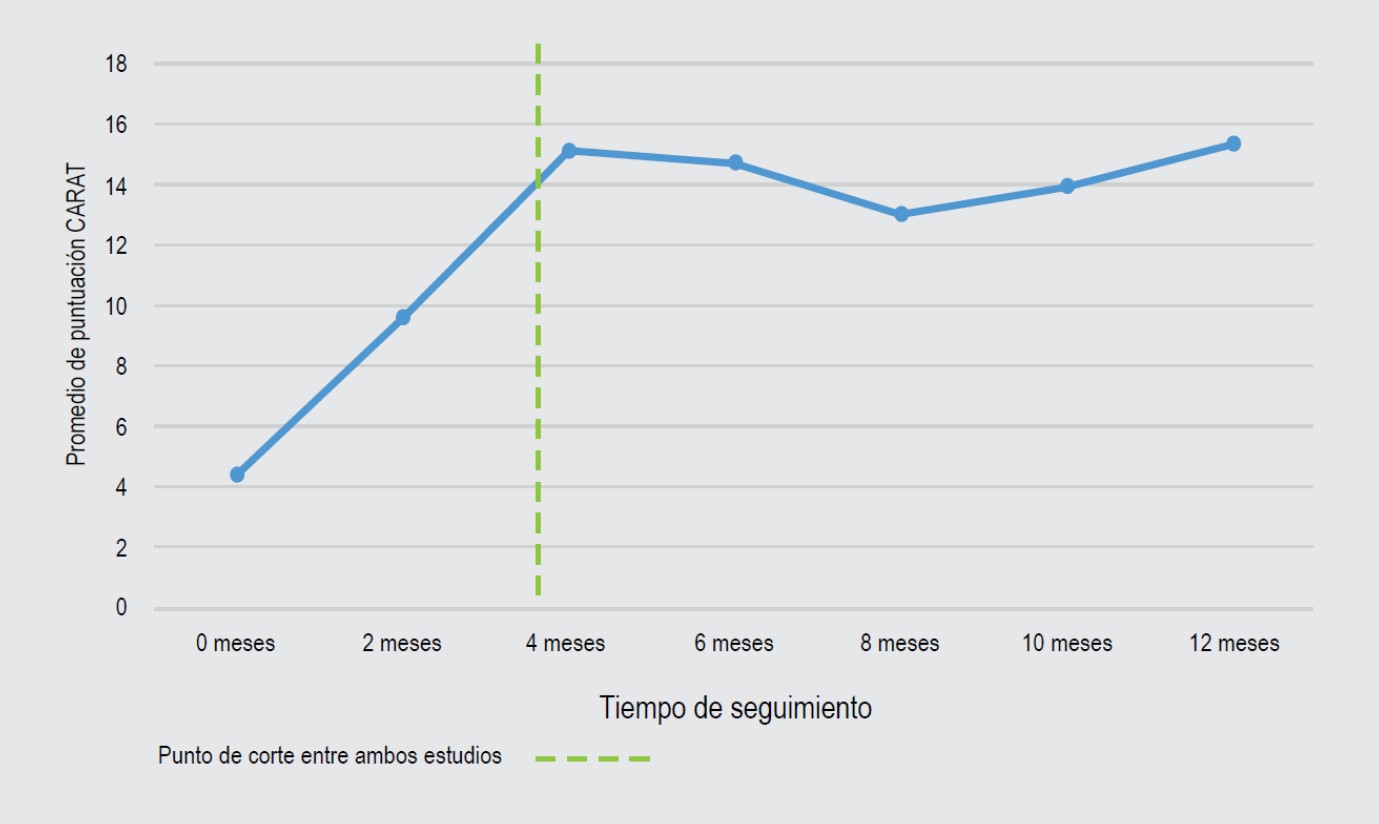
Figura 1. Eficacia de inmunoterapia subcutánea para alergia respiratoria evaluada por puntuación de cuestionario CARAT.
Discusión
De acuerdo con los resultados obtenidos, el esquema de inmunoterapia administrado en el Servicio de Alergia e Inmunología Clínica del Hospital Universitario de Puebla demostró ser eficaz utilizando un método de evaluación validado y estandarizado como el CARAT, ya implementado anteriormente.14,15,17 Llama la atención que en el presente estudio, en comparación a lo publicado sobre la fase de inducción,19 a partir del cuarto mes de tratamiento se observó una discreta y paulatina disminución de la puntuación CARAT, lo que podría explicarse por el periodo de administración de la ITA y el uso inicial del tratamiento farmacológico; sin embargo, posteriormente se observó un incremento significativo de la puntuación a partir del octavo mes de seguimiento, lo que puede deberse al mayor grado de desensibilización alérgica, caracterizado por un aumento de anticuerpos bloqueadores IgG4, citocinas antinflamatorias como IL-10 y una marcada disminución de LsTh2.13
La frecuencia de reacciones adversas locales desde el inicio del esquema de ITA demostró un grado de seguridad similar al mencionado en la literatura.19,20 En el estudio inicial se observó una mayor frecuencia de reacciones adversas locales a la ITA durante los primeros cuatro meses del esquema, en comparación con los últimos ochos meses analizados, lo cual se relaciona con lo reportado en la literatura.19 Hubo una mayor presentación de reacciones adversas sistémicas durante el desarrollo del presente estudio, sin embargo, ninguna grave, según los criterios sugeridos por la Organización Mundial de Alergia.16
Los presentes resultados concuerdan con los de revisiones sistemáticas previas, en las que se ha demostrado que la inmunoterapia subcutánea reduce en forma importante los datos clínicos de asma o rinitis alérgica, con cambios significativos en los cuestionarios de evaluación de síntomas y con bajo riesgo de reacciones adversas.21,22
Conclusiones
Los resultados demuestran que la fase de mantenimiento del esquema de inmunoterapia subcutánea utilizado en el Servicio de Alergia e Inmunología Clínica del Hospital Universitario de Puebla, basado en la Guía Mexicana de Práctica Clínica de Inmunoterapia 2011, tiene un perfil de eficacia y seguridad significativamente adecuado para el manejo del asma o rinitis alérgica.
Con esto reafirmamos la importancia de seguir los lineamientos nacionales e internacionales sobre las recomendaciones del uso de ITA, con el fin de brindar un óptimo tratamiento basado en evidencia científica.











 text new page (beta)
text new page (beta)




