Introducción
El síndrome de Lemmel o ictericia obstructiva intermitente es una afección infrecuente que fue descrita por primera vez en 1934. Lemmel observó que la presencia de divertículos duodenales próximos a la papila de Vater podría favorecer al desarrollo de enfermedades pancreatobiliares, y se define como ictericia obstructiva por divertículo duodenal periampular que comprime el conducto biliar común causando dilatación retrógrada de la vía biliar intrahepática y extrahepática1.
El duodeno es la segunda región anatómica, después del colon, en donde con más frecuencia se presentan los divertículos gastrointestinales. Estos divertículos pueden ser pseudodivertículos, que consisten en bolsas de mucosa, carentes de capa muscular, o divertículos verdaderos (congénitos), siendo los primeros los más frecuentes. Los divertículos duodenales tienen una incidencia del 5-10% en la población general; su prevalencia aumenta con la edad, llegando hasta un 15-20% a los 80 años de edad2.
La coledocolitiasis ocurre con una incidencia del 20-40% en los pacientes con divertículos duodenales periampulares; el 41% de los pacientes con divertículos duodenales yuxtapapilares no presentan coledocolitiasis.
Solo el 1% de los divertículos presentan complicaciones. La colangitis es una de estas complicaciones que deber ser tratada y diagnosticada de manera oportuna, dada su alta tasa de morbilidad y mortalidad, acorde con las guías de Tokyo de 2018, mediante antibioticoterapia y, dependiendo del grado, drenaje biliar electivo o de urgencia3.
En este artículo presentamos el caso de una paciente de 68 años con cuadros de ictericia de repetición. Además, se llevó a cabo una investigación en PubMed utilizando las palabras clave [diverticulum], [duodenum], [lemmel’s syndrome], [acute cholangitis], [juxtapapillary diverticula], [periampullary duodenal diverticulum] y [obstructive jaundice], y se seleccionaron los 15 artículos más relevantes en cuanto a presentación de caso clínico, complicaciones, diagnóstico y tratamiento.
Caso clínico
Mujer de 68 años, ama de casa, escolaridad secundaria, proveniente de una zona rural, con antecedente de hipertensión de larga evolución actualmente en control, obesidad de grado II, y resto negado.
Inicia el cuadro 48 horas antes de su ingreso con dolor abdominal transfictivo en el cuadrante superior derecho, fiebre, escalofríos y coloración amarillenta percibida por sus familiares. Durante el interrogatorio, la paciente refiere un cuadro similar hace 6 meses que fue manejado por medio particular, con remisión.
En la exploración física muestra una temperatura de 39 °C, frecuencia cardiaca de 98 latidos por minuto, frecuencia respiratoria de 16 respiraciones por minuto y presión arterial de 135/75 mmHg. La paciente está intranquila, consciente y orientada. Se observa ictericia en la piel y los tegumentos, mucosa oral semihidratada, sin adenopatías cervicales. Exploración cardiopulmonar sin compromiso aparente. Abdomen globoso a expensas de panículo adiposo, dolor a la palpación en el cuadrante superior derecho, Murphy negativo, no se palpan visceromegalias, rebote negativo, a la percusión timpanismo en mesogastrio, y peristalsis audible (6 por minuto).
Los estudios de laboratorio a su ingreso reportaron: hemoglobina 13 g/dl, hematocrito 41%, leuocitos 14,000, neutrófilos 12,000, plaquetas 153,000, bilirrubina total 3.5 mg/dl, bilirrubina directa 2.6 mg/dl, fosfatasa alcalina 526, gamma-glutamiltransferasa 65 UI/l, aspartato aminotransferasa 173 UI/l, alanina aminotransferasa 225 UI/l, albúmina 4, tiempo de protombina 16, tiempo de tromboplastina parcial 25, INR (International Normalized Ratio) 0.9, amilasa 250 UI/l y lipasa 300 UI/l.
Se inicia manejo por sospecha diagnóstica de colangitis por datos de inflamación sistémica (fiebre, escalofríos, leucocitos > 10,000) y datos de colestasis (ictericia > 2 mg/dl, elevación de fosfatasa alcalina y alteración de las pruebas de función hepática).
Se solicita estudio ecográfico que con reporta vesícula biliar normal sin litos en su interior, colédoco de 10 mm, coledocolitiasis y tumor en la cabeza del páncreas.
Se integra diagnóstico definitivo de colangitis de grado II según la guía de Tokyo (fiebre > 39 °C, leucocitos > 12,000) y se inicia manejo antibiótico con ceftriaxona (1 g/12 h por vía intravenosa) y metronidazol (500 mg/8 h por vía intravenosa), rehidratación y analgesia.
Como parte del protocolo diagnóstico se solicitan resonancia magnética (RM) y colangio-RM, que identifican un divertículo duodenal descrito como una cavidad de pared delgada, en la pared medial de la segunda porción del duodeno, además de coledocolitiasis y litiasis vesicular (Fig. 1). En la reconstrucción de la colangiografía se aprecia un divertículo de aproximadamente 3 cm que comprime la vía biliar, además de dilatación de la vía biliar de hasta 23 mm, con dos litos (uno en el tercio inferior del colédoco y otro por debajo de la carina) (Fig. 2).
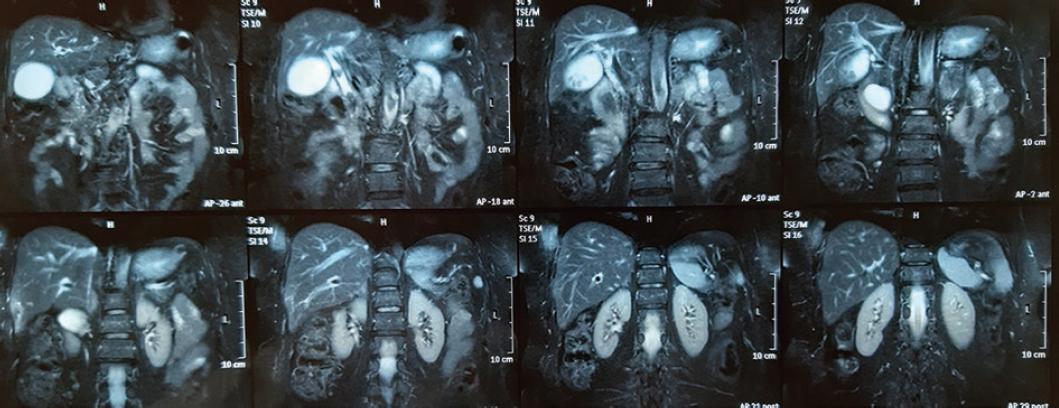
Figura 1 Resonancia magnética en la que se observan cálculos biliares, colelitiasis, imagen quística en la cabeza del páncreas y dilatación de la vía biliar.
Ante dichos hallazgos se solicita duodenoscopia más colangiografía retrógrada endoscópica (CPRE) con la finalidad de realizar esfinterotomía, descompresión y drenaje de la vía biliar. Durante el procedimiento no es posible canular el ámpula de Vater, por un lito impactado en ella (Fig. 3) y divertículo Noda C, Boix IIa, además de ámpula fibrótica (Fig. 4) (Vídeo 1).
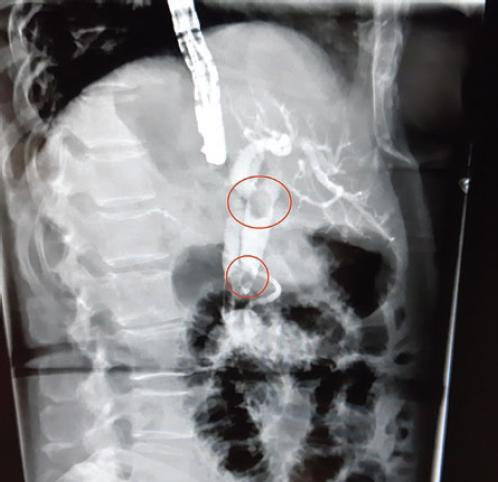
Figura 3 Colangiopancreatografía retrógrada endoscópica que muestra la vía biliar intrahepática y extrahepática dilatada, con lito en la confluencia de los conductos hepáticos y en el tercio inferior.
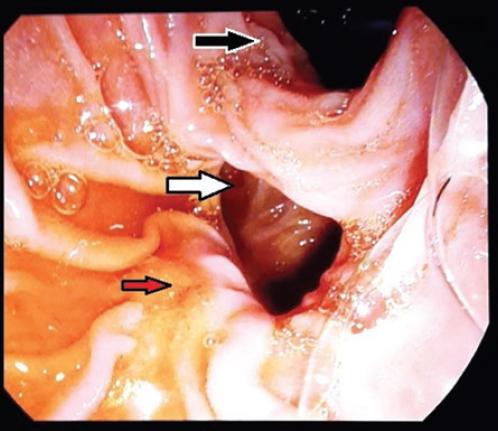
Figura 4 Visión retroversión endoscópica en colangiopancreatografía retrógrada endoscópica que muestra el divertículo (flecha blanca), el ámpula de Vater (flecha roja) y la primera porción del duodeno (flecha negra).
Se programa de manera electiva para colecistectomía y exploración de la vía biliar, la cual se realiza sin complicaciones, con los siguientes hallazgos: divertículo en la segunda porción del colédoco de 5 × 5 cm, vesícula biliar de 15 × 5 × 2 cm y colédoco de 3 cm de diámetro con múltiples litos (seis en total), el de mayor tamaño de 3 × 3 × 2 cm. Se realiza dilatación del ámpula de Vater. El tiempo quirúrgico fue de 150 minutos y el sangrado fue de 100 ml (Fig. 5).
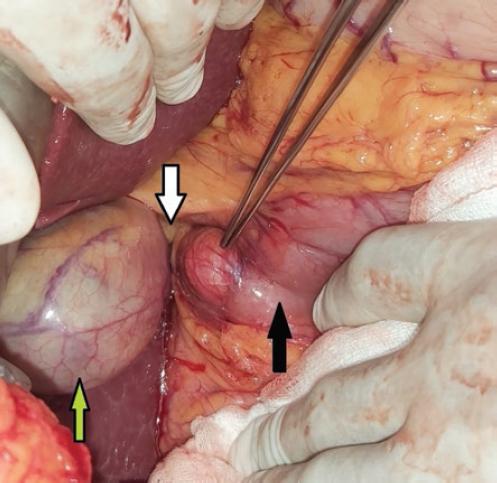
Figura 5 Divertículo duodenal señalado con la pinza de disección, colédoco (flecha blanca), duodeno (flecha negra) y vesícula biliar (flecha verde).
La paciente evoluciona favorablemente con remisión de la colangitis, tolera la dieta a las 12 horas de la intervención y se decide su egreso a las 72 horas, sin complicaciones. En su seguimiento al mes y 2 meses permanece sin cuadro de colangitis.
Discusión
Los divertículos duodenales fueron descritos por primera vez en 1710 por el patólogo francés Chomel, pero no fue hasta 1934 cuando Lemmel los describió como causa de ictericia obstructiva intermitente. El duodeno es el primer lugar del intestino delgado en cuanto a incidencia de divertículos, y el segundo lugar de todo el tracto digestivo después del colon. El 6% de los divertículos duodenales aparecen en la primera porción, el 53-75% en la segunda porción, el 12% en la tercera porción y el 24% en la cuarta porción4,5.
Los divertículos duodenales se pueden clasificar por su origen en divertículos congénitos, que poseen todas las capas de la pared duodenal y generalmente se asocian con malformaciones o alteraciones pancreatobiliares, y divertículos adquiridos (pseudodivertículos, carentes de capa muscular), desarrollados por un debilitamiento progresivo del músculo liso.
El síndrome de Lemmel es una afección poco frecuente en la literatura, debido a que los divertículos duodenales rara vez presentan síntomas y suelen ser diagnosticados de manera incidental. El 75% de estos divertículos son periampulares. Los que se localizan a 2.5 cm del ámpula de Vater son yuxtapapilares. Esta localización prevalente se asocia con zonas de debilidad por el ingreso de estructuras anatómicas de la vía biliar y pancreática. Solo el 10% de estos divertículos presentan sintomatología y solo el 1% tienen complicaciones, dentro de las cuales se encuentran, en orden de frecuencia, sangrado de tubo digestivo alto, diverticulitis, úlcera, perforación, colangitis, pancreatitis crónica, fístulas duodenocolónicas y esteatorrea. La transformación maligna es excepcional y solo ocurre relacionada con la inclusión de tejido pancreático o gástrico ectópico4,5.
Las manifestaciones clínicas de este síndrome incluyen ictericia a expensas de la bilirrubina directa, dolor abdominal, colangitis o mimetizando tumores periampulares, siendo la colangitis la manifestación más grave y se deben priorizar su diagnóstico y tratamiento según las guías de Tokyo de 2018.
La fisiopatología de este síndrome se puede explicar con tres procesos fundamentales, los cuales pueden ser sucesivos o simultáneos:
– La irritación mecánica directa del divertículo periampular puede causar inflamación crónica de la ámpula, lo que conduce a fibrosis.
– Los divertículos periampulares causan disfunción del esfínter de Oddi, lo que produce estasis y reflujo biliar desde el duodeno hacia el colédoco.
– La parte distal del conducto biliar común o el ámpula pueden ser comprimidos por el divertículo periampular.
Estos tres procesos favorecen el reflujo de contenido duodenal, el sobrecrecimiento bacteriano, la estasis biliar y la producción de cálculos biliares6,7.
El estudio de imagen desempeña un papel importante para identificar y diagnosticar el síndrome de Lemmel; para evitar un manejo erróneo, el uso de tomografía y RM, el divertículo periampular aparece como una cavidad de pared delgada en la pared medial de la segunda porción del duodeno. En algunas ocasiones puede llenarse de fluido y confundirse con un absceso pancreático, una neoplasia quística de la cabeza del páncreas o metástasis a los nódulos linfáticos; la estructura del divertículo se observa mejor después de la administración de contraste oral, pudiendo evaluar su tamaño antes y después de la administración, ya que en general su tamaño se duplica, haciendo más evidente la compresión de la vía biliar. El contraste intravenoso es de utilidad para diferenciar tumores biliopancreáticos o pseudoquistes, ya que las paredes del divertículo muestran un leve realce homogéneo (en la fase venosa), después de 45 segundos de su inyección6-8.
En pacientes asintomáticos se recomienda el tratamiento no quirúrgico o conservador, bajo la premisa «molestia que no moleste, no la molestes».
Actualmente, la CPRE es el método de referencia para el diagnóstico y el tratamiento, por la posibilidad de excluir otras posibles causas, como coledocolitiasis y tumores, y llevar a cabo la esfinterectomía endoscópica como tratamiento. El objetivo en estos casos es aliviar la obstrucción biliopancreática.
Existen dos clasificaciones endoscópicas para los divertículos duodenales: la clasificación de Noda (Tabla 1) y la de Boix (Tabla 2). Ambas sirven de apoyo para planear el procedimiento de CPRE y predecir falla y dificultad de la canulación de la papila, así como complicaciones como perforación, hemorragia y pancreatitis9,10.
Tabla 1 Clasificación de Noda (divertículo duodenal) (129 pacientes)
| Divertículo | Relación papila-divertículo | Frecuencia |
|---|---|---|
| Tipo A | Papila mayor se encuentra localizada lejos del divertículo duodenal | 19% |
| Tipo B | Papila se localiza adyacente al divertículo | 26% |
| Tipo C | Papila se localiza en el margen del divertículo | 47% |
| Tipo D | Papila localizada dentro del divertículo | 8% |
Tabla 2 Clasificación de Boix (divertículo duodenal) (400 pacientes sometidos a colangiopancreatografía retrógrada endoscópica)
| Divertículo | Relación papila/divertículo | Frecuencia | |
|---|---|---|---|
| Tipo I | Papila localizada dentro del divertículo | Ia: arriba Ib: izquierda Ic: abajo Id: derecha |
16.3% |
| Tipo II | Papila localizada en el margen del divertículo | IIa: margen apical izquierdo IIb: margen apical derecho IIc: centro del margen izquierdo o derecho IId: entre dos divertículos |
10.2% |
| Tipo III | Papila localizada cerca del divertículo | 6.5% |
Boix, et al.9 analizaron 400 pacientes sometidos a CPRE, de los cuales 131 presentaron divertículos duodenales, y clasificaron la dificultad de canulación en grados: grado 1, canulación profunda fácil; grado 2, necesidad de guía de alambre o esfinterotomo especial; grado 3: dificultad de canulación que requiere técnica especiales, como esfinterotomía con aguja-cuchilla; y grado 4, imposibilidad para canulación. Estos autores concluyen que no existe diferencia en la dificultad de canulación en los pacientes con divertículos duodenales.
La intervención endoscópica es la primera línea de manejo. En su estudio, Horaguchi, et al.10 analizaron dos grupos de 129 pacientes, uno con presencia de divertículos y otro sin divertículos, y determinaron la dificultad de canulación de ambos grupos y las complicaciones, que fueron el 12.4% en el grupo con divertículos y el 10.1% en el grupo sin divertículos. Los pacientes con divertículos de tipo papilar presentaron complicaciones en un 50%.
El tratamiento quirúrgico llevado a cabo mediante diverticulectomía o derivación biliodigestiva está reservado para aquellos casos en los que hay perforación o hemorragia posterior a la CPRE, o cuando es imposible la canulación endoscópica por dificultades como litos > 20 mm, ampula intradiverticular, incapacidad para canulación, falta de equipo, inexperiencia, lito impactado en el colédoco distal o panlitiasis9,11.
Se puede considerar el tratamiento quirúrgico cuando se trate de un paciente joven sin comorbilidad importante, puesto que, a pesar de realizar un tratamiento endoscópico adecuado, los síntomas biliares son recurrentes y se precisan largos periodos de observación.
La diverticulectomía simple se asocia a una alta morbimortalidad debido al riesgo de lesión del conducto biliopancreático, por lo que se sugiere localizar el ámpula de Vater por duodenotomía, de forma anterógrada por el cístico o por coledocotomía. Otra intervención que puede ser de utilidad es la técnica de rendez-vous, que consiste en la introducción de una sonda transcística hasta franquear la papila duodenal mayor y efectuar la papilotomía con esfinterotomo de aguja, o introduciendo una guía hidrófila transcística y capturándola en el duodeno, obteniendo buenos resultados12.
Conclusiones
El síndrome de Lemmel es una afección rara que se ha reportado poco en la literatura mundial. Aunque la prevalencia de divertículos duodenales es relativamente alta, la presentación de síntomas y de complicaciones no lo es. El síndrome de Lemmel puede causar complicaciones graves y debe considerarse como posibilidad diagnóstica en pacientes con ictericia recurrente y colangitis.
El diagnóstico requiere estudios de imagen con doble contraste para descartar otras patologías y documentar el divertículo y la compresión de la vía biliar.
Se recomienda el manejo endoscópico con CPRE como método de referencia para el diagnóstico y el tratamiento, siendo altamente efectiva, poco invasiva y con una baja tasa de complicaciones.
El manejo quirúrgico se reserva para la falla o las complicaciones en la CPRE, pacientes con complicaciones propias del divertículo duodenal, pacientes jóvenes que no puedan recibir seguimiento y concomitancia con defectos biliopancreáticos.











 text new page (beta)
text new page (beta)



