Introducción
El cáncer de páncreas es la séptima causa de muerte por cáncer en el mundo. La supervivencia a 5 años es menor del 9%1. Se estima que aproximadamente el 20% son resecables con fines potencialmente curativos2. Por lo tanto, el diagnóstico temprano es crucial para ofrecer al paciente el tratamiento adecuado y mejorar su pronóstico.
Desde su introducción en 1992, la biopsia con aguja fina (con o sin aspiración) guiada por ultrasonido endoscópico (BAF-USE) se ha convertido en una herramienta indispensable en el estudio de las lesiones adyacentes al tracto gastrointestinal, así como en el estudio de las lesiones gastrointestinales subepiteliales3. Es una técnica segura, poco invasiva, efectiva y altamente precisa, en especial para lesiones sólidas del páncreas4-7. Las complicaciones asociadas a este procedimiento son bajas y en general se reportan en el 0-2% de los casos8,9. Su limitación más importante es que el espécimen citológico puede tener escasa celularidad y falta de arquitectura histológica4.
La evaluación citológica rápida en sala (ROSE, rapid on-site evaluation) consiste en la revisión inmediata de las muestras obtenidas por BAF-USE, en términos de suficiencia y diagnóstico preliminar10,11. Actualmente la evidencia es controversial, pues la BAF-USE se ha consolidado como una técnica con alto rendimiento diagnóstico (85-87%), alta sensibilidad (94-96%) y alta especificidad (95-100%), aun sin la adición de ROSE3,6,7,12. Más allá de esto, las llamadas agujas histológicas de segunda generación han mostrado resultados promisorios en cuanto a suficiencia, estructura celular y rendimiento diagnóstico13,14.
Alcanzar un alto rendimiento diagnóstico requiere sobrepasar múltiples pasos limitantes, principalmente la experiencia del endosonografista, las características de la aguja, la técnica de adquisición de tejido y la experiencia del patólogo15. Por todo esto, la disponibilidad de ROSE podría mejorar la toma de muestra por BAF-USE de lesiones sólidas del páncreas en centros en los que se está iniciando con el ultrasonido endoscópico, en aquellos donde hay médicos en entrenamiento y en aquellos con bajo volumen. El objetivo de este estudio fue comparar la eficacia diagnóstica de la ROSE durante las BAF-USE de lesiones pancreáticas sólidas como parte de la experiencia inicial en un centro de referencia nacional en México.
Método
Se realizó un estudio retrolectivo y comparativo. Se incluyeron todos los pacientes de ambos sexos, mayores de 18 años, con indicación de BAF-USE por presentar lesiones sólidas del páncreas, en el período de enero a julio de 2017, que fueron atendidos en el servicio de endoscopia del Centro Médico Nacional 20 de Noviembre. El estudio fue aprobado por el comité de ética institucional y todos los pacientes dieron su consentimiento informado por escrito antes del procedimiento. Las biopsias fueron tomadas por dos endosonografistas y la sedación fue asistida por el servicio de anestesiología.
Los resultados de las biopsias fueron divididos en dos grupos: un grupo con ROSE, en el cual se realizó una revisión citológica en la sala de endoscopia hasta considerar que la muestra fue adecuada y posteriormente se envió al servicio de patología para el análisis definitivo, y otro grupo sin ROSE, en el cual las biopsias fueron preservadas en formol al 10% y enviadas al servicio de patología.
Técnica
Las BAF-USE fueron tomadas con aguja 22G, sin aspiración, con estilete y retirada lenta; se dieron al menos dos pases con cinco entradas en cuatro direcciones con movimiento en abanico (Figs. 1 y 2). Se utilizó un ecoendoscopio lineal EG-530UT acoplado a la consola SU-8000 (Fujifilm Corporation, Minato-Ku, Tokio, Japón).
Definiciones
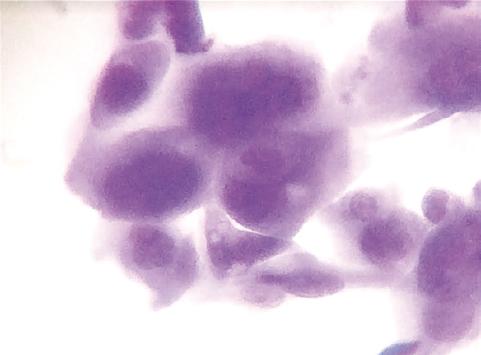
- Muestra adecuada: cuando un patólogo analizaba la muestra y confirmaba la presencia de células glandulares o ductales suficientes para poder hacer un diagnóstico histopatológico. En el grupo con ROSE, si la muestra analizada en la sala de endoscopia no era adecuada se tomaba otro pase hasta confirmar que fuera adecuada (Figs. 3 y 4).
- Muestra inadecuada: se definió cuando hubo acelularidad, necrosis, ausencia de células glandulares o ductales, o material insuficiente para diagnóstico, y cuando fue reportada textualmente como inadecuada.
- Diagnóstico final: cuando se dio el reporte definitivo en el servicio de patología para descartar o confirmar la presencia de atipia o malignidad.
Análisis estadístico
Para evaluar los resultados se utilizó estadística descriptiva mediante frecuencias, porcentajes, medianas y rangos. Las diferencias entre los grupos se analizaron mediante las pruebas de chi al cuadrado o exacta de Fisher para variables categóricas y t de Student o U de Mann Whitney para variables continuas, según fuera lo apropiado. El análisis estadístico se realizó con SPSS (versión 21, IBM Corp., Armonk, Nueva York, EUA).
Resultados
Se incluyeron 23 pacientes, la mediana de edad fue de 59 años (rango: 46-77) y 12 (52.2%) fueron del sexo femenino. En 10 pacientes (43.5%) se realizó BAF-USE sin evaluación en la sala de endoscopia (grupo sin ROSE) y en 13 pacientes (56.5%) se realizó evaluación citológica rápida en sala (grupo con ROSE). En la tabla 1 se muestran las principales características de la población, así como la localización y el tamaño de las lesiones pancreáticas.
Tabla 1 Características generales de los pacientes estudiados
| Grupo con ROSE (n = 13) (% o rango) | Grupo sin ROSE (n = 10) (% o rango) | p | |
|---|---|---|---|
| Edad, años | 60 (47-77) | 58 (46-72) | 0.39 |
| Sexo femenino | 6 (46.2) | 6 (60) | 0.68 |
| Localización de la lesión | 0.87 | ||
| Cabeza del páncreas | 8 (61) | 7 (70) | |
| Proceso uncinado | 3 (23.1) | 1 (10) | |
| Cuerpo del páncreas | 1 (7.7) | 1 (10) | |
| Cola del páncreas | 1 (7.7) | 1 (10) | |
| Tamaño de la lesión | 0.22 | ||
| < 30 mm | 8 (61.5) | 3 (30) | |
| ≥ 30 mm | 5 (38.5) | 7 (70) | |
| Pases durante BAF-USE | 2 (2-3) | 3 (3-4) | 0.21 |
BAF-USE: biopsia con aguja fina guiada por ultrasonido endoscópico; ROSE: rapid on-site evaluation.
En la tabla 2 se detallan los diagnósticos por citología para las 23 lesiones estudiadas a partir de las BAF-USE. En el grupo sin ROSE, cinco muestras (50%) fueron inadecuadas, mientras que en el grupo con ROSE las 13 muestras (100%) fueron adecuadas, con una diferencia significativa (p = 0.007). El número de pases realizados fue menor en el grupo con ROSE, sin haber diferencias significativas al compararlo con el grupo sin ROSE (2 vs. 3; p = 0.21). Del grupo sin ROSE, solo un paciente (10%) tuvo diagnóstico de malignidad, en comparación con 10 pacientes (76.9%) en el grupo con ROSE (p = 0.003) (Tabla 3).
Tabla 2 Diagnóstico histológico de las lesiones en todos los pacientes estudiados
| Tipo de lesión | Frecuencia absoluta (n) | Frecuencia relativa (%) |
|---|---|---|
| Adenocarcinoma pancreático | 8 | 34.8 |
| Atipia celular, no concluyente | 5 | 21.7 |
| Tumor neuroendocrino | 3 | 13.1 |
| Lesiones benignas | 2 | 8.7 |
| Material insuficiente | 5 | 21.7 |
| Total | 23 | 100 |
Tabla 3 Muestra considerada adecuada y diagnóstico definitivo en el reporte final de histopatología
| Grupo con ROSE (n = 13) (56.5%) (%) | Grupo sin ROSE (n = 10) (43.5%) (%) | p | |
|---|---|---|---|
| Muestra adecuada y suficiente | 13 (100) | 5 (50) | 0.007 |
| Diagnóstico de malignidad | 11 (84) | 2 (20) | 0.003 |
ROSE: rapid on-site evaluation.
La tasa diagnóstica de la BAF-USE en el grupo sin ROSE fue del 20%, en comparación con el 84.6% en el grupo con ROSE (p = 0.003).
Discusión
El USE es la técnica más útil para el diagnóstico del cáncer de páncreas16, con un rendimiento global superior al 83%3,7,17. En México, aún son pocos los hospitales que cuentan con esta herramienta. En nuestro centro se encuentra disponible desde el año 2015, lo cual ha sido un verdadero reto, pues crear un centro de referencia ha requerido la capacitación del personal, la divulgación de su utilidad y el apoyo de los servicios involucrados. Al analizar nuestros resultados encontramos un gran número de citologías reportadas como negativas o sin muestra suficiente. Este fue el motor para invitar a los patólogos a evaluar algunos casos en nuestra sala.
La ROSE ha demostrado ser útil en múltiples estudios11. En el metaanálisis realizado por Hébert-Magee, et al.18 se incluyeron 34 estudios con un total de 3,644 pacientes y se encontró una sensibilidad global del 88.6% para el diagnóstico de adenocarcinoma pancreático, con una especificidad del 99.3%. La ROSE se mantuvo como un determinante del rendimiento diagnóstico de la BAF-USE. Por otro lado, en el metaanálisis y revisión sistemática de Kong, et al.19 se evaluaron 1299 pacientes y no se encontraron diferencias cuando se añadía ROSE a la evaluación de biopsias pancreáticas y de ganglios linfáticos. Estas controversias en la evidencia hacen difícil saber el rol actual de la ROSE, por lo que algunos expertos consideran que es un «lujo útil y deseable»2, aunque no indispensable. Adicionalmente, de forma reciente se han incorporado las agujas de corte histológico de segunda generación. Estas agujas no fueron utilizadas en el presente estudio, pero vale la pena mencionar el metaanálisis del grupo de Todd Baron et al.,13 en el que se comparó la utilidad de las agujas tradicionales con las histológicas de segunda generación, en escenarios con ROSE y sin ella. Los autores concluyeron que utilizar agujas histológicas de segunda generación resulta equiparable a utilizar una aguja tradicional y tener ROSE13. Con estas contradicciones en la evidencia, es difícil saber la utilidad real de la ROSE, pues esto refleja la complejidad de un procedimiento en el que el éxito depende de factores relacionados con el endoscopista, el tipo de aguja, la técnica empleada, el número de pases, el procesamiento de la muestra y la experiencia del patólogo o citotecnólogo3,20,21.
En nuestra experiencia inicial, el uso de ROSE resultó en un mayor número de muestras adecuadas, un mayor rendimiento diagnóstico y un mayor número de diagnósticos definitivos de malignidad (Tablas 2 y 3). Una de las limitantes de nuestro estudio fue el tamaño de la muestra; sin embargo, es un centro que recientemente ha incorporado al ultrasonido endoscópico, por lo que consideramos que puede representar la realidad de muchos centros que buscan añadir esta tecnología a sus unidades de endoscopia. También creemos que el haber invitado al servicio de patología a la sala de endoscopia fue un paso importante para mejorar la participación multidisciplinaria de forma más directa en el abordaje de pacientes con lesiones pancreáticas sólidas. Este cambio impactó en la forma en que ellos evalúan estos casos, pues les hace entender el gran esfuerzo que representa obtener estas muestras. Esta es la importancia real que encontramos en nuestro trabajo: exponer nuestra experiencia a otros centros en donde la tasa diagnóstica de las biopsias por ultrasonido endoscópico es aún baja.











 text new page (beta)
text new page (beta)