INTRODUCCIÓN
El melón (Cucumis melo L.) es un fruto que tiene alta calidad, así como alto contenido nutricional y compuestos antioxidantes, lo que hace de una hortaliza comercialmente importante y aceptada por los consumidores (Beaulieu 2005, Kader 2009 y FAOSTAT 2012). La calidad de este fruto está asociada con procesos bioquímicos, condiciones ambientales y factores bióticos que afectan el color, firmeza, sabor y aroma (Uzogara 2000).
En el melón tipo Cantaloupe, la coloración naranja en la piel del fruto es un indicador de cosecha, además de una forma esférica, red intensa, pulpa de coloración salmón, aroma intenso y peso promedio por fruto entre 700 y 1200 g (Nicolás et al. 1989). La concentración de SST o °Brix se usa como índice de clasificación, por lo que melones con menos de 9 °Brix son considerados no comerciables, mientras que de 9 a 12 °Brix son los más aptos para comercialización (Bower et al. 2002). En tanto que Burger et al. (2003) mencionan que la calidad de un fruto para el consumo no debe determinarse por un factor de forma aislada, sino por la combinación de todas las propiedades físico-químicas, por lo que muchos investigadores refieren que una de las formas para evaluar la calidad de los frutos es mediante características sensoriales, físicas y el contenido de azúcares (Kader 2009).
Los reguladores de crecimiento, controlan los procesos fisiológicos y bioquímicos de las plantas, lo que impacta en la dormancia, tamaño del fruto, desarrollo del cultivo, floración, cuajado del fruto, regulación de la composición química de las plantas y el suministro de minerales (Nickell 1978). Por ejemplo la giberelina (GA3) estimula el alargamiento de las células (Dugardeyn et al. 2008), el ácido-3-indolacético (AIA) activa el crecimiento de las plantas (Mella et al. 1997) y el ácido naftaleno acético (ANA) regula el flujo de metabolitos (Ravi et al. 2005, Montaño y Méndez 2009b). Además el ANA reduce la abscisión de los frutos, y aumenta la maduración de los frutos cosechados (Yuan y Li 2008, Unrath et al. 2009, Brackmann et al. 2014). La aplicación de ANA en el cultivo de guayaba (Psidium guajava L.) reduce la caída del fruto e incrementa el rendimiento (Iqbal et al. 2009). Mientras que en el cultivo de melón, la aplicación de 100 mg L-1 de ANA 14 d después de floración (DDF) induce mayor tamaño del fruto, rendimiento (Montaño y Méndez 2009a) y la concentración de sólidos solubles totales (Montaño y Méndez 2009b). Mientras que Barzegar et al. (2015) reportan que la aplicación del ANA aumentó el contenido de glucosa, fructosa y sucrosa en el melón.
El aroma del melón es resultado de mezclas complejas de compuestos volátiles (COV), que están asociados con la maduración climatérica (Shalit et al. 2001). Los frutos climatéricos, como el melón Cantaloupe, tienen corta vida de anaquel y despiden más aroma que los no climatéricos, ya que algunos compuestos aromáticos son producidos solamente por rutas dependientes de etileno (Wang et al. 2011). Al respeto, Beaulieu y Grimm (2001) reportan la presencia de 240 compuestos volátiles relacionados con la calidad del fruto del melón tipo Cantaloupe. Aunque existe evidencia del efecto del ácido naftalenacético en la producción de los cultivos y el incremento en la calidad de los frutos, pocos estudios relacionan a este fitoregulador con los componentes de calidad de melones tipo Cantaloupe, por tal motivo el objetivo del presente estudio fue determinar la relación del ácido naftalenacético sobre la calidad y los componentes de rendimiento en frutos de melones 'Navigator' y 'Thunderbird' de tipo Cantaloupe.
MATERIALES Y MÉTODOS
Establecimiento experimental
El ensayo se realizó de febrero a junio de 2014 en el campo experimental del Instituto de Ciencias Agrícolas de la Universidad Autónoma de Baja California, se utilizaron los cultivares de melón 'Navigator' y 'Thunderbird' (Tipo Cantaloupe), los cuales se establecieron en cuatro parcelas experimentales para cada cultivar, el trasplante se realizó en suelo franco-arcilloso en camas de 2.0 m de ancho y 10 m de largo a hilera sencilla con 0.30 m de distancia entre plantas para tener una densidad de 16 666 plantas ha-1.
Cada parcela experimental consistió de 80 m2 donde se aplicaron los tratamientos de 0.1, 0.2 y 0.4 mg L-1 de ácido naftalenacético y un testigo (0 mg L-1), realizando tres aplicaciones de cada tratamiento, la primera aplicación se realizó al inicio de la floración femenina, mientras que la segunda y tercera aplicación se realizó en intervalos de ocho días. Se empleó como fuente del fitoregulador el producto comercial Amcotone H, 0.45% I.A kg-1. Los tratamientos se aplicaron con una bomba manual con capacidad de 15 L y boquilla tipo abanico. Una vez que los frutos de cada parcela experimental alcanzaron la madurez fisiológica (1/2 slip), se cosecharon y se trasladaron al laboratorio de Fisiología y Manejo de Poscosecha para la medición de las variables de calidad.
Antes del trasplante se aplicó al suelo 2.0 L ha-1 de Trifluralina 480 CE, para el control de maleza, posteriormente el control de maleza se realizó de forma manual. Las plantas se fertilizaron con 172, 83 y 268 kg por hectárea de nitrógeno, fósforo y potasio, respectivamente; durante el ciclo del cultivo de 110 d. También se aplicaron 67 y 24 kg de calcio y magnesio a partir de los 60 d después del trasplante, al inicio de la floración y en cosecha. La fertilización y los riegos se realizaron mediante cinta de riego por goteo (4 h diarias) con separación de 20 cm entre goteros y gasto de 0.684 L ha-1. El control de la mosquita blanca (Bemisia tabaci) se realizó mediante aplicaciones de Spiromesifen a razón de 0.5 L ha-1. Cuando las plantas tuvieron las primeras flores femeninas, se colocaron colmenas en la parte central del experimento para garantizar la polinización (Sánchez et al. 2016).
Experimento de laboratorio
Se utilizó un muestreo no destructivo con cinco frutos frescos como unidad experimental para el peso, diámetro longitudinal (DL) y transversal (DT) fruto. El peso se determinó con una balanza digital modelo V11P3 (OHAUS®) usando como unidad de medición el kilogramo (kg), mientras que los diámetros, polar (DT) y longitudinal (DL) se midieron en centímetros (cm), con una cinta métrica. Para determinar la concentración de SST, firmeza de pulpa, color de pulpa y compuestos volátiles, se utilizó un muestreo destructivo de cinco frutos frescos como unidad experimental. La concentración de SST se determinó con un refractómetro ABBE Leica Marl II, colocando dos gotas de extracto de pulpa del fruto, para reportarlo en oBrix (AOAC 1998). La firmeza de pulpa se determinó en cinco puntos de la pulpa de las dos partes opuestas de la sección ecuatorial de cada fruto con la metodología propuesta por Bourne (1980), con un texturómetro Chatillon-DFI00 (North Carolina), con punta tipo cilindro y diámetro de 8 mm, las unidades se expresaron en Newtons.
El color de la pulpa se determinó con un espectrofotómetro de esfera X-Rite SP62, en las dos partes opuestas de la sección ecuatorial de cada fruto por tratamiento, tomado cinco puntos de lectura al azar de cada fruto. Los resultados se expresaron en luminosidad (L), cromaticidad (C), y ángulo Hue (oH) (Minolta 1994).
Los compuestos volátiles se midieron con una nariz electrónica con sensor de superficie de onda acústica (zNose 7100). Se utilizaron 3 g de pulpa fresca en cada fruto analizado, posteriormente se depositó en un vial de cristal de 40 mL sellado con papel encerado (Parafilm) durante media hora hasta lograr la estabilización de los compuestos volátiles (COV) a temperatura del laboratorio. Previo a la lectura de los análisis en frutos, se utilizó el programa MicroSense para leer la información de los COV, también se conectó la nariz electrónica a un tanque de gas helio con 99.99% de pureza con un controlador de presión, la nariz electrónica se calibró con una solución estándar (alcanos C6-C14), obteniendo los principales compuestos aromáticos de la muestra de un fruto tipo Cantalopue, previamente se originó una huella de aromas, con rangos de temperatura estandarizados con espacio de onda acústica de 60oC, columnas 40oC, válvula de 165oC, salida de 200oC, columna máxima de 200oC, trap de 250oC, y caudal de flujo de 3.5 ccm. Posteriormente se tomó un vial con muestra de fruta y se le colocó una jeringa estéril en la tapa del vial que permitió que la bomba succionara los aromas producidos, y luego se utilizó gas helio para conducir los compuestos volátiles hacia el sensor de la nariz electrónica, los resultados se expresaron en Cts.
Análisis estadístico
Se realizó un análisis de varianza con un diseño experimental completamente al azar para las variables peso, longitud polar, longitud ecuatorial, SST, firmeza de pulpa, color de pulpa y compuestos volátiles, cuando se detectaron diferencias significativas se realizó una comparación multiple de medias con la prueba de Tukey (α ≤ 0.05), los análisis se realizaron con el paquete estadístico Statistix 8.0. También se realizó un análisis de componentes principales para observar las diferencias de las variables mediante el programa XLstat versión 1.02, para el análisis se seleccionaron las variables que presentaron diferencias significativas entre tratamientos.
RESULTADOS
En la Tabla 1, se observa que los tres tratamientos de ANA no afectaron la luminosidad y los ángulos oHue de la pulpa de los frutos del melón 'Navigator' en comparación con los frutos del tratamiento testigo. Para el melón 'Thunderbird', el tratamiento de 0.4 mg L-1 disminuyó 2.8, 3.5 y 2.8% la luminosidad de la pulpa de los frutos en comparación con los tratamientos de 0.1, 0.2 y 0 mg L-1, respectivamente. Este mismo tratamiento (0.4 mg L-1) disminuyó 1.7% los ángulos oHue con respecto a la dosis de 0.2 mg L-1 y no tuvo diferencias significativas con respecto al testigo y los frutos con 0.1 mg L-1 de ANA.
Tabla 1 Influencia del ácido naftalenacético sobre la luminosidad (L), cromaticidad (C), y ángulo de color (oHue) en frutos de dos cultivares de melón.
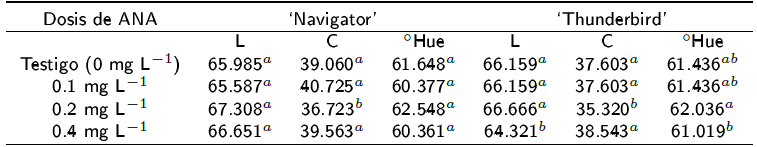
Medias con la misma letra en la columna son estadísticamente iguales (Tukey, α ≤ 0.05).
Los frutos del melón 'Navigator' cosechados de plantas tratadas con 0.4 mg L-1 de ANA presentaron 20.9% más firmeza de pulpa que los frutos del tratamiento testigo (Tabla 2), en general la aplicación de los tratamientos de ANA produjeron mayor firmeza en los frutos de melón 'Navigator'. Mientras que en los melones 'Thunderbird' sucedió lo contrario, los frutos del tratamiento testigo (0 mg L-1) tuvieron la mayor firrmeza en comparación con los frutos de plantas tratadas con 0.4 mg L-1, lo que sugiere un efecto negativo de los tratamientos de ANA con la firmeza de los frutos. El ANA indujo mayor concentración de SST en el melón 'Navigator' en los tratamientos de 0.1 y 0.4 mg L-1, con incrementos de 10.1 y 6.8% en comparación con el testigo. Mientras que en el contenido de SST disminuyó en el melón 'Thunderbird', con respecto el testigo.
Tabla 2 Influencia del ácido naftalenacético sobre la firmeza (N), sólidos solubles totales (SST), peso de frutos, longitud ecuatorial (LE) y longitud polar (LP) en frutos de dos cultivares de melón.
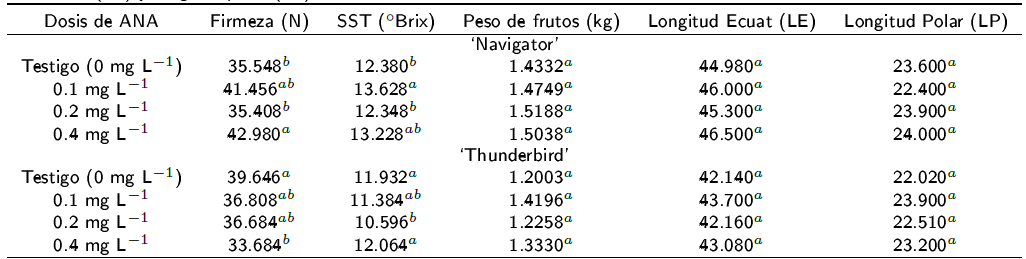
Medias con la misma letra en la columna son estadísticamente iguales (Tukey, α ≤ 0.05).
Los tratamientos de ANA no tuvieron efecto significativo en el peso, longitud ecuatorial y polar del fruto en ambos cultivares de melón. El melón 'Navigator' tuvo valores promedios de 1.4827 kg, 45.695 cm, y 23.475 cm para peso, longitud ecuatorial y longitud polar, respectivamente. Mientras que en los melones 'Thunderbird' los valores fueron de 1.2947 kg, 42.77 cm, y 22.907 cm para el peso, longitud ecuatorial y polar de los frutos, respectivamente. Estos resultados sugieren que los frutos del melón 'Navigator' fueron un 14.5% más pesados, un 6.8% más grandes de diámetro ecuatorial y un 2.5% mayor de diámetro polar, que los frutos del melón 'Thunderbird'.
En la Tabla 3 se observa que el tratamiento con 0.2 mg L-1 de ANA, incrementó la concentración de propionato de etilo en los frutos del melón 'Navigator', al compararlo con el tratamiento testigo. En tanto que los tratamientos con 0.2 y 0.4 mg L-1 de ANA indujeron mayor concentración de acetato de butilo que los tratamientos con 0.1 y 0 mg L-1 de ANA. Mientras que estos mismos tratamientos no tuvieron efecto significativo en la concentración isobutirato de etilo, acetato de etilo, hexanato de etilo y E-2 nonenal en los frutos del melón 'Navigator' con respecto al testigo. Para el melón 'Thunderbird', las dosis de ANA indujeron mayor concentración de isobutirato de etilo y acetato de etilo con respecto a los frutos del testigo. Mientras que para los compuestos volátiles; propionato de etilo, acetato de butilo, hexanato de etilo y E-2 nonenal no se encontraron diferencias estadísticas.
Tabla 3 Influencia del ácido naftalenacético sobre los compuestos volátiles de frutos de dos cultivares de melón.
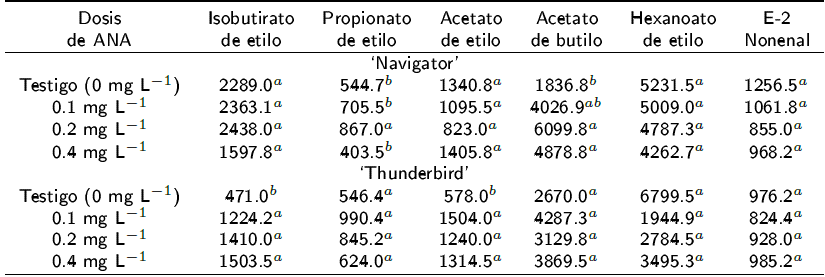
Medias con la misma letra en la columna son estadísticamente iguales (Tukey, α ≤ 0.05).
El análisis de componentes principales muestra que para los melones 'Navigator', los primeros dos componentes principales explican el 87.65% de la variación total de las variables analizadas (Figura 1). Mientras que para los melones 'Thunderbird' los primeros dos componentes principales explican el 93.91% del total de la variación de las variables (Figura 1). Para el cultivar 'Navigator', los primeros dos componentes principales indican que los frutos provenientes de plantas tratadas con ANA muestran un comportamiento diferente en comparación con los frutos de las plantas testigo, presentando mayor contenido de sólidos solubles totales, firmeza, acetato de butilo y propionato de etilo (Figura 1). Resultados similares se observan en los melones 'Thunderbird', indicando los primeros dos componentes principales que los frutos provenientes de plantas tratadas con 0.2 y 0.4 mg L-1 de ANA tuvieron un comportamiento diferente en comparación con los frutos de las plantas testigo y del tratamiento con 0.1 mg L-1. Presentando los frutos de las plantas testigo del melón 'Thunderbird' la mayor firrmeza y característica de color (oHue) (Figura 1).
DISCUSIÓN
Los tratamientos de ANA indujeron mayor firmeza en los melones 'Navigator', mientras que en los frutos de melones 'Thunderbird' no tuvieron los mismos efectos de firmeza. Al respecto algunos estudios, indican que las aplicaciones de ANA aumenta la maduración de los frutos, debido a la acción de ACC sintasa que induce la producción de etileno (Unrath et al. 2009, Brackmann et al. 2014); este efecto del ANA pudo haber incrementado la maduración de los frutos de los melones 'Thunderbird', lo que indujo menor firmeza de fruto. La respuesta obtenida en los melones 'Thunderbird', coincide con los resultados obtenidos por Yuan y Li (2008), quienes con 20 mg L-1 de ANA tuvieron menor firmeza de fruto en manzanas red Delicious. Mientras que Marini et al. (1993), indican que la aplicación de ANA estimula la maduración y se reduce la firmeza de los frutos de manzana red Delicious. En tanto que el efecto positivo del ANA en los melones 'Navigator', se puede deber a las características genotípicas del cultivar, lo que coincide con Menezes et al. (1998), quienes señalan que la diferencia de firmeza en frutos de melón puede deberse a la dosis ANA y al genotipo evaluado.
Los resultados muestran que los tres tratamientos de ANA pueden mejorar la calidad de fruto del melón 'Navigator', incrementando el contenido de SST de, lo que coincide con Montaño y Méndez (2009a), quienes registraron mayor contenido de SST en frutos de melón cv Edisto 47, con aplicaciones de ácido naftalenacético a los 14 d después de la floración. Mientras que Barzegar et al. (2015) mencionan que el aumento de la dosis de ANA en frutos de melón, incrementa la concentración de SST. En el presente estudio con la concentración de 0.4 mg L-1 de ácido naftalenacético se obtuvo la mayor concentración de SST en el melón 'Navigator'. Es probable que la mayor concentración de SST pueda atribuirse a una mayor eficiencia fotosintética de las hojas y al aumento de la translocación de los asimilados dentro de los frutos, en respuesta a la estimulación hormonal provocado por el ANA.
Los frutos provenientes de plantas tratadas con 0.1, 0.2 y 0.4 mg L-1 del ANA tuvieron un incremento en los compuestos aromáticos en ambos cultivares, los melones 'Navigator' tuvieron mayores niveles de acetato de butilo y propionato de etilo, y los melones 'Thunderbird' presentaron los mayores niveles de isopropionato de etilo y acetato de etilo. Estos resultados coinciden con los reportados por Vallone et al. (2013) quienes reportan que estos melones presentan ésteres y aldehidos como el grupo más abundante de compuestos volátiles, pero los compuestos de menor intensidad son el acetato de etilo y acetato de butilo. La diferencia en los tipos de compuestos aromáticos entre el 'Navigator' y 'Thunderbird' probablemente se relaciona con la variedad y los procesos de maduración de los frutos (Aubert y Chanforan 2007). De acuerdo con Maroto (1990) los factores como; la dosis de regulador de crecimiento, el material vegetativo, el cultivar y las condiciones ambientales pueden influir en la respuesta de las plantas y los frutos. Al respecto Senesi et al. (2005) mencionan que las concentraciones altas de acetato de etilo están asociadas con un alto grado de maduración.
CONCLUSIONES
El uso de ANA en dosis de 0.1 y 0.4 mg L-1, incrementa la firmeza, sólidos solubles totales y cromaticidad de los frutos del cultivar de melón 'Navigator'. Los tratamientos de ANA no tuvieron efecto significativo en el peso, la longitud ecuatorial y polar de los frutos de ambos cultivares de melón evaluados.











 text new page (beta)
text new page (beta)



