Antecedentes
Los sarcomas son tumores malignos poco frecuentes que surgen a partir de tejido mesenquimal derivado del ectodermo. En 1998 Gaudin et al., clasificaron por primera vez en dos tipos, incluido el sarcoma prostático (SP) y los tumores de estroma de potencial maligno incierto (TEPMI). Representan menos del 1% de todos los cánceres diagnosticados anualmente en los Estados Unidos. Histopatológicamente, las células mesenquimales pueden madurar en músculo estriado y liso, cartílago, hueso, tejido adiposo y fibroso, dando una amplia gama de presentaciones clínicas.1
El pronostico global es malo independientemente de la modalidad de tratamiento. En el sarcoma de próstata el subtipo histológico parece tener importancia pronóstica, siendo los tipos más frecuentes rabdomiosarcoma, leiomiosarcoma, carcinosarcoma y sarcoma indiferenciado.1
Expertos informaron que el síntoma común de los pacientes que portan SP y TEPMI era la retención urinaria y que el antígeno prostático específico (APE) en la sangre a menudo permanece en un nivel normal. Sin embargo, con la baja incidencia, la información clínica aún no es clara. Aquí informamos un caso de SP en un hombre de 18 años con hematuria persistente y retención urinaria, discutimos los hallazgos en la cistoscopia, resección transuretral de próstata y la estrategia de tratamiento y el diagnóstico diferencial.1,2
Caso clínico
Se trata de un joven de 18 años de edad, admitido por primera vez en la sala de urgencias de Centro Médico del Instituto de Seguridad Social del Estado de México y Municipios (ISSEMyM) por retención aguda de orina, precedida de hematuria macroscópica, la exploración rectal digital de la próstata destacó asimetría y un nódulo dependiente de lóbulo izquierdo; se coloco sonda Foley transuretral 22 fr, lavado vesical y cistoclisis continúa hasta remisión de la hematuria, sin embargo persistió al grado que fue necesario la transfusión de dos hemoderivados por síndrome anémico; se realizó cistoscopia de urgencia al encontrar alteraciones hemodinámicas y resección transuretral de próstata/biopsia, con coagulación selectiva, una ves estabilizado desde el punto de vista hemodinámico y sin sangrado activo se decide ingreso hospitalario, donde se completa protocolo de hematuria (Figura 1).

Figura1 Cistoscopia posterior a evacuación de coágulos, destaca irregularidad del lóbulo izquierdo y el crecimiento discordante con la edad del paciente.
Los estudios de laboratorio documentaron además de anemia grado II de la OMS, infección de tracto urinario (ITU) y el urocultivo determinó positivo para E. Coli, multisensible. El resto se encontraban dentro de parámetros normales. Como parte del protocolo de hematuria solicitamos urotomografía la cual documentó próstata asimétrica, dependiente de lóbulo izquierdo, con zona hipodensa de 29 unidades Hounsfield (UH) que reforzaba a la aplicación de medio de contraste hasta 80 UH; el resto del estudio se encontraba dentro de parámetros normales (Figura. 1).
Se sometió a prostatectomía radical y el reporte definitivo de patología fue rabdomiosarcoma embrionario, positivo a miogenina y desmina. En la descripción microscópica se identifican fragmentos de tejido prostático en los que se identifica neoplasia maligna de estirpe mesenquimatoso con extensa necrosis, patrón de crecimiento solido o difuso, con células pequeñas de escaso citoplasma con núcleo hipercromático y abundantes mitosis. Inmunohistoquímica; miogenina positivo en los núcleos de la células neoplásicas, viomentina positivo en el citoplasma de las células neoplásicas, citoqueratina AE1/AE3 negativo, enolasa neuronal especifica negativo, CD99 negativo, CD45 negativo.
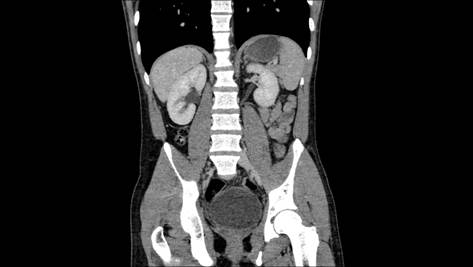
El paciente fue dado de alta al septimo día de la prostatectomía radical, con sonda Foley transuretral 22 fr, 3 vías, sin cistoclisis, y sin drenaje; cita cada 3 meses con tomografía abdominopélvica simple y contraste IV, tomografía de tórax simple, los primeros 6 meses y luego a los 6 meses, sin documentarse datos de recurrencia o compromiso ganglionar, mejorando la mecánica miccional al cuarto mes por completo (Figuras 2 y 3).

Figura 2 Tele de tórax a los 3 meses de la prostatectomía radical, sin datos de metástasis pulmonar.
Discusión
Los sarcomas del tejido blando pueden surgir a partir en cualquier parte del organismo. Son tumores poco frecuentes y casi siempre malignos originados a partir de tejido mesenquimal que deriva del ectodermo, se caracterizan por la expansión del estroma especializado de la próstata.2-5
El sarcoma primario de próstata es una variante rara y de pobre pronóstico. Se han estudiado posibles factores de riesgo como prostatitis, trauma perineal, biopsia de próstata previa y radiación. Los subtipos más comunes incluyen leiomiosarcoma, rabdomiosarcoma, histiocitoma fibroso maligno y los no clasificados. Rabdomiosarcoma es el reporte histopatológico definitivo más común, cerca de 40% en niños y en segundo lugar con 25% es el leiomiosarcoma. El rabdomiosarcoma en adultos tiene mayor potencial maligno y peor respuesta al tratamiento en comparación con niños.2,3
Leiomiosarcoma de próstata, variante con curso clínico agresivo. Con una mortalidad > al 90% a los 15 meses de diagnóstico, la recurrencia y las metástasis a pulmón son muy comunes y esperadas a pesar de la cirugía radical completa, el histopatológico demostró grado tumoral alto, 3 y 4, según la clasificación de Broders. Esta variante histológica generalmente recurre y resulta en la muerte, no hay una forma optima de tratamiento aunque la cirugía radical es la base. El histiocitoma maligno fibroso representa 0.1 a 0.24 % de todas las neoplasias prostáticas, hay muy poca información al respecto pero se describe como un tumor compuesto de células gigantes rápidamente progresivo con márgenes tumorales no circunscritos, además de marcado pleomorfismo que dificulta el diagnóstico temprano y la extirpación completa, que naturalmente impactan en una sobrevida similar a la variantes previas y en la que aun no hay forma optima de tratamiento.4,6-8
Existen alrededor de 50 reportes hasta el momento, muestran una distribución bimodal, apareciendo 15% antes de la primera década de la vida y un 30% después de la séptima década de la vida. El rabdomiosarcoma con mayor incidencia durante la niñez mientras que el leiomiosarcoma afecta principalmente a adultos jóvenes (< de 50 años).1,2,4
En la mayoría de los pacientes evaluados el síntoma inicial fue la retención aguda de orina y hematuria, aunque se han reportado otros como; dolor anal, sangrado transrectal, dolor abdominal.4,5
Los niveles de APE son normales, esto se debe a que el sitio de producción del APE es casi exclusivo por las células epiteliales de la próstata y glándulas periuretrales, depositado en el interior de las células en gránulos y vesículas citoplasmáticas, por lo no compromete el estroma prostático.4,5
En inmunohistoquimica el sarcoma de próstata es típicamente positivo para vimentina y CD34, con lo que se corrobora de la misma forma que el APE dentro de parámetros normales y la inmunohistoquimica clásica orientan al diagnóstico pero no son criterios diagnósticos (Tabla 1).4
Tabla 1
| Año de referencia | Edad | Síntoma Inicial | APE, ng/dl | CD34 | Vimentina |
| Zhan et al., 2014.9 | 22 | Disuria, polaquiuria. | 1.2 | - | positivo |
| Muglia et al., 2011.10 | 52 | Retención aguda de orina. | 7.5 | - | - |
| Rojas et al., 2013.11 | 39 | Retención aguda de orina. | 1.0 | - | - |
| Tamada et al., 2011.12 | 26 | Disuria y hematuria. | 0.44 | + | positivo |
Debido a la falta de sintomatología clásica, hay un subdiagnóstico o asemeja un cuadro clínico similar al crecimiento prostático benigno, en muchos casos esté mismo se documenta y el diagnóstico es por hallazgo de patología, sin sospecha de cáncer de próstata.5
La exploración rectal digital generalmente describe nódulos y la perdida de los limites prostáticos.5,13
Las características por ultrasonido transrectal más importantes para sarcoma de próstata son aumento de tamaño y márgenes irregulares, en el ultrasonido pélvico; se documenta próstata grande hipovascular. La tomografía abdominopélvica sin contraste exhibe una próstata aumentada de tamaño mal definida similar a la del caso que presentamos. La tomografía con contraste intravenoso (IV) generalmente muestra una próstata con zonas de necrosis y cambios quísticos debido al grado alto de diferenciación y crecimiento. La resonancia magnética (RM) muestra características similares en relación a una glándula prostática aumentada de tamaño, irregular y heterogénea, probablemente una característica importante es el reforzamiento periférico hiperintenso en T1, y en la zona central hipointenso en T1. El papel de la tomografía por emisión de positrones (PET/CT) sigue en estudio sin lograr hasta este momento ser sensible como método diagnóstico.1,13
Cuando el tumor es muy grande puede invadir los tejido adyacentes; la vejiga y el recto son los más vulnerables, presentado además la sintomatología descrita, dolor abdominal y aumento en la frecuencia de micción. Las metástasis tempranas no son raras en pacientes con SP, en el caso que describimos no se documentaron a los 12 meses de seguimiento, ni manifestó síntomas relacionados con dolor abdominal o aumento en la frecuencia miccional.13,14
Macroscópicamente el tumor muestra un patrón sólido que en ocasiones se fusiona con áreas quísticas, en tumores de alto grado también se describen zonas de necrosis y hemorragia. El tamaño no esta relacionado con el grado del tumor, como en otras patologías del ámbito urooncológico. El SC se clasifica microscópicamente según el grado de atipia celular; como la proliferación de células estromales con huso y ovoides, núcleos atípicos y necrosis. La resección quirúrgica sigue siendo el tratamiento de primera línea, por medio de prostatectomía radical, cistoprostatectomía y la exentaración pélvica, excepto cuando se evidencian metástasis. La radioterapia (RT) y la quimioterapia (QT) hasta el momento no muestran resultados contundentes. No se ha logrado un consenso sobre el mejor enfoque terapéutico. En los pacientes con metástasis en el momento del diagnóstico se debe ofrecer un enfoque multimodal que incluye quimioterapia con vincristina, actinomicina y ciclofosfamida y radioterapia local.13-15
Sin embargo al ser tumores voluminosos y con tendencia a la diseminación es difícil resecar completamente el tumor. Por lo que para hacer un plan quirúrgico adecuado es de suma importancia adquirir imágenes detalladas del tamaño, ubicación, estado de adhesión a órganos y/o estructuras del tumor, distribución vascular y metástasis antes de la cirugía. De acuerdo a lo anterior la resección y radicalidad total de la próstata es la oportunidad de prevenir recurrencia y diseminación de células cancerosas.13,15
En nuestro caso se realizó la prostatectomía radical con QT a base de adriamicina sin RT, se recabo el reporte de histopatología y los bordes se reportaron negativos. A los 12 meses no hay datos de recurrencia.4,6
El SP, en especial el rabdomiosarcoma es un subtipo de sarcoma del estroma prostático raro y altamente agresivo. No existe un enfoque terapéutico estándar para el sarcoma de próstata en general. 15
Lograr diferenciar el SP con otras patologías oncológicas y no oncológicas es muy importante ya que determina el tratamiento y pronóstico. Consideramos que el diagnóstico diferencial debe ser con CPO, absceso prostático y obviamente el adenocarcinoma de próstata.1











 text new page (beta)
text new page (beta)