Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Chapingo serie ciencias forestales y del ambiente
versão On-line ISSN 2007-4018versão impressa ISSN 2007-3828
Rev. Chapingo ser. cienc. for. ambient vol.27 no.3 Chapingo Set./Dez. 2021 Epub 04-Mar-2024
https://doi.org/10.5154/r.rchscfa.2020.12.078
Artículos científicos
Valor nutricional y degradación térmica de compuestos bioactivos en hongos comestibles silvestres
1 Universidad Autónoma Chapingo, Posgrado en Ciencia y Tecnología Agroalimentaria. km 38.5 Carretera México-Texcoco. C. P. 56230. Texcoco, Estado de México, México.
2 Universidad Autónoma Chapingo, Laboratorio de Productos Naturales, Departamento de Preparatoria Agrícola. km 38.5 Carretera México-Texcoco. C. P. 56230. Texcoco, Estado de México, México.
3 Universidad Autónoma Chapingo, Posgrado en Ingeniería Agrícola y Uso Integral del Agua. km 38.5 Carretera México-Texcoco. C. P. 56230. Texcoco, Estado de México, México.
4 Universidad Politécnica Metropolitana de Puebla. Popocatépetl s/n, Reserva Territorial Atlixcáyotl, Tres Cerritos. C. P. 72480. Puebla, Puebla, México.
Introducción:
El potencial nutricional de los hongos comestibles silvestres y la pérdida de sus propiedades nutracéuticas durante la cocción han sido poco explorados.
Objetivo:
Evaluar el contenido nutricional y el efecto del tratamiento térmico sobre las propiedades nutracéuticas en las especies silvestres Lactarius indigo (Schwein.) Fr. (hongo azul), Ramaria flava (Schaeff.) Quél. (escobetilla) e Hypomyces lactifluorum (Schwein.) Tul. & C. Tul. (hongo enchilado), recolectadas en bosque templado de pino y encino de la Sierra Norte de Puebla.
Materiales y métodos:
Los hongos se recolectaron en compañía de “hongueras tradicionales”. La composición proximal se cuantificó de acuerdo con los métodos de la AOAC. El efecto del tratamiento térmico se evaluó a 50 y 92 °C en intervalos de 10 a 60 minutos. El contenido fenólico total se determinó por el método Folin-Ciocalteu y la capacidad antioxidante mediante los ensayos ABTS y FRAP.
Resultados y discusión:
R. flava y L. indigo tuvieron los porcentajes más altos de proteína (24.02 %) y fibra cruda (14.64 %) en base seca, respectivamente. El hongo R. flava presentó el contenido fenólico más alto (4.40 mg equivalentes de ácido gálico por gramo de base seca) y la mayor capacidad antioxidante (23.65 µmol equivalentes de trolox por gramo de base seca). La cinética de degradación de los compuestos fue de primer orden; H. lactifluorum y R. flava tuvieron la mayor pérdida de fenoles y antioxidantes, respectivamente.
Conclusión:
Los hongos estudiados mostraron alto valor nutricional y conservaron más de 50 % de sus propiedades antioxidantes después del procesamiento térmico.
Palabras clave: Lactarius indigo; Ramaria flava; Hypomyces lactifluorum; fuente de nutracéuticos; cinética de degradación
Introduction:
Nutritional potential of wild edible mushrooms and loss of their nutraceutical properties during cooking have been little examined.
Objective:
To evaluate the nutritional content and effect of heat treatment on nutraceutical properties in the wild species Lactarius indigo (Schwein.) Fr. (blue mushroom), Ramaria flava (Schaeff.) Quél. (changle) and Hypomyces lactifluorum (Schwein.) Tul. & C. Tul. (lobster mushroom), collected in temperate pine and oak forests of the Sierra Norte de Puebla.
Materials and methods:
The mushrooms were collected in the company of “traditional mushroom collectors”. Proximal composition was quantified according to AOAC methods. The effect of heat treatment was evaluated at 50 and 92 °C at 10 to 60 min intervals. Total phenolic content was determined by the Folin-Ciocalteu method and antioxidant capacity by ABTS and FRAP assays.
Results and discussion:
R. flava and L. indigo had the highest percentages of protein (24.02 %) and crude fiber (14.64 %) on dry basis, respectively. R. flava had the highest phenolic content (4.40 mg gallic acid equivalents per gram dry basis) and the highest antioxidant capacity (23.65 µmol trolox equivalents per gram dry basis). Degradation kinetics of the compounds was first order; H. lactifluorum and R. flava had the highest loss of phenols and antioxidants, respectively.
Conclusion:
The mushrooms studied showed high nutritional value and retained more than 50 % of their antioxidant properties after thermal processing.
Keywords: Lactarius indigo; Ramaria flava; Hypomyces lactifluorum; source of nutraceuticals; degradation kinetics
Ideas destacadas:
Hongos analizados: Lactarius indigo, Hypomyces lactifluorum y Ramaria flava.
El efecto del tratamiento térmico se evaluó a 50 y 92 °C en intervalos de 10 a 60 minutos.
La cinética de degradación de los compuestos fenólicos y antioxidantes fue de primer orden.
Los hongos conservaron más de 50 % de sus compuestos antioxidantes después del tratamiento térmico.
L. indigo, H. lactifluorum y R. flava tienen potencial nutracéutico.
Introducción
En México, desde la época prehispánica, los hongos comestibles silvestres han sido un recurso alimenticio para diversos grupos étnicos de comunidades aisladas (Ruan-Soto, Ordaz-Velázquez, García-Santiago, & Ovando, 2017). De acuerdo con Garibay-Orijel y Ruan-Soto (2014), existen alrededor de 371 taxones de hongos comestibles silvestres en el territorio mexicano. En la Sierra Norte de Puebla, México, algunas comunidades nahuas mantienen la tradición de identificar y recolectar hongos comestibles para el autoconsumo y la comercialización en mercados locales (Contreras, Vázquez, & Ruan, 2018). Las mujeres conocidas como “hongueras tradicionales” son las protagonistas sociales en la recolección, procesamiento y comercialización de hongos silvestres; además, se encargan de transmitir el conocimiento ancestral para la discriminación de las especies comestibles y venenosas y para el reconocimiento de las asociaciones simbióticas entre hongos y árboles (Contreras et al., 2018; Garibay-Orijel, Ramírez-Terrazo, & Ordaz-Velázquez, 2012; Jasso-Arriaga, Martínez-Campos, & Dorantes-Coronado, 2019). En diversas comunidades aledañas al municipio de Zacapoaxtla, la recolección y comercialización de hongos en la temporada de lluvias es de gran importancia para la economía familiar, debido a la obtención de ingresos monetarios y suministros complementarios para los hogares (Estrada-Martínez, Guzmán, Cibrián-Tovar, & Ortega, 2009).
Los hongos Lactarius indigo (Schwein.) Fr. (hongo azul), Ramaria flava (Schaeff.) Quél. (escobetilla) e Hypomyces lactifluorum (Schwein.) Tul. & C. Tul. (hongo enchilado), debido a su sabor, consistencia y color, tienen gran demanda y aceptabilidad en el mercado, aunque solo hay oportunidad de consumirlos en la época de lluvias. Hypomyces lactifluorum de la familia Hypocreaceae es el resultado del parasitismo por el ascomiceto H. lactifluorum (Nectriaceae; Hypocreales) sobre Russula spp. o Lactarius spp.; el hongo crece en el basidiocarpo del hospedador, deformando su sombrero, tallo y branquias. Esta especie es muy demandada en los mercados populares por su color y sabor (Guzmán, 2008; Rochon, Paré, Khasa, & Fortin, 2009). El hongo L. indigo de la familia Russulaceae se ha inventariado en los estados de Chiapas, Hidalgo y Querétaro (León-Guzmán, Silva, & López, 1997; López-Vázquez, Prieto-García, Gayosso-Canales, Otazo, & Villagómez, 2017; Ruan-Soto, 2018); el extracto acuoso de esta especie exhibe actividad antibacteriana y citotóxica (Ochoa-Zarzosa, Vázquez-Garcidueñas, Robinson-Fuentes, & Vázquez-Marrufo, 2011). Con respecto a R. flava (familia Gomphaceae), el extracto etanólico de los cuerpos fructíferos presenta actividad antibacteriana y antifúngica moderada (Liu, Wang, Zhao, & Wang, 2013).
Los hongos se caracterizan por tener proteínas de buena calidad, alto contenido de fibra dietética y bajo contenido en grasas (Agrahar-Murugkar & Subbulakshmi, 2005; Barros, Venturini, Baptista, Estevinho, & Ferreira, 2008; Wang et al., 2014). Asimismo, los hongos poseen vitaminas primarias como la tiamina, riboflavina, niacina, tocoferol y vitamina D; sin embargo, esta última no se encuentra en los hongos cultivados (Cheung, 2010; Mattila et al., 2001; Sahagún, 2020). Entre las sustancias bioactivas presentes en los hongos destacan los compuestos fenólicos (flavonoides, ácidos fenólicos y cinámicos), tocoferoles, ácido ascórbico y carotenoides. Estas sustancias protegen a las células del daño oxidativo producido por los radicales libres (Ferreira, Barros, & Abreu, 2009; Sari, Prange, Lelley, & Hambitzer, 2017). Otros compuestos de interés son los β-glucanos; estos polisacáridos estimulan el sistema inmunitario, inhiben células tumorales, controlan la concentración de lípidos en la sangre y son una fuente de prebióticos que estimulan el crecimiento de la microbiota intestinal (Liu et al., 2012; Sawangwan, Wansanit, Pattani & Noysang, 2018; Vaz et al., 2010). Por lo anterior, los hongos son reconocidos como alimentos nutracéuticos (Barros et al., 2008).
El procesamiento y preservación de los hongos comestibles silvestres para su consumo, ya sea asados o cocidos al vapor, la mayoría de las veces implica un tratamiento térmico (Haro-Luna, Ruan-Soto, & Guzmán-Dávalos, 2019), el cual incluye la transferencia simultánea de calor y humedad; por tanto, es importante encontrar un modelo cinético que permita explorar su influencia sobre el contenido fenólico. En hongos cultivados como Pleurotus ostreatus (Jacq.) P. Kumm. y Agaricus bisporus (J. E. Lange), Imbach, Jaworska, Pogòn, Bernas, y Duda-Chodak (2015) demostraron que los compuestos fenólicos se degradan durante el proceso de cocción. En tal contexto, el objetivo de este trabajo fue evaluar el contenido nutricional y el efecto del tratamiento térmico sobre los compuestos fenólicos y la capacidad antioxidante de L. indigo, R. flava y H. lactifluorum. Estas especies se seleccionaron con base en el conocimiento micológico tradicional de recolectoras y vendedoras de hongos comestibles silvestres en el mercado de Zacapoaxtla, Puebla.
Materiales y métodos
Material micológico
Para seleccionar el material de estudio se hizo un recorrido en el mercado del municipio de Zacapoaxtla con el fin de localizar a las “hongueras tradicionales”, poseedoras del conocimiento micológico tradicional. Estas personas brindaron orientación y acompañamiento en la recolecta (septiembre del 2018) de alrededor de 20 especies de hongos comestibles, de las cuales se eligieron L. indigo, H. lactifluorum y R. flava con base en su abundancia y frecuencia de consumo (Figura 1).
La recolecta se hizo en la comunidad La Loma, municipio de Zacapoaxtla, Puebla, México (19° 49' 38.6” LN y -97 36' 10.7” LO a 2 140 m) (Figura 2). El tipo de vegetación es bosque templado de pino-encino. En la zona se encontraron individuos maduros de Pinus pseudostrobus Brongn.; dominancia de encinos como Quercus castanea Née, Q. laurina Bonpl., Q. crassifolia Bonpl. y Q. rugosa Née; individuos de Alnus acuminata Kunth, Buddleja sp. y Juniperus spp. cercanos a caminos y carreteras; y presencia de herbáceas de las familias Asteraceae, Lamiaceae y Fabaceae.
Las especies fúngicas se determinaron con base en la literatura siguiente: Guzmán (1977); Chacón, Guzmán, Montoya-Bello, y Bandala-Muñoz (1995); Montoya-Bello (1987); Mata et al. (2003); y Montoya y Bandala (2005). Las descripciones se hicieron a partir de cortes de los cuerpos fructíferos para observación en microscopio estereoscópico y compuesto; posteriormente, se hicieron tinciones con hidróxido de potasio y azul de lactofenol. Los nombres científicos, derivados a partir de las observaciones, se cotejaron con el estudio etnomicológico de Contreras et al. (2018) y se verificó la vigencia del nombre científico en la base de datos de Index Fungorum (2021). Un ejemplar de cada especie se depositó en la colección del herbario de la División de Ciencias Forestales de la Universidad Autónoma Chapingo (UACh).

Figura 1 Especies de hongos recolectadas en la comunidad La Loma, municipio de Zacapoaxtla, Puebla, México: a) Hypomyces lactifluorum, b) hongueras tradicionales, c) Ramaria flava, d) Lactarius indigo y e) zona de recolecta.
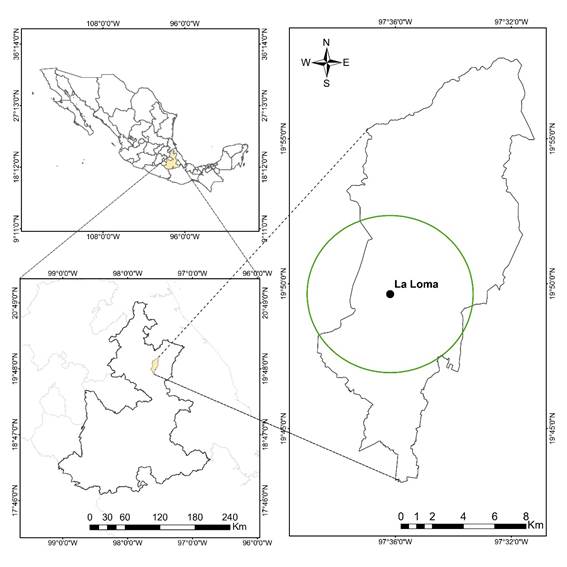
Figura 2 Ubicación de la zona de recolecta de los hongos comestibles silvestres en el municipio de Zacapoaxtla, Puebla, México.
De cada una de las tres especies de hongos comestibles silvestres se recolectaron aproximadamente 2 kg de cuerpos fructíferos. Los hongos cultivados A. bisporus y P. ostreatus se adquirieron en un supermercado de la Ciudad de México; estos se estudiaron para hacer una comparación directa con las especies silvestres. Los cuerpos fructíferos se limpiaron del exceso de tierra y hojarasca; la parte basal del estípite, cuando se encontraba dañada, se retiró con una navaja. Todos los ejemplares se liofilizaron y conservaron en congelación a -18 °C hasta su análisis.
Reactivos e instrumentación
Los reactivos Folin-Ciocalteu, carbonato de sodio, acetato de sodio trihidratado 2,4,6-tripiridil-s triazine (TPTZ), cloruro de hierro (III) hexahidratado, catequina, cloruro de aluminio, acetato de potasio, persulfato de potasio, 2,2-azinobis,3-etilbenzotiazolino-6-sulfónico (ABTS) y los ácidos 6-hidroxi-2,5,7,8-tetrametilcromano-2-carboxilico (trolox) y gálico corresponden a productos Sigma Aldrich (St. Louis, Mo., EUA). Las absorbancias para la cuantificación de fenoles, flavonoides y capacidad antioxidante se midieron en un lector de microplacas Synergy 2 Microplate Reader, software Gen5 (BioTek Instruments Inc., Winooski, VT, EUA).
Propiedades nutricionales y potencial nutracéutico
La composición proximal de los hongos liofilizados se determinó por triplicado de acuerdo con los métodos de la AOAC (2005). La proteína cruda (N x 6.25) se estimó por el método Kjeldahl, el extracto etéreo se obtuvo por Soxhlet y el contenido de cenizas se determinó por incineración a 550 °C.
La composición nutracéutica se evaluó in vitro; para ello,
se obtuvieron extractos con metanol al 80 % siguiendo el método reportado
por Hernández-Rodríguez et al. (2016). El contenido fenólico total en cada
extracto se cuantificó por el método de Folin-Ciocalteu adaptado a
microplacas (Hernández-Rodríguez et al., 2016). La curva de calibración se
preparó a partir de una disolución stock de ácido gálico en
el intervalo lineal de concentraciones de 2.5 a 29.0 µg∙mL-1. Los
resultados se expresaron como miligramos equivalentes de ácido gálico por
gramo de muestra en base seca (mg EAG∙
Determinación de carotenoides totales
Los carotenoides se determinaron en H. lactifluorum de
acuerdo con el procedimiento de Camargo, Xavier, Alves, Flanch, y Ruffo
(2015) con algunas modificaciones. La muestra liofilizada (0.2 g) y
protegida de la luz se mezcló con 10 mL de una solución de hexano/acetona
(6:4, v/v), se agitó en vortex por 1 min y se incubó por 10 min a 150 rpm.
El sobrenadante se separó por filtración y se obtuvo el espectro
ultravioleta-visible (UV-VIS) en el que se observó un máximo a 450 nm,
correspondiente a los carotenoides. El intervalo de la curva de calibración
del β-caroteno fue de 0.5 a 4.0 µg∙mL−1. Los resultados se
expresaron como miligramos de β-caroteno por gramo de muestra en base seca
(mg EβC∙
Capacidad antioxidante
La capacidad antioxidante de los extractos se evaluó mediante los ensayos
ABTS (Re et al., 1999) y FRAP (ferric reducing
ability of plasma; Benzie & Strain, 1996) adaptados a
microplacas. Las curvas de calibración de trolox se prepararon en rangos de
concentración de 5.0 a 60 μM y de 3.8 a 46.0 μM, para ABTS y FRAP,
respectivamente. Los resultados se expresaron como micromoles equivalentes
de trolox por gramo de muestra en base seca (µm ET∙
Tratamiento térmico
La cinética de degradación del contenido fenólico total y la pérdida de la capacidad antioxidante de los hongos se evaluaron a 50 °C (temperatura cercana al inicio de la degradación de compuestos fenólicos; Zhou et al., 2016) y 92 °C (punto de ebullición del agua en el sitio de experimentación) por 0, 10, 20, 30, 40, 50 y 60 min para cada temperatura. En cada especie, una porción (0.5 g) previamente liofilizada se transfirió a un tubo Pyrex® y se hidrató con 10 mL de agua destilada. Las muestras se colocaron en un baño termostático de agua precalentada a cada una de las temperaturas de estudio y se retiraron a intervalos de tiempo de 10 hasta 60 minutos. Inmediatamente, las muestras se enfriaron en un baño de agua con hielo y se liofilizaron; en cada una se determinó, por triplicado, el contenido fenólico total y la capacidad antioxidante.
Análisis de datos
Los fenoles, flavonoides y carotenoides totales, así como la capacidad antioxidante, se determinaron por triplicado y se obtuvieron las medias y la desviación estándar. El contenido de nutrientes se comparó entre las especies mediante un diseño completamente al azar y se utilizó, como estadístico de análisis, la prueba de medias de Tukey (P ≤ 0.05).
El orden de reacción de la cinética de degradación de los compuestos fenólicos se determinó graficando la concentración de fenoles totales con respecto al tiempo, probando los modelos cinéticos de primer y segundo orden:
donde,
k = constante de velocidad de degradación (mol∙g-1∙min-1) de los compuestos antioxidantes durante el tratamiento térmico
t = tiempo del tratamiento (s)
CA y CA0 = concentraciones de los compuestos fenólicos en el tiempo t y en el tiempo 0, respectivamente.
Resultados y discusión
El Cuadro 1 presenta los resultados del análisis proximal de los hongos comestibles silvestres en estudio. El contenido de humedad (87 a 90 %) no presentó diferencias significativas y fue menor (P ≤ 0.05) que el reportado para las mismas especies recolectadas en Querétaro, México (Yahia, Gutiérrez-Orozco, & Moreno-Pérez, 2017). El contenido de cenizas en R. flava fue menor (P ≤ 0.05) que en H. lactifluorum y L. indigo; en general, las tres especies presentaron mayor contenido que los hongos silvestres y comerciales (0.17 a 1.17 %) evaluados por Álvarez-Parrilla, de la Rosa, Martínez, y González (2007) en Chihuahua, México. Por otro lado, el contenido de fibra dietética de los hongos silvestres (7.58 a 14.64 %) fue menor en comparación con el encontrado por Manzi, Aguzzi, y Pizzoferrato (2001) en A. bisporus y P. ostreatus. Con respecto a la proteína cruda, H. lactifluorum tuvo el contenido más bajo; sin embargo, resultó superior al determinado en A. bisporus (13.75 %) y P. ostreatus (8.58 %) por Jaworska, Pogoń, Bernaś, y Duda-Chodak (2015), y al encontrado en R. flava (14.47 %) y L. indigo (13.42 %) por Silva y Lo (1997). Estas diferencias podrían ser explicadas por las condiciones edafoclimáticas y el tipo de sustrato en el que los hongos se desarrollan (Kalač, 2013). Según Cheung (2010), la calidad proteica de los hongos es mejor que la de los vegetales, ya que contienen todos los aminoácidos proteicos; por lo tanto, dichos especímenes constituyen un alimento alternativo para las personas vegetarianas. El perfil de macronutrientes reveló que las tres especies son una fuente importante de proteínas con bajo contenido en grasas. Estas propiedades han sido descritas para otros hongos comestibles silvestres (Cheung, 2010).
La composición de nutrientes de las especies estudiadas es de gran importancia para mantener una dieta balanceada y representa una alternativa ante la falta de recursos de los consumidores locales para la adquisición de alimentos convencionales ricos en proteínas.
Cuadro 1. Composición proximal (gramos por 100 g de peso seco) de los hongos comestibles silvestres recolectados en Zacapoaxtla, Puebla, México.
| Especie | Cenizas | Proteína cruda | Lípidos totales | Fibra cruda | Carbohidratos |
|---|---|---|---|---|---|
| Lactarius indigo | 12.93 ± 1.79 a | 23.29 ± 1.30 a | 3.19 ± 0.25 a | 14.64 ± 0.22 a | 45.95 ± 0.00 c |
| Ramaria flava | 7.77 ± 0.46 b | 24.02 ± 0.42 a | 1.20 ± 0.34 b | 7.58 ± 0.09 c | 59.43 ± 0.00 a |
| Hypomyces lactifluorum | 15.06 ± 0.03 a | 20.27 ± 0.78 b | 2.67 ± 0.15 a | 12.08 ± 0.36 b | 49.92 ± 0.00 b |
Letras diferentes en cada columna indican diferencias significativas de acuerdo con la prueba de Tukey (P < 0.05). Los valores son el promedio ± la desviación estándar calculados para tres repeticiones por muestra.
Composición nutracéutica
El Cuadro 2 muestra que R.
flava tuvo mayor contenido fenólico (P <
0.05) que H. lactifluorum y L. indigo; sin
embargo, la concentración más alta se encontró en A.
bisporus que, en conjunto con P. ostreatus, se
estudiaron para hacer una comparación directa con las especies silvestres.
Las concentraciones de fenoles totales fueron menores comparadas con las
determinadas por Yahia et al. (2017)
para L. indigo, H. lactifluorum y R. flava
(6.6, 6.33 y 7.26 mg EAG∙
Cuadro 2 Compuestos bioactivos totales y capacidad antioxidante (expresados en base seca) de los hongos silvestres comestibles recolectados en Zacapoaxtla, Puebla, y de dos especies comerciales (Agaricus bisporus y Pleurotus ostreatus).
| Fenoles totales (mg EAG gdb -1) | Carotenoides totales (mg EβC gdb -1) | Flavonoides totales (mg EC gdb -1) | ABTS (µmol ET gdb -1) | FRAP (µmol ET gdb -1) | |
|---|---|---|---|---|---|
| Lactarius indigo | 2.92 ± 0.02 c | NC | 0.83 ± 0.05 b | 10.42 ± 0.02 c | 9.03 ± 0.01 c |
| Ramaria flava | 4.40 ± 0.01 b | NC | 2.25 ± 0.04 a | 23.65 ± 0.02 b | 20.17 ± 0.02 a |
| Hypomyces lactifluorum | 2.98 ± 0.04 c | 0.117 | ND | 5.78 ± 0.03 e | 3.75 ± 0.02 d |
| Agaricus bisporus | 6.81 ± 0.03 a | NC | NC | 26.64 ± 0.04 a | 18.79 ± 0.03 b |
| Pleurotus ostreatus | 1.57 ± 0.01 d | NC | NC | 7.47 ± 0.01 d | 2.47 ± 0.01 e |
Ensayos para determinar la capacidad antioxidante (µmol ET: micromoles equivalentes de trolox): ABTS = 2,2-azinobis,3-etilbenzotiazolino-6-sulfónico, FRAP = poder antioxidante férrico reductor. mg EAG, mg EβC, mg EC: miligramos equivalentes de ácido gálico, catequina y caroteno, respectivamente. ND = no detectado, NC = no cuantificado. Los valores con letras diferentes en cada columna indican diferencias significativas de acuerdo con la prueba de Tukey (P < 0.05). Los valores son el promedio ± la desviación estándar calculados para tres repeticiones por muestra.
Por otro lado, como se muestra en el Cuadro
2, la concentración de flavonoides totales en R.
flava, respecto al contenido fenólico total, corresponde al
51.1 %, mientras que en H. lactifluorum, dichos compuestos
no se detectaron, probablemente por el método de extracción utilizado. Las
concentraciones de flavonoides en L. indigo y R.
flava fueron inferiores a las obtenidas por Yahia et al. (2017) para las mismas
especies, pero en el caso de L. indigo (con base en
catequina, 0.83 mg EC∙
En el espectro UV-VIS del extracto de hexano/acetona de H.
lactifluorum se observó un máximo a una longitud de onda de 450
nm, característico de los carotenoides (Camargo et al., 2015). El contenido
de carotenoides en este hongo fue superior al encontrado en hongos
comestibles silvestres de Polonia y Portugal (Barros, Ferreira, Queirós,
Ferreira, & Baptista, 2007; Robaszkiewichz, Bartosz, Lawrynowicz, &
Soszynski, 2010) y en frutos como Artocarpus heterophyllus
Lam (0.0018 a 0.0079 mg∙
Capacidad antioxidante
Los agentes antioxidantes reducen radicales libres mediante dos mecanismos: por la trasferencia de electrones o por la transferencia de átomos de hidrógeno. Los ensayos ABTS y FRAP permiten medir la reducción de radicales libres mediante el mecanismo de transferencia de electrones (Ozgen, Reese, Tulio, Scheerens, & Miller, 2006); por tanto, estos dos métodos se usaron para corroborar la capacidad antioxidante en los extractos polares de los hongos bajo estudio. Los hongos mostraron diferencia significativa en la capacidad antioxidante en cada uno de los ensayos; A. bisporum y R. flava tuvieron los valores más altos, mientras que H. lactifluorum y P. ostreatus presentaron los más bajos (Cuadro 2). De acuerdo con los resultados descritos por Yahia et al. (2017), R. flava también tuvo la mayor capacidad antioxidante, seguido de L. indigo y H. lactifluorum. Debido a que los carotenoides son compuestos con propiedades antioxidantes sería recomendable probar la capacidad antioxidante en extractos no polares.
En general, las muestras con mayor capacidad antioxidante también tuvieron mayor contenido fenólico (Cuadro 2). Según Cheung, Cheung, y Ooi (2003), las propiedades antioxidantes de los hongos se atribuyen principalmente a compuestos de bajo peso molecular como los flavonoides, ácidos fenólicos y cinámicos. En años recientes, la demanda en el consumo de componentes bioactivos ha sido creciente, por lo tanto, los hongos son una buena alternativa.
Los compuestos fenólicos en los alimentos de origen vegetal (Faller & Fialho, 2009; Kalogeropoulos, Grigorakis, Mylona, Falirea, & Andrikopoulos, 2006) y en los hongos (Jaworska et al., 2015) pueden ser afectados por el procesamiento térmico. De acuerdo con Patras, Bruton, Tiwari, y Butler (2011) es recomendable el empleo de un modelo cinético que prediga la influencia del procesamiento de los alimentos sobre parámetros críticos de calidad. El orden de reacción correspondiente a la cinética de degradación de los compuestos en los hongos se determinó graficando la concentración de fenoles totales contra el tiempo (0 a 60 min) a 50 y 92 °C, probando los modelos cinéticos de primer y segundo orden, hasta encontrar relación lineal. Los parámetros cinéticos se obtuvieron aplicando las ecuaciones Ln(CA/CA0) = -kt (primer orden) y (1/CA -1/CA0) = kt (segundo orden). De acuerdo con el Cuadro 3, los dos modelos presentaron coeficientes de determinación aceptables; no obstante, el modelo matemático de primer orden tuvo coeficientes de determinación mayores.
Cuadro 3 Constantes de velocidad (k) de degradación de compuestos fenólicos en hongos silvestres Hypomyces lactifluorum, Ramaria flava y Lactarius indigo.
| Especie | Temperatura (ºC) | Primer orden | Segundo orden | ||
|---|---|---|---|---|---|
| k* | R2 | k* | R2 | ||
| H. lactifluorum | 50 | 4 x 10-5 | 0.9930 | 1 x 10-5 | 0.9910 |
| 0.9916 | 0.9883 | ||||
| 0.9895 | 0.9868 | ||||
| 92 | 0.0002 | 0.9828 | 8 x 10-5 | 0.9535 | |
| 0.9798 | 0.9463 | ||||
| 0.9821 | 0.9528 | ||||
| R. flava | 50 | 6 x 10-5 | 0.9926 | 2 x 10-5 | 0.9884 |
| 0.9857 | 0.9805 | ||||
| 0.9868 | 0.9799 | ||||
| 92 | 0.0001 | 0.9885 | 3 x 10-5 | 0.9939 | |
| 0.9908 | 0.9936 | ||||
| 0.9887 | 0.9909 | ||||
| L. indigo | 50 | 7 x 10-5 | 0.9675 | 3 x 10-5 | 0.9589 |
| 0.9713 | 0.9632 | ||||
| 0.9769 | 0.9697 | ||||
| 92 | 0.0001 | 0.9963 | 4 x 10-5 | 0.9982 | |
| 0.9964 | 0.9894 | ||||
| 0.9941 | 0.9900 | ||||
*Los valores mostrados son el promedio de tres repeticiones.
De forma similar, la cinética de degradación de la capacidad antioxidante de los hongos se determinó a 50 y 92 °C con intervalos de 10 a 60 minutos. Las constantes de velocidad de la pérdida de capacidad antioxidante para cada especie se muestran en el Cuadro 4. La aplicación del modelo cinético de primer orden tuvo coeficientes de correlación más altos.
Cuadro 4 Constantes de velocidad (k) de degradación de la capacidad antioxidante en hongos silvestres Hypomyces lactifluorum, Ramaria flava y Lactarius indigo.
| Especie | T (ºC) | Parámetro | Primer orden | Segundo orden | ||
|---|---|---|---|---|---|---|
| k* | R2 | k* | R2 | |||
| H. lactifluorum | 50 | ABTS | 4 x 10-5 | 0.9853 | 8 x 10-5 | 0.983 |
| 0.9907 | 0.991 | |||||
| 0.9926 | 0.993 | |||||
| FRAP | 8 x 10-5 | 0.9753 | 2 x 10-5 | 0.9638 | ||
| 0.9659 | 0.952 | |||||
| 0.9796 | 0.9694 | |||||
| 92 | ABTS | 0.0566 | 0.994 | 0.0117 | 0.9903 | |
| 0.9942 | 0.9929 | |||||
| 0.9913 | 0.9921 | |||||
| FRAP | 0.0001 | 0.9921 | 4 x 10-5 | 0.9751 | ||
| 0.9891 | 0.9705 | |||||
| 0.9912 | 0.9742 | |||||
| R. flava | 50 | ABTS | 6 x 10-5 | 0.9803 | 3 x 10-6 | 0.9709 |
| 0.9802 | 0.9708 | |||||
| 0.9833 | 0.9744 | |||||
| FRAP | 8 x 10-5 | 0.9409 | 5 x 10-6 | 0.9275 | ||
| 0.9411 | 0.9281 | |||||
| 0.9371 | 0.9235 | |||||
| 92 | ABTS | 0.0001 | 0.992 | 6 x 10-6 | 0.9921 | |
| 0.9907 | 0.9898 | |||||
| 0.9926 | 0.9911 | |||||
| FRAP | 0.0003 | 0.9423 | 3 x 10-5 | 0.8227 | ||
| 0.943 | 0.8247 | |||||
| 0.942 | 0.8221 | |||||
| L. indigo | 50 | ABTS | 7 x 10-5 | 0.9854 | 7 x 10-6 | 0.9819 |
| 0.9847 | 0.9784 | |||||
| 0.9865 | 0.9818 | |||||
| FRAP | 5 x 10-5 | 0.9753 | 6 x 10-6 | 0.9656 | ||
| 0.982 | 0.9734 | |||||
| 0.9838 | 0.9767 | |||||
| 92 | ABTS | 9 x 10-5 | 0.9778 | 1 x 10-5 | 0.9797 | |
| 0.9793 | 0.9807 | |||||
| 0.9774 | 0.9793 | |||||
| FRAP | 8 x 10-5 | 0.9905 | 1 x 10-5 | 0.9915 | ||
| 0.9854 | 0.9879 | |||||
| 0.99 | 0.9907 | |||||
*Los valores mostrados son el promedio de tres repeticiones. Ensayos para determinar la capacidad antioxidante: ABTS = 2,2-azinobis,3-etilbenzotiazolino-6-sulfónico, FRAP = poder antioxidante férrico reductor.
La Figura 3 muestra el comportamiento lineal cuando se aplica el modelo cinético de primer orden, tanto del contenido fenólico total como de la capacidad antioxidante (ABTS y FRAP), en las especies sometidas a tratamiento térmico de 50 y 92 °C desde un tiempo 0 a 60 minutos. En las tres variables evaluadas se observa la misma tendencia, a medida que el tiempo y temperatura de cocción incrementan también la degradación de compuestos fenólicos y antioxidantes se eleva. El hongo H. lactifluorum presentó mayor degradación de fenoles totales cuando se aplicó una temperatura de 92 °C por 60 min y R. flava mostró mayor disminución de capacidad antioxidante a una temperatura de cocción de 92 °C.

Figura 3 Pérdida del contenido fenólico total y de la capacidad antioxidante (ensayos ABTS [2,2-azinobis,3-etilbenzotiazolino-6-sulfónico] y FRAP [poder antioxidante férrico reductor]) en hongos comestibles silvestres a dos temperaturas durante 60 minutos de calentamiento. CA y CA0: concentraciones de los compuestos (fenólicos y antioxidantes) en el tiempo t y en el tiempo 0, respectivamente.
De acuerdo con los resultados, las pérdidas de contenido fenólico total fueron 14 % para H. lactifluorum y 21 % en R. flava bajo condiciones de 50 °C por 60 min, pero a mayor temperatura (92 °C, 60 min), la reducción varió de 31 % para L. indigo a 48 % para H. lactifluorum. Estas pérdidas son inferiores a las reportadas por Jaworska et al. (2015) para A. bisporus (38 %) y P. ostreatus (65 %) cocinados en estofado. En otro trabajo realizado por Öztürk, Öztürk, y Duru (2014) se encontró que, antes de cocinar, el extracto metanólico de R. flava contenía 5.9 mg de fenoles por gramo de extracto y, después de cocinar, la concentración aumentó a 9.84 mg de fenoles por gramo de extracto; estos resultados difieren de los obtenidos en el presente trabajo. La aplicación de tratamientos térmicos en alimentos ricos en antioxidantes disminuye su contenido, debido a la naturaleza termosensible de estos compuestos. De acuerdo con Blessington et al. (2010), las diferencias observadas de pérdida podrían estar relacionadas con la naturaleza química de los compuestos fenólicos de cada una de las especies y con la complejidad de la matriz en la que están unidos a biomoléculas como carbohidratos, grasa o proteínas.
Con respecto a la capacidad antioxidante, en el caso del ensayo FRAP, el intervalo de pérdida varió entre 26 % para L. indigo y 74 % para R. flava, mientras que para ABTS, la pérdida fue de 29 % para L. indigo y 34 % para R. flava. En general, la pérdida de capacidad antioxidante fue inferior que la reportada por Jaworska et al. (2015) para A. bisporus (50.34 % [ABTS] y 53.55 % [FRAP]) y P. ostreatus (53.39 % [ABTS] y 48.52 % [FRAP]).
El estudio cinético de la disminución del contenido fenólico total y de la capacidad antioxidante de los hongos evaluados es de gran utilidad para la optimización de temperaturas y tiempos de cocción; por ejemplo, de acuerdo con la información proporcionada por personas del municipio de Zacapoaxtla, Puebla, la preparación de los hongos recolectados consiste en un tratamiento térmico a ebullición por un tiempo de 20 minutos. Con esta información, se puede estimar la pérdida del contenido fenólico total y la capacidad antioxidante de cada una de las especies (Cuadros 3 y 4); además, se podría recomendar disminuir la temperatura de cocción para la preservación de los compuestos bioactivos.
Conclusiones
Lactarius indigo, Hypomyces lactifluorum y Ramaria flava representan una fuente importante de compuestos nutricionales y bioactivos benéficos para la salud. Los hongos presentaron alto contenido de proteína (20 a 24 %) y bajo contenido de lípidos (1 a 3.2 %). Con respecto al contenido de compuestos fenólicos (2.9 a 4.4 mg equivalentes de ácido gálico), H. lactifluorum tuvo la mayor degradación. Por otra parte, R. flava mostró la mayor capacidad antioxidante, que disminuyó cuando la temperatura y el tiempo de cocción aumentaron; sin embargo, las tres especies conservaron más del 50 % de sus propiedades antioxidantes después del procesamiento térmico. Para evitar o reducir la degradación de los compuestos bioactivos, se recomienda la reducción de la temperatura de cocción, la cual es cercana o igual a la de ebullición. Es importante generar estrategias de conservación, reproducción y comercialización de hongos silvestres, y posicionarlos como un alimento funcional de temporada que amalgame el desarrollo social, el empoderamiento de la mujer y la conservación forestal.
REFERENCIAS
Agrahar-Murugkar, D., & Subbulakshmi, G. (2005). Nutritional value of edible wild mushrooms collected from the Khasi hills of Meghalaya. Food Chemistry, 89(4), 599-603. doi: 10.1016/j.foodchem.2004.03.042 [ Links ]
Alvarez-Parrilla, E., de la Rosa, L. A., Martínez, N. R., & González, G. A. A. (2007). Total phenols and antioxidant activity of commercial and wild mushrooms from Chihuahua, México. Ciencia y Tecnología Alimentaria, 5(5), 329-334. doi: 10.1080/11358120709487708 [ Links ]
AOAC International. (2005). Official methods of analysis of AOAC (18th ed.). Arlington, TX, USA: Author. [ Links ]
Aquino-Bolaños, E. N., Urrutia-Hernández, T. A., López Del Castillo-Lozano, M., Chavéz-Servia, J. L., & Verdalet-Guzmán, I. (2013). Physicochemical parameters and antioxidant compounds in edible squash (Cucurbita pepo) flower stored under controlled atmospheres. Journal of Food Quality, 36(5), 302-308. doi: 10.1111/jfq.12053 [ Links ]
Barros, L., Ferreira, M.-J., Queirós, B., Ferreira, I. C. F. R., & Baptista, P. (2007). Total phenols, ascorbic acid, β-carotene and lycopene in Portuguese wild edible mushrooms and their antioxidant activities. Food Chemistry, 103(2), 413-419. doi: 10.1016/j.foodchem.2006.07.038 [ Links ]
Barros, L., Venturini, B. A., Baptista, P., Estevinho, L. M., & Ferreira, I. C. (2008). Chemical composition and biological properties of portuguese wild mushrooms: a comprehensive study. Journal of Agricultural and Food Chemistry, 56(10), 3856-3862. doi: 10.1021/jf8003114 [ Links ]
Benzie, I. F. F., & Strain, J. J. (1996). The ferric reducing ability of plasma (FRAP) as a measure of “antioxidant power”: The FRAP assay. Analytical Biochemistry, 239(1), 70-76. doi: 10.1006/abio.1996.0292 [ Links ]
Blessington, T., Nzaramba, M. N., Scheuring, D. C., Hale, A. L., Reddivari, L., & Miller, J. C. Jr. (2010). Cooking methods and storage treatments of potato: effects of carotenoids, antioxidant activity and phenolics. American Journal of Potato Research, 87, 479e491. doi: 10.1007/s12230-010-9150-7 [ Links ]
Camargo, L., Xavier, V., Alves, J., Flach, A., & Ruffo, S. (2015). Bioactive compounds and antioxidant activity in pre-harvest camu-camu [Myrciaria dubia ( H. B. K.) Mc Vaugh] fruits. Scientia Horticulturae Journal, 186, 223-229. doi: 10.1016/j.scienta.2015.02.031 [ Links ]
Contreras, C. L. E. U., Vázquez, G. A., & Ruan-Soto, F. (2018). Etnomicología y venta de hongos en un mercado del Noroeste del estado de Puebla, México. Scientia Fungorum, 47, 47-55. Retrieved from http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S2594-13212018000100047&lng=es&tlng=es [ Links ]
Chacón, S., Guzmán, G., Montoya-Bello, L., & Bandala-Muñoz, V. M. (1995). Guía ilustrada de los hongos del Jardín Botánico Francisco Javier Clavijero de Xalapa, Veracruz y áreas circunvecinas. Xalapa, Veracruz, México: Instituto de Ecología, A. C. [ Links ]
Cheung, P. C. K. (2010). The nutritional and health benefits of mushrooms. Nutrition Bulletin, 35(4), 292-299. doi: 10.1111/j.1467-3010.2010.01859.x [ Links ]
Cheung, L. M., Cheung, P. C. K., & Ooi, V. E. C. (2003). Antioxidant activity and total phenolics of edible mushroom extracts. Food Chemistry, 81(2), 249-255. doi: 10.1016/S0308-8146(02)00419-3 [ Links ]
de Faria, A. F., de Rosso, V. V., & Mercadante, A. Z. (2009). Carotenoid composition of jackfruit (Artocarpus heterophyllus), determined by HPLC-PDA-MS/MS. Plant Foods for Human Nutrition, 64(2), 108-115. doi: 10.1007/s11130-009-0111-6 [ Links ]
Estrada-Martínez, E., Guzmán, G., Cibrián, T. D., & Ortega, P. R. (2009). Contribución al conocimiento etnomicológico de los hongos comestibles silvestres de mercados regionales y comunidades de la Sierra Nevada (México). Revista Interciencia, 34(2), 25-33. Retrieved from http://ve.scielo.org/scielo.php?script=sci_arttext&pid=S0378-18442009000100006&lng=es&tlng=es [ Links ]
Faller, A., & Fialho, E. (2009). The antioxidant capacity and polyphenol content of organic and conventional retail vegetables after domestic cooking. Food Research International, 42(1), 210-215. doi: 10.1016/j.foodres.2008.10.009 [ Links ]
Ferreira, I., Barros, L., & Abreu, R. (2009). Antioxidants in wild mushrooms. Current Medicinal Chemistry, 16(12), 1543-1560. doi: 10.2174/092986709787909587 [ Links ]
Garibay-Orijel, R., Ramírez-Terrazo, A., & Ordaz-Velázquez, M. (2012). Women care about local knowledge, experiences from ethnomycology. Journal of Ethnobiology and Ethnomedicine, 8(1), 25. doi: 10.1186/1746-4269-8-25 [ Links ]
Garibay-Orijel, R., & Ruan-Soto, F. (2014). Listado de los hongos silvestres consumidos como alimento tradicional en México. In A. Moreno-Fuentes, & R. Garibay-Orijel (Eds.), La etnomicología en México, estado del arte. México: CONACYT-UAEH-UNAM. Retrieved from http://www.scielo.org.mx/scielo.php?script=sci_nlinks&pid=S2594-1321201800010004700019&lng=en [ Links ]
Guzmán, G. (1977). Identificación de los hongos comestibles, venenosos y alucinantes y destructores de la madera. Mexico: Ed. Limusa. [ Links ]
Guzmán, G. (2008). Diversity and use of traditional Mexican medicinal fungi. A review. International Journal of Medicinal Mushrooms, 10(3), 209-217. Retrieved from https://inecol.repositorioinstitucional.mx/jspui/bitstream/1005/120/1/8311_2008-10203.pdf [ Links ]
Haro-Luna, M. X., Ruan-Soto, F., & Guzmán-Dávalos, L. (2019). Traditional knowledge, uses, and perceptions of mushrooms among the Wixaritari and mestizos of Villa Guerrero, Jalisco, Mexico. IMA Fungus, 10(1), 16. doi: 10.1186/s43008-019-0014-6 [ Links ]
Hernández-Rodríguez, G., Espinosa-Solares, T., Hernández-Eugenio, G., Villa-García, M., Reyes-Trejo, B., & Guerra-Ramírez, D. (2016). Influence of polar solutions on the extraction of phenolic compounds from capulin fruits (Prunus serotina). Journal of the Mexican Chemical Society, 60(2), 73-78. Retrieved from http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1870-249X2016000200073&lng=es&tlng=en [ Links ]
Index Fungorum (2021). Retrieved from http://www.indexfungorum.org/Names/Names.asp [ Links ]
Jasso-Arriaga, X., Martínez-Campos, Á. R., & Dorantes-Coronado, E. J. (2019). Más allá de la comercialización de hongos comestibles silvestres en la comunidad de San Antonio Acahualco, México. AGROProductividad, 12(5), 9-17. doi: 10.32854/agrop.v0i0.1396 [ Links ]
Jaworska, G., Pogoń, K., Bernaś, E., & Duda-Chodak, A. (2015). Nutraceuticals and antioxidant activity of prepared for consumption commercial mushrooms Agaricus bisporus and Pleurotus ostreatus. Journal of Food Quality, 38(2), 111-122. doi: 10.1111/jfq.12132 [ Links ]
Kalogeropoulos, N., Grigorakis, D., Mylona, A., Falirea, A., & Andrikopoulos, N. K. (2006). Dietary evaluation of vegetables pan-fried in virgin olive oil following the greek traditional culinary practice. Ecology of Food and Nutrition, 45(2), 105-123. doi: 10.1080/03670240500530642 [ Links ]
Kalač, P. (2013). A review of chemical composition and nutritional value of wild-growing and cultivated mushrooms. Journal of the Science of Food and Agriculture, 93(2), 209-218. doi: 10.1002/jsfa.5960 [ Links ]
Kubola, J., & Siriamornpun, S. (2011). Phytochemicals and antioxidant activity of different fruit fractions (peel, pulp, aril and seed) of Thai gac (Momordica cochinchinensis Spreng). Food Chemistry, 127(3), 1138-1145. doi: 10.1016/j.foodchem.2011.01.115 [ Links ]
León-Guzmán, M. F., Silva, I., & López, M. G. (1997). Proximate chemical composition, free amino acid contents, and free fatty acid contents of some wild edible mushrooms from Querétaro, México. Journal of Agricultural and Food Chemistry, 45(11), 4329-4332. doi: 10.1021/jf970640u [ Links ]
Liu, Y. T., Sun, J., Luo, Z. Y., Rao, S. Q., Su, Y. J., Xu, R. R., & Yang, Y. J. (2012). Chemical composition of five wild edible mushrooms collected from Southwest China and their antihyperglycemic and antioxidant activity. Food and Chemical Toxicology, 50(5), 1238-1244. doi: 10.1016/j.fct.2012.01.023 [ Links ]
Liu, K., Wang, J., Zhao, L., & Wang, Q. (2013). Anticancer, antioxidant and antibiotic activities of mushroom Ramaria flava. Food and Chemical Toxicology, 58, 375-380. doi: 10.1016/j.fct.2013.05.001 [ Links ]
López-Vazquéz, E., Prieto-García, F., Gayosso-Canales M., Otazo, S. E. M., & Villagómez I. J. R. (2017). Phenolic acids, flavonoids, ascorbic acid, β-glucans and antioxidant activity in mexican wild edible mushrooms. Italian Journal of Food Science, 29(4), 766-774. doi: 10.14674/IJFS-838 [ Links ]
Manzi, P., Aguzzi, A., & Pizzoferrato, L. (2001). Nutritional value of mushrooms widely consumed in Italy. Food Chemistry, 73(3), 321-325. doi: 10.1016/S0308-8146(00)00304-6 [ Links ]
Mata, M., Halling, R., & Mueller, G. M. (2003). Macrohongos de Costa Rica (vol. 2). Santo Domingo de Heredia, Costa Rica: Ed. INBio. [ Links ]
Mattila, P., Konko, K., Eurola, M., Pihlava, J. M., Astola, J., Vahteristo, L., Hietaniemi, V., …Piironen, V. (2001). Contents of vitamins, mineral elements, and some phenolic compounds in cultivated mushrooms. Journal of Agriculture and Food Chemistry, 49(5), 2343-2348. doi: 10.1021/jf001525d [ Links ]
Montoya-Bello, L., Bandala-Muñoz, V. M. & Guzmán, G. (1987). Especies de hongos (principalmente Agaricales) poco conocidas en el estado de Veracruz. Veracruz, México: INIREB. [ Links ]
Montoya, L., & Bandala, V. M. (2005). Revision of Lactarius from Mexico: additional new records. Persoonia - Molecular Phylogeny and Evolution of Fungi, 18(4), 471-483. Retrieved from https://www.semanticscholar.org/paper/Revision-of-Lactarius-from-Mexico.-Additional-new-Montoya-Bandala/f19788701722dbc9c39ab849179477d1fb3fbb63 [ Links ]
Ochoa-Zarzosa, A., Vázquez-Garcidueñas, M. S., Robinson-Fuentes, V. A., & Vázquez-Marrufo, G. (2011). Antibacterial and cytotoxic activity from basidiocarp extracts of the edible mushroom Lactarius indigo (Schw.) Fr. (Russulaceae). African Journal of Pharmacy and Pharmacology, 5(2), 281-288. doi: 10.5897/AJPP10.032 [ Links ]
Ozgen, M., Reese, R. N., Tulio, A. Z., Scheerens, J. C., & Miller, A. R. (2006). Modified 2,2-azino-bis-3-ethylbenzothiazoline-6-sulfonic acid (ABTS) method to measure antioxidant capacity of selected small fruits and comparison to ferric reducing antioxidant power (FRAP) and 2,2′-diphenyl-1- picrylhydrazyl (DPPH) methods. Journal of Agricultural and Food Chemistry, 54(4), 1151-1157. doi: 10.1021/jf051960d [ Links ]
Öztürk, M., Tel, G., Öztürk, F. A., & Duru, M. E. (2014). The cooking effect on two edible mushrooms in anatolia: Fatty acid composition, total bioactive compounds, antioxidant and anticholinesterase activities. Records of Natural Products, 8(2), 189-194. Retrieved from https://www.semanticscholar.org/paper/The-Cooking-Effect-on-Two-Edible-Mushrooms-in-%3A-%2C-%2C-%C3%96zt%C3%BCrk-Tel/a2a000bec1e0a09bac31933c9dab19b5f4a71fd2 [ Links ]
Patras, A., Brunton, N. P., Tiwari, B. K., & Butler, F. (2011). Stability and degradation kinetics of bioactive compounds and colour in strawberry jam during storage. Food and Bioprocess Technology, 4(7), 1245-1252. doi: 10.1007/s11947-009-0226-7 [ Links ]
Pumtes, P., Rojsuntornkitti, K., Kongbangkerd, T., & Jittrepotch, N. (2016). Effects of different extracting conditions on antioxidant activities of Pleurotus flabellatus. International Food Research Journal, 23(1), 173-179. Retrieved from https://www.semanticscholar.org/paper/Effects-of-different-extracting-conditions-on-of-Pumtes-Rojsuntornkitti/11f3c97bdc0f73c1276c40f2430fedb725972087?p2df [ Links ]
Rao, A. V., & Rao, L. G. (2007). Carotenoids and human health. Pharmacological Research, 55(3), 207-216. doi: 10.1016/j.phrs.2007.01.012 [ Links ]
Re, R., Pellegrini, N., Proteggente, A., Pannala, A., Yang, M., & Rice-Evans, C. (1999). Antioxidant activity applying an improved abts radical cation decolorization assay. Free Radical Biology and Medicine, 26(9), 1231-1237. doi: 10.1016/S0891-5849(98)00315-3 [ Links ]
Robaszkiewicz, A., Bartosz, G., Lawrynowicz, M., & Soszyński, M. (2010). The role of polyphenols, β-carotene, and lycopene in the antioxidative action of the extracts of dried, edible mushrooms. Journal of Nutrition and Metabolism, Article ID 173274. doi: 10.1155/2010/173274 [ Links ]
Rochon, C., Paré, D., Khasa, D. P., Fortin, J. A. (2009). Ecology and management of the lobster mushroom in an eastern Canadian jack pine stand. Canadian Forest Service Publications, 39, 2080-2091. Retrieved from https://cfs.nrcan.gc.ca/publications?id=30735 [ Links ]
Ruan-Soto, F., Ordaz-Velázquez, M., García-Santiago, W., & Ovando, E. (2017). Traditional processing and preservation of wild edible mushrooms in Mexico. Annals of Food Processing and Preservation, 2(1), 1013. Retrieved from https://www.jscimedcentral.com/FoodProcessing/foodprocessing-2-1013.pdf [ Links ]
Ruan-Soto, F. (2018). Recolección de hongos comestibles silvestres y estrategias para el reconocimiento de especies tóxicas entre los tsotsiles de Chamula, Chiapas, México. Scientia Fungorum, 48, 1-13. doi: 10.33885/sf.2018.48.1179 [ Links ]
Sahagún, F. V. (2020). Aprovechamiento sostenible de hongos comestibles; hacia una seguridad alimentaria. Meio Ambiente, 2(5), 45-55. Retrieved from https://www.meioambientebrasil.com.br/index.php/MABRA/article/view/97 [ Links ]
Shahidi, F., & Ambigaipalan, P. (2015). Phenolics and polyphenolics in foods, beverages and spices: Antioxidant activity and health effects-A review. Journal of Functional Foods, 18(B), 820-897. doi: 10.1016/j.jff.2015.06.018 [ Links ]
Sari, M., Prange, A., Lelley, J. I., & Hambitzer, R. (2017). Screening of beta-glucan contents in commercially cultivated and wild growing mushrooms. Food Chemistry, 216, 45-51. doi: 10.1016/j.foodchem.2016.08.010 [ Links ]
Sawangwan, T., Wansanit, W., Pattani, L., & Noysang, C. (2018). Study of prebiotic properties from edible mushroom extraction. Agriculture and Natural Resources, 52(6), 519-524. doi: 10.1016/j.anres.2018.11.020 [ Links ]
Silva, I., & Lo, M. G. (1997). Proximate chemical composition, free amino acid contents, and free fatty acid contents of some wild edible mushrooms from Querétaro, México. Journal Agricultural and Food Chemistry, 45(11), 4329-4332. doi: 10.1021/jf970640u [ Links ]
Vaz, J. A., Heleno, S. A., Martins, A., Almeida, G. M., Vasconcelos, M. H., & Ferreira, I. C. F. R. (2010). Wild mushrooms Clitocybe alexandri and Lepista inversa: In vitro antioxidant activity and growth inhibition of human tumour cell lines. Food and Chemical Toxicology, 48(10), 2881-2884. doi: 10.1016/j.fct.2010.07.021 [ Links ]
Wang, X. M., Zhang, J., Wu, L. H., Zhao, Y. L., Li, T., Li, J. Q., …Liu, H. G. (2014). A mini-review of chemical composition and nutritional value of edible wild-grown mushroom from China. Food Chemistry, 151, 279-285. doi: 10.1016/j.foodchem.2013.11.062 [ Links ]
Yahia, E. M., Gutiérrez-Orozco, F., & Moreno-Pérez, M. A. (2017). Identification of phenolic compounds by liquid chromatography-mass spectrometry in seventeen species of wild mushrooms in Central Mexico and determination of their antioxidant activity and bioactive compounds. Food Chemistry, 226, 14-22. doi: 10.1016/j.foodchem.2017.01.044 [ Links ]
Zhou, L., Cao, Z., Bi, J., Yi, J., Chen, Q., Wu, X., & Zhou, M. (2016). Degradation kinetics of total phenolic compounds, capsaicinoids and antioxidant activity in red pepper during hot air and infrared drying process. International Journal of Food Science & Technology, 51(4), 842-853. doi: 10.1111/ijfs.13050 [ Links ]
Agradecimientos
Los autores desean agradecer el financiamiento del Consejo Nacional de Ciencia y Tecnología (CONACYT) y de la Dirección General de Investigación y Posgrado de la Universidad Autónoma Chapingo. Asimismo, agradecemos a las mujeres recolectoras de hongos que nos acompañaron a buscar las especies estudiadas y a la Dra. Emma Estrada Martínez por su orientación en la identificación de estas.
Recibido: 16 de Diciembre de 2020; Aprobado: 07 de Mayo de 2021











 texto em
texto em 


