Introducción
Colombia es uno de los países más ricos en diversidad biológica en el mundo. Tal diversidad está representada en 59 áreas naturales protegidas pertenecientes al Sistema de Parques Nacionales Naturales, que representan 142 682 km2 de la superficie nacional. El Santuario de Fauna y Flora de Iguaque (SFFI) es un área protegida perteneciente a la región andina colombiana, que abarca ecosistemas de páramo y bosque andino, y es de importancia vital como proveedor de servicios ecosistémicos, como el abastecimiento de agua para el consumo de los municipios de Villa de Leyva, Arcabuco y Chíquiza (Ministerio del Medio Ambiente, 2017a).
El páramo es un ecosistema tropical de montaña, único por los servicios ambientales que presta, dentro de los que se destaca la regulación y conservación del recurso hídrico. Se sitúa entre el límite superior de los bosques alto-andinos y el límite inferior de las zonas nivales, entre los 3 100 y 4 000 msnm. Su temperatura es baja y por lo general muy húmeda debido a las frecuentes lluvias y neblina. En Latinoamérica, sólo Venezuela, Ecuador, Perú y Costa Rica cuentan con páramos tropicales, ubicados, casi todos, salvo los de la Sierra Nevada de Santa Marta y los de Costa Rica, en la cordillera de los Andes (Greenpeace, 2013).
En Colombia, los páramos abarcan 29 061.3 km2, equivalentes apenas al 2.5% del territorio continental; sin embargo, representan el 50% de ecosistemas paramunos del mundo (Ministerio del Medio Ambiente, 2017b); además, dan origen a las cuencas hídricas que abastecen gran parte del país, suministrando agua a 70% de la población colombiana (Vásquez & Buitrago, 2011). Se estima que la producción de agua de alta montaña (> 2 744 msnm) es de 66.5 km3/año, cantidad que corresponde a un 3% del volumen total anual de precipitación del país (Avellaneda-Torres, Torres, & León-Sicard, 2014). Además, los páramos son centros de endemismo de flora (8%) y fauna, fundamentales para mitigar los efectos del cambio climático debido a la capacidad de su vegetación y suelos para retener diez veces más la cantidad de carbono que un metro cuadrado de bosque seco tropical (Vásquez & Buitrago, 2011).
Un 50% de los páramos en Colombia está vinculado con zonas protegidas (Gómez, Moreno, Andrade, & Rueda, 2016), sin embargo son objeto de procesos de transformación y degradación debido principalmente a prácticas de agricultura intensiva, conversión a sistemas de ganadería extensiva, explotación minera y establecimiento de infraestructura (Cabrera & Ramírez, 2014), generando pérdida del ecosistema nativo del 15.9% (Gómez et al., 2016) y afectando la calidad del recurso hídrico. El SFFI no ha sido ajeno a esta afectación, pues posee infraestructura para la sede administrativa, zona de camping, centro de visitantes y restaurante, para el servicio a visitantes que practican ecoturismo.
En los últimos años, las comunidades aledañas al SFFI y los usuarios que se benefician de la captación de agua proveniente de la quebrada Mamarramos presentaron reclamos por el deterioro de la calidad del agua. Para dar respuesta, los administrativos del SFFI implementaron sistemas de tratamiento de agua residual doméstica in situ en la sede administrativa, centro de visitantes y área de camping, a fin de disminuir el impacto de las aguas residuales sobre la quebrada y asegurar que las bocatomas localizadas aguas abajo cumplan con los parámetros establecidos por la legislación colombiana para uso de agua con fines de potabilización.
Teniendo en cuenta lo anterior, la calidad del recurso hídrico debe ser monitoreada de manera frecuente para la ejecución de acciones preventivas o correctivas. Con el propósito de valorar la calidad del agua se han empleado varias metodologías, entre las que se incluyen la comparación de las variables con la normatividad vigente; indicadores de calidad y contaminación (ICA e ICOS, respectivamente) para transformar los datos de variables fisicoquímicas y microbiológicas del agua, en un valor que califica y cualifica la fuente (Companhia Ambiental do Estado de São Paulo, 2014; Ramírez, Restrepo, & Viña, 1997); indicadores hidrobiológicos, a partir de la composición de macroinvertebrados en un cuerpo de agua; índice de calidad ecológica (ICE), que permite integrar la información de abundancia de cada familia de macroinvertebrados y las variables fisicoquímicas en un único valor que expresa un gradiente ambiental de calidad de agua (Haase & Nolte, 2008).
El objetivo de este estudio fue evaluar la calidad del agua de la quebrada Mamarramos, a partir de índices hidrobiológicos y fisicoquímicos, así como del Índice de Calidad Ecológica, para determinar el efecto de la actividad antrópica en el Santuario de Fauna y Flora de Iguaque.
Materiales y métodos
Zona de estudio
El estudio se realizó en la quebrada Mamarramos, perteneciente al SFFI, que se forma por la confluencia de las quebradas Francos y Carrizal. Para caracterizar la calidad del agua de la quebrada y el efecto de la actividad antrópica en el SFFI, se identificaron 10 puntos de monitoreo distribuidos en las quebradas Carrizal, Francos y Mamarramos, teniendo en cuenta la ubicación de bocatomas, presencia de sistemas de tratamiento de aguas residuales y características topográficas (Figura 1).
Se realizaron tres jornadas de muestreo durante la estación seca del año. La descripción de los puntos de muestreo se presenta en la Tabla 1.
Tabla 1 Descripción de los puntos de muestreo. QC: quebrada Carrizal; QF: quebrada Francos; QM: quebrada Mamarramos; S: estación seca; CI: campo de infiltración.
| Estación de muestreo | Nombre | Altitud (msnm) | Coordenadas geográficas |
|---|---|---|---|
| QC, antes de bocatoma | QCS01 | 3037 ± 8 | 5° 41' 48.2'' N, 73° 27' 95'' O |
| QC, después del CI del centro de visitantes | QCS02 | 2897 ± 4 | 5° 42' 11''N, 73° 27' 25.5''O |
| QC, después del CI del área administrativa | QCS03 | 2839 ± 3 | 5° 42' 26.6 ''N, 73° 27' 28.6''O |
| QC, antes de la confluencia con la QF | QCS04 | 2827 ± 3 | 5° 42' 29.4''N, 73° 27' 28.7''O |
| QF, antes de bocatoma | QFS01 | 2860 ± 8 | 5° 42' 15.9''N, 73° 27' 12''O |
| QF, antes del CI de la zona de camping | QFS02 | 2856 ± 9 | 5° 42' 33.1''N, 73° 27' 32.6''O |
| QF, después del CI de la zona de camping | QFS03 | 2849 ± 4 | 5° 42' 25.7''N, 73° 27' 24.4''O |
| QF, antes de la confluencia con la QC | QFS04 | 2827 ± 3 | 5° 42' 29.4''N, 73° 27' 28.7''O |
| QM, después de la unión de QF y QC | QMS01 | 2810 ± 4 | 5° 42' 32.6''N, 73° 27' 31.3''O |
| QM, después de bocatoma | QMS02 | 2718 ± 3 | 5° 42' 42.5'', 73° 27' 54.7''O |
Macroinvertebrados
La captura de macroinvertebrados se llevó a cabo por recolección manual (Roldán, 2003), en un área de 10 m2, mediante la técnica de coriotopos propuesta por Rincón (1996). Cada coriotopo se muestreó en un área aproximada de 1 m2 utilizando una red de mano, con ojo de malla de 450 μm y un área de 0.1 m2. Los coriotopos seleccionados para cada estación de muestreo fueron los siguientes: musgos y piedras en corriente rápida y lenta, cascada, hojarasca, salpicadura y ribera (Medellin, Ramírez, & Rincón, 2004). Los muestreos se realizaron en horas diurnas, de 9:00 am a 5:00 p.m., teniendo en cuenta el tiempo de mayor actividad de los macroinvertebrados. Los organismos colectados se conservaron en recipientes plásticos sumergidos en solución transeau (agua, etanol al 90% y formol al 40%, en proporciones 6:3:1, respectivamente) a un volumen 1:1 de solución y 20 ml de agua destilada (Arcos-Pulido & Gómez, 2006; Corredor & Forero, 2011). Los macroinvertebrados fueron identificados hasta el nivel de familia, utilizando un estereoscopio marca Nikon SMZ 745 T, acompañado de un sistema de iluminación NI-150 Nikon Instrumets Inc. Para la determinación taxonómica de los especímenes se aplicaron claves de diferentes autores y guías de campo (Bouchard, 2004; Clifford, 1991; Domínguez & Fernández, 2009; McCafferty, 1983; Merritt, Cummins, Hunt, Company, & Wallace, 1996; Roldán, 1988, 2003; Springer, Ramírez, & Hanson, 2010).
Se construyó la curva de diversidad acumulada, a partir de los datos acumulados del índice de diversidad de Shannon y la abundancia de organismos capturados, para establecer la representatividad de la muestra (Ramirez, 2006). Para el cálculo de los índices BMWP/Col e ICOBIO, se siguió el procedimiento descrito por Roldán (2003), y Ramírez y Viña (1998), respectivamente.
Parámetros fisicoquímicos
La recolección, preservación, transporte y almacenamiento de muestras se realizó de acuerdo con las recomendaciones de los métodos estándar (APHA, AWWA, & WEF, 2012). Se realizaron análisis in situ de turbiedad (TD), con un turbidímetro portátil marca Hach; oxígeno disuelto (OD); conductividad (CD); pH, y temperatura, utilizando un multiparámetro marca Hach. Además se realizaron mediciones de caudal y se colectaron muestras en cada punto para analizar los siguientes parámetros: demanda bioquímica de oxígeno (DBO5), coliformes totales (CT), coliformes fecales (CF), sólidos totales (ST), sólidos suspendidos totales (SST), sólidos disueltos totales (SDT), nitrógeno total kjendahl (NTK), nitratos (NO3), fósforo total (PT), fosfatos (PO4), dureza total (DT), alcalinidad total (AT) y cloruros (Cl-). Todos los análisis de laboratorio se realizaron con base en los métodos estándar (APHA, AWWA, & WEF, 2012). Teniendo en cuenta temperatura, oxígeno disuelto y altitud, se calculó la concentración de saturación con la ecuación propuesta por Whipple y Whipple, citada por Romero-Rojas (1999), y el porcentaje de saturación de oxígeno en cada punto de monitoreo. El caudal en los puntos QFS01, QFS02, QMS01 y QMS02 se determinó con el método de área-velocidad (Instituto de Hidrología, Meteorología y Estudios Ambientales, 2007), usando un micromolinete marca Rickly Hidrológica; en los puntos QCS01, QCS02, QCS04 y QFS03 se aforó con el método volumétrico ((Instituto de Hidrología, Meteorología y Estudios Ambientales, 2007).
Con los resultados de los parámetros fisicoquímicos se calcularon los índices de contaminación por mineralización-ICOMI y materia orgánica-ICOMO a partir de la metodología establecida por Ramírez, Restrepo y Viña (Ramírez et al., 1997). El ICOMI es el valor promedio de los índices de cada una de las tres variables que integra (conductividad, dureza y alcalinidad), las cuales se definen en un rango entre 0 y 1. Índices cercanos a cero (0) reflejan muy baja contaminación por mineralización; por el contrario, índices cercanos al máximo valor posible (1) indican un alto grado de contaminación (Jimenez & Velez, 2006). El ICOMO es el valor promedio de cada una de las tres variables que integra (DBO5, CT y porcentaje de saturación de oxígeno) (Ramírez et al., 1997).
Asimismo, se calculó el índice de calidad de agua de la Compañía de Tecnología de Saneamiento Ambiental de Brasil (ICA-CETESB), que incluye parámetros fisicoquímicos y microbiológicos relacionados con el nivel de riesgo sanitario presente en el agua (Companhia Ambiental do Estado de São Paulo, 2014). La Ecuación (1) representa el ICA-CETESB, el cual es el producto de la multiplicación de nueve parámetros elevados a un valor atribuido en función de la importancia del parámetro. La sumatoria de todos los puntajes obtenidos de las diferentes características se califican de acuerdo con las categorías consignadas en la Tabla 2.
Tabla 2 Categorización según ICA-CETESB (Companhia Ambiental do Estado de São Paulo, 2014).
| Clase | Calidad | Rango |
|---|---|---|
| I | Óptima | 80-100 |
| II | Buena | 52-79 |
| III | Dudosa | 37-51 |
| IV | Inadecuada | 20-36 |
| V | Pésima | 0-19 |
Donde:
ICA = Índice de Calidad de Agua (número entre 0 y 100).
q i = calidad del parámetro, número entre 0 y 100, obtenido de la respectiva curva media de variación de calidad, en función de su concentración.
w i = peso correspondiente, un número entre 0 y 1, atribuido en función de su importancia para la conformación global de la calidad.
i = número de parámetros, variando de 1 a 9 (n = 9, o sea, número de parámetros que componen el ICA).
Índice de calidad ecológica
Este índice utiliza diferentes técnicas estadísticas mutivariantes (Haase & Nolte, 2008) a partir de la siguiente secuencia:
1. Construcción de las matrices de entrada a partir de los valores medios y visualización de la estructura por análisis de componentes principales (Biplot). La sumatoria de las abundancias de macroinvertebrados en los 10 puntos de muestreo se clasificó con base en los criterios de bioindicación propuestos por Roldán (2003) y, en paralelo, se construyó la matriz de resultados de los análisis fisicoquímicos obtenidos.
2. Determinación de un gradiente ambiental desde un Análisis de Correlación Canónica (ACC), técnica desarrollada por Hotelling (1936).
3. Reescalamiento de los samples scores obtenidos del ACC (Haase & Nolte, 2008).
4. Obtención de los puntajes óptimos y de tolerancias para cada taxón, a partir de un análisis de promedios ponderados (Weighted Averaging, WA), desarrollado por Whittaker (1973), utilizando los puntajes escalados.
5. Construcción del ICE, a partir de la ecuación propuesta por Haase y Nolte (2008)).
Finalmente, se agruparon los puntos de muestreo considerando el valor del ICE, utilizando un cluster jerárquico aglomerativo. El ICE se calificó de acuerdo con las categorías consignadas en la Tabla 3.
Resultados y discusión
Macroinvertebrados
Se colectaron 7 521 individuos, distribuidos en ocho clases, 16 órdenes y 57 familias (Tabla 4). De las familias identificadas, las que presentaron mayor frecuencia fueron: Leptoceridae (19%), Calamoceratidae (11.8%), Psephenidae (10.8%), Helicopsychidae (9.7%) y Planariidae (7.7%). Al analizar el material colectado, las familias que presentaron mayor frecuencia representan el 59% del total de los individuos capturados durante las tres jornadas de muestreo. Todas las familias capturadas son representantes de cuerpos lóticos y tienen valoraciones de bioindicación para agua de buena calidad, posiblemente asociados con su ubicación en una zona de reserva, en donde se destacan algunas características propias de sistemas acuáticos de alta montaña: lechos rocosos y nivel de conservación de los bosques riparios (Morelli & Verdi, 2014).
Tabla 4 Familias y abundancias de macroinvertebrados.
| Familia | QFS01 | QFS02 | QFS03 | QFS04 | QCS01 | QCS02 | QCS03 | QCS04 | QMS01 | QMS02 | Total |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Ampullariidae | 1 | 3 | 22 | 26 | |||||||
| Anomalopsy-chidae | 1 | 2 | 1 | 1 | 5 | ||||||
| Baetidae | 51 | 22 | 1 | 7 | 79 | 8 | 2 | 3 | 7 | 48 | 228 |
| Blataridae | 1 | 2 | 1 | 4 | |||||||
| Blephariceridae | 1 | 2 | 1 | 1 | 5 | ||||||
| Calamoceratidae | 66 | 81 | 66 | 82 | 69 | 76 | 108 | 89 | 101 | 150 | 888 |
| Ceratopogonidae | 2 | 11 | 3 | 1 | 4 | 4 | 2 | 4 | 3 | 3 | 37 |
| Chironomidae | 20 | 28 | 14 | 31 | 17 | 32 | 30 | 10 | 39 | 26 | 247 |
| Chordodidae | 1 | 1 | |||||||||
| Chrysomelidae | 1 | 1 | 6 | 2 | 2 | 1 | 2 | 15 | |||
| Curculionidae | 1 | 1 | 2 | ||||||||
| Dixidae | 2 | 2 | 6 | 1 | 10 | 7 | 6 | 18 | 52 | ||
| Dolichopodidae | 1 | 1 | |||||||||
| Dytiscidae | 1 | 2 | 1 | 4 | |||||||
| Elmidae | 3 | 2 | 7 | 3 | 1 | 5 | 2 | 4 | 4 | 10 | 41 |
| Empididae | 1 | 1 | 1 | 1 | 2 | 1 | 7 | ||||
| Entomobrydae (Collembola) | 1 | 3 | 1 | 5 | |||||||
| Ephydridae | 1 | 1 | |||||||||
| Girinidae | 2 | 2 | |||||||||
| Glossossoma-tidae | 172 | 42 | 22 | 22 | 40 | 34 | 40 | 19 | 20 | 21 | 432 |
| Helicopsychidae | 6 | 69 | 79 | 40 | 18 | 58 | 83 | 44 | 244 | 89 | 730 |
| Hyalellidae | 24 | 25 | 7 | 28 | 8 | 8 | 1 | 22 | 123 | ||
| Hydracnidiae | 2 | 1 | 4 | 1 | 2 | 5 | 6 | 21 | |||
| Hydrobiosidae | 15 | 9 | 15 | 12 | 25 | 13 | 20 | 16 | 19 | 6 | 150 |
| Hydrophilidae | 1 | 2 | 3 | 3 | 1 | 10 | |||||
| Hydropsychi-dae | 22 | 10 | 12 | 5 | 5 | 12 | 8 | 22 | 12 | 24 | 132 |
| Hydroptilidae | 1 | 1 | 2 | ||||||||
| Isopoda | 1 | 3 | 1 | 85 | 11 | 28 | 12 | 9 | 1 | 151 | |
| Isotomidae (Collembola) | 1 | 1 | |||||||||
| Lampiridae | 1 | 2 | 2 | 5 | |||||||
| Leptoceridae | 76 | 199 | 275 | 122 | 64 | 86 | 115 | 62 | 157 | 305 | 1461 |
| Leptohyphidae | 3 | 2 | 7 | 6 | 1 | 5 | 1 | 7 | 34 | 15 | 81 |
| Leptophlebidae | 10 | 22 | 7 | 5 | 13 | 9 | 8 | 2 | 9 | 24 | 109 |
| Libellulidae | 1 | 1 | |||||||||
| Muscidae | 2 | 2 | |||||||||
| Perlidae | 6 | 5 | 6 | 7 | 8 | 17 | 7 | 21 | 9 | 75 | 161 |
| Phylipotamidae | 2 | 2 | 1 | 1 | 6 | ||||||
| Pisauridae | 4 | 4 | 3 | 15 | 7 | 10 | 1 | 2 | 11 | 57 | |
| Planariidae | 48 | 56 | 38 | 28 | 44 | 66 | 86 | 26 | 141 | 46 | 579 |
| Polidesmidie | 2 | 3 | 1 | 1 | 7 | ||||||
| Polycentropo-didae | 1 | 1 | 3 | 6 | 2 | 2 | 1 | 16 | |||
| Psephenidae | 68 | 94 | 95 | 88 | 67 | 90 | 138 | 54 | 11 | 107 | 812 |
| Pseudothel-phusidae | 1 | 1 | |||||||||
| Psychodidae | 1 | 1 | |||||||||
| Ptilodactilidae | 6 | 18 | 15 | 11 | 20 | 31 | 33 | 13 | 19 | 11 | 177 |
| Puduridae | 1 | 1 | |||||||||
| Pyralidae | 3 | 3 | |||||||||
| Scirtidae | 54 | 18 | 17 | 12 | 40 | 29 | 47 | 27 | 46 | 17 | 307 |
| Simuliidae | 21 | 74 | 17 | 8 | 11 | 31 | 10 | 49 | 17 | 46 | 284 |
| Sphaeriidae | 1 | 7 | 4 | 2 | 1 | 2 | 2 | 1 | 20 | ||
| Staphilinidae | 1 | 3 | 5 | 1 | 4 | 6 | 8 | 4 | 11 | 6 | 49 |
| Synlestidae | 1 | 1 | 1 | 1 | 4 | ||||||
| Tabanidae | 1 | 2 | 3 | ||||||||
| Tipulidae | 7 | 4 | 2 | 12 | 5 | 4 | 3 | 4 | 1 | 42 | |
| Torridincolidae | 1 | 1 | |||||||||
| Tubificidae | 2 | 1 | 3 | ||||||||
| Xiphocentro-nidae | 1 | 3 | 1 | 5 | |||||||
| Total de individuos | 700 | 817 | 724 | 509 | 691 | 663 | 848 | 519 | 965 | 1 085 | 7 521 |
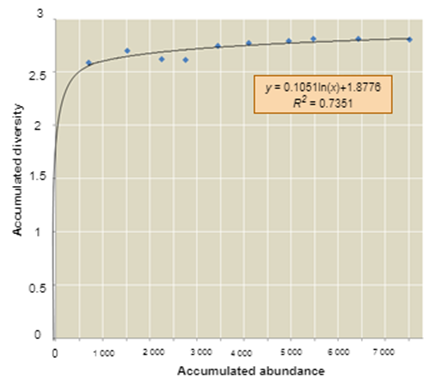
El valor obtenido en la curva de acumulación de taxones fue de 83% (Gamarra et al., 2017), demostrando que el número de puntos de monitoreo, las técnicas y actividades relacionadas con la captura, y el esfuerzo de muestreo de los macroinvertebrados fueron suficientes para alcanzar alta representatividad (González-Valdivia et al., 2017). Los valores de diversidad de Shannon, presentados en la Figura 2, fueron de 2.7 ± 0.09, reflejando las condiciones naturales del ecosistema en el momento del muestreo e indicando alta diversidad, con base en lo reportado por Ramírez (2006) para zonas prístinas de alta montaña.
En la Tabla 5 se muestra los resultados obtenidos para el BMWP/Col., los cuales fueron superiores a 120 en todos los puntos de muestreo evaluados.
Tabla 5 Índice BMWP/Col.
| Muestra | QFS01 | QFS02 | QFS03 | QFS04 | QCS01 | QCS02 | QCS03 | QCS04 | QMS01 | QMS02 |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 124 | 99 | 119 | 99 | 125 | 153 | 134 | 129 | 158 | 119 |
| 2 | 151 | 162 | 165 | 135 | 151 | 116 | 145 | 172 | 150 | 168 |
| 3 | 158 | 149 | 151 | 147 | 135 | 135 | 136 | 152 | 148 | 230 |
De acuerdo con el índice BMWP/Col., la calidad del agua para los puntos QFS02 y QFS04 sobre la quebrada Francos registraron un valor de 99 en el primer muestreo, calificando como aceptable, indicando agua ligeramente contaminada (Roldán, 2003). Este resultado se asocia con la cercanía con el sistema de tratamiento de aguas residuales generadas en la zona de camping. Los ocho puntos restantes fueron clasificados como aguas limpias, con valores superiores a 101 (Roldán, 2003). A pesar de la proximidad en los valores obtenidos, la tabla de calificación para el BMWP establece que hasta 100 las aguas se califican como ligeramente contaminadas; valores superiores a 100 estarán en la categoría de aguas limpias a muy limpias (Roldán, 2003). Tal diferencia se asocia con los rangos establecidos por este índice desde sus inicios (Alba-Tercedor, 1996); sin embargo, valores cercanos a dichos límites (99 o 101) se podrán considerar de la misma calidad, para este caso, aguas limpias.
El índice BMWP/Col. en la segunda y tercera jornada de muestreo calificó el agua en los 10 puntos de muestreo como buena, coincidiendo con lo reportado por Luna (2009) y Medellin et al. (2004). Al establecer relación entre los datos de los estudios previos y el presente trabajo, se puede demostrar que las condiciones de la quebrada Mamarramos han sido ligeramente afectadas a través del tiempo.
Parámetros fisicoquímicos
Los valores promedio y desviaciones estándar de las características fisicoquímicas medidas en las quebradas se muestran en la Tabla 6. La temperatura del agua fue similar en los muestreos 1 y 2 para cada punto de monitoreo (con excepción del punto 4 sobre la quebrada los Francos). Para el tercer muestreo se presentó un aumento en la temperatura de un 1.5 °C (con excepción del punto 3 sobre la quebrada los Francos, el cual permanece constante para todas las fechas de muestreo). La concentración de OD varió entre 6.6 y 7.7 mg/l en la primera y tercera jornada de muestreo, y en el segundo muestreo osciló entre 7.2 y 8.6 mg/l. El porcentaje de saturación de oxígeno para la quebrada Carrizal, Francos y Mamarramos fue de 97.9 ± 1.7%, 93.9 ± 3.1% y 97.7 ± 1.8%. La conductividad en las quebradas Carrizal y Mamarramos fue inferior a la registrada en la quebrada Francos en aproximadamente un 50%. Sin embargo, todos los valores obtenidos en las quebradas (de 26.6 a 73.8 µS/cm) corresponden a conductividad baja, propia de agua dulce, indicando ser apta para ciertas especies de peces e invertebrados. El pH en las tres quebradas fue ligeramente ácido o cercano a la neutralidad, y los valores de conductividad fueron bajos, siendo propios de ecosistemas acuáticos de alta montaña, favoreciendo la diversidad de especies (Roldán, 2012).
Tabla 6 Características fisicoquímicas de las quebradas Carrizal, Francos y Mamarramos.
| Parámetro | Unidad | QCS01 | QCS02 | QCS03 | QCS04 | QFS01 | QFS02 | QFS03 | QFS04 | QMS01 | QMS02 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| OD | mg/l | 7.8 ± 0.6 | 7.7 ± 0.4 | 7.8 ± 0.5 | 7.3 ± 0.3 | 7.2 ± 0.3 | 7.0 ± 0.2 | 7.0 ± 0.3 | 6.9 ± 0.3 | 7.5 ± 0.3 | 7.4 ± 0.2 |
| Conductividad | µs/cm | 34.2 ± 4.2 | 33.6 ± 4.3 | 32.5 ± 3.7 | 27.7 ± 0.9 | 18.4 ± 1.8 | 58.2 ± 14.5 | 55.8 ± 12.2 | 53.1 ± 9.6 | 37.7 ± 2.1 | 36.4 ± 1.9 |
| pH | un. | 6.8 ± 0.2 | 7.0 ± 0.5 | 7.1 ± 0.4 | 7.3 ± 0.4 | 7.2 ± 0.5 | 7.5 ± 0.3 | 7.3 ± 0.5 | 7.3 ± 0.5 | 6.9 ± 0.1 | 7.2 ± 0.4 |
| TC | 10.4 ± 0.8 | 11.5 ± 1.2 | 11.6 ± 0.6 | 12.8 ± 0.7 | 11.5 ± 0.8 | 13.4 ± 0.7 | 13.8 ± 1.4 | 13.3 ± 1.3 | 12.8 ± 0.5 | 12.7 ± 1.2 | |
| Turbiedad | UNT | 2.0 ± 2.1 | 0.6 ± 0.2 | 1.0 ± 0.7 | 0.6 ± 0.1 | 0.7 ± 0.2 | 1.0 ± 0.3 | 0.8 ± 0.2 | 1.4 ± 0.6 | 0.9 ± 0.4 | 0.7 ± 0.2 |
| Alcalinidad | mg/l | 15.5 ± 8.3 | 15.7 ± 2.0 | 7.2 ± 6.9 | 25.0 ± 9.0 | 20.7 ± 13.7 | 23.0 ± 4.4 | 20.5 ± 10.0 | 23.7 ± 14.8 | 12.7 ± 3.4 | 15.7 ± 4.8 |
| Dureza | mg/l | 0.0 | 0.0 | 0.0 | 0.0 | 5.5 ± 6.7 | 9.7 ± 11.9 | 14.3 ± 9.4 | 2.3 ± 4.0 | 8.8 ± 6.2 | 4.2 ± 5.2 |
| ST | mg/l | 20.0 ± 10.4 | 5.3 ± 8.1 | 30.3 ± 20.3 | 3.7 ± 19.6 | 2.7 ± 14.4 | 8.3 ± 2.3 | 21.7 ± 2.3 | 27.7 ± 1.2 | 24.3 ± 20.2 | 5.7 ± 9.2 |
| SST | mg/l | 0.9 ± 1.3 | 5.5 ± 27.2 | 1.8 ± 1.0 | 2.5 ± 0.8 | 4.1 ± 5.8 | 2.6 ± 3.9 | 1.6 ± 0.6 | 7.9 ± 9.8 | 1.3 ± 0.3 | 1.4 ± 0.7 |
| DBO | mg/l | 0.7 ± 0.3 | 0.4 ± 0.1 | 0.5 ± 0.3 | 1.3 ± 1.3 | 0.4 ± 0.3 | 0.4 ± 0.2 | 0.6 ± 0.3 | 0.6 ± 0.2 | 0.3 ± 0.3 | 0.5 ± 0.2 |
| NTK | mg/l | 1.1 ± 0.5 | 1.1 ± 0.5 | 1.8 ± 0.9 | 1.1 ± 0.5 | 1.8 ± 0.9 | 6.8 ± 8.2 | 1.8 ± 0.9 | 1.6 ± 1.1 | 1.6 ± 1.1 | 1.1 ± 0.5 |
| Nitratos | mg/l | 0.6 ± 0.3 | 0.6 ± 0.3 | 0.8 ± 0.1 | 0.5 ± 0.5 | 1.3 ± 0.7 | 1.0 ± 0.4 | 1.0 ± 0.4 | 0.8 ± 0.7 | 0.6 ± 0.5 | 0.6 ± 0.5 |
| Fósforo | mg/l | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.2 ± 0.1 | 0.0 | 0.0 | 0.0 | 0.0 |
| Fosfatos | mg/l | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 |
| Cloruros | mg/l | 0.4 ± 0.6 | 0.9 ± 0.2 | 0.8 ± 0.8 | 0.6 ± 0.5 | 0.6 ± 0.4 | 0.5 ± 0.2 | 0.9 ± 0.7 | 0.5 ± 0.2 | 0.6 ± 0.4 | 0.5 ± 0.2 |
| Caudal | l/s | 6.7 ± 2.4 | 9.4 ± 3.9 | * | 10.1 ± 3.4 | 4.2 ± 2.1 | 4.0 ± 1.3 | 7.6 ± 2.1 | * | 13.1 ± 8.0 | 12.4 ± 10.6 |
La turbiedad presentó valores inferiores a 2 UNT en todos los puntos de monitoreo, con excepción del punto QCS01 en el segundo muestreo, que arrojó un valor de 4.4 UNT, indicando escasa presencia de sólidos suspendidos en el agua, coincidiendo con los valores obtenidos de este parámetro (< 20 mg/l). La alcalinidad estuvo entre 2 y 40 mg/l de CaCO3, en todos los puntos de muestreo. En la quebrada Francos, la dureza estuvo entre 0 y 25 mg/l de CaCO3, registrando los valores más elevados de este parámetro; la quebrada Carrizal no presentó dureza (0 mg/l de CaCO3), y en la quebrada Mamarramos se obtuvieron valores entre 0 y 16 mg/l de CaCO3.
La materia orgánica, en términos de DBO (< 1 mg/l), demuestra que la microcuenca tiene buena calidad y se encuentra en un ambiente oligosaprobio (Ramírez et al., 1997). Además, los valores de porcentaje de saturación de oxígeno disuelto en todos los puntos son altos, evidenciando buena calidad del agua (Lynch & Poole., 1979). En cuanto a los nutrientes, el contenido de nitrógeno total kjendahl, nitratos, fósforo total y ortofosfatos fue mínimo, clasificando a la microcuenca como oligotrófica (Ramírez et al., 1997). Los resultados de coliformes totales y fecales mostraron valores inferiores a 1 UFC, indicando escasa contaminación microbiológica en todos los puntos de muestreo. Lo anterior confirma la poca influencia de los sistemas de tratamiento de aguas residuales sobre los cuerpos de agua, ya que éstas son unas de las principales fuentes de fósforo y nitrógeno y, por tanto, de eutroficación de los ecosistemas acuáticos.
El caudal presentado en el primer, segundo y tercer muestreo para cada una de las quebradas fue el siguiente: Francos, 4.5 ± 1.7, 7.3 ± 2.5 y 4.0 ± 2.0 l/s; Carrizal, 6.2 ± 1.6, 12.3 ± 2.7 y 7.7 ± 1.1 l/s; y Mamarramos, 7.8 ± 0.9, 23.4 ± 1.6 y 7.0 ± 2.8. El caudal registró valores más altos en el segundo muestreo debido a lluvias aisladas que se presentaron en días anteriores a la toma de muestras.
La Tabla 7 muestra los resultados promedio de los índices obtenidos en cada punto de muestreo durante las tres jornadas.
Tabla 7 Índices de contaminación y de calidad del agua.
| Punto de muestreo | ICOMO | ICOMI | ICA-CETESB |
|---|---|---|---|
| QCS01 | 0.101 ± 0.016 | 0.021 ± 0.003 | 93.54 ± 0.88 |
| QCS02 | 0.100 ± 0.010 | 0.020 ± 0.003 | 94.76 ± 0.90 |
| QCS03 | 0.097 ± 0.012 | 0.020 ± 0.003 | 94.32 ± 1.10 |
| QCS04 | 0.105 ± 0.005 | 0.016 ± 0.001 | 94.40 ± 1.55 |
| QFS01 | 0.114 ± 0.011 | 0.009 ± 0.001 | 94.31 ± 0.98 |
| QFS02 | 0.110 ± 0.006 | 0.043 ± 0.014 | 88.74 ± 4.95 |
| QFS03 | 0.109 ± 0.005 | 0.040 ± 0.012 | 94.29 ± 0.65 |
| QFS04 | 0.117 ± 0.007 | 0.038 ± 0.009 | 93.85 ± 1.14 |
| QMS01 | 0.100 ± 0.007 | 0.024 ± 0.002 | 94.51 ± 0.85 |
| QMS02 | 0.102 ± 0.001 | 0.023 ± 0.002 | 95.03 ± 0.06 |
El ICOMI se calcula a partir de la conductividad, dureza y alcalinidad. Sin embargo, dureza y alcalinidad presentaron valores bajos en todas las quebradas, de modo que el ICOMI sólo fue calculado teniendo en cuenta la conductividad. Este índice presentó valores de 0.02 para todas las fechas de muestreo. En la quebrada Francos (a partir del punto QFS02), el ICOMI estuvo entre 0.2 y 0.4 debido al incremento en la conductividad, alcalinidad y dureza en esta fuente de agua. Los valores obtenidos del ICOMI confirmaron la escasa presencia de sales en el agua, beneficiando la diversidad de especies. El ICOMO se encontró entre 0.08 y 0.11, indicando que el efecto producido por aguas residuales domésticas provenientes de los sistemas de tratamiento del SFFI es mínimo, por ser quebradas de alta montaña, lo cual favorece la oxigenación de éstas. Tal índice fue influenciado sólo por el oxígeno disuelto, ya que los valores de DBO y coliformes en los puntos de muestreo fueron bajos y, en consecuencia, los IDBO e Icoliformes fueron nulos. Este índice obtuvo resultados muy bajos, por lo que el grado de contaminación por materia orgánica es mínimo.
Los resultados del ICA-CETESB presentados mostraron valores superiores a 80 en todos los puntos de muestreo, clasificando a las tres quebradas como cuerpos de agua con calidad óptima para destinación del recurso como fuente de abastecimiento de sistemas de potabilización para consumo humano. El punto QFS02 mostró el valor más bajo del ICA- CETESB (88.7) debido a que parámetros como alcalinidad, conductividad, dureza y fósforo presentaron valores más altos en comparación con los otros puntos, corroborando lo identificado a través del biplot de las características fisicoquímicas frente a los puntos de muestreo.
Los parámetros fisicoquímicos analizados confirman buena calidad de las tres quebradas en todos los puntos de muestreo, con capacidad de reaireación, oligotróficas y poco grado de mineralización de la microcuenca, coincidiendo con los resultados obtenidos en estudios anteriores (Medellin et al., 2004).
Índice de Calidad Ecológica, ICE
Los 2 507 organismos colectados en promedio por muestreo (7 521 macroinvertebrados colectados en los tres muestreos), se categorizaron en 10 grupos (Roldán, 2003). De acuerdo con lo establecido por Prat y Rieradevall (1992), 65% de los individuos indica condiciones naturales en el río (G08 al G10); 28%, estrés ambiental en el río (G06 y G07), y el 7% restante corresponde a problemas de contaminación en el río (G01 a G05). Estos resultados confirman que la microcuenca Mamarramos conserva las condiciones prístinas, correspondientes a una reserva natural de alta montaña (Tabla 8), pero hay evidencia de una leve afectación de la quebrada por los datos registrados en los grupos G01 a G05.
Tabla 8 Grupo de individuos por muestreo.
| Grupo | Familias | Numero promedio de individuos por muestreo |
|---|---|---|
| G02 | Chironomidae, Muscidae | 83 |
| G03 | Ceratopogonidae, Ephydridae, Hydrophilidae, Tipulidae, Tipulidae/Hexatoma | 30 |
| G04 | Chrysomelidae, Dolichopodidae, Empididae, Sphariidae, Synlestidae | 15 |
| G05 | Blataridae, Curculionidae, Entomobrydae (Collembola), Isopoda, Isotomidae (Collembola), Puduridae, Sinlestidae, Tabanidae, Torridincolidae | 57 |
| G06 | Elmidae, Libellulidae, Pisauridae, Polidesmidie, Staphilinidae | 52 |
| G07 | Vacupernius, Planariidae, Psychodidae, Scirtidae | 646 |
| G08 | Helicopsychidae/Helicopsyche, Leptoceridae, Leptoceridae/Atanatolica, Leptoceridae, Pseudothelphusidae, Simuliidae/Simulium | 825 |
| G09 | Ampullaridae, Dytiscidae, Girinidae, Hydracnidiae, Hydrobiosidae, Hydrobiosidae/ Atopsyche, Leptophlebidae/Farrodes, Phylipotamidae, Polycentropodidae/Cyrellus, Polycentropodidae/Polycentropus, Xiphocentronidae | 113 |
| G10 | Anomalopsychidae, Blephariceridae, Calamoceratidae, Chordodidae, Lampiridae, Perlidae/Anacroneuria, Psephenidae/Psephenops, Ptilodactilidae, Tubificidae | 686 |
La relación entre los puntos de muestreo con los macroinvertebrados y las variables fisicoquímicas se observan en los biplot, construidos a partir de las dos primeras componentes, en cada caso, resultado del análisis de componentes principales (ver Figura 3). El biplot para macroinvertebrados muestra relación entre los individuos del G08 con los puntos QMS01, QMS02 y QCS03 debido a que 50% de los individuos asociados con G08 se encontró en estas estaciones; 53% de los individuos del G05 se colectó en el punto QFS01 (ver Figura 3a). El biplot para fisicoquímicos muestra la relación entre los valores de dureza con los puntos de muestreo QFS02 y QFS03, confirmando los resultados obtenidos para este parámetro (ver Figura 3b).
En el análisis de correlación canónica, el primer eje explicó 72.7% de la variación y los cinco restantes entre 1 a 10%. Las variables fisicoquímicas que se relacionaron negativamente con el primer eje debido a los bajos valores en todos los puntos de muestreo fueron AT, DT, SS, NTK y NO3. La relación entre las variables fisicoquímicas, los grupos de individuos y puntos de muestreo se observa en la Figura 4. La longitud de la flecha mide la importancia de la variable en la construcción de la componente, destacándose DBO, NO3, DT y ST. El punto de muestreo QFS01 está en el extremo contrario a ST, indicando valores bajos en este punto. En contraste, QFS04 está en la misma dirección de SS, evidenciando valores altos de este parámetro. Los puntos de muestreo QCS01, QFS01, QMS02 y QCS03 se ubican separados de las variables fisicoquímicas, confirmando los menores valores de estas variables (ver Figura 4).
Los scores fueron redimensionados a una escala entre 1 y 10, donde 1 representa agua contaminada y 10 agua limpia. Los puntajes se calcularon a partir de un modelo de promedios ponderados, dando como resultado un coeficiente de determinación de R 2 = 0.83. El optimum corresponde al puntaje de cada familia en el gradiente de variación ambiental y tolerance describe la amplitud ecológica a lo largo del gradiente ambiental, datos necesarios para el cálculo del ICE (Tabla 9).
Tabla 9 Valor óptimo y tolerancia por familia.
| Grupo | Optimum | Tolerance |
|---|---|---|
| G03 | 8.077 | 2.586 |
| G04 | 6.250 | 2.324 |
| G05 | 5.750 | 3.696 |
| G06 | 6.143 | 4.163 |
| G07 | 6.122 | 3.495 |
| G08 | 6.160 | 3.304 |
| G09 | 6.760 | 3.474 |
| G10 | 6.595 | 3.454 |
El índice de calidad ecológico ICE se obtuvo a partir de la relación entre abundancia, tolerance y optimum propuesta por Haase y Nolte (2008). Los valores del ICE para cada estación en el presente estudio fluctuaron entre 6.35 y 6.43. Todos los valores superiores a 6.1 están asociados con buena calidad ecológica (Tabla 10).
Tabla 10 Resultados ICE para la microcuenca Mamarramos.
| Puntos de muestreo | ICE | Calidad | |
|---|---|---|---|
| 1 | QCS01 | 6.42 | Buena |
| 2 | QCS02 | 6.43 | Buena |
| 3 | QCS03 | 6.37 | Buena |
| 4 | QCS04 | 6.43 | Buena |
| 5 | QFS01 | 6.36 | Buena |
| 6 | QFS02 | 6.39 | Buena |
| 7 | QFS03 | 6.36 | Buena |
| 8 | QFS04 | 6.38 | Buena |
| 9 | QMS01 | 6.35 | Buena |
| 10 | QMS02 | 6.38 | Buena |
Después se agruparon los puntos de muestreom considerando el valor del ICE, utilizando un cluster jerárquico aglomerativo. Los puntos de muestreo QCS01, QCS02 y QCS04, asociados con la quebrada Carrizal, registraron valores altos del ICE. Por otro lado, los puntos QFS01, QFS03 de la quebrada los Francos y QMS01, asociado con la quebrada Mamarramos, registraron los valores inferiores. Sin embargo, todos los puntos presentaron valores superiores a 6.1 (buena calidad ecológica).
Finalmente, es evidente que los efluentes de los sistemas de tratamiento de aguas residuales implementados en el SFFI no están generando impacto negativo en la calidad del agua de las quebradas, como se verificó con los resultados obtenidos a través de los índices fisicoquímicos, la presencia de especies de macroinvertebrados sensibles a contaminación y por el índice de calidad ecológica que calificó todos los puntos de muestreo con valores superiores a 6.1.
Conclusiones
El agua de la quebrada Mamarramos, en los puntos de muestreo evaluados, fue valorada como de excelente calidad. El resultado de los parámetros e índices fisicoquímicos está en concordancia con las familias de macroinvertebrados encontrados. El índice BMWP/Col clasificó la zona de estudio como aguas limpias, demostrando que para la estación seca, el cuerpo hídrico tiene las condiciones adecuadas para sostener la biodiversidad. Sin embargo, hay evidencia de una leve afectación de la quebrada por la presencia de macroinvertebrados de los grupos G01 a G05, indicando la necesidad de continuar con el seguimiento a través de los monitoreos en la zona de estudio.
Por último, el índice de calidad ecológica calificó todos los puntos de muestreo con valores altos, confirmando la buena calidad del agua de la quebrada Mamarramos en el periodo evaluado.











 text new page (beta)
text new page (beta)