Introducción
La industrialización produce efluentes que transportan compuestos tóxicos, entre los que se encuentran los metales, cuyas descargas a cuerpos de agua es la fuente principal de contaminación y, como consecuencia, de diversas enfermedades (ATSDR, 2012). El agua y los sedimentos de lagos y lagunas se convierten en receptores de diversas sustancias contaminantes, mismas que pueden incorporarse a las cadenas tróficas (Theoneste, Gang, Jing, Xu, & Lei, 2013; Lemus, Castañeda, & Chung, 2014), representando un riesgo para la biota, debido a la bioacumulación y biomagnificación en órganos y tejidos de diversas especies acuáticas y terrestres (Sobrino, Cáceres, & Rosas, 2007). Otras fuentes no menos importantes son las descargas municipales, de origen agrícola y emisión de partículas. De las sustancias que se descargan a los cuerpos de agua superficiales, 42% corresponde a los metales y su destino son los sedimentos. Los sedimentos son matrices compuestas por materia orgánica en diversos estados de descomposición, material particulado orgánico e inorgánico de origen biológico y antrópico (Chen ( White, 2004).
Los metales pesados son contaminantes que por su persistencia y transporte a grandes distancias alcanzan con cierta facilidad los cuerpos de aguas superficiales, manifestando un riesgo potencial para la biota. Estos contaminantes pueden provenir de diversas fuentes, como actividades petroleras, agrícolas, metalúrgicas, azucareras, e incluso urbanas y sanitarias (herbicidas e insecticidas). La elevada toxicidad de metales tiende a bioacumularse en la biota e ingresar a la cadena trófica al biomagnificarse hasta llegar a los organismos superiores, incluyendo el hombre (Herrera, Rodríguez, Coto, Salgado, & Borbón, 2012).
Los ríos son receptores de residuos generados por las actividades humanas, a través de efluentes que aportan sustancias peligrosas, especialmente metales como plomo, cadmio, cromo, mercurio y manganeso, entre otros, los cuales suelen depositarse en el sedimento, y estar suspendidos o disueltos en la columna de agua (Rodríguez, Ruíz, & Vertiz, 1994). Estos ríos transportan los contaminantes a lo largo de su cauce y cuando desbordan pueden depositarlos en cuerpos de agua, como lagunas y manantiales. La Laguna de la Ilusiones en Villahermosa, Tabasco, México, está rodeada por dos grandes ríos: Usumacinta y Grijalva. Esta zona presenta elevadas tasas de precipitación, que han llevado al desbordamiento de dichos ríos; además, las condiciones climatológicas favorecen la potencial transferencia de contaminantes desde la atmósfera hacia la Laguna en particular, y a los demás cuerpos de agua en lo general (Palma, Cisneros, Moreno, & Rincón, 2007).
A continuación se indican algunos ejemplos que ilustran la magnitud de la contaminación por metales en el país. Los sedimentos superficiales en el sistema hidrológico Zahuapan-Atoyac revelan concentraciones de As y Pb que oscilaron entre 1.3-127.7 mg kg-1 y 27.3-89.5 mg kg-1, respectivamente (García-Nieto et al., 2011). Rosales-Hoz y Carranza-Edwards (1998) detectaron niveles de metales en sedimento del río Coatzacoalcos, en intervalos que oscilan de 21.2-53.5 mg kg-1 para Pb, 2.1-2.7 mg kg-1 para Cd y 21.6-152.7 mg kg-1 para Cr total, respectivamente; en el mismo río, González-Mille et al. (2010) encontraron Pb (4-22 mg kg-1), Cr+6 (9-93 mg kg-1) y Mn (76.7-2 129 µg kg-1).
Los metales pesados se bioacumulan en especies acuáticas, como ostiones, almejas, camarones y algunas especies de peces. Lango-Reynoso, Landeros-Sánchez y Castañeda-Chávez (2010) determinaron la bioacumulación de As, Cd y Pb en ostión de la laguna Tamiahua, en Veracruz; los valores medios encontrados fueron 4.02 mg kg-1 para As; 11.77 mg kg-1 para Cd, y 0.48 mg kg-1 para Pb. El cadmio superó los límites máximos permisibles de consumo que establecen las normas sanitarias para bivalvos y representan un riesgo para la salud humana. La contaminación en agua y en sedimento de la Laguna de las Ilusiones puede modificar el equilibrio de las poblaciones, principalmente las más susceptibles. Gamboa, Gamboa, Saldívar y Espejel (2007) cuantificaron Pb en sangre de cocodrilo (Cocodrylus Moreletti); los valores obtenidos (6.55-15.34 µg dl-1) son mayores que los permitidos para la vida acuática.
No hay estudios recientes sobre evaluaciones ambientales y ecotoxicológicas relacionados con la Laguna de las Ilusiones. A continuación se mencionan los pocos estudios que se han reportado: en el periodo 1992-1994, el P (10.6 mg l-1) y el N total (4.1 mg l-1) presentes en la laguna la catalogaban como un cuerpo de agua hipertrófico, cuya morfología detrítica y escasa mezcla hidráulica impedía los cambios de agua, favoreciendo la persistencia de sustancias conservativas y no conservativas (Rodríguez et al., 1994). De manera general, el contenido de contaminantes en los cuerpos de agua se incrementa a través del tiempo; en 1994, 30% de los ríos mexicanos estaba contaminado por Hg y Pb; en la actualidad, 95% se reporta como contaminados. La concentración de Pb en sedimentos superficiales en 1992 era de 158.68 µg g-1 en la Laguna de las Ilusiones (Villanueva & Botello, 1992); hoy, se desconoce.
La Laguna de las Ilusiones, ícono de la ciudad de Villahermosa, Tabasco, alberga una gran diversidad de especies acuáticas y terrestres, por lo que fue declarada reserva ecológica desde 1995 (Semarnat, 2000). Sin embargo, está sometida desde hace varios años a la presión de las actividades antrópicas que depositan de manera directa e indirecta desechos agrícolas, urbanos e industriales, que contribuyen al detrimento de su valor ecológico (Semarnat-Conanp, 2014). Prácticamente son nulos los estudios que abordan la contaminación en la Laguna de la Ilusiones, en particular por metales pesados; sin embargo, hay muchos ejemplos de contaminación por metales en diversos ríos de México, que sugieren que un cuerpo de agua con las condiciones de la Laguna de las Ilusiones puede considerarse como un sitio potencialmente contaminado. El objetivo de este trabajo fue determinar parámetros fisicoquímicos y metales (Pb, Cd, Mn, Zn, Cr, Al y Ni) en agua y sedimento superficial de la Laguna de las Ilusiones, y si representan un riesgo por efectos adversos a la vida acuática.
Materiales y métodos
Ubicación del sitio de estudio
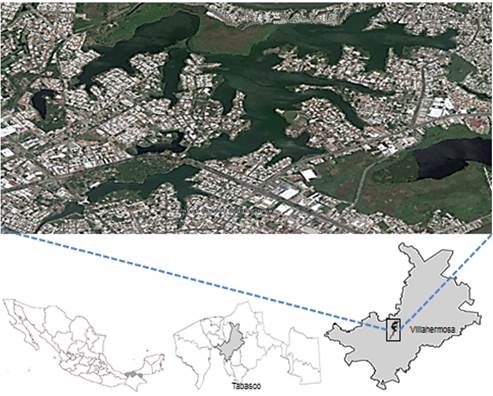
El estado de Tabasco se localiza al sureste de la república mexicana. Cuenta con una extensión territorial de 24 738 km2, clima cálido húmedo, con lluvias en verano, con un intervalo de temperatura media anual de 24 a 28 0C y precipitación anual de 1 500 a 2 000 mm (Palma et al., 2007). La Laguna de las Ilusiones se ubica en la región hidrológica RH30 y en la cuenca Grijalva-Usumacinta. Está en el área urbana de Villahermosa (170 59´ 22´´ a 180 01´ 22´´ N y 920 55´ 20´´a 920 56´ 40´´ O); se asienta en la provincia fisiográfica de la llanura costera del Golfo de México y ocupa una superficie de 160 hectáreas, entre los ríos Mezcalapa y Carrizal, a una altura promedio de 10 msnm (metros sobre el nivel del mar) (Figura 1). En 1995 fue decretada por el estado como área natural protegida, con carácter de reserva ecológica, para la conservación del cuerpo de agua, flora y fauna. La superficie ocupada ha disminuido un promedio de 30 hectáreas en un periodo de 10 años debido a las obras de urbanización de la ciudad de Villahermosa (Semarnat-Conanp, 2014; Sernapam, 2014).
Colecta de matrices ambientales
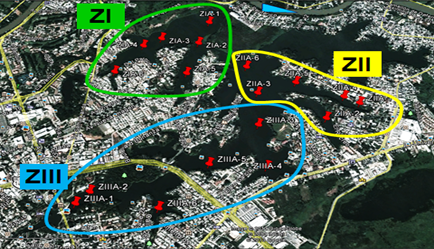
La Laguna de las Ilusiones se dividió en tres zonas y en cada zona se ubicaron, con base en la metodología propuesta por Torres-Dosal et al. (2006), seis sitios de muestreo (Figura 2). En cada uno se recolectaron seis muestras de agua en botes de polietileno; en frascos de vidrio se recolectó el sedimento superficial. Para la determinación de metales en agua se utilizaron frascos de polietileno de un litro, conteniendo 1 ml de ácido nítrico concentrado para evitar pérdidas por volatilización. En el muestreo de sedimento se emplearon frascos de color ámbar de dos litros. Las muestras se transportaron y conservaron a 4 0C hasta el momento de su análisis (NOM-001-ECOL-1996; Semarnat, 1996b). Se hicieron dos muestreos de agua: uno en abril de 2013 y el otro en septiembre de 2014.
Caracterización fisicoquímica
Agua
La determinación de los parámetros fisicoquímicos del agua se realizó in situ con el equipo multiparamétrico marca HANNA, modelo HI 9828. Se registró potencial de hidrógeno (pH); temperatura (0C); conductividad eléctrica (CE, µS cm-1); potencial óxido-reducción (POR, mV); oxígeno disuelto (OD, mg l-1); sólidos disueltos totales (SDT, mg l-1). En laboratorio se determinó la demanda química de oxígeno (DQO, mg l-1) por el método de reflujo cerrado con dicromato de potasio (NMX-AA-030-SCFI-2001).
Sedimentos
Las muestras de sedimento superficial se recolectaron con una draga de plástico en recipientes color ámbar de dos litros de capacidad. Se transportaron y mantuvieron a 4 0C hasta su análisis. Se secaron en una estufa a 60 0C por 72 horas; después se homogenizaron mecánicamente en un mortero de ágata y se tamizaron en malla de 600 µm. Los sedimentos se caracterizaron mediante la determinación de la textura por el método de Bouyoucos; el contenido de materia orgánica, por el método de Walkley y Black; el pH, por el método electrométrico. Se utilizó un potenciómetro marca Denver Instruments, modelo 215. La conductividad eléctrica fue por extracto de saturación (NOM-021-Semarnat-2000).
Cuantificación de metales en agua y sedimento
Previo a la cuantificación de metales, las muestras de agua y sedimento se colocaron en un horno de microondas marca Marcks, modelo 907501, y se evaluaron mediante los métodos EPA 3050 y 3052, respectivamente (EPA, 2000). La cuantificación de metales se llevó a cabo en un espectrofotómetro de absorción atómica, modelo Analyst 300, equipado con detector de ionización de flama, previamente calibrado con materiales de referencia certificados con trazabilidad del Instituto Nacional de Estándares (NIST) (Benavides et al., 2007; SCFI, 2001b). Los valores medios obtenidos para cada uno de los parámetros medidos fueron sometidos al análisis de varianza (ANOVA) con p < 0.05.
Resultados y discusión
En la Figura 3 se observan las propiedades fisicoquímicas determinadas en las muestras de agua en las tres zonas de la laguna. Los valores de pH en agua oscilaron entre 8.9 y 9.6, y se encuentran por arriba de los límites (6.5-9.0) permitidos por la Guía canadiense de la calidad de agua dulce; también el límite inferior (8.9) es mayor que el permitido (5.5) por la NOM-002-Semarnat-1996 (Semarnat, 1996a). Además, el valor más alto (9.6) lo presentó la zona III y el menor (8.9) la zona I. Presumiblemente, se debe a la presencia de iones de carbonato e hidróxido que pueden provenir de los residuos antrópicos y de los minerales naturales solubles.
La temperatura del agua se comportó en el rango de 28.8 a 29.9 0C. Fue inferior al límite permitido por la normatividad mexicana (40 0C). El POR varió en las tres zonas, desde 5 mV en la zona I hasta 80 mV en la zona II. Por su parte, el OD presentó valores desde 7 hasta 11 mg l-1, similares a los límites (no menor a 5 mg l-1) propuestos por la EPA (EPA, 2000) y por la Guía canadiense de la calidad del agua (9.5 mg l-1). Mientras que para la CE fueron de 225 a 275 µS cm-1, valores por debajo de 2 500 µS cm-1, propuesto por la NOM-069-ECOL-1994, típicos de cuerpos de agua dulce. El intervalo resultante (105-155 mg O2 l-1) para DQO está, de acuerdo con la Conagua (2012), clasificada como contaminada (40 < DQO < 200) y para los SDT (114-137 mg l-1) son similares a los reportados por la Secretaría de Energía, Recursos Naturales y Protección Ambiental (Sernapam) en 2012 y 2013 (Tabla 1). Los parámetros fisicoquímicos se muestran en la Figura 4.
Tabla 1 Parámetros (NOM-021-Semarnat-2000).
| Año | Puntos de muestreo | pH | T (°C) | CE (µS/cm) | OD (ppm) | SDT (ppm) | DQO (mg/l) |
|---|---|---|---|---|---|---|---|
| 2011 | Cencali (n = 1) | 6.7± 0.4 | 26.9 ± 1.6 | 249 ± 54.0 | 5.2 ± 1.7 | 180.8 ± 64 | 48.4 ± 8.2 |
| Ilusiones (n = 6) | 8.5 ± 0.7 | 27.6 ± 0.6 | 233.1 ± 25 .3 | 8.13 ± 2.48 | 166.1 ± 36.9 | 47.5 ±6.4 | |
| 2012 | Cencali (n = 1) | 6.9 ± 0.4 | 28.8 ± 2.7 | 197.8 ± 4.2 | 8.1 ± 2.9 | 181.3 ± 29.2 | 67 ± 9.0 |
| Ilusiones (n = 6) | 8.3± 0.9 | 28.3 ± 2.9 | 223.2 ± 52.0 | 8.0 ±2.3 | 165.6 ± 40.6 | 59.5 ± 8.7 | |
| 2013 | Cencali (n = 1) | 7.7 ±1.2 | 27± 1.7 | 246.6 ± 27.7 | 8.8± 2.1 | 216 ± 40.3 | 34 ± 9.3 |
| Ilusiones (n = 6) | 8.4 ± 0.7 | 28.8 ± 1.5 | 264.5 ± 41.1 | 9.5± 2.0 | 170.2 ± 19.9 | 66 ± 9.2 |
En los sedimentos, el pH osciló desde 5.9, moderadamente ácido, hasta 8.4, medianamente alcalino (NOM-021-Semarnat-2000). Los valores de 1 a 11% de MO indican que son de origen volcánico y la CE tuvo efectos despreciables de salinidad porque tienen un intervalo de 4 a 28 µS cm-1.
La granulometría para la zona I arrojó valores promedio de 67.2% de arena, 17.2% de arcilla y 15.4% de limo; la zona II fue de 75.4% de arena, 14.5% de arcilla y 10% de limo; la zona III, con 69.2% de arena, 16.1% de arcilla y 14.6% de limo, en referencia al triángulo de textura usado por el Departamento de Agricultura de Estados Unidos de América. Los resultados de las tres zonas corresponden a una clasificación textural que va de arenosa a franco arenosa moderadamente gruesa (USDA, 2014).
En la Tabla 2 se observa la concentración de los metales cuantificados en el agua: Cd de 2.2 a 5.6 µg l-1; Ni de 2.2 a 7.8 µg l-1; Cr de 28 a 64.4 µg l-1; Mn de 38.9 a 112.2 µg l-1; Zn de 12.2 a 79.2 µg l-1; Al de 218 a 1 385 µg l-1; Pb, ND a 0.1 µg l-1. Todos se encuentran por debajo de la NOM-001-Semarnat-1996 (Semarnat, 1996b). Sin embargo, para el Cr y Cd, el cociente de peligro (conc. de ref./media) es mayor a la unidad. También se aprecian las concentraciones de los metales encontrados en el sedimento (Tabla 3): Cd de 1.1 a 4.0 mg kg-1; Ni de 21.4 a 75.3 mg kg-1; Cr de 23.1 a 99.5 mg kg-1; Mn de 42.4 a 341.9 mg kg-1; Zn de 13.8 a 193.2 mg kg-1; Pb, ND de 204 mg kg-1; Al de 4 404.9 a 73 593.6 mg kg-1. Aquí, el cociente de peligro es mayor a la unidad para todos los metales encontrados, excepto para Zn y el Mn. De acuerdo con la legislación de Canadá y Estados Unidos, cuando el cociente de peligro es mayor que la unidad, ya existe un riesgo potencial para la vida acuática.
Tabla 2 Metales pesados en aguas superficiales.
| Zona | Mn | Ni | Cd | Pb | Cr | Zn | Al |
| Z1A1 | 96.7 | ( 5.6 | 3.3 | ( 55.6 | 49.9 | 21.7 | 894.4 |
| Z1A2 | 101.1 | 4.4 | 4.4 | ( 44.4 | 46.8 | 28.1 | 634.4 |
| Z1A3 | 104.4 | 2.2 | 2.2 | ( 44.4 | 55.0 | 28.0 | 1 385.6 |
| Z1A4 | 108.9 | 7.8 | 4.4 | ( 11.1 | 50.2 | 28.3 | 175.6 |
| Z1A5 | 75.6 | 2.2 | 3.3 | ( 33.3 | 59.8 | 53.7 | 584.4 |
| Z1A6 | 112.2 | ( 3.3 | 4.4 | ( 55.6 | 49.1 | 32.7 | 484.4 |
| ZIIA1 | 63.3 | 6.7 | 4.4 | ( 22.2 | 64.4 | 23.6 | 541.1 |
| ZIIA2 | 53.3 | 7.8 | 3.3 | ( 55.6 | 58.6 | 79.2 | 351.1 |
| ZIIA3 | 65.6 | ( 1.1 | 4.4 | ( 22.2 | 61.9 | 26.3 | 621.1 |
| ZIIA4 | 51.1 | ( 3.3 | 4.4 | ( 44.4 | 64.4 | 20.2 | 696.7 |
| ZIIA5 | 72.2 | 7.8 | 5.6 | ( 44.4 | 63.3 | 26.1 | 790.0 |
| ZIIA6 | 53.3 | ( 3.3 | 2.2 | ( 66.7 | 49.9 | 58.7 | 1 155.6 |
| ZIIIA1 | 51.7 | 6.7 | 3.9 | ( 27.8 | 59.3 | 23.7 | 472.2 |
| ZIIIA2 | 45.6 | ( 3.3 | 5.6 | ( 44.4 | 33.9 | 24.6 | 598.9 |
| ZIIIA3 | 43.3 | 5.6 | 4.4 | ( 33.3 | 28.0 | 43.6 | 374.4 |
| ZIIIA4 | 46.7 | ( 2.2 | 4.4 | ( 55.6 | 30.7 | 18.8 | 764.4 |
| ZIIIA5 | 45.0 | 0.0 | 3.9 | ( 50.0 | 45.1 | 24.9 | 311.7 |
| ZIIIA6 | 38.9 | 3.3 | 4.4 | ( 44.4 | 30.4 | 65.9 | 184.4 |
( bajo: límite de detección bajo. Todas las concentraciones están en µg. l-1.
Tabla 3 Metales pesados en sedimentos superficiales.
| Concentración (mg/kg) | Mn | Ni | Cd | Pb | Cr | Zn | Al (%) |
| Z I S1 | 75.3 | 18.6 | 1.9 | 9.0 | 91.2 | 33.6 | 5 257 (0.5) |
| Z I S2 | 42.4 | 41.3 | 1.7 | 24.4 | 71.9 | 300.3 | 42 753 (4.3) |
| Z I S3 | 114.4 | 30.9 | 1.6 | 7.5 | 61.2 | 66.9 | 17 433 (1.7) |
| Z I S4 | 53.2 | 21.4 | 1.1 | ND | 37.9 | 42.3 | 30 020 (3.0) |
| Z I S5 | 57.4 | 24.7 | 2.2 | 21.2 | 24.4 | 80.9 | 12 322 (1.2) |
| Z I S6 | 92.1 | 28.3 | 3.2 | 204.7 | 38.0 | 193.2 | 19 404 (1.9) |
| Z II S1 | 102.7 | 21.7 | 2.6 | 17.0 | 23.1 | 26.9 | 2 563 (0.3) |
| Z II S2 | 47.7 | 24.8 | 2.9 | 57.5 | 34.7 | 84.3 | 19 227 (1.9) |
| Z II S3 | 124.6 | 30.3 | 3.3 | 37.4 | 50.8 | 35.5 | 21 887 (2.2) |
| Z II S4 | 123.0 | 26.1 | 3.2 | 40.3 | 66.4 | 13.8 | 17 752 (1.8) |
| Z II S5 | 158.1 | 28.7 | 3.4 | 38.5 | 70.6 | 44.2 | 15 629 (1.6) |
| Z II S6 | 47.3 | 33.9 | 2.9 | 23.8 | 58.7 | 52.1 | 20 353 (2.0) |
| Z III S1 | 114.3 | 29.1 | 2.2 | 44.8 | 78.1 | 45.5 | 20 584 (2.1) |
| Z III S2 | 152.7 | 23.8 | 2.7 | 22.2 | 44.0 | 43.8 | 4 405 (0.4) |
| Z III S3 | 82.3 | 42.1 | 3.1 | 35.7 | 63.2 | 80.3 | 66 074 (6.6) |
| Z III S4 | 341.9 | 26.3 | 2.7 | 29.4 | 99.5 | 34.1 | 32 673 (3.3) |
| Z III S5 | 44.7 | 33.2 | 3.0 | 24.1 | 71.9 | 86.1 | 73 811 (7.4) |
| Z III S6 | 75.8 | 52.1 | 4.0 | 137.9 | 74.0 | 47.3 | 73 594 (7.4) |
| Media ± DE | 102.8 ± 70.1 | 29.9 ± 8.4 | 2.6 ± 0.7 | 42.8 ± 50.3 | 58.9 ± 21.8 | 72.8 ± 69.1 | 2.8 ± 2.2 |
| *LEL (NJ-DEP) | 630 | 16 | 0.6 | 31 | 26 | 120 | 2.55 |
| ISQG (CSQG) | - | - | 0.6 | 35 | 37.3 | 123 | - |
| *CP (media/LEL) | 0.2 | 1.9 | 4.3 | 1.4 | 2.3 | 0.6 | 1.1 |
Conclusiones
En el sitio de estudio, los valores de pH en agua oscilaron entre 8.9 y 9.6, considerados como alcalinos, y se encuentran por arriba de los límites (6.5-9.0) permitidos por la Guía canadiense de la calidad de agua dulce. La temperatura del agua (28.8-29.9 0C) fue inferior al límite permitido por la normatividad mexicana (40 0C). El oxígeno disuelto presentó valores similares a los establecidos por la EPA y por la Guía canadiense de la calidad del agua. El valor de DQO clasifica al cuerpo de agua como contaminado de acuerdo con la Conagua (2012) (40 < DQO < 200 mg l-1). Los valores de CE y SDT se encuentran dentro de los parámetros establecidos por la Sernapam. Todos los metales pesados determinados en el agua ―Cd, Ni, Cr, Mn, Zn, Al y Pb― están por debajo de la NOM-001-Semarnat-1996 (Semarnat, 1996b).
En los sedimentos, el pH osciló desde 5.9, moderadamente ácido, hasta 8.4, medianamente alcalino, de acuerdo con la NOM-021-Semarnat-2000. El porcentaje de materia orgánica indica que es de origen volcánico y la conductividad eléctrica tuvo efectos despreciables de salinidad. La granulometría en las tres zonas de muestreo corresponde a una clasificación textural, que va de arenosa a franco arenosa moderadamente gruesa (USDA, 2014). La concentración de Cd, Ni, Cr, Mn, Zn, Pb y Al en los sedimentos se encuentra dentro de las normas mexicanas; sin embargo, al ser comparados los valores obtenidos con las normas canadienses y americanas, sobrepasan los criterios de metales pesados establecidos para cuerpos de agua dulce. Esto indica que la biota ha sido afectada, al acumularse altas concentraciones de dichos metales en el sistema de estudio, por lo que las autoridades deben tomar conciencia de lo peligros inminentes a los que pueden estar expuestas las poblaciones cercanas.











 text in
text in