Femenino de 54 años con disnea moderada de cuatro años de evolución, que en los últimos seis meses ha pasado a ser de medianos esfuerzos, manejada por cardiólogo con amlodipino 2.5 mg y clopidogrel, agregándose sildenafil 100 mg ¼ BID. Al interrogatorio intencionado refiere que tolera 2 km de caminata diario. A la exploración física: 48 k, estatura de 158 cm, IMC 19.2, TA 100/60 mmHg, temp 36.6 oC; FR 22 rpm, FC 120 lpm. SaO2 93%; cráneo, cara y cuello sin alteraciones; auscultación cardiaca sin soplos, con componente pulmonar del segundo ruido reforzado. Abdomen sin visceromegalia. Extremidades sin cianosis y sin hipocratismo digital. El electrocardiograma (Figura 1) mostró: ritmo sinusal, frecuencia 120 lpm; AQRS +80-90; bloqueo de rama derecha del haz de His con datos de hipertrofia y sobrecarga de presión de ventrículo derecho. Teleradiografía de tórax con cardiomegalia grado II a expensas de crecimiento de aurícula derecha, y prominencia del arco de la arteria pulmonar. Se efectúa diagnóstico de hipertensión pulmonar secundaria a probable cardiopatía de corto circuito no detectada previamente. Se solicitó tomografía computarizada, la imagen de localizador tomográfico (Figura 2) mostró cardiomegalia grado II y prominencia del arco de la arteria pulmonar (Figuras 3, 4 y 5). Los estudios revelaron: conducto arterioso permeable tipo “b” de Krichenko de 18 mm, corto circuito de izquierda derecha. Hipertensión pulmonar (Figura 6) con fracción de expulsión del ventrículo izquierdo de 50%, fracción de expulsión del ventrículo derecho de 27.5% y dilatación biventricular. Se propuso la realización de cateterismo cardiaco con prueba de balón para posible aplicación de Amplatzer, canalizándose a solicitud de la paciente a Hospital de Alta Especialidad por parte de Seguro Popular de la Secretaría de Salud para su atención subsecuente.
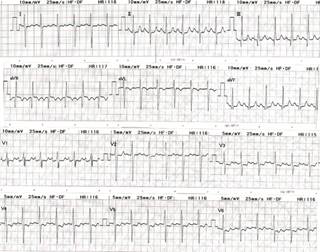
Figura 1: Electrocardiograma que muestra: ritmo sinusal, frecuencia 120 lpm; AQRS +80-90; hipertrofia del ventrículo derecho y bloqueo de rama derecha del haz de His en paciente femenino de 54 años con conducto arterioso persistente.
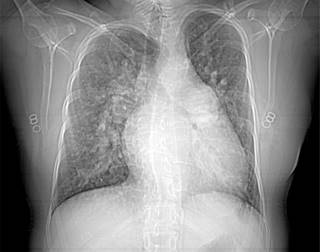
Figura 2: Imagen de localizador torácico de tomografía en la que se aprecia cardiomegalia, severo abombamiento de la arteria pulmonar principal y arco aórtico que desvían la tráquea a la derecha y presencia de escoliosis derecha a nivel dorsal.
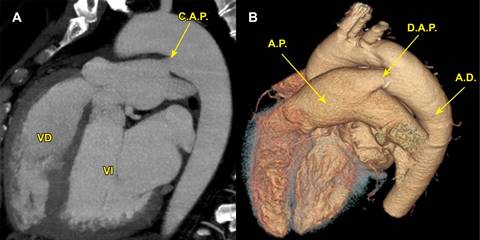
Figura 3: Tomografía computarizada (A) que revela conducto arterioso permeable en paciente de 54 años de edad. En (B) imagen renderizada en volumen 3D por tomografía que muestra un ducto arterioso permeable, amplio; nótese la dilatación severa de la arteria pulmonar.
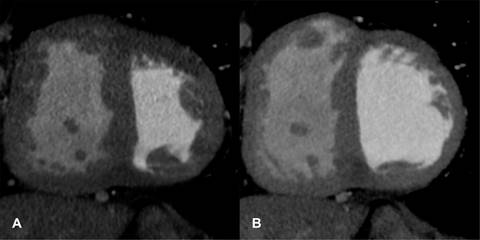
Figura 4: Imagen tomográfica en eje corto del ventrículo izquierdo en (A) sístole y (B) diástole que muestra desviación a la izquierda del septum interventricular que condiciona forma en “D”.
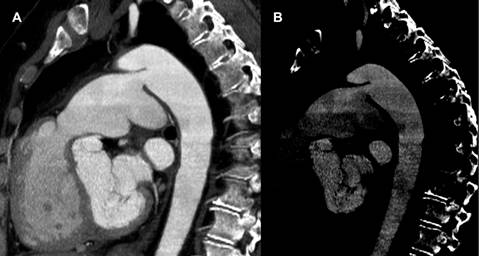
Figura 5: Imágenes de angio-cine-tomografía torácica (A) y (B) que demuestran paso de contraste bidireccional entre la aorta descendente y la arteria pulmonar.

Figura 6: Tomografía de tórax (A) en corte coronal con ventana pulmonar que muestra dilatación de la arteria pulmonar, con subsiguiente hipertrofia de las arterias intrapulmonares. Tomografía de tórax en corte axial (B) con ventana pulmonar que revela: incremento de tamaño e hipertrofia de las arterias intrapulmonares de predominio derecho.
La incidencia de PCA es uno en 2,000 nacimientos. El PCA representa entre 5 y 10% de todas las cardiopatías congénitas.1 Sin embargo, sí se incluyen niños con PCA “silencioso” (aquellos descubiertos incidentalmente por ecocardiografía realizada para otro propósito), la incidencia se ha estimado en uno en 500 a favor del género femenino con relación 2:1.
La historia clínica de los pacientes con PCA varía de manera considerable, desde individuos totalmente asintomáticos hasta pacientes con insuficiencia cardiaca congestiva grave o síndrome de Eisenmenger. Ya que la mayoría de los pacientes con PCA compensan bien (incluso con un cortocircuito moderado de izquierda a derecha y permanecen asintomáticos durante la infancia) los años de sobrecarga de volumen, llegan a provocar síntomas de insuficiencia cardiaca congestiva en la edad adulta. En estos pacientes, los síntomas pueden manifestarse con el inicio de fibrilación auricular resultante del crecimiento de la aurícula izquierda progresiva y crónica. Por último, un PCA previamente bien tolerado puede llegar a ser clínicamente significativo cuando sus efectos se combinan con afecciones adquiridas como cardiopatía isquémica o estenosis aórtica calcificada.
Los hallazgos del examen físico varían tanto como el historial médico. El hallazgo distintivo es un soplo continuo, localizado en el borde esternal izquierdo superior, a menudo denominado soplo de “maquinaria”, descrito y denominado soplo de Gibsom2 (descrito en 1900), su irradiación es hacia el lado izquierdo del esternón y a región infraclavicular izquierda, ocasionalmente se puede escuchar un ruido diastólico en el ápex cardiaco en pacientes con cortocircuitos ductales moderados o grandes, por lo que el impulso del ventrículo izquierdo será prominente y la presión del pulso se incrementa; por lo regular, el murmullo vesicular es normal, incluso con un cortocircuito grande, a menos que exista problema pulmonar agregado.3
El cierre del conducto está claramente indicado para cualquier niño o adulto que sea sintomático debido a una derivación significativa de izquierda a derecha a través del PCA.4
En pacientes asintomáticos con cortocircuito significativo de izquierda a derecha que da como resultado un agrandamiento del corazón izquierdo, el cierre está indicado para minimizar el riesgo de complicaciones en el futuro. El ecocardiograma establece el diagnóstico,5 siendo requerido el cateterismo cardiaco para la evaluación diagnóstica completa de la hemodinámica antes del cierre percutáneo. Es particularmente importante en adultos con PCA, en quienes es imperativo evaluar en su totalidad la resistencia vascular pulmonar y el grado de derivación antes de la intervención. En pacientes con presión arterial pulmonar elevada, la evaluación de la resistencia vascular pulmonar y su respuesta a agentes vasodilatadores como oxígeno, nifedipina, prostaciclina, sildenafil y óxido nítrico pueden ser útiles para determinar la conveniencia del cierre del conducto. La evaluación de la hemodinámica durante la oclusión temporal de la prueba con un catéter con balón también puede proporcionar información importante sobre la conveniencia del cierre.6











 text new page (beta)
text new page (beta)


