Services on Demand
Journal
Article
Indicators
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista mexicana de ingeniería química
Print version ISSN 1665-2738
Rev. Mex. Ing. Quím vol.10 n.2 Ciudad de México Aug. 2011
Ingeniería ambiental
Revisión de variables de diseño y condiciones de operación en la electrocoagulación
Review of design variables and operation conditions in electrocoagulation
M. Piña–Soberanis1*, A. Martín–Domínguez1, C.A. González–Ramírez2, F. Prieto–García2, A. Guevara–Lara2 y J.E. García–Espinoza3
1 Instituto Mexicano de Tecnología del Agua (IMTA), Jiutepec, Morelos, México. *Autor para la correspondencia. E–mail: mpina@tlaloc.imta.mx
2 Universidad Autónoma del Estado de Hidalgo (UAEH), Centro de Investigaciones Químicas, Pachuca de Soto, Hidalgo, México.
3 Estudiante de postgrado de la Facultad de Ingeniería, Universidad Nacional Autónoma de México, UNAM, México.
Recibido 30 de Agosto 2010.
Aceptado 13 de Abril 2011.
Resumen
En este documento se presenta una revisión bibliográfica sobre los fundamentos teóricos más importantes de la electrocoagulación, se analizan algunos diseños y se muestran los resultados más relevantes al aplicarla al tratamiento de agua para la remoción de diversos contaminantes de origen orgánico e inorgánico. Se enumeran algunas de sus ventajas con respecto a la coagulación química, se hace un análisis comparativo de los diseños experimentales utilizados, así como de las metodologías aplicadas, a fin de poder identificar las principales variables que intervienen en los mecanismos de remoción, tales como: la densidad de corriente; el tipo de material, tamaño y distancia en los electrodos; el tipo de conexiones utilizadas; el amperaje y voltaje aplicado; el pH, temperatura y conductividad del agua; el tiempo de residencia y el tipo de flujo utilizado. De la literatura especializada que fue consultada se concluye que los mecanismos que intervienen en la electrocoagulación no han sido aún claramente entendidos y hay pocas consideraciones de los factores que influyen en la efectiva remoción de especies iónicas, especialmente iones metálicos en el agua.
Palabras clave: electrocoagulación, electrodos, tratamiento de agua, diseño, iones metálicos.
Abstract
This document presents a bibliogr aphical review o f the most important theoretical principles on electrocoagulation; it also analyzes some designs and shows the most relevant results of electrocoagulation, as applied to the treatment of water for the purpose of eliminating several organic and inorganic pollutants. Some advantages of chemical coagulation are listed. Additionally, a comparative analysis of the experimental designs used and of the applied methodologies is made, so as to be able to identify the main variables that operate in removal mechanisms, such as current density, type of material used on the electrodes and their size, distance between electrodes, type of connections used, applied amperage and voltage, pH, temperature and water conductivity, as well as residence time and type of flow used. The specialized literature that was consulted shows that the mechanisms of electrocoagulation have not yet be en clearly understood and thereis little consideration of the factors that influence the effective removal of ionic species, especially metallic ions in water.
Keywords: electrocoagulation, electrodes, water treatment, design, metallic ions.
1 Introducción
La electrocoagulación (EC) es una tecnología de tratamiento que ha empezado a tomar auge en las últimas décadas, aunque su desarrollo se llevó a cabo a principios del siglo pasado y fue patentada en los Estados Unidos en 1909. En su forma más sencilla un reactor de electrocoagulación es una celda electrolítica constituida por un ánodo y un cátodo. Cuando los electrodos se conectan a una fuente de poder externa, el material del ánodo será electroquímicamente corroído por oxidación y el cátodo estará sujeto a reducción. Sin embargo, se han probado arreglos más eficientes como por ejemplo un par de ánodos y un par de cátodos conectados en serie o en paralelo lo que disminuye la pasivación de los electrodos. Mameriy col. (2001).
Los iones liberados durante la electrocoagulación forman largas cadenas de polihidróxidos, los cuales son diferentes a los formados en la coagulación convencional cuando se añaden sales químicas, debido a que tienen diferente estructura hidratada. Esta situación permite retirar, retener y desecar con mayor facilidad los lodos residuales. Los flocs formados de esta forma son menos hidratados, conteniendo menos agua ligada y por lo tanto se compactan más fácilmente, Martín y col. (2008).
Durante la formación de los hidróxidos metálicos, la generación de los iones está acompañada de la concentración electroforética de partículas alrededor del electrodo, las cuales neutralizan su carga coagulando. La corriente aplicada obliga a los iones OH– a migrar hacia el ánodo, por lo que el pH en la capa límite es más alto que en el resto de la solución, lo que favorece la formación de hidróxidos del metal del electrodo, Martín y col. (2008).
El hidróxido formado remueve los contaminantes presentes en el agua por complejación o atracción electrostática. Adicionalmente, en la proximidad de los electrodos el aumento de la concentración de los hidróxidos con carga positiva atrae aniones como los bicarbonatos y los sulfates que propician la precipitación del calcio y el magnesio, originando así un ablandamiento parcial del agua. Los mecanismos de remoción en electrocoagulación incluyen oxidación, reducción, coagulación, absorción, adsorción, precipitación y flotación, Parga y col. (2005).
Los iones Al3+ ó Fe2+ son coagulantes muy eficientes para la floculación de partículas, por lo que en EC son frecuentemente utilizados electrodos de hierro o de aluminio. Los iones de aluminio hidrolizado pueden formar largas cadenas de Al–O–Al–OH las cuales pueden adsorber químicamente una gran cantidad de contaminantes, Shen y col. (2003). El aluminio es normalmente usado para el tratamiento de agua potable y el hierro para el tratamiento de aguas residuales. En el caso del hierro, el Fe(OH)3 forma un coloide café rojizo y dependiendo del pH y de la disponibilidad de iones ferrosos, puede reaccionar con el oxígeno disuelto para dar Fe3O4, Yousuf y col. (2001).
Las reacciones químicas que se llevan a cabo en el ánodo son las siguientes: Chen (2004).
Para ánodo de aluminio:

En condiciones alcalinas:

En condiciones acidas:

Para ánodo de hierro:

En condiciones alcalinas:

En condiciones acidas:

La electrólisis del agua produce oxígeno e hidrógeno de la siguiente forma:
En el ánodo:

En el cátodo es:

Entre las principales ventajas de la EC sobre el método de coagulación química se reportan las siguientes:
1. La EC requiere equipos relativamente simples, es fácil de utilizar y su operación es flexible, Chen y col. (2002).
2. Durante el tratamiento el líquido no es enriquecido con aniones y el contenido de sales no se incrementa, como en el caso del tratamiento químico convencional, Phutdhawong y col. (2000).
3. Se produce hasta un 50% menos de lodos, así como un agua con menor concentración de sólidos disueltos (turbiedad), haciendo más factible su reutilización, Ogutveren y col. (1997), Tsouris y col. (2001).
4. Los flocs formados por EC son similares a los flocs producidos por coagulación química, excepto que los primeros tienden a ser mucho más largos, contienen menos agua superficial, son ácido–resistentes y son más estables, por ello pueden ser separados más rápido por filtración.
5. La EC tiene la ventaja de remover las partículas coloidales más pequeñas, debido a que el campo eléctrico aplicado incrementa su movimiento facilitando la coagulación, Yousuf y col. (2001).
6. El proceso de EC evita el uso de agentes químicos, eliminando así el problema de neutralizar el exceso de químicos y por lo tanto la posibilidad de una contaminación secundaria provocada por los mismos, cuando la coagulación química es utilizada, Yousuf y col. (2001).
7. Las burbujas de gas producidas durante la electrólisis pueden transportar los contaminantes a la superficie de la solución, donde éstos pueden ser más fácilmente concentrados, colectados y removidos.
8. Los procesos electrolíticos en la celda de EC son controlados eléctricamente sin dispositivos mecánicos lo que requiere menos mantenimiento.
9. Los componentes del sistema pueden ser fabricados localmente.
10. Las unidades son más compactas.
11. La remoción de arsénico trivalente mediante EC es mayor que en la coagulación química empleando cloruro férrico, Ratnay col. (2004).
Con el incremento de los parámetros reguladores de las normas de agua potable y las regulaciones ambientales para las descargas de aguas residuales, las tecnologías electroquímicas han tomado nuevamente importancia en todo el mundo durante las dos últimas décadas. Existen diversas industrias que aplican procesos electroquímicos para la recuperación de metales, potabilización de agua, tratamiento de descargas de agua residuales procedentes de tenerías, industrias de electroplatinados, industrias textil, entre otras, Chen (2004).
Aun cuando se ha aplicado exitosamente la EC en el tratamiento de distintos tipos de aguas de desecho ya sea domésticas Chen y col. (2002), industriales Phutdhawong y col. (2000); Shen y col. (2003); Carmona y col. (2006), con alto contenido orgánico Chen y col. (2000), con presencia de colorantes Xiong y col. (2001) o simplemente para agua potable Mameri y col. (2001); Jiang y col. (2002) esta tecnología no ha sido aceptada como un sistema convencional de tratamiento Holt y col. (2004) debido a sus elevados costos.
Lo que también ha limitado su implementation a gran escala es la falta de un procedimiento sistemático en el diseño y en la operación del sistema, que reduzca particularmente el problema de la pasivación de los electrodos y el costo de operación Holt y col. (2004). El diseño de reactores a escala industrial se basa en criterios empíricos debido a la falta de modelos disponibles que incluyan los principales factores que permitan su optimización Chen y col. (2002). Dichos modelos deberán considerar factores que influyen en las etapas fisicoquímica, electroquímica e hidráulica del proceso, así como sus interacciones.
La mayoría de los estudios han estado encaminados a la determinación de la potencia eléctrica requerida para producir una cantidad controlada de coagulante y obtener las características adecuadas de operación como son: las propiedades de transporte, tiempo de residencia, voltaje, potencial Z, pH, constituyentes químicos del agua y características de los electrodos que optimicen el proceso para una condición específica de operación. Sin embargo, los mecanismos de la electrocoagulación no han sido aún claramente entendidos y en la mayoría de los trabajos existentes sólo se establecen las eficiencias para las condiciones de prueba y no se analizan los factores que influyen en la efectiva remoción de especies iónicas, especialmente iones metálicos de agua.
El presente trabajo muestra una revisión bibliográfica de 46 estudios relacionados con la electrocoagulación en los últimos 23 años (Tabla 1), enfatizando los resultados que muestran el análisis de las principales variables de operación, como son: la densidad de corriente; el tamaño, material y distancia de electrodos; las conexiones utilizadas; el amperaje y voltaje aplicado; el pH, temperatura y conductividad del agua; el tiempo de residencia, tipo de flujo utilizado y costos de operación.
2 Aplicaciones de la electrocoagulación
El análisis de la información existente muestra que una gran variedad de partículas disueltas y suspendidas pueden ser removidas de manera efectiva de soluciones acuosas por electrólisis, Phutdhawong y col. (2000). Entre algunas aplicaciones de la EC se encuentran: la clarificación de aguas residuales y con fines de potabilización, Chen y col. (2002); la remoción de cromato, cianuro y arsénico de efluentes industriales, Balasubramanian y col. (2001), de fluoruro en agua para consumo humano, Mameri y col. (2001), de materia orgánica soluble, Tsai y col. (1996), de aceites en emulsión, Hosny (1996), Biswas y col. (1991); la recuperación de compuestos fenólicos, Phutdhawong y col. (2000) y tánicos, Chowwanapoonpohn y col. (2003), entre otros. El agua tratada por EC se convierte en agua clara, limpia, sin olor y lista para reutilizarse.
Otros autores, Mohammad y col. (2009) han realizado una amplia revisión bibliográfica para conocer los tipos de contaminantes removidos y su eficiencia mediante procesos de electrocoagulación y electrocoagulación–flotación. En su artículo consideran el agua contaminada con aceite, agua de desecho de la industria textil (colorantes), compuestos fenólicos, aguas residuales municipales e industriales, metales pesados en aguas residuales, turbiedad y metales pesados en agua potable, nitratos, nitritos, amoniaco y fluoruros. En el caso de la industria textil, mencionan que la eficiencia de la EC depende del pH, de la concentración del colorante, la densidad de corriente aplicada y el tiempo de residencia.
También reportan que los procesos de EC son más eficientes que la coagulación química en el tratamiento del agua potable. Para el caso de los nitratos, nitritos y amoniaco, es factible la EC, pero se requiere de más investigación ya que no se han establecido los mecanismos de remoción. De igual manera, la defluoración del agua es efectiva empleando la EC, pero no hay suficiente información relacionada con los complejos formados de Al–F.
3 Configuraciones hidráulicas y eléctricas
El arreglo de los electrodos puede ser de forma mono–polar o bi–polar y los materiales pueden ser aluminio o hierro, en forma plana o paquetes de láminas (ver Fig. 1a).

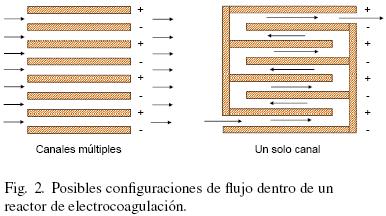
Dependiendo de la orientación de los electrodos (placas), el flujo dentro de la celda de electrocoagulación puede ser vertical u horizontal (Fig. 1b). El agua fluye a través de los espacios entre las placas, que pueden ser canales múltiples o un solo canal como se aprecia en la Fig. 2. Los canales múltiples es un arreglo simple, pero normalmente la velocidad de flujo en cada canal es baja. Cuando no es posible reducir la pasivación en la superficie de los electrodos, se recomienda incrementar la velocidad del flujo utilizando un sistema con un solo canal, Chen (2004).
También se han utilizado electrodos bipolares con celdas en paralelo. En este caso el electrodo "sacrificable" se localiza entre dos electrodos paralelos sin ninguna conexión eléctrica. Sólo los electrodos monopolares se conectan a la fuente externa de poder. Este tipo de arreglos resuelve en parte la disminución de la eficiencia de la electrocoagulación por formación de una capa de óxido sobre los electrodos.
Otra forma de aumentar la eficiencia de esta técnica es utilizar corriente alterna que retarda los mecanismos normales de ataque de los electrodos, sin embargo, los campos de corriente alterna pueden desestabilizar el sistema. También se ha aplicado esta tecnología en unidades de lecho fluidizado equipados con metales no consumibles y con partículas de aluminio sometidas a flujo turbulento. La agitación es mantenida con aire comprimido, Xiong y col. (2001).
Es importante también considerar los tiempos de residencia en el reactor, ya que de este depende el tamaño del mismo. Algunos autores como Deshpande (2010) emplean mayores tiempos de residencia para incrementar la dosis del coagulante, lo que mejora la eficiencia de remoción, pero aumenta el tamaño de las unidades y por lo tanto los costos de inversión.
En este mismo sentido se debe considerar el tipo de flujo, es decir, si se trata de un sistema en lotes (batch) o en continuo, la configuración de los electrodos y los tipos de conexión (bipolar y monopolar) que repercuten en la eficiencia y en el costo. Sin embargo, la tabla 1 muestra que la información publicada hasta el momento está enfocada principalmente a las eficiencias de remoción de los contaminantes, sin mostrar detalles de los diseños de los prototipos utilizados y sin profundizar en la influencia de las variables involucradas en los procesos.
Otros autores, Martín y col. (2008) evaluaron la incidencia del gradiente de velocidad en el mezclado (coagulación) con la eficiencia en la remoción de arsénico (As) en agua para consumo humano utilizando un reactor de EC a flujo pistón con electrodos de hierro (Fe). Encontraron que existe una clara tendencia a que la eficiencia del Fe producido y removido aumente al aumentar el gradiente de velocidades en el mezclado (G) y el producto del G con el tiempo t (Gt).
4 Material de los electrodos
En el caso de la EC con ánodos de sacrificio, la selección del material del electrodo va a depender de la naturaleza y afinidad que tenga el contaminante que se pretende remover con el coagulante producido, es decir, si se quiere remover material suspendido, el coagulante debe propiciar una desestabilización de los coloides para que éstos se aglutinen y posteriormente sean separados por precipitación. En el caso de elementos disueltos se busca que el coagulante los adsorba o los retenga mediante algún mecanismo fisicoquímico. Cuando se trata de electrodos inertes como el acero inoxidable, el titanio, platino, níquel, grafito, etc., el mecanismo de remoción es debido a que se presenta una reducción electroquímica del agua en el cátodo incrementándose el pH propiciando la formación de sales básicas poco solubles e hidróxidos de metales polivalentes que precipitan, Gorodovykh y col. (1987).
La utilización de electrodos de aluminio tiende a ser minimizada con respecto a los de hierro, debido a los problemas de disposición de los lodos conteniendo ese metal y a la alta pasivación de los electrodos Morante y col. (2002), Wan y col. (1991), Sin embargo, Mohammad y col. (2009) en su revisión concluyen que de acuerdo a los resultados experimentales de diversos autores, los electrodos de Al son mas eficientes que los de Fe para la remoción de aceites. En el caso de metales pesados se puede remover de manera muy eficiente el arsénico (As) y el cadmio de aguas residuales. Para As la remoción es muy eficiente utilizando electrodos de Fe considerando mecanismos de adsorción de los hidróxidos de Fe con las especies de As.
Electrodos inertes como el titanio y el paso de una corriente alterna, también remueve iones metálicos y promueve la coagulación de sólidos suspendidos. En este caso el movimiento electroforético concentra las partículas de carga negativa en el ánodo y por neutralización de cargas se facilita la coagulación, Martín y col. (2008).
En Mohammad y col. (2009) se comparó la eficiencia de remoción de la Demanda Química de Oxígeno (DQO), turbiedad, fenoles, hidrocarburos y grasas utilizando electrodos de aluminio (Al) e hierro (Fe) a diferentes tiempos de electrólisis (2.5, 5, 10, 15 y 20 minutos), y se encontró que en general se remueven más fenoles e hidrocarburos con electrodos de Al. Con electrodos de Fe se remueve más turbiedad y grasas y no hay una diferencia importante para la remoción de la DQO utilizando electrodos de Fe y Al. Del análisis se concluyó que la eficiencia y capacidad de los procesos de electrocoagulación dependen de la naturaleza del agua residual y de las concentraciones de los contaminantes.
En la Tabla 2 se muestra el porcentaje de estudios analizados, con relación al tipo de contaminante, material de los electrodos y tipo de flujo utilizado. Se observa una mayor frecuencia de experimentaciones hacia los procesos en lotes (batch) para tratar contaminantes inorgánicos utilizando electrodos de aluminio.
Para poder observar un comportamiento general de la frecuencia en relación a las condiciones experimentales realizadas (lotes y continuo) y al tipo de material empleado en los electrodos se elaboró un gráfico (Fig. 3) donde se resume la revisión bibliográfica de la tabla 1 y la hecha por Mohammad y col. (2009). En algunos casos se utilizaron cátodos de acero inoxidable u otro elemento resistente a la corrosión como el grafito, Pt y Ti. Se omitieron los datos experimentales de Russell, (1988) y Baklan y col. (1996) de la tabla 1 debido a que no reportaron el tipo de flujo utilizado.
El color, en la mayoría de los casos mostrados en la Fig. 3, es proveniente de pigmentos de la industria textil; en los metales pesados están incluidos el Cr+6, Cd+2, Se, St, Ni, Cr, Zn, Pb, CN, As y un caso para el sílice que utilizaron electrodos de hierro y aluminio (tabla 1); en las aguas residuales urbanas e industriales se reportaron las remociones de detergentes, pesticidas, humus, carbón orgánico total, DQO, DBO y compuestos fenólicos. El aluminio como ánodo de sacrificio sigue siendo el mayormente utilizado para el tratamiento de aguas residuales y para metales pesados se utilizan más los ánodos de hierro. También se observa en la Fig. (3) una mayor tendencia hacia las pruebas en lotes (batch) debido al mayor control y simplicidad de operación que éstos presentan.
5 Condiciones fisicoquímicas del agua
Las condiciones de operación de la electrocoagulación dependen de la química del medio acuoso, especialmente de la conductividad y el pH, pero también influyen el tamaño de partículas, el tipo de electrodos, el tiempo de retención, el espaciamiento entre electrodos y la concentración de los contaminantes, Martín y col. (2008).
También hay que tomar en cuenta que las características fisicoquímicas del agua pueden modificar las propiedades de los contaminantes, afectando así su remoción, tal es el caso del pH y la temperatura del agua, los cuales deben ser controladas para minimizar los efectos adversos a los mecanismos de remoción. Los efectos del pH en el agua se ven reflejados en la eficiencia de la corriente y en la solubilidad de los hidróxidos metálicos, se ha encontrado una mejor eficiencia de remoción a pH cercanos a 7. Por otro lado, a pesar de que no se ha investigado a profundidad el efecto de la temperatura en la EC, se ha encontrado que la eficiencia de la corriente aplicada para el aluminio se incrementa hasta los 60° C, efecto que se atribuye a la destrucción de la película de óxidos de aluminio que se forma en la superficie de los electrodos. Chen (2004), Tsouris (2001).
Por otra parte, no se observa en los estudios analizados la utilización de los criterios que establece la literatura sobre la coagulación química, como son: gradientes y tiempos de mezclado, floculación, etc., Arboleda (2000) y AWWA (1999), los cuales deben aplicarse y cumplirse en el proceso de la electrocoagulación y deben utilizarse para el diseño de reactores electroquímicos.
Ejemplos de esto se pueden ver en los trabajos publicados por Gorodo–vykh (1987), Renk (1988), Poon (1997), Kovatcheva (1999), Ciorba (2000), Balasubramaniam (2001), Chartrand (2003) y Azarian (2007) quienes no presentan información básica como la caída de potencial en el reactor ni la conductividad del agua en la que se llevaron a cabo las pruebas.
De las 38 publicaciones presentadas en la Tabla 1, solo 12 reportan la conductividad con la que realizaron sus experimentos, Morante (2002) muestra un caso extremo de conductividad elevada (1.2 E6 juS/cm) para la remoción de grasas, aceites y DQO. Una ventaja que se observa en el tratamiento de aguas residuales, en comparación con fuentes de agua natural, es la mayor conductividad de la primera que permite disminuir los costos del tratamiento por un menor consumo de energía., Jiang (2002), Paul A. (1996) y Zaied (2008).
6 Características electroquímicas
La selección de los parámetros analizados en la tabla 1 se realizó con base en la relación que guardan entre ellos en un proceso electroquímico. En el caso del voltaje o diferencia de potencial, que es definida como la resistencia en ohmios (Ω) al paso de una corriente eléctrica en amperios (A) aplicada en un circuito eléctrico (Ley de Ohm), se requiere considerar principalmente la conductividad eléctrica del electrolito y la separación de los electrodos. Esto finalmente determina el consumo de energía del proceso y por consiguiente el costo del tratamiento.
La densidad de corriente, donde se relaciona la cantidad de corriente eléctrica aplicada por unidad de área de electrodos (A/área), se evalúa con respecto a la pasivación de los electrodos, es decir, a densidades de corriente altas hay una mayor probabilidad de que se presente la pasivación del material, pero densidades de corriente bajas implican un mayor volumen de reactor y por lo tanto mayores tiempos de residencia. Deshpande (2010), Ghosh (2008).
Un valor muy elevado de densidad de corriente puede disminuir significativamente la eficiencia de la corriente debido a la producción de oxígeno y además influye en la pasivación de los electrodos, algunos autores recomiendan valores entre 20–25 A/m2, Chen (2004).
Siendo la densidad de corriente uno de los parámetros de mayor relevancia en la EC, autores como Renk (1988), Biswas (1991), Matteson (1995), Tsai (1996), Paul (1996), Bertazzoli (1997), Ógütveren (1997), Xiong (2001), GH Azarian (2007) y Amir (2007) no lo reportan en sus publicaciones.
En la tabla 1 se aprecian valores de densidades de corriente que van de 0.00023, Morante (2002), a 0.073 A/cm2, Chartrand (2003), aunque en la mayoría de los casos se procura operar a densidades de corrientes bajas para evitar la pasivación de los electrodos.
Hay autores que no mencionan la distancia ni el tamaño de los electrodos y/o su área activa, tal es el caso de Gorodo–vykh (1987), Renk (1988), Balasubramaniam (2001) y Chartrand (2003). Estos parámetros de operación son importantes para establecer la resistencia del sistema al paso de la corriente, y por lo tanto los costos por consumo de energía.
7 Influencia de iones presentes en el sistema
Hay estudios que muestran Chen (2004), que la presencia de NaCl reduce el efecto adverso de la presencia de otros iones como  ,
, 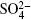 , que en presencia de Ca2+ ó Mg2+ forman una película aislante en la superficie de los electrodos que los pasiva. La presencia de sal también ayuda a disminuir el consumo de energía al aumentar la conductividad, además, cuando hay cloruros en el agua se pueden presentar las reacciones siguientes en presencia de una corriente eléctrica, lo que favorece la desinfección:
, que en presencia de Ca2+ ó Mg2+ forman una película aislante en la superficie de los electrodos que los pasiva. La presencia de sal también ayuda a disminuir el consumo de energía al aumentar la conductividad, además, cuando hay cloruros en el agua se pueden presentar las reacciones siguientes en presencia de una corriente eléctrica, lo que favorece la desinfección:
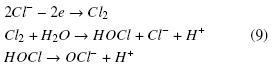
8 Costos de operación
En cuanto a los costos de operación, Jaing y col. (2002) compararon la electrocoagulación contra la coagulación química con flotación por aire disuelto, y reportaron que el costo se incrementó conforme la densidad de corriente aumentaba, y que el costo por el consumo de los electrodos de aluminio representaba de un 70 a 90% del costo total.
Otros autores, Nielson y col. (2005), mencionan que los costos por concepto de material del electrodo, en el caso de utilizar aluminio, es de CAN$7/kg, lo que para dosificaciones de 81 mgAl/L genera un costo del agua tratada (sólo por material de electrodos) de CAN$0.57/m3.
Conclusiones
En general, en la mayoría de los artículos revisados solo se muestran las eficiencias de remoción sobre algún tipo de contaminante, bajo las condiciones específicas en que se llevaron a cabo las pruebas, ya sea en lotes (batch) o en continuo y no se describen los detalles de los modelos experimentales empleados ni de todas las variables experimentales que son muy útiles para poder tratar de interpretar los posibles mecanismos que se llevan a cabo en el sistema sobre algún contaminante en específico. Tampoco se observa el uso de los criterios de la coagulación química aplicados a la electrocoagulación y que son fundamentales para realizar diseños apropiados al tipo de contaminante que se pretende remover.
Se puede decir que la electrocoagulación funciona adecuadamente como una tecnología alterna en el tratamiento de aguas residuales y agua potable, ya que los resultados mostrados en los documentos analizados, cumplen con las expectativas del investigador sobre los requerimientos específicos de cada caso, pero es necesario seguir investigando para poder establecer, en cada caso, los mecanismos mediante los cuales interactúan los contaminantes y el coagulante generado, así como definir el papel que juegan en tales mecanismos la presencia de otros elementos disueltos en el agua.
Por otro lado, se recomienda que en futuras investigaciones se definan, además de los contaminantes que se pretenden remover, de manera clara y completa el control de variables de operación de mayor relevancia en los procesos electroquímicos, como son el voltaje, la densidad de corriente, el material de los electrodos, la distancia entre los electrodos, el tipo de conexión entre éstos, su tamaño y área activa, así también se deben establecer las características fisicoquímicas del electrolito como son el pH, la conductividad y la temperatura. También, en ese mismo sentido se deben definir claramente las condiciones de flujo y tiempos de residencia, ya que de éstos depende su factibilidad de ser aplicados a grandes escalas.
Referencias
Arboleda Valencia J. (2000). Teoría y Práctica de la purificación del agua. McGraw–Hill, Tercera edición, Sao Paulo, Brasil. [ Links ]
AWWA American Water Works Association. (1999). Water Quality & Treatment. McGraw–Hill., Quinta edición. [ Links ]
Azarian G.H., Mesdaghinia A.R., Vaezi F., Nabizadeh R., Nematollahi D. (2007). Algae Removal by electro–coagulation process, application for treatment of the effluent from industrial wastewater treatment plant. Iranian Journal of Public Health 36, 57–64. [ Links ]
Balasubramanian N. y Madhavan K. (2001). Arsenic Removal from industrial effluent through electrocoagulation. Chemical Engineering Technology 24, 519–521. [ Links ]
Baklan V. Yu. y Kolesnikova I. P. (1996). Influence of electrode material on the electrocoagulation. Journal of Aerosol Science 27, 209–210. [ Links ]
Bertazzoli R., Widner R. C., Lanza M.R.V., Di Iglia R.A., Sousa F.B.M. (1997). Electrolytic removal of metals using a flow–through cell with a reticulated vitreous carbon cathode. Journal of the Brazilian Society 8, 487–493. [ Links ]
Biswas N. y Lazarescu G. (1991). Removal of oil from emulsions using electrocoagulation. International Journal of Environmental Studies 38, 65–75. [ Links ]
Burns S. E., Yiacoumi S., Tsouris C. (1997). Microbubble generation for environmental and industrial separations. Separation and Purification Technology 11, 221–232. [ Links ]
Chartrand M.M.G. y Bunce N.J. (2003). Electrochemical remediation of acid mine drainage. Journal of Applied Electrochemistry 33, 259–264. [ Links ]
Ciorba G.A., Radovan C., Vlaicu I. y Pitulice L. (2000). Correlation between organic component and electrode material: Consequences on removal of surfactants from wastewater. Electrochimica Acta 46, 297–303. [ Links ]
Chen X., Chen G. y Yue Po L. (2002). Novel electrode system for electroflotation of wastewater. Environmental Science & Technology 36, 778–783 [ Links ]
Chen G. (2004). Electrochemical technologies in wastewater treatment. Separation and Purification Technology 38, 11–41. [ Links ]
Chen, X, Chen, G. y Yue, L.P. (2002). Investigation on the electrolysis voltage of electrocoagulation. Chemical Engineering Science 57, 2449–2455. [ Links ]
Chowwanapoonpohn S., Chewchanwuttiwong S., Garson M. J. y Buddhasukh, D. (2003). Electrocoagulation and recovery of tannins from tree barks. Journal of Applied Electrochemistry 33, 647–650. [ Links ]
Den W., Wang C.J. (2008). Removal of silica from brackish water by electrocoagulation pretreatment to prevent fouling of reverse osmosis membranes. Separation and Purification Technology 59, 318–325. [ Links ]
Deshpande, A. M., Satyanarayan, S. y Ramakant, S. (2010). Treatment of high–strength pharmaceutical wastewater by electrocoagulation combined with anaerobic process. Water Science and Technology–WST–61.2. IWA Publishing. [ Links ]
Emamjomeh M.M., Sivakumar M. (2009). Fluoride removal by a continuous flow electrocoagulation reactor. Journal of Environmental Management 90, 1204–1212. [ Links ]
Emamjomeh M.M., Sivakumar M. (2009). Review of pollutants removed by electrocoagulation and electrocoagulation/flotation processes. Journal of Environmental Management 90, 1663–1679. [ Links ]
Ghosh D., Medhi C.R., Purkait M.K. (2008). Treatment of fluoride containing drinking water by electrocoagulation using monopolar and bipolar electrode connections. Chemosphere 73, 1393–1400. [ Links ]
Gorodovykh V. E., Kaplin A. A., Svishchenko N. M., Obraztsov S. V. (1987). Purification of water by electrocoagulation with an alternating asymmetrical current for stripping voltammetry. Zhurnal Analiticheskoi Khimii 42, 1024–1026. [ Links ]
Hernlem B. J., Tsai L. S. (2000). Chlorine generation and disinfection by electroflotation. Journal of Food Science 65, 834–837. [ Links ]
Hosny A.Y. (1996). Separating oil from oil–water emulsions by electroflotation technique. Separations Technology 6, 9–17 [ Links ]
Hossein Mahvi A. y Bazrafshan E. Removal of Cadmium from Industrial Effluents by Electrocoagulation Process Using Aluminum Electrodes. World Applied Sciences Journal (2007). [ Links ]
Jiang J. Q., Graham N. J. D., André C. M., Kelsall G. H., Brandon N. P., Chipps M. J. (2002). Comparative performance of an electro coagulation/flotation system with chemical coagulation/dissolved air flotation: A pilot–scale trial. Electrolytic treatment of turbid water in package plant. Water Science and Technology: Water Supply 2, 289–297. [ Links ]
Jumpatong K., Buddhasukh D. (2003). Electrocoagulation of some heavy metals. Contributed paper Chiang Mai Journal of Science 30 (1), 33–40. [ Links ]
Kovatcheca Valeria K., Parlapanski Marin D. (1999). Sono–electrocoagulation of iron hydroxides. Colloids and Surfaces A: Physicochemical and Engineering Aspects 149, 603–608. [ Links ]
Lescuras–Darrou V., Lapicque F., Valentin G. (2001). Electrochemical ferrate generation for waste water treatment using cast irons with high silicon contents. Journal of Applied Electrochemistry 32, 57–63 [ Links ]
Mameri N., Loucini H., Belhocine D., Grib H., Piron D. L., Yahiat Y. (2001). Defluoridation of sahara water by small plant electro coagulation using bipolar aluminium electrodes. Separation and Purification Technology 24, 113–119. [ Links ]
Martín D.A., Rivera H.M.L., Piña S.M., Pérez C.S. (2008). Incidencia del gradiente de velocidad en la eficiencia de la electrocoagulación para remover arsénico en un reactor a flujo pistón. Interciencia, Revista de Ciencia y Tecnología 33, 503–509. [ Links ]
Matteson Michael J., Dobson Regina L., Glenn Robert W. Jr., Kukunoor S. Nagesh, Waits William H. III, Clayfield Eric J. (1995). Electrocoagulation and separation of aqueous suspensions of ultra fine particles. Colloids and Surfaces A: Physicochemical and Engineering Aspects 104, 101–109. [ Links ]
Morante G.G. (2002). Electrocoagulación de aguas residuales. Revista Colombiana de Física 34, 484–487. [ Links ]
Morales Posada N.B., Acosta Niño G.E. (2010). Sistema de electrocoagulación como tratamiento de aguas residuales galvánicas. Ciencia e Ingeniería Neogranadina 20, 33–44. [ Links ]
Ögütveren Ülker B., Koparal S. (1997). Electrocoagulation for oil–water emulsion treatment. Journal of Environmental Science and Health 32, 2507–2520. [ Links ]
Paul A. B. (1996). Electrolytic treatment of turbid water in package plant. 22nd WEDC Conference, New Delhi India, 35–47. [ Links ]
Parga J.R., Cocke D.L., Valenzuela J.L., Gomes J.A., Kesmez M., Irwin G., Moreno H., Weir M. (2005). Arsenic removal via electrocoagulation from heavy metal contaminated groundwater in La Comarca Lagunera México. Journal of Hazardous Materials B124, 247–254. [ Links ]
Phutdhawong W., Chowwanapoonpohn S., Buddhasukh D. (2000). Electrocoagulation and subsequent recovery of phenolic compounds. Analytical Sciences 16, 1083–1084. [ Links ]
Poon C. P. C. (1997). Electroflotation for groundwater decontamination. Journal of Hazardous Materials 55, 159–170 [ Links ]
Pouet M. –F. and Grasmick A. (1995). Urban wastewater treatment by electrocoagulation and flotation. Water Science & Technology 31, 275–283. [ Links ]
Pouet M–F, Persin F., Rumeau M. (1992). Intensive treatment by electrocoagulation–flotation–tangential flow micro filtration in areas of high seasonal population. Water Science and Technology 25, 247–253 [ Links ]
Ratna Kumar P., Chaudhari S., Khilar K.C., Mahajan S.P. (2004). Removal of arsenic from water by electrocoagulation. Chemosphere 55, 1245–1252. [ Links ]
Renk R. (1988). Treatment of Hazardous Wastewaters by Electrocoagulation. Research Engineer. Western Research Institute. [ Links ]
Sanfan W. (1991). Studies on economic property of pretreatment process of brackish using electrocoagulation (EC) method. Desalination 82, 365–373. [ Links ]
Subramanyan V., Jothinathan L., Jeganathan J., Ganapathy S. (2009). Remediation of phosphate–contaminated water by electrocoagulation with aluminium, aluminium alloy and mild steel anodes. Journal of Hazardous Materials 164, 1480–1486. [ Links ]
Tsai C. T., Lin S. T., Shue Y. C., Su P. L. (1996). Electrolysis of soluble organic matter in leachate from landfills. Water Research 31, 3073–3081. [ Links ]
Tsouris C., DePaoli D. W., Shor J. T., Hu M.Z. –C., Ying T.–Y. (2001). Electrocoagulation for magnetic seeding of colloidal particles. Colloids and Surfaces. A: Physicochemical and Engineering Aspects 177, 223–233 [ Links ]
Xiong Y., Strunk P.J., Xia H., Zhu X., Karlson H.T. (2001). Treatment of dye wastewater containing acid orange II using a cell with three–phase three–dimensional electrode. Water Research 35, 4226–4230 [ Links ]
Yousuf M., Mollah A., Schennach R., Parga J.R., Cocke D.L. (2001). Electrocoagulation (EC)–science and applications. Journal of Hazardous Materials B84, 29–41. [ Links ]
Zaied M., Bellakhal N. (2009). Electrocoagulation treatment of black liquor from paper industry. Journal of Hazardous Materials 30,995–1000. [ Links ]














