La miocarditis eosinofílica (ME) es una inflamación miocárdica aguda causada por la infiltración tisular de eosinófilos, debido a su elevado número en sangre periférica1-3. Las causas frecuentes son parasitosis y toxicidad farmacológica, mientras que la enfermedad granulomatosa con poliangeítis (EGPA) es rara y su diagnóstico, de descarte1-3.
Presentamos el caso de una mujer de 28 años, con antecedentes de asma bronquial y rinitis alérgica en la infancia, que consultó por disnea progresiva, parestesias en muslo y pie derechos, pérdida de peso y sudoración nocturna de ocho semanas de evolución, cuadro por el cual había recibido previamente una dosis única de corticosteroide de depósito en otro centro. Se hospitalizó en unidad coronaria por presentar insuficiencia cardiaca (IC) congestiva de predominio derecho, sin hipoperfusión periférica. El electrocardiograma mostró taquicardia sinusal y microvoltaje, y la radiografía de tórax cardiomegalia y derrame pleural bilateral (Fig. 1). En el laboratorio se detectó eosinofilia (12%; 1,900 eosinófilos/mm3 ), proteína C reactiva 20 mg/dl, troponina I ultrasensible 22 y 21 ng/l, y proBNP (péptido natriurético tipo B) 8,042 pg/ml. El ecocardiograma transtorácico (ETT) reveló dilatación e hipocinesia global del ventrículo izquierdo (VI) con fracción de eyección (FeVI) del 21%, strain longitudinal global 6%, excursión del anillo tricuspídeo de 12 mm, insuficiencia mitral moderada y presión sistólica pulmonar de 36 mmHg (Fig. 2). Ante el diagnóstico de IC aguda por miocardiopatía dilatada con FeVI severa, con sospecha de miocarditis, se inició tratamiento con furosemida endovenosa.

Figura 1 Ecocardiograma transtorácico. A: vista apical de 4 cámaras que evidencia miocardiopatía dilatada con dilatación de las cuatro cámaras cardiacas. B: vista apical de 4 cámaras con Doppler color que evidencia insuficiencia mitral y tricuspídea. C: strain longitudinal global del ventrículo izquierdo (VI) disminuido.
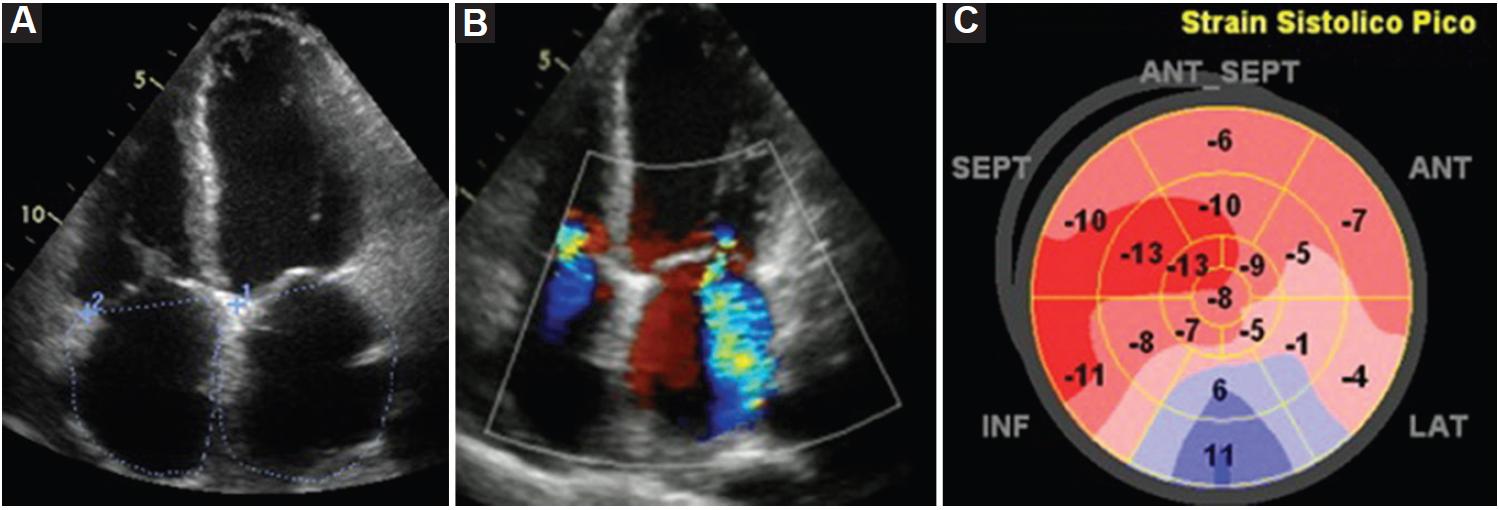
Figura 2 Radiografía de tórax y electrocardiograma (ECG) al ingreso. A: radiografía de tórax que evidencia congestión pulmonar, derrame pleural y cardiomegalia. B: ECG que evidencia taquicardia sinusal y microvoltaje.
Se realizó resonancia magnética cardiaca (RMC) a los siete días de la hospitalización (nueve semanas posteriores al inicio de los síntomas), que confirmó los hallazgos del ETT pero no evidenció edema ni realce tardío con gadolinio (Fig. 3). La angiografía coronaria confirmó la ausencia de lesiones coronarias obstructivas. Las serologías y cultivos para VIH, influenza, enterovirus, adenovirus, citomegalovirus, Epstein-Barr, tuberculosis, Mycoplasma, clamidia y Coxiella fueron negativas. El dosaje de anticuerpos citoplasmáticos antineutrófilos, antimieloperoxidasa y antiproteinasa 3 fue negativo. Por persistencia del derrame pleural, se realizó una tomografía axial computarizada que reveló derrame pleural bilateral de predominio izquierdo, adenomegalias mediastinales, retroperitoneales e inguinales, y esplenomegalia. Se efectuó toracocentesis izquierda, que mostró exudado inflamatorio mononuclear, con cultivo negativo para gérmenes comunes y micobacterias.

Figura 3 Imagen de resonancia magnética nuclear cardiaca. A: imagen de cine, que evidencia miocardiopatía dilatada con adelgazamiento de los espesores miocárdicos. B: ausencia de edema y realce tardío con gadolinio endovenoso en secuencia de inversión-recuperación.
Dada la eosinofilia creciente, la elevación de inmunoglobulina E y la intensificación de las parestesias en muslo y pie derechos, se efectuó una biopsia de médula ósea que evidenció infiltración eosinofílica y descartó mutaciones de FIP1L1-PDGFRA y BCR-ABL1, y un electromiograma que reveló infiltración axonal y denervación aguda del nervio tibial posterior que se atribuyeron a infiltración eosinofílica. Se efectuó una biopsia endomiocárdica (BEM) que reveló infiltración eosinofílica miocárdica con apoptosis celular y necrosis sin granulomatosis (Fig. 4).

Figura 4 Imagen de anatomía patológica (400x) obtenida por biopsia endomiocárdica. Las flechas señalan infiltrados de eosinófilos en forma difusa o por acúmulos.
Con los estudios anteriormente efectuados, se diagnosticó ME secundaria a hipereosinofilia por EGPA. Se inició tratamiento con 500 mg de metilprednisolona tres días consecutivos, con desaparición de la eosinofilia, continuando con metilprednisona oral y 750 mg/día de ciclofosfamida por seis días, con posterior resolución de la IC. Luego del alta hospitalaria, la paciente continuó asintomática, sin eosinofilia y con mejoría de la FeVI hasta un 44% a tres meses de seguimiento.
Discusión
La ME es una inflamación miocárdica aguda por infiltración de eosinófilos que causan apoptosis celular y necrosis miocárdica, asociado frecuentemente a eosinofilia en sangre periférica. Las etiologías incluyen infecciones virales, parasitosis, reacciones a fármacos, trastornos mieloproliferativos agudos, vasculitis y la EGPA o síndrome de Churg-Strauss1-3, como es el caso que presentamos. La EGPA es una vasculitis granulomatosa necrotizante sistémica asociada a eosinofilia que compromete arterias de mediano y pequeño calibre, siendo infrecuente y de diagnóstico por descarte1-3. El compromiso cardiaco se observa en hasta el 60% de los casos y el 48% de las formas fatales, cuyas manifestaciones clínicas incluyen dolor torácico, palpitaciones, IC, shock cardiogénico o muerte súbita1-3.
Los criterios diagnósticos de EGPA incluyen asma, eosinofilia periférica mayor al 10% del recuento de leucocitos, mononeuropatía o polineuropatía, infiltrados pulmonares, anomalías en senos paranasales y biopsia con eosinófilos extravasculares4. Cuatro criterios positivos son diagnósticos (sensibilidad y especificidad del 85 y 99.7%, respectivamente)4 y nuestro paciente presentaba los seis criterios descritos. El diagnóstico de la ME por EGPA se basa en la presencia de infiltrados miocárdicos por eosinófilos en la BEM1-3. La RMC aporta información diagnóstica y pronóstica al detectar realce tardío y edema con un patrón intramiocárdico o parcheado5, no presentes en nuestro caso debido al tiempo transcurrido desde el inicio de los síntomas hasta su realización, dando tiempo a la resolución del proceso inflamatorio inicial (estadio subagudo). Estimamos además que el tratamiento con corticosteroides al inicio del cuadro (ocho semanas antes de su hospitalización) abortó el desarrollo de mayor lesión, edema y fibrosis miocárdica.
El tratamiento se basa en la inmunosupresión. Se sugiere iniciar prednisona 1 g/día durante tres días y continuar con 0.5-1.5 mg/kg/día oral hasta su remisión. Se recomienda adicionar ciclofosfamida, que podría luego reemplazarse por azatioprina, que tiene menos efectos adversos6. El pronóstico depende del inicio precoz del tratamiento, y el compromiso cardiaco, renal o encefálico son marcadores de evolución desfavorable6.
La descripción de este caso resalta su difícil diagnóstico, que debe sospecharse en casos de IC, eosinofilia, antecedentes de asma bronquial y neuropatía periférica. El ETT y la RMC son fundamentales inicialmente, y la BEM certifica el diagnóstico. El tratamiento inmunosupresor resuelve la hipereosinofilia y puede revertir la afección miocárdica.











 text new page (beta)
text new page (beta)


