Introducción
En la estenosis aórtica se produce de forma progresiva una disminución del área de la válvula aórtica, lo que genera una restricción a la salida del flujo sanguíneo del ventrículo izquierdo (VI) hacia la aorta. Las causas más frecuentes son: degenerativa, reumática y congénita. La estenosis aórtica degenerativa se presenta en el 5% de los adultos mayores de 65 años, de los cuales el 11% tienen estenosis aórtica severa. Se considera «severa» cuando el orificio de la válvula aórtica es menor de 1 cm2 y la gradiente media transvalvular aórtica es igual o mayor de 40 mmHg.
Los pacientes con estenosis aórtica severa inicialmente son asintomáticos, sin embargo, en la evolución presentan disnea, angina y síncope, produciendo deterioro en la calidad de vida y aumento de la mortalidad1-5. El riesgo de muerte súbita en pacientes asintomáticos es del 1% al año y en los sintomáticos este riesgo aumenta a 3-5% a los seis meses. La cirugía de reemplazo valvular aórtico ha demostrado conseguir una reducción significativa de la mortalidad en estos pacientes5-7. En los pacientes con contraindicación o alto riesgo para la cirugía de reemplazo valvular aórtico, el implante percutáneo de la prótesis aórtica es una alternativa segura y efectiva.
De esta manera, la estenosis aórtica severa es una condición de alto riesgo, que requiere un manejo interdisciplinario para reducir la morbilidad y mortalidad. Por la Dirección de Guías de Práctica Clínica, Farmacovigilancia y Tecnovigilancia del Instituto de Evaluación de Tecnologías en Salud e Investigación (IETSI), junto con especialistas del Instituto Nacional Cardiovascular (INCOR) y del Seguro Social del Perú (EsSalud) elaboraron la guía de práctica clínica (GPC) basada en evidencias, que emitió recomendaciones y puntos de buenas prácticas clínicas (BPC) para la evaluación y el tratamiento de pacientes con estenosis aórtica severa. El presente artículo es un resumen de dicha GPC.
Metodología
El procedimiento seguido para la elaboración de la presente GPC está detallado en su versión extensa, la cual puede descargarse de la página web del IETSI del EsSalud (http://www.essalud.gob.pe/ietsi/guias_pract_clini.html).
En resumen, se aplicó la siguiente metodología:
—Conformación del grupo elaborador de la guía local (GEG—Local). Este estuvo conformado por metodólogos y médicos especialistas en cardiología, cardiología intervencionista y cirugía cardiovascular.
—Formulación de preguntas. En concordancia con los objetivos y alcances de esta GPC, el GEG—Local formuló siete preguntas clínicas (Tabla 1), cada una de las cuales tuvo una o más preguntas PICO (Population, Intervention, Comparator, Outcome). A su vez, cada pregunta PICO pudo tener uno o más desenlaces (o outcomes) de interés.
Tabla 1 Preguntas clínicas abordadas
Tema Preguntas clínicas Evaluación inicial Pregunta 1: En pacientes con estenosis aórtica, ¿qué sistema de clasificación de severidad se debería usar? Tratamiento Pregunta 2: En pacientes con estenosis aórtica severa, ¿qué sistema de graduación de riesgo quirúrgico se debería usar: STS o EuroSCORE II? Pregunta 3: En pacientes con estenosis aórtica severa asintomática, ¿se debería realizar el reemplazo valvular aórtico temprano o esperar que el paciente desarrolle síntomas? Pregunta 4: En pacientes con estenosis aórtica severa sintomática, ¿se debería realizar SAVR o TAVR? Pregunta 5: En pacientes con estenosis aórtica severa en los que se decida realizar TAVR, ¿cuál debería ser la vía de abordaje de primera elección para el TAVR? Pregunta 6: En pacientes con estenosis aórtica severa en los que se decida realizar TAVR y quienes, además, presenten enfermedad arterial coronaria severa, ¿se debe realizar PCI? Pregunta 7: ¿Debería conformarse un Heart Team que decida el tratamiento del paciente con estenosis aórtica severa? EuroSCORE II: European System for Cardiac Operative Risk Evaluation II; PCI: intervención coronaria percutánea; SAVR: reemplazo valvular aórtico quirúrgico; STS: Society of Thoracic Surgeons Risk Score; TAVR: reemplazo valvular aórtico percutáneo.
—Búsqueda y selección de la evidencia. Para cada pregunta PICO se realizó la búsqueda y selección de la evidencia. Para ello, durante enero—febrero del 2018 se buscaron revisiones sistemáticas (RS) publicadas como artículos científicos (mediante búsquedas sistemáticas en PubMed) o realizadas como parte de una GPC previa (mediante una búsqueda sistemática de GPC sobre el tema) (Anexo 1). Cuando se encontraron RS de calidad aceptable, se escogió una para la toma de decisiones, la cual se actualizó cuando el GEG—Local lo consideró necesario. Cuando no se encontró ninguna RS de calidad aceptable, se realizó una búsqueda de novo de estudios primarios.
—Evaluación de la calidad de la evidencia. La calidad de la evidencia, para cada desenlace de cada pregunta PICO, se consideró alta, moderada, baja o muy baja (Tabla 2). Para evaluar la calidad de la evidencia se siguió la metodología de Grading of Recommendations Assessment, Development, and Evaluation (GRADE)8 y se usaron tablas de perfiles de evidencias de GRADE (Anexo 2). Finalmente, se le asignó a la pregunta PICO el nivel de calidad más bajo alcanzado por alguno de estos desenlaces.
Tabla 2 Significado de los niveles de calidad de la evidencia y de la fuerza de la recomendación
Significado Calidad de la evidencia (⊕⊕⊕⊕) Alta Es muy probable que el verdadero efecto sea similar al efecto estimado (⊕⊕⊕○) Moderada Es moderadamente probable que el verdadero efecto sea similar al efecto estimado, pero es posible que sea sustancialmente diferente (⊕⊕○○) Baja Nuestra confianza en el efecto estimado es limitada. El verdadero efecto podría ser sustancialmente diferente al efecto estimado (⊕○○○) Muy baja Tenemos muy poca confianza en el efecto estimado. El verdadero efecto muy probablemente sea sustancialmente diferente al efecto estimado Implicación de la fuerza de la recomendación Recomendación fuerte (a favor o en contra) El GEG-Local cree que todos o casi todos los profesionales que revisan la evidencia disponible seguirían esta recomendación. En la formulación de la recomendación se usa el término «se recomienda» Recomendación débil (a favor o en contra) El GEG-Local cree que la mayoría de los profesionales que revisan la evidencia disponible seguirían esta recomendación, pero un grupo de profesionales podrían no seguirla. En la formulación de la recomendación se usa el término «se sugiere» GEG-Local: grupo elaborador de la guía local.
—Formulación de las recomendaciones. El GEG—Local revisó la evidencia seleccionada para cada pregunta clínica en reuniones periódicas y formuló recomendaciones fuertes o débiles (Tabla 2) usando la metodología GRADE9. Para ello, se consideraron: 1) beneficios y daños de las opciones; 2) valores y preferencias de los pacientes; 3) aceptabilidad por parte de los profesionales de salud; 4) factibilidad de las opciones en los establecimientos de salud del EsSalud, y 5) uso de recursos. Luego de discutir estos criterios para cada pregunta, el GEG—Local formuló las recomendaciones por consenso o por mayoría simple. Asimismo, el GEG—Local formuló puntos de BPC, usualmente con base en su experiencia clínica.
—Revisión por expertos externos. La presente GPC fue revisada en reuniones con médicos especialistas representantes de otras instituciones y tomadores de decisiones. Asimismo, su versión extensa fue enviada por vía electrónica a expertos externos para su revisión (mencionados en la sección de agradecimientos). El GEG—Local tuvo en cuenta los resultados de estas revisiones para modificar las recomendaciones finales.
—Aprobación de la GPC. La presente GPC fue aprobada para su uso en el EsSalud, con Resolución N.°47 — IETSI — ESSALUD — 2018.
—Actualización de la GPC. La presente GPC tiene una validez de tres años. Al acercarse al fin de este periodo se procederá a realizar una RS de la literatura para su actualización, luego de la cual se decidirá si se actualiza la presente GPC o se procede a realizar una nueva versión.
Recomendaciones
La presente GPC abordó siete preguntas clínicas, en relación con dos temas: la evaluación inicial y el tratamiento de la estenosis aórtica severa. Con base en dichas preguntas se formularon nueve recomendaciones (una recomendación fuerte y ocho recomendaciones débiles), 16 puntos de buena práctica clínica y un flujograma (Tabla 3 y Fig. 1).
Tabla 3 Lista completa de recomendaciones
| Pregunta N° | Enunciado | Tipo* | Fuerza y dirección† | Calidad de la evidencia† |
|---|---|---|---|---|
| Evaluación inicial | ||||
| 1 | Para clasificar a los pacientes diagnosticados con estenosis aórtica en estenosis aórtica leve, moderada o severa, se recomienda usar el sistema de clasificación de estenosis aórtica propuesto por la guía de AHA/ACC 2014 (no modificada en la actualización AHA/ACC 2017). | BPC | ||
| Tratamiento | ||||
| 2 | En pacientes con estenosis aórtica severa con indicación de SAVR o TAVR, sugerimos aplicar los sistemas de puntuación de EuroSCORE II y STS para evaluar el riesgo quirúrgico para reemplazo valvular | R | Débil a favor | Muy baja (⊕⊖⊖⊖) |
| Se clasificará a los pacientes con estenosis aórtica severa según su riesgo quirúrgico como: — Riesgo bajo. STS o EuroSCORE II <4%, sin fragilidad ni comorbilidades y sin impedimentos para el procedimiento específico — Riesgo intermedio. STS o EuroSCORE II entre 4 y 8%, con fragilidad no más que leve o con compromiso de no más de un órgano/sistema mayor que no mejorará postoperatoriamente, e impedimentos mínimos para el procedimiento específico — Riesgo alto. STS o EuroSCORE II >8%, o con fragilidad moderada a severa, con compromiso de no más de 2 órganos/sistemas mayores que no mejorarán postoperatoriamente, o un posible impedimento para el procedimiento específico — Riesgo prohibitivo. Riesgo preoperatorio de mortalidad y morbilidad >50% al año, con compromiso de ≥3 órganos/sistemas mayores que no mejorarán postoperatoriamente, fragilidad severa, o un impedimento severo para el procedimiento específico |
BPC | |||
| 3 | En pacientes con estenosis aórtica severa asintomática sugerimos no realizar reemplazo valvular aórtico temprano de forma sistemática | R | Débil a favor | Muy baja (⊕⊖⊖⊖) |
| Los pacientes con estenosis aórtica severa asintomática serán programados para reemplazo valvular temprano si tienen alguna de las siguientes condiciones: — Pacientes con FEVI <50% — Calcificación severa en válvula aórtica (≥3,000 AU en hombres o ≥1,600 AU en mujeres) — Un rápido incremento en la velocidad transaórtica (>0.3 m/s de incremento por año) — Estenosis aórtica muy severa (velocidad transaórtica ≥5.5 m/s o gradiente de presión media ≥60 mmHg) — Cambios hemodinámicos adversos (síntomas o disminución de la presión arterial) durante la prueba de esfuerzo — Hipertensión pulmonar severa sin otra explicación |
BPC | |||
| Los pacientes con estenosis aórtica severa asintomática deberán ser evaluados clínicamente cada 6 meses o cuando el paciente presente síntomas relacionados a la enfermedad (disnea, angina o síncope) | BPC | |||
| Los pacientes con estenosis aórtica severa asintomática que empiecen a desarrollar síntomas serán evaluados para estratificación de riesgo y programación de reemplazo valvular aórtico | BPC | |||
| 4 | En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año se debe realizar el reemplazo valvular aórtico | BPC | ||
| En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y riesgo quirúrgico bajo sugerimos la realización de SAVR como primera opción de tratamiento | R | Débil a favor | Muy baja (⊕⊖⊖⊖) | |
| En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y riesgo quirúrgico intermedio sugerimos la realización de SAVR como primera opción de tratamiento | R | Débil a favor | Muy baja (⊕⊕⊕⊖) | |
| En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y riesgo quirúrgico alto sugerimos la realización de SAVR o TAVR | R | Débil a favor | Muy baja (⊖⊖⊖⊖) | |
| En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año que sean catalogados como inoperables sugerimos la realización de TAVR como primera opción de tratamiento | R | Fuerte a favor | Moderada (⊕⊖⊖⊖) | |
| En los pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y riesgo quirúrgico bajo, considerar como tratamiento de primera elección el SAVR, sin necesidad de una evaluación previa por el Heart Team | BPC | |||
| En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y que tengan riesgo quirúrgico intermedio (que además tengan criterios de fragilidad, edad muy avanzada, índice de masa corporal inadecuado o una comorbilidad severa), riesgo quirúrgico alto, o que sean considerados inoperables: realizar una evaluación por el Heart Team para decidir su tratamiento | BPC | |||
| En pacientes con estenosis aórtica severa sintomática, en situaciones de emergencia, descompensación aguda o en una cirugía no cardíaca, y que tengan indicación de reemplazo valvular: considerar realizar valvulotomía percutánea como terapia puente para SAVR o TAVR | BPC | |||
| En pacientes con estenosis aórtica severa sintomática que tengan una expectativa de vida menor a un año, contraindicar SAVR y TAVR y realizar tratamiento paliativo | BPC | |||
| En pacientes con estenosis aórtica severa sintomática que sean sometidos a TAVR, seguir los procedimientos establecidos en las guías de procedimientos o protocolos locales | BPC | |||
| Las discordancias en la estratificación de riesgo o tratamiento serán decididas por el Heart Team | BPC | |||
| 5 | En pacientes con estenosis aórtica severa en los que se decida realizar TAVR, recomendamos que el abordaje de primera elección sea el transfemoral | R | Débil a favor | Muy baja (⊕⊖⊖⊖) |
| Cuando la vía transfemoral no sea posible, el Heart Team evaluará cada caso particular para definir el posible uso de otros abordajes, como a través de la subclavia, el transapical o el transaórtico. El Heart Team tomará esta decisión con base en estudios de imagen invasivos y/o no invasivos | BPC | |||
| 6 | En pacientes con estenosis aórtica severa en los que se decida realizar TAVR, que además presenten enfermedad arterial coronaria severa, sugerimos realizar PCI | R | Débil a favor | Muy baja (⊕⊖⊖⊖) |
| En pacientes con estenosis aórtica severa en los que se decida realizar TAVR, que además presenten enfermedad arterial coronaria severa para la cual se haya decidido realizar PCI, sugerimos que el PCI sea realizado antes del TAVR | R | Débil a favor | Muy baja (⊕⊖⊖⊖) | |
| Realizar revascularización miocárdica (PCI para aquellos sometidos a TAVR o cirugía de revascularización coronaria para aquellos sometidos a SAVR) cuando se encuentre enfermedad arterial coronaria severa (reducción ≥70% en el diámetro de alguna arteria coronaria mayor o reducción ≥50% en el diámetro del tronco de la coronaria izquierda) | BPC | |||
| 7 | Los establecimientos de salud que realicen cirugía cardiovascular en pacientes con estenosis aórtica severa de riesgo quirúrgico intermedio, alto y/o riesgo prohibitivo deberían conformar un Heart Team que estará a cargo de decidir el tratamiento del paciente | BPC | ||
| El Heart Team debe estar conformado al menos por: — Un cardiólogo clínico con experiencia en patología valvular — Un cardiólogo experto en imagen cardiovascular — Un cardiólogo intervencionista — Un cirujano cardiovascular con experiencia en patología valvular |
BPC | |||
EuroSCORE II: European System for Cardiac Operative Risk Evaluation II; FEVI: fracción de eyección del ventrículo izquierdo; PCI: intervención coronaria percutánea; SAVR: reemplazo valvular aórtico quirúrgico; STS: Society of Thoracic Surgeons Risk Score; TAVR: reemplazo valvular aórtico percutáneo.
*Recomendación (R) o punto de buenas prácticas clínicas (BPC).
†La fuerza, dirección y calidad de la evidencia solo se establecen para las recomendaciones, no para los puntos de BPC.
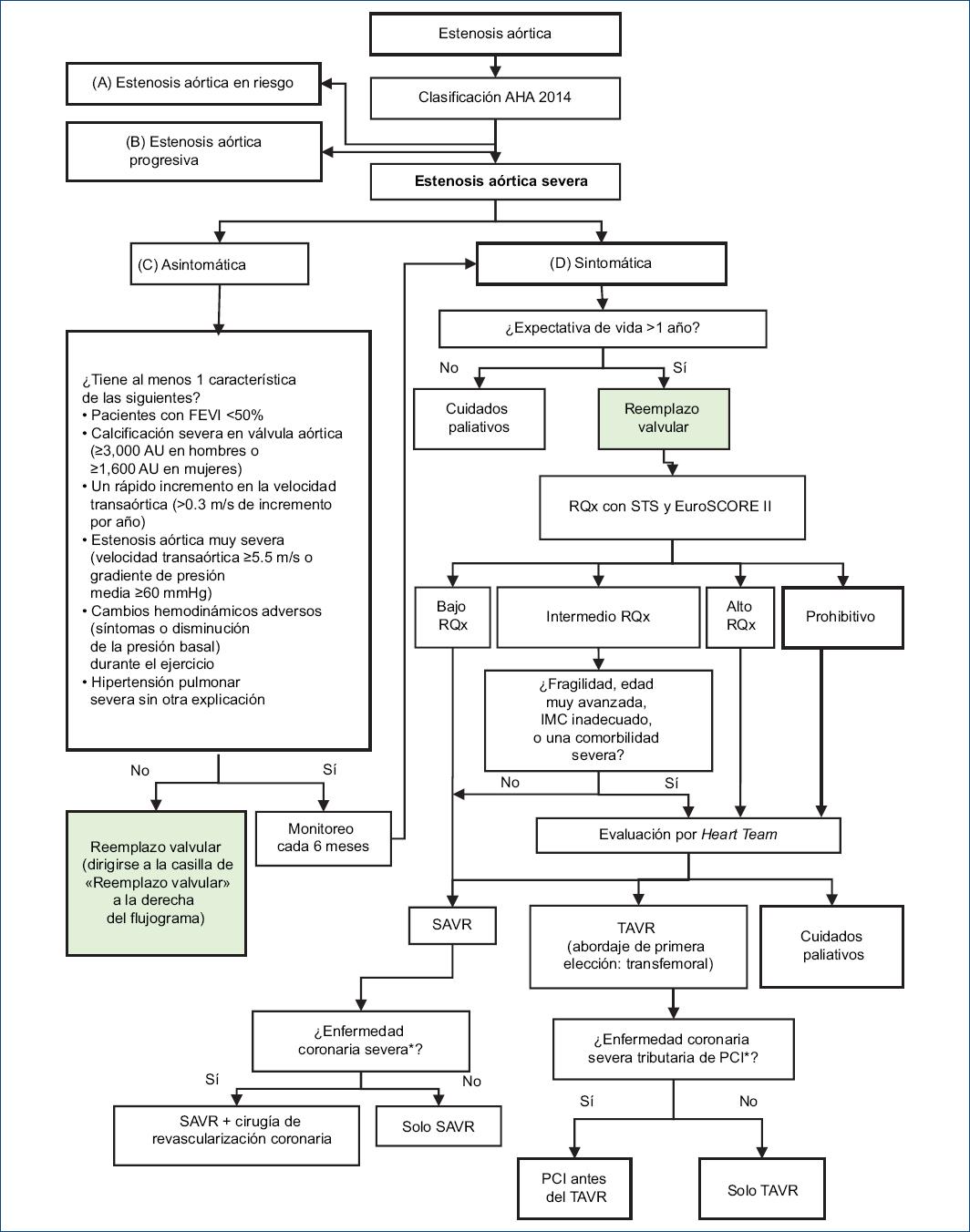
Figura 1 Flujograma de evaluación y tratamiento de la estenosis aórtica severa. AHA: American Heart Association; EuroSCORE II: European System for Cardiac Operative Risk Evaluation II; FEVI: fracción de eyección del ventrículo izquierdo; IMC: índice de masa corporal; PCI: intervención coronaria percutánea; RQx: riesgo quirúrgico; SAVR: reemplazo valvular aórtico quirúrgico; STS: Society of Thoracic Surgeons Risk Score; TAVR: reemplazo valvular aórtico percutáneo. *Enfermedad coronaria severa: reducción ≥70% en el diámetro de alguna arteria coronaria mayor, o reducción ≥50% en el diámetro del tronco de la coronaria izquierda
En los pacientes con estenosis aórtica, el médico debe decidir qué criterios utilizará para realizar el diagnóstico de estenosis aórtica severa (pregunta 1). Luego deberá decidir el tratamiento y para ello debe determinar cuál sistema de graduación de riesgo de riesgo quirúrgico usará (pregunta 2), cómo tratará a los pacientes asintomáticos (pregunta 3) y cuándo optará por el reemplazo valvular aórtico quirúrgico (SAVR, Surgical Aortic Valve Replacement) o por el reemplazo valvular aórtico percutáneo (TAVR, Transcatheter Aortic Valve Replacement) en pacientes sintomáticos (pregunta 4). Si se decide realizar un TAVR, se debe decidir la vía de abordaje (pregunta 5) y la posibilidad de realizar o no una intervención coronaria percutánea si el paciente además presenta enfermedad arterial coronaria severa (pregunta 6). Finalmente, para el manejo de los pacientes con estenosis aórtica severa es necesario determinar si se requerirá de un grupo de expertos o Heart Team (pregunta 7).
A continuación, se expondrán las recomendaciones para cada pregunta clínica, así como un resumen del razonamiento seguido para llegar a cada recomendación.
Pregunta 1. En pacientes con estenosis aórtica, ¿qué sistema de clasificación de severidad se debería usar?
Recomendaciones y puntos de buena práctica clínica
Para clasificar a los pacientes diagnosticados con estenosis aórtica en estenosis aórtica leve, moderada o severa, se recomienda usar el sistema de clasificación de estenosis aórtica propuesto por la guía de la American Heart Association/American College of Cardiology (AHA/ACC) 2014 (no modificada en la actualización del 2017). BPC.
De la evidencia a la decisión
En todo paciente con estenosis aórtica se debe determinar la severidad. Esta clasificación tiene una implicación pronóstica y de tratamiento. En los pacientes con estenosis aórtica leve o moderada se realizará observación clínica y monitorización periódica. En aquellos con estenosis aórtica severa sintomática se evaluará el reemplazo valvular.
Se han desarrollado diferentes sistemas de clasificación de la severidad de los pacientes con estenosis aórtica. Nuestra búsqueda sistemática encontró clasificaciones en las GPC de la AHA/ACC 200610 y 2014, actualizada en 201711, la European Society of Cardiology/European Asociation for Cardio-Thoracic Surgery (ESC/EACTS) 201712 y la Sociedad Brasileña de Cardiología/Sociedad Interamericana de Cardiología (SBC/SIAC Brasil) 201113; además de una clasificación propuesta por Lancelotti14. No se encontraron estudios que hayan comparado los distintos tipos de clasificación entre sí. Es por ello que no se emitieron recomendaciones, sino puntos de BPC.
Planteamiento de buena práctica clínica
Por consenso se escogió el sistema de clasificación de la AHA/ACC 201411 (Tabla 4), ya que actualmente es el más conocido y usado, en la práctica clínica y en los ensayos clínicos. La actualización del 2017 de la guía de la AHA/ACC 2014 no modificó esta clasificación15.
Tabla 4 Estadios de la estenosis aórtica según AHA/ACC (2014)11
| Grado | Definición | Anatomía valvular | Medidas hemodinámicas de la válvula aórtica | Consecuencias hemodinámicas | Síntomas | FEVI | ||
|---|---|---|---|---|---|---|---|---|
| Ca++ | Movilidad | Criterios indispensables | Medidas adicionales | |||||
| A | En riesgo de EA | + | Normal | Vmáx aórtica <2 m/s | - | Ninguno | Normal | |
| B | EA progresiva | ++ | ↓a↓↓ | EA leve: Vmáx aórtica 2.0-2.9 m/s o ΔP media <20 mmHg | - | Ninguno | Normal | |
| EA moderada: Vmáxaórtica 3.0-3.9 m/s o ΔP media <20-39 mmHg | ||||||||
| C: EA severa asintomática | ||||||||
| C1 | EA severa asintomática | +++ | ↓↓↓ | EA severa: Vmáx aórtica ≥4 m/s o ΔP media ≥40 mmHg | AVA ≤1.0 cm2 (o AVAi ≤0.6 cm2/m2) | — Disfunción diastólica del VI — Hipertrofia leve del VI |
— Ninguna — Test de ejercicio es razonable para confirmar la sintomatología |
Normal |
| EA muy severa: Vmáx aórtica ≥5.0 m/s o ΔP media ≥60 mmHg | ||||||||
| C2 | EA severa asintomática con disfunción del VI | +++ | ↓↓↓ | EA severa: Vmáx aórtica ≥4 m/s o ΔP media ≥40 mmHg | AVA ≤1.0 cm2 (o AVAi ≤0.6 cm2/m2) | Ninguna | <50% | |
| D: EA severa sintomática | ||||||||
| D1 | EA severa sintomática con gradiente alto | ++++ | ↓↓↓↓ | Vmáx aórtica ≥4 m/s o ΔP media ≥40 mmHg | AVA ≤1.0 cm2 (o AVAi ≤0.6 cm2/m2), pero puede ser mayor con EA/IA combinada | — Disfunción diastólica del VI — Hipertrofia del VI — HTP puede estar presente |
— Disnea al ejercicio o tolerancia al ejercicio disminuida — Angina al ejercicio — Síncope o presíncope al ejercicio |
Normal o ↓ |
| D2 | EA severa sintomática con bajo flujo/bajo gradiente y FEVI reducido | ++++ | ↓↓↓↓ | AVA ≤1.0 cm2 con Vmáx aórtica <4 m/s o ΔP media <40 mmHg | Prueba de estrés dobutamina muestra un AVA ≤1.0 cm2 | — Disfunción diastólica del VI — Hipertrofia del VI |
— Falla cardíaca — Angina — Síncope o presíncope |
<50% |
| En reposo | Con Vmáx aórtica ≥4 m/s con cualquier flujo | |||||||
| D3 | EA severa sintomática con bajo gradiente y FEVI normal o | ++++ | ↓↓↓↓ | AVA ≤1.0 cm2 con Vmáx aórtica <4 m/s o ΔP media <40 mmHg | AVAi ≤0.6 cm2/m2 e <35 ml/m2 | — Grosor incrementado de la pared del VI — Cámara del VI pequeña — Llenado diastólico restrictivo | — Falla cardíaca — Angina — Síncope o presíncope |
≥50% |
| EA severa sintomática con bajo flujo paradójico | Medido cuando el paciente está normotenso (PA sistólica <140 mmHg) | |||||||
AVA: área valvular aórtica; AVAi: índice del área valvular aórtica; Ca++: calcificación de válvula; ΔP media: diferencia de presiones medias transaórticas; EA: estenosis aórtica; FEVI: fracción de eyección del ventrículo izquierdo; HTP: hipertensión pulmonar; IA: insuficiencia aórtica; PA: presión arterial; Vmáx transaórtica: velocidad máxima transaórtica; VI: ventrículo izquierdo.
Pregunta 2. En pacientes con estenosis aórtica severa, ¿qué score de sistema de graduación de riesgo quirúrgico se debería usar: STS o EuroSCORE II?
Recomendaciones y puntos de buena práctica clínica
—En pacientes con estenosis aórtica severa con indicación de SAVR o TAVR, sugerimos aplicar las puntuaciones de EuroSCORE II (European System for Cardiac Operative Risk Evaluation II) y STS (Society of Thoracic Surgeons Risk Score) para evaluar el riesgo quirúrgico para reemplazo valvular. Recomendación débil a favor, muy baja calidad de evidencia (⊕⊝⊝⊝).
-
—Se clasificará a los pacientes con estenosis aórtica severa según su riesgo quirúrgico como:
Riesgo bajo. STS o EuroSCORE II <4%, sin fragilidad ni comorbilidades y sin impedimentos para el procedimiento específico.
Riesgo intermedio. STS o EuroSCORE II entre 4 y 8%, con fragilidad no más que leve o con compromiso de no más de un órgano/sistema mayor que no mejorará postoperatoriamente e impedimentos mínimos para el procedimiento específico.
Riesgo alto. STS o EuroSCORE II >8% o con fragilidad moderada a severa, con compromiso de no más de dos órganos/sistemas mayores que no mejorarán postoperatoriamente o un posible impedimento para el procedimiento específico.
Riesgo prohibitivo. Riesgo preoperatorio de mortalidad y morbilidad >50% al año, con compromiso de tres o más órganos/sistemas mayores que no mejorarán postoperatoriamente, fragilidad severa o un impedimento severo para el procedimiento específico. BPC.
De la evidencia a la decisión
Los pacientes con estenosis aórtica severa requieren tratamiento de reemplazo valvular aórtico, por lo cual es necesario evaluar el riesgo quirúrgico en estos pacientes. Los sistemas de puntuación de riesgo quirúrgico más difundidos y conocidos son el EuroSCORE II16 y el STS17. Ambos predicen el riesgo de mortalidad y morbilidad después de la cirugía de reemplazo valvular. El EuroSCORE II está disponible en www.euroscore.org y el STS en http://riskcalc.sts.org/stswebriskcalc/#/calculate.
Para contestar esta pregunta se evaluaron tres subpoblaciones: pacientes intervenidos con SAVR, pacientes intervenidos con TAVR y pacientes intervenidos con una u otra intervención indistintamente. Se encontraron RS de estudios observacionales para cada subpoblación. En pacientes sometidos a SAVR, una RS (5 estudios, n = 11,791) concluyó que el STS sobreestima la mortalidad18. En pacientes sometidos a TAVR, una RS (24 estudios, n = 12,346) concluyó que el EuroSCORE II infraestima la mortalidad19. En pacientes sometidos a SAVR o TAVR, una RS (10 estudios, n = 13,856) concluyó que el STS sobreestima la mortalidad18.
Debido a estos resultados heterogéneos, se decidió formular una recomendación a favor de la aplicación de ambos sistemas de puntuación para tomar la decisión sobre qué intervención realizar. Debido a que la calidad de la evidencia es muy baja y que no todos los médicos aceptarían tal medida, al igual que los pacientes, pues implicaría una mayor cantidad de evaluaciones y tiempo, se decidió dar una fuerza de recomendación débil.
Planteamiento de buena práctica clínica
Se decidió usar los puntos de corte propuestos por el MA de Singh (2017)20 y la guía ESC/EACTS 201712 para clasificar a los pacientes con estenosis aórtica severa en bajo riesgo (<4%), riesgo intermedio (4-8%) y alto riesgo (>8%); tanto con el STS como con el EuroSCORE II21,22. Finalmente, se decidió adoptar la recomendación del consenso de expertos de la ACC23 de incluir otros criterios como fragilidad, comorbilidades e impedimentos para el procedimiento específico.
Pregunta 3. En pacientes con estenosis aórtica severa asintomática, ¿se debería realizar el reemplazo valvular aórtico temprano o esperar que el paciente desarrolle síntomas?
Recomendaciones y puntos de buena práctica clínica
—En pacientes con estenosis aórtica severa asintomática, sugerimos no realizar reemplazo valvular aórtico temprano de forma sistemática. Recomendación débil en contra, muy baja calidad de evidencia ⊕⊕⊝⊝⊝.
-
—Los pacientes con estenosis aórtica severa asintomática serán programados para reemplazo valvular temprano si tienen alguna de las siguientes condiciones:
Pacientes con fracción de eyección del ventrículo izquierdo (FEVI) <50%.
Calcificación severa en válvula aórtica (≥3,000 unidades aganston [AU] en hombres o ≥1,600 AU en mujeres).
Un rápido incremento en la velocidad valvular transaórtica (>0.3 m/s de incremento por año).
Estenosis aórtica muy severa (velocidad transaórtica ≥5.5 m/s o gradiente de presión media ≥60 mmHg).
Cambios hemodinámicos adversos (síntomas o disminución de la presión arterial) durante la prueba de esfuerzo.
Hipertensión pulmonar severa sin otra explicación. BPC.
—Los pacientes con estenosis aórtica severa asintomática deberán ser evaluados clínicamente cada seis meses o cuando el paciente presente síntomas relacionados a la enfermedad (disnea, angina o síncope). BPC.
—Los pacientes con estenosis aórtica severa asintomática que empiecen a desarrollar síntomas serán evaluados para estratificación de riesgo y programación de reemplazo valvular aórtico. BPC.
De la evidencia a la decisión
Se define como paciente con estenosis aórtica severa asintomática a aquel paciente que no reporta síntomas24. Aproximadamente más de la mitad de los pacientes con estenosis aórtica severa son asintomáticos al momento del diagnóstico6. El tratamiento de estos pacientes es controvertido.
Una RS25 (4 estudios observacionales, n = 1,300) comparó el reemplazo valvular aórtico temprano frente al tratamiento conservador y reportó similar mortalidad de cualquier causa o de causa cardiovascular. Esto indicaría que probablemente el beneficio a corto plazo de realizar intervenciones tempranas en este grupo de pacientes es pequeño. Sin embargo, la falta de ensayos clínicos aleatorizados (ECA)26 impide establecer claramente el potencial beneficio de una intervención temprana.
Un potencial beneficio de la intervención temprana podría ser el retraso en el inicio de los síntomas y la posibilidad de un tratamiento definitivo en los pacientes que no pueden regresar a consulta. En nuestra institución, la disponibilidad de turnos operatorios para el reemplazo valvular aórtico es limitada, por lo que esta intervención se debe realizar en pacientes con estenosis aórtica severa sintomática, ya que tienen un riesgo más alto de muerte que los asintomáticos. Por ello se decidió formular una recomendación en contra de realizar el reemplazo valvular aórtico temprano de forma sistemática. Debido a que la calidad de la evidencia es muy baja, la poca aceptabilidad por parte de los pacientes debido a que son asintomáticos, que pocos médicos aceptarían realizar el procedimiento de manera precoz y la poca factibilidad se decidió dar una fuerza de recomendación débil.
Planteamiento de buena práctica clínica
Con base en las recomendaciones de dos GPC11,12, algunos subgrupos de pacientes asintomáticos pueden ser considerados para reemplazo valvular aórtico temprano, debido al mayor riesgo de mortalidad. Además, se consideró por consenso que los pacientes con estenosis aórtica severa asintomática deberían ser evaluados cada seis meses o cuando el paciente presente síntomas relacionados a la enfermedad. Asimismo, se consideró que cuando estos pacientes desarrollen síntomas deberán ser sometidos a una intervención de reemplazo valvular.
Pregunta 4. En pacientes con estenosis aórtica severa sintomática, ¿se debería realizar el reemplazo valvular aórtico quirúrgico o el reemplazo valvular aórtico percutáneo?
Recomendaciones y puntos de buena práctica clínica
En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año se debe realizar el reemplazo valvular aórtico. BPC.
En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y riesgo quirúrgico bajo, sugerimos la realización de SAVR como primera opción de tratamiento. Recomendación debil a favor, muy baja calidad de evidencia ⊕⊕⊝⊝⊝.
En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y riesgo quirúrgico intermedio, sugerimos la realización de SAVR como primera opción de tratamiento. Recomendación debil a favor, muy baja calidad de evidencia ⊕⊝⊝⊝.
En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y riesgo quirúrgico alto, sugerimos la realización de SAVR o TAVR. Recomendación debil a favor, muy baja calidad de evidencia ⊕⊕⊝⊝⊝.
En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año que sean catalogados como inoperables, sugerimos la realización de TAVR como primera opción de tratamiento. Recomendación fuerte a favor, moderada calidad de evidencia ⊕⊕⊕⊝.
En los pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y riesgo quirúrgico bajo, considerar como tratamiento de primera elección la SAVR, sin necesidad de una evaluación previa por el Heart Team. BPC.
En pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año y que tengan riesgo quirúrgico intermedio (que además tengan criterios de fragilidad, edad muy avanzada, índice de masa corporal inadecuado o una comorbilidad severa), riesgo quirúrgico alto o que sean considerados inoperables: realizar una evaluación por el Heart Team para decidir su tratamiento. BPC.
En pacientes con estenosis aórtica severa sintomática, en situaciones de emergencia, descompensación aguda o en una cirugía no cardíaca y que tengan indicación de reemplazo valvular: considerar realizar valvulotomía percutánea como terapia puente para SAVR o TAVR. BPC.
En pacientes con estenosis aórtica severa sintomática que tengan una expectativa de vida menor a un año, contraindicar SAVR y TAVR y realizar tratamiento paliativo. BPC.
En pacientes con estenosis aórtica severa sintomática que sean sometidos a TAVR, seguir los procedimientos establecidos en las guías de procedimientos o protocolos locales. BPC.
Las discordancias en la estratificación de riesgo o el tratamiento serán decididas por el Heart Team. BPC.
De la evidencia a la decisión
Esta pregunta aborda el manejo de pacientes con estenosis aórtica severa sintomática. En estos pacientes se debe realizar el SAVR o el TAVR.
Para esta pregunta se evaluaron las siguientes subpoblaciones: pacientes con riesgo quirúrgico bajo, intermedio, alto y pacientes inoperables. Un paciente es definido como riesgo quirúrgico bajo, intermedio y alto cuando obtiene valores <4, 4-8 y >8%, respectivamente, en cualquiera de los índices propuestos (EuroSCORE II o STS)12,20,27. Un paciente inoperable es definido como aquel que tiene riesgo preoperatorio de mortalidad y morbilidad >50% al año, con compromiso de ≥3 órganos/sistemas mayores que no mejorarán postoperatoriamente, fragilidad severa o un impedimento severo para el procedimiento específico28.
En pacientes con bajo riesgo quirúrgico, una RS29 (2 ECA y 4 estudios observacionales, n = 3,484) encontró que el TAVR, en comparación al SAVR, presenta similar mortalidad por cualquier causa a los 30 días y al año, mayor mortalidad tardía, menor riesgo de lesión renal aguda, similar riesgo de accidente cerebrovascular (ACV), mayor riesgo de complicaciones vasculares mayores y necesidad de implante de marcapasos permanente. Con base en estos resultados heterogéneos y debido a que se consideró que el TAVR requiere mayor uso de recursos, se decidió formular una recomendación a favor del SAVR. Debido a que la calidad de la evidencia es baja, así como la no totalidad de aceptación por parte de los pacientes y médicos, esta recomendación tuvo una fuerza débil.
En pacientes con riesgo quirúrgico intermedio, las RS de Singh20 (3 ECA y 5 estudios observacionales, n = 4,752) y Sardar27 (2 ECA y 5 estudios observacionales, n = 4,601) encontraron que el TAVR, en comparación con el SAVR, presenta similar mortalidad por cualquier causa a los 30 días y al año, similar riesgo de ACV, similar riesgo de infarto de miocardio, menor riesgo de lesión renal aguda, menor riesgo de sangrado mayor y mayor necesidad de implante de marcapasos permanente. Con base en estos resultados heterogéneos y además el hecho de que el balance de beneficios y riesgos de la intervención no favoreció el uso del TAVR, a pesar de que esta intervención requiere mayor uso de recursos se decidió formular una recomendación a favor del SAVR. Como la calidad de la evidencia es baja, no sería del todo aceptado por médicos y pacientes, y la factibilidad, se decidió dar una fuerza de recomendación débil.
En pacientes con alto riesgo quirúrgico, el ECA PARTNER 1 (n = 699), con resultados publicados al año30, tres años31 y cinco años de seguimiento32; se encontró que el TAVR, en comparación con el SAVR, presenta similar mortalidad por cualquier causa a los 30 días, al año, tres y cinco años, mayor riesgo de ACV, similar riesgo de ataque isquémico transitorio, menor riesgo de insuficiencia renal aguda, similar riesgo de infarto agudo de miocardio, mayor riesgo de complicación vascular mayor y menor riesgo de sangrado mayor. Debido a que la calidad de la evidencia fue baja, y debido a que los médicos y pacientes preferirían TAVR, pero por la poca factibilidad y excesivo uso de recursos se decidió formular una fuerza de recomendación débil para usar alguna de las intervenciones (SAVR o TAVR). En pacientes inoperables pero con expectativa de vida de más de un año también se cuentan con resultados del ECA PARTNER 1 (n = 358), publicados al año28, dos33, tres34 y cinco años de seguimiento24; se encontró que el TAVR presenta menor mortalidad por cualquier causa que el tratamiento médico. Por ello, se decidió formular una recomendación a favor del TAVR. Debido a que la calidad de la evidencia fue moderada y que sería aceptado tanto por médicos como por los pacientes, esta recomendación tuvo una fuerza de recomendación fuerte.
Planteamiento de buena práctica clínica
—Se consideró que en pacientes con estenosis aórtica severa sintomática con expectativa de vida de más de un año se debe buscar realizar el reemplazo valvular aórtico para aliviar los síntomas y disminuir la mortalidad. Asimismo, se consideró que en los pacientes con una expectativa de vida menor a un año no estaría justificada la realización de SAVR o TAVR11,24,34.
—Se estableció por consenso que un equipo multidisciplinario, o Heart Team, debería decidir el tratamiento de todos los pacientes con estenosis aórtica severa sintomática que sean considerados inoperables o de alto riesgo quirúrgico; así como aquellos con riesgo quirúrgico intermedio que además sean frágiles o tengan edad avanzada, índice de masa corporal inadecuada o una comorbilidad severa15.
—Se consideró la realización de valvuloplastia aórtica como tratamiento temporal de algunos pacientes que tengan indicación de reemplazo valvular y que se encuentren en situaciones de emergencia. Se debe tener en cuenta que este tratamiento es efectivo durante 6 o 12 meses, ya que luego la válvula aórtica vuelve a presentar estenosis11,35,36.
—Finalmente, se consideró importante señalar que el TAVR debe ser realizado siguiendo las guías de procedimientos o protocolos locales y que las discordancias en la estratificación de riesgo o tratamiento deberían ser evaluadas por el Heart Team.
Pregunta 5. En pacientes con estenosis aórtica severa en los que se decida realizar reemplazo valvular aórtico percutáneo, ¿cuál debería ser la vía de abordaje de primera elección para este?
Recomendaciones y puntos de buena práctica clínica
—En pacientes con estenosis aórtica severa en los que se decida realizar TAVR, recomendamos que el abordaje de primera elección sea el transfemoral. Recomendación débil a favor, muy baja calidad de la evidencia ⊕⊝⊝⊝.
—Cuando la vía transfemoral no sea posible, el Heart Team evaluará cada caso particular para definir el posible uso de otros abordajes como a través de la subclavia, el transapical o el transaórtico. El Heart Team tomará esta decisión con base en estudios de imagen invasivos y/o no invasivos. BPC.
De la evidencia a la decisión
Una vez que se haya decidido realizar TAVR, se debe establecer la vía de abordaje para el implante de válvula aórtica transcatéter, siendo las más comunes en nuestro medio: la transfemoral (TF), a través de la subclavia (TSc) y la transapical (TA).
Para contestar esta pregunta se evaluaron dos comparaciones: TF vs. TSc y TF vs. TA. En cuanto a la comparación entre TF y TSc, una RS (6 estudios observacionales, n = 4,504) encontró que la mortalidad a los 30 días, mortalidad al año, complicaciones mayores a los 30 días y la lesión renal aguda fueron similares entre ambos grupos37. Sin embargo, se decidió favorecer el abordaje TF por ser más sencillo y aceptado por los profesionales.
En cuanto a la comparación entre TF y TA, las RS consideradas encontraron que la mortalidad a los 30 días38 y la lesión renal aguda39 fueron menores en el grupo de TF, en tanto que las complicaciones vasculares fueron mayores en el grupo de TF40; y la mortalidad al año40, el implante de marcapasos definitivo y la hemorragia a los 30 días fueron similares en ambos grupos41. Se consideró que la mortalidad a los 30 días y la lesión renal aguda son los desenlaces clínicamente más relevantes, por lo que se decidió favorecer el abordaje TF.
Por lo tanto, debido a los beneficios, y sobre todo al menor riesgo de complicaciones, se decidió formular una recomendación a favor del uso de la vía TF. Debido a que la calidad de la evidencia es muy baja, la vía de acceso para TAVR puede depender de factores anatómicos, de ciertas comorbilidades, y de la no totalidad de aceptabilidad por parte de médicos y pacientes del uso siempre de esta vía de acceso, se decidió formular una fuerza de recomendación débil.
Pregunta 6. En pacientes con estenosis aórtica severa en los que se decida realizar reemplazo valvular aórtico percutáneo y quienes, además, presenten enfermedad arterial coronaria severa, ¿se debe realizar intervención coronaria percutánea?
Recomendaciones y puntos de buena práctica clínica
—En pacientes con estenosis aórtica severa en los que se decida realizar TAVR, que además presentan enfermedad arterial coronaria severa, sugerimos realizar intervención coronaria percutánea (PCI). Recomendación débil a favor, muy baja calidad de la evidencia ⊕⊝⊝⊝.
—En pacientes con estenosis aórtica severa en los que se decida realizar TAVR, que además presentan enfermedad arterial coronaria severa para la cual se haya decidido realizar PCI, sugerimos que el PCI sea realizado antes del TAVR. Recomendación débil a favor, muy baja calidad de la evidencia ⊕⊝⊝⊝.
—Realizar revascularización miocárdica (PCI para aquellos sometidos a TAVR o cirugía de revascularización coronaria para aquellos sometidos a SAVR) cuando se encuentre enfermedad arterial coronaria severa (reducción ≥70% en el diámetro de alguna arteria coronaria mayor o reducción ≥50% en el diámetro del tronco de la coronaria izquierda). BPC.
De la evidencia a la decisión
Aproximadamente la mitad de los pacientes con estenosis aórtica severa presentan enfermedad coronaria crónica6. En los pacientes que serán sometidos a TAVR y que además tengan enfermedad coronaria severa, se debe decidir si se realizará una PCI y, de hacerlo, si se realizará previamente o en el mismo momento (concomitante) que el TAVR.
Con respecto a la decisión de realizar o no PCI, una RS (7 estudios observacionales, n = 1,631) comparó pacientes sometidos a TAVR con PCI y sometidos a TAVR sin PCI, y encontró que la mortalidad a los 30 días, a los 6 meses y al año, la mortalidad cardiovascular, así como las complicaciones vasculares del sitio de acceso, fueron similares42. Esta evidencia sugiere la PCI de la enfermedad coronaria severa podría realizarse sin mayores riesgos en estos pacientes. Por ello, se decidió formular una recomendación a favor de la realización de la PCI.
Con respecto a la decisión de si realizar la PCI previamente o concomitante al TAVR, una RS (7 estudios observacionales, n = 1,631) que comparó pacientes sometidos a PCI antes y concomitante al TAVR encontró que la falla renal fue mayor en el grupo concomitante, en tanto que la mortalidad a los 30 días y las complicaciones vasculares en el sitio de acceso fueron similares entre los grupos42. En ese mismo sentido, un estudio observacional (n = 65) encontró que la mortalidad fue similar entre estos grupos43. Debido al menor riesgo de falla renal y a la complejidad de realizar la PCI concomitante a TAVR en nuestro contexto, se decidió formular una recomendación a favor de la realización de PCI antes del TAVR.
Debido a que la calidad de la evidencia es muy baja, la regular aceptabilidad por parte de los médicos y pacientes, y la poca factibilidad de realizar este procedimiento se decidió dar una fuerza de recomendación débil.
Planteamiento de buena práctica clínica
Se consideró pertinente adoptar el punto de BPC de la guía AHA/ACC 201444, sobre la necesidad de realizar revascularización miocárdica (PCI para aquellos sometidos a TAVR o cirugía de revascularización coronaria para aquellos sometidos a SAVR) en aquellos pacientes con enfermedad arterial coronaria severa (definida como reducción ≥70% en el diámetro de alguna arteria coronaria mayor o reducción ≥50% en el diámetro del tronco de la coronaria izquierda).
Pregunta 7. ¿Debería conformarse un Heart Team que decida el tratamiento del paciente con estenosis aórtica severa?
Recomendaciones y puntos de buena práctica clínica
—Los establecimientos de salud que realicen cirugía cardiovascular en pacientes con estenosis aórtica severa de riesgo quirúrgico intermedio, alto y/o riesgo prohibitivo deberían conformar un Heart Team que estará a cargo de decidir el tratamiento del paciente. BPC.
-
—El Heart Team debe estar conformado al menos por:
De la evidencia a la decisión
El Heart Team es un equipo multidisciplinario y colaborativo que tiene como objetivo la toma de decisiones sobre el tratamiento de pacientes con estenosis aórtica severa con riesgo intermedio, alto o prohibitivo45,46. En la búsqueda realizada no se encontraron estudios que hayan evaluado la eficacia del Heart Team, por lo cual no se emitieron recomendaciones, pero sí se establecieron puntos de BPC en consenso.
Planteamiento de buena práctica clínica
Se consideró que los establecimientos de salud que realicen cirugía cardíaca en pacientes con estenosis aórtica severa y que presentan alto riesgo quirúrgico requieren decidir entre la realización de SAVR y TAVR46 en el Heart Team. Para la conformación del Heart Team se consideraron las recomendaciones de otros autores15,26,46-52, así como la factibilidad según el contexto local. De esta manera, se estableció por consenso que el Heart Team debería estar conformado al menos por: un cardiólogo clínico con experiencia en patología valvular, un cardiólogo experto en imagen cardiovascular, un cardiólogo intervencionista certificado en TAVR y un cirujano cardiovascular con experiencia en patología valvular.
Contribuciones de autoría
Todos los autores participaron en la realización de la guía. JHM, ATR, CAAR y JEFC se encargaron de las búsquedas sistemáticas y la evaluación de calidad de los estudios para cada pregunta. Todos los autores participaron en la discusión de los estudios encontrados y la formulación de las recomendaciones y puntos de BPC. Todos los autores revisaron y aprobaron la versión final del artículo.
Responsabilidades éticas
Protección de personas y animales
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Supplementary Data
Supplementary data are available at Revista Archivos de Cardiología de México online (http://www.desarrollo-archivoscardio.ml/index.php). These data are provided by the corresponding author and published online for the benefit of the reader. The contents of supplementary data are the sole responsibility of the authors.











 text in
text in 


