Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Archivos de cardiología de México
On-line version ISSN 1665-1731Print version ISSN 1405-9940
Arch. Cardiol. Méx. vol.80 n.2 Ciudad de México Apr./Jun. 2010
Artículo de revisión
Acerca de la denominación actual de infartos miocárdicos
On the actual nomenclature of myocardial infarcts
Gustavo A. Medrano,1 Alberto Aranda,2 Gabriela Meléndez,3 Alfredo de Micheli.4
1 Ex jefe del Departamento de Electrovectocardiografía.
2 Departamento de Anatomía Patológica.
3 Departamento de Resonancia Magnética.
4 Investigador del INCICh. Coautor correspondiente.
Instituto Nacional de Cardiología Ignacio Chávez, México.
Correspondencia:
Dr. Alfredo De Micheli,
Juan Badiano N° 1, Col. Sección XVI,
Delegación Tlalpan, C.P.14080. México D.F.
Teléfono: 5573 2911, Ext. 1297.
Correo electrónico: alessandro.micheli@cardiologia.org.mx
Recibido el 13 de octubre de 2009.
Aceptado 18 de abril de 2010.
Resumen
Se examinan algunos criterios acerca de los infartos definidos en la literatura actual como inferiores e inferolaterales. Con este fin, se describen los aspectos anatómicos del corazón aislado e in situ. Se analizan también las relaciones de este último con otros órganos torácicos circunvecinos. Se representa, de manera esquemática, el corazón como una pirámide con base triangular y sus lados y bordes en relación con las paredes de la caja torácica. Se resume, además, la orientación espacial de los principales vectores resultantes de los procesos de despolarización y repolarización ventriculares. Se subraya la utilidad del registro de las derivaciones unipolares torácicas posteriores V7, V8, V9 y del círculo torácico electrocardiográfico. Esto permite detectar la existencia de un infarto miocárdico agudo en regiones medias y básales de la pared inferolateral del corazón y su verdadera extensión. Con base en cotejos electroanatómicos previos, se concluye que las derivaciones V7 – V9 exploran los segmentos inferior e inferolateral en su tercio basal y medio, anteriormente denominados regiones cardiacas posterolaterales. Los registros electrocardiográficos proporcionan datos esencialmente funcionales y las imágenes obtenidas por resonancia magnética dan una información sobre todo estructural. Por lo tanto, ambos procedimientos de exploración cardiaca no deben contraponerse, sino integrarse.
Palabras clave: Corazón aislado; Corazón in situ; Infartos miocárdicos; México.
Abstract
Certain criteria are examined for infarctions currents defined as inferior or inferolateral. To do this, certain considerations on the anatomical aspects of isolated and in situ heart are laid out. The topographical relationship of the in situ heart with other adjacent thoracic organs is described. The heart is schematically represented as a pyramid with a triangular base and its walls and borders are related to walls of the thorax. The spatial orientation of the main resulting vectors from ventricular depolarization and repolarization are summarized also. Usefulness of registering the unipolar thoracic leads V7, V8, V9 or a complete electrocardiographic thoracic circle, is underlined. This method allows to detect for of the existence of an acute myocardial infarction in the inferior and inferolateral segments in as third basal and mid cardiac regions previously denominated posterolateral. On the base of previous electro–anatomical comparisons, it is concluded that the thoracic posterior leads V7 – V9, as well as the magnetic resonance images, explore the same heart regions. Therefore, these two methods: electrocardiography which is an essentially functional method and magnetic resonance that especially focus on structural changes are not contradictory but rather complementary tests.
Key words: Isolated heart; In situ heart; Myocardial infarcts; Mexico.
Introducción
Hace tiempo se han propuesto cambios de la nomenclatura de los infartos miocárdicos posteriores y posterolaterals. Se ha afirmado asimismo la imposibilidad de reconocer infartos posteriores y posterolaterales basales. Pero cabe mencionar que, de acuerdo a la "Nómina Anatómica Internacional", se considera como base del corazón a la que es posterior, se dirige hacia atrás y se relaciona con el esófago y la columna vertebral, situándose en el mediastino posterior. Por su parte, debe subrayarse la importancia del proceso de activación miocárdica.
Datos anatómicos
Las discrepancias anatómicas surgen del considerar al corazón como órgano aislado en comparación con el corazón in situ. En el primer caso se configura una cara posterior, que corresponde a la inferior o diafragmática del corazón in situ.
La identificación de la cara posterior del corazón se establece en la mayoría de los textos clásicos de anatomía humana, como el Testut–Latarget1 y el "Atlas de ilustraciones" de Netter,2 entre otros. Debido a su estrecha relación con esta cara, otras estructuras toman el adjetivo "posterior". Así tenemos a la arteria coronaria descendente posterior que debiera ser llamada interventricular inferior, y al músculo papilar posteromedial del ventrículo izquierdo, que debiera denominarse inferoseptal. Ciertos autores,3 proponen estos cambios de la nomenclatura a comenzar por la enseñanza de la anatomía. Pero tales cambios, que podrían introducirse en forma lenta, ocasionan la discrepancia entre la terminología anatómica clásica y la utilizada en la actualidad. Por eso parecería más adecuado integrar el conocimiento de que la cara inferior o diafragmática del corazón constituye en realidad la llamada posterior. Otro elemento de confusión estriba en que, en el corazón in situ, la porción más posterior o dorsal del órgano corresponde a la base, pero no debe confundirse la base con la cara posterior del corazón, lo que sería un grave error conceptual. La importancia de entender la cara inferior o diafragmática como posterior estriba en que esta terminología ha sido utilizada en forma rutinaria.3
El corazón in situ tiene su eje anatómico a 40°–45° sobre la línea horizontal, que corresponde al diafragma; por lo tanto, no toda la pared cardiaca posterior se apoya en el diafragma así que, desde un punto de vista semántico estricto, tampoco el nombre de pared diafragmática sería correcto. Tenemos, por tanto, una pared inferoapical y otra inferobasal: la primera está en relación directa con el diafragma sobre el cual se apoya y la segunda asciende en sentido dorsal (o craneodorsal), alejándose del diafragma. La pared inferior comprende ambos ventrículos, pero mayoritariamente el izquierdo por la levorrotación cardiaca, y termina en el surco auriculoventricular. De hecho, ambas aurículas forman parte de la base, aunque en el corazón aislado también parte de las aurículas está incluida en la cara posterior. Consideramos que no deben soslayarse los conceptos anatómicos que durante tantos años han demostrado su utilidad y nos han permitido entender cuando hablamos de infartos posteroapicales y posterobasales en el corazón aislado y debemos integrarlos correctamente como inferoapicales e inferobasales en el corazón in situ.
Agregamos ahora algunas consideraciones anatómicas sobre el corazón in situ, que son importantes para el entendimiento de la activación miocárdica y la visualización eléctrica del corazón. Debe tenerse presente que el corazón tiene forma piramidal, con la punta roma localizada abajo y a la izquierda, en íntima relación topográfica con la parrilla costal, a nivel de la línea medioclavicular y del quinto espacio intercostal izquierdo (EII), en los corazones horizontales, y del sexto en los verticales. Su eje mayor se dirige oblicuamente en sentido craneal, dorsal y a la derecha, mientras que su base, ancha, se sitúa dorsalmente y se relaciona con el esófago y la columna vertebral, situándose entre la sexta y la novena vértebras dorsales. La aurícula izquierda forma parte de la base y se sitúa dorsalmente.
La mayor masa cardiaca se localiza en el mediastino medio, en íntima relación con el diafragma al que se fija, permitiéndole una movilidad apreciable gracias al ligamento pericardiofrénico, acorde con los cambios de posición y rotación de dicho órgano. Los hilios pulmonares (venosos y bronquiales) y las venas cavas, en conjunto con el cayado y la porción descendente de la aorta, así como el tronco y las ramas de la arteria pulmonar, lo fijan más estrechamente a los hilios pulmonares y a la pleura mediastinal. Por eso, el ventrículo izquierdo, sea en posición ortostática, sea en posición sentada, sea en decúbito dorsal, tiene una porción alejada del diafragma y situada en el espacio inferolateral izquierdo. Estos datos se confirman por los estudios radiológicos clásicos (telerradiografía en inspiración y espiración), así como por los estudios angiocardiográficos en decúbito dorsal y lateral. No debe olvidarse un hecho importante: la telerradiografía de tórax se toma en inspiración forzada y en una fracción de segundo, por lo que se abate el diafragma alrededor de un espacio intercostal (2.5 a 3.5 cm) y la silueta cardiaca es obtenida en sístole o diástole. Con otros métodos de exploración, se necesitan tiempos de exposición más prolongados para su integración y resolución. También los procedimientos más útiles y más empleados, como la ecocardiografía, necesitan de varios cortes para integrar los diagnósticos requeridos. Se sabe que las relaciones de las caras del corazón cambian discretamente respecto a las paredes de la caja torácica, pero sus nombres (anterior, inferior e izquierda) no varían. La masa cardiaca mayor, i.e. el ventrículo izquierdo, cuando existe levocardia, se halla más cerca de la parrilla costal anterior y lateral media del tórax.
Adoptamos la definición del corazón como una pirámide triangular (Figura 1) con base dorsocraneal y vértice caudoventral. La cara anterior se denomina esternocostal por su estrecha relación con el esternón. La cara lateral corresponde al borde libre, obtuso, del ventrículo izquierdo y al borde lateral de la aurícula izquierda. La porción apical de la cara inferior se apoya sobre el diafragma. La cara diafragmática está constituida por las porciones posteroapicales de ambos ventrículos, aunque en mayor proporción por la del ventrículo izquierdo debido a la levorrotación cardiaca. La base se halla en relación con las vértebras torácicas seis a nueve y por eso se denomina también cara dorsal.

La Figura 2 muestra un corte transversal de un corazón aislado, a nivel de la porción media de los ventrículos, identificada por la presencia de los músculos papilares. Hay una zona blanquecina, que corresponde a un infarto antiguo. Ahora bien ¿en dónde se localiza? Desde el punto de vista anatómico, reconocemos su cara posterior aplanada, mientras que su cara anterior es convexa. Por lo tanto, puede clasificarse el infarto como posterior medio biventricular. Pero, si utilizamos la terminología imaginológica, debemos definirlo como un infarto inferior e inferoseptal con extensión al ventrículo derecho.

Acerca de la segmentación del miocardio
Por lo que toca a la segmentación del miocardio ventricular, podemos decir que ésta es una metodología propuesta hace muchos años y utilizada para la localización de una zona infartada y su probable correlación con la coronaria responsable. Cada segmento ventricular es irrigado por una rama arterial llamada coronaria segmentaria. Dado que los infartos son más frecuentes en el ventrículo izquierdo, la segmentación mencionada importa sobre todo en esta cámara cardiaca.4
Las modernas técnicas de imaginología permiten el análisis preciso de los segmentos miocárdicos ventriculares. Se han desarrollado varios métodos de segmentación, algunos de ellos ya estandarizados. Puesto que tales métodos se aplican en el corazón in situ, han impulsado una nueva terminología. Así que la cara, clásicamente considerada como posterior, se define ahora como inferior. De hecho, se traza un eje largo vertical (dos cámaras), que corresponde a las porciones anterior e inferior del corazón, un eje largo horizontal (cuatro cámaras), en el que se evalúa el septo, la pared lateral y el ápex del ventrículo izquierdo, y que delimita las porciones derecha, izquierda y ápex.
Las sociedades norteamericanas de ecocardiografía, cardiología nuclear, imaginología, angiocardiografía y resonancia magnética han expresado la recomendación de dividir el ventrículo izquierdo en 17 segmentos (aunque existe una segmentación previa en 12 segmentos, en la que se empleaba todavía el término posterolateral).5,6 La valoración de los diferentes segmentos se realiza en el eje corto a tres niveles del ventrículo izquierdo: basal, medio y apical.7 Los niveles basal y medio comprenden seis segmentos cada uno: 1. Basal anterior, 2. Basal anteroseptal, 3. Basal inferoseptal, 4. Basal inferior, 5. Basal inferolateral, 6. Basal anterolateral, 7. Medio anterior, 8. Medio anteroseptal, 9. Medio inferoseptal, 10. Medio inferior, 11. Medio inferolateral, 12. Medio anterolateral. En el nivel apical, hay cuatro segmentos: 13. Anterior, 14. Septal, 15. Inferior, 16. Lateral. El segmento 17 corresponde al ápex, que constituye la punta del corazón en donde no existe cavidad.
Desde el punto de vista semántico y de acuerdo con esta terminología originada por el estudio imaginológico del corazón in situ, ya no se evidencian segmentos posteriores, por lo que no se menciona la cara posterior. Pero ésta puede reconocerse en el examen anatómico del corazón aislado.8,9 Tal vez sería oportuno integrar ambos procedimientos de exploración cardiaca: la del corazón in situ y la del corazón aislado o señalar qué tipo de exploración se está realizando: si la del corazón aislado, se trata de la cara posterior; si la del corazón in situ, se trata de la cara inferior.
Como ya se ha mencionado, una de las aplicaciones más importantes de la segmentación cardiaca es la asignación de territorios coronarios y, pese a la gran variabilidad de la distribución de dichas arterias, se considera que los segmentos inferiores e inferoseptales: tercio basal y medio, i. e. segmentos 3, 4, 9 y 10, se sitúan en el territorio de la coronaria derecha. Por otro lado, los segmentos laterales basales o inferolateral tercio medio (segmentos 5, 6, 11) pertenecen al territorio de la arteria circunfleja. El territorio de la coronaria descendente anterior izquierda comprende los segmentos anterior y anteroseptal tercio basal y medio, tercio medio de la pared anteroseptal, así como la punta del corazón (segmentos 1, 2, 7, 8, 12, 13, 14, 15, 16 y 17).10
En resumen, con respecto a la segmentación del miocardio ventricular, las regiones posteriores medio–inferiores del corazón aislado corresponden a los segmentos 3, 4 ,9 y 10 del corazón in situ, que son dependientes de la coronaria derecha. A su vez, las regiones posterobasales del corazón aislado, están comprendidas en el territorio de la arteria coronaria derecha.
Según publicación reciente,10 la relación de la arteria segmentaria es bastante constante respecto a segmentos del territorio de la coronaria descendente anterior, mientras que resulta muy variable en los territorios de la coronaria derecha y de la arteria circunfleja. Sin embargo, debe mencionarse que, para los cotejos electroanatómicos, los autores han utilizado el electrocardiograma convencional de doce derivaciones, no el círculo torácico completo ni el parcial (ECG de 15 derivaciones).
Datos electrofisiológicos: El centro eléctrico del corazón se halla en la parte anteroinferior de la cavidad auricular izquierda, a nivel del cuarto espacio intercostal izquierdo y la línea paraesternal homolateral. Dicho centro es prácticamente el mismo para las aurículas y los ventrículos, aunque en los vectocardiogramas amplificados se observa una pequeña enucleación del punto de inicio de la curva ventricular (asa Q). Esto se debe a que el asa auricular (P) se inicia en la línea isoceléctrica (espacio T–P) y la curva ventricular (QRS) comienza en la fase de repolarización auricular (espacio Ta). El eje que pasa por el centro eléctrico del corazón se sitúa en la intersección del plano frontal, que corta el tórax a nivel del cuarto cartílago costoesternal o en el cuarto espacio intercostal izquierdo a nivel de la sexta vértebra dorsal. Se forman así cuatro cuadrantes: anterosuperior, anteroinferior, posteroinferior y posterosuperior. Para localizar el centro eléctrico cardiaco, podemos basarnos en los frentes de activación que se dirigen hacia delante, arriba, abajo, etc. El plano sagital, que corta el tórax en sentido vertical y anteroposterior a nivel de V2 o, mejor dicho, sobre la línea paraesternal izquierda, hace aumentar el número de segmentos analizables y permite localizar de manera más precisa los frentes de despolarización. Estos últimos se suceden en el tiempo y en el espacio y pueden estar aislados (raramente) o acompañados por otros que se suman, manifestándose así como promedios. Deben relacionarse, por tanto, con el proceso de activación miocárdica. Cuando esta última es normal, predominan generalmente los frentes septales –el inicial y el originado en la masa septal derecha–, los de la pared libre ventricular izquierda y los que se originan en la regiones basales posteriores de ambos ventrículos.
Infartos inferiores e inferolaterales
Infartos laterales: En presencia de infartos localizados en porciones laterales del ventrículo izquierdo si la zona afectada, aun siendo transmural, no se extiende hacia el tercio inferior de la pared libre ventricular, no da generalmente complejos QS en aVL ni en V5 y V6. En 9 casos de nuestra serie publicada en 1960,8 la zona de infarto se situaba en los dos tercios superiores de la pared libre ventricular izquierda. Pero solamente en uno había ondas Q patológicas en aVL; en los demás, el infarto se localizaba en regiones paraseptales izquierdas altas o medias con invasión septal discreta o sin ella.9
En el diagnóstico topográfico de infarto,10 un factor de error se debe a la ausencia de ondas Q anormales, i. e. anchas, empastadas y no interpolables, en el momento en que se registró el electrocardiograma. De hecho, las ondas Q patológicas aparecen durante la evolución favorable del síndrome, paralelamente a disminución apreciable del desnivel del segmento RS–T y a la acentuación de la negatividad de la onda T.11 Esta buena evolución del síndrome de infarto se presenta habitualmente en el curso de una reperfusión miocárdica exitosa por procedimientos farmacológicos (fibrinolisis) o intervencionistas (angioplastia coronaria) o quirúrgicos (puentes coronarios).
B. Infartos del tercio basal y medio de la pared inferior (ya posteroinferiores): En la década de 1950, se comenzó a denominar infartos dorsales12 aquellos localizados en regiones posteriores medias y basales. Tal denominación se originó por la relación anátomo–topográfica de las zonas miocárdicas afectadas con la sección dorsal de la columna vertebral, i.e. con la sexta vértebra dorsal. Esta relación resulta bien definida por la angiocardiografía en posición de decúbito dorsal o lateral.13 Dado que, en los enfermos en estudio, el electrodo de la pierna izquierda con frecuencia se orienta sólo hacia la mitad o el tercio inferior del ventrículo izquierdo, el ángulo sólido correspondiente, o sea la región que descansa sobre la cúpula diafragmática, se desplaza hacia la línea medioclavicular izquierda. Dicha situación hace que la línea de la derivación aVF se incline hacia la aurícula izquierda y sea tangencial a la región considerada y aun al surco auriculoventricular posterior y porciones circunvecinas de la masa ventricular izquierda. Por eso no se registran signos directos de miocardio inactivable o sea necrosis. Sin embargo, los fenómenos eléctricos, registrados en derivaciones anatómicamente y eléctricamente opuestas, predominan sobre aquellos originados en regiones laterales del ventrículo izquierdo y en la masa septal derecha. Esto da lugar a un aumento de voltaje de las ondas R en las derivaciones derechas y las anteriores izquierdas, específicamente V2 – V4 y en menor proporción V1, así como a una depresión del segmento ST y del punto J en V2 y V3.14 No sólo está afectado el voltaje de la onda R, sino que su vértice se inscribe tardíamente entre 35 y 50 mseg o más, si coexiste una hipertrofia ventricular izquierda, frecuente en los sujetos con hipertensión arterial sistémica.15 A veces, dichos signos pueden coincidir con los originados en la masa septal derecha anterosuperior (corazones horizontales con dextrorrotación moderada). Pero el hecho de que los tiempos de activación se incrementen hacia la izquierda inclina a considerarlos propios de la cara anterior del ventrículo izquierdo. Los registros vectocardiográficos avalan igualmente el significado de los cambios morfológicos y cronológicos señalados.
Debe tenerse presente el hecho de que, mientras el infarto posteroinferior se manifiesta en las derivaciones bajas aVF, DM y DIN, cuando la posición cardiaca es intermedia, el infarto estrictamente posterior causa aumento de voltaje de las ondas R –y prolongación del tiempo de inicio de la deflexión intrinsecoide (TIDI)– en las derivaciones precordiales izquierdas y transicionales hasta tiempos acordes a los de activación de la cara anterior media y de la anterolateral del ventrículo izquierdo: 35 – 45 mseg.16 Pueden registrarse tiempos mayores cuando coexiste hipertrofia ventricular izquierda o un bloqueo de la subdivisión anterior izquierda (BSAI). Por eso, conviene tomar un círculo torácico completo17 o al menos las derivaciones V7, V8 y V9 en el quinto o cuarto espacio intercostal izquierdo –a nivel de la séptima vértebra dorsal18– ya que las derivaciones torácicas posteriores derechas normalmente registran con frecuencia morfologías QS ó Qr. Por otra parte, la onda R aumenta de voltaje en V1, y V2 cuando la zona de infarto invade la pared anterolateral izquierda.19
Desde hace tiempo varios autores20–24 están registrando las derivaciones V7 V8 y V9, cuando existe la sospecha clínica de infartos posteriores. Estas derivaciones se registran habitualmente en el quinto espacio intercostal izquierdo: V7 sobre la línea axilar posterior, V8 a nivel de la línea escapular media y V9 sobre el borde paraespinal izquierdo. En la Unidad Coronaria de nuestro Instituto, se toma un círculo torácico completo17 en los sujetos infartados desde la década de 1980. Esto nos ha permitido efectuar varios cotejos electro–anatómicos,25–29 todos con resultado positivo por lo que toca a la localización del infarto posterior o posterolateral.
Presentamos ahora un ejemplo de infarto posterolateral izquierdo o inferolateral extenso, detectado por registros unipolares torácicos y confirmado por las imágenes de medicina nuclear y resonancia magnética.
Ejemplo:
Hombre de 56 años con Hipertensión Arterial Sistémica, diagnosticada dos años antes de su ingreso en nuestro Instituto. El 25 de enero de 2009 presentó un síndrome de infarto miocárdico agudo, por lo que fue internado aquí el día siguiente y se le realizó angiografía coronaria. Ésta demostró una enfermedad trivascular, que afectaba el tronco de la coronaria izquierda. Un ecocardiograma del mismo día mostró hipertrofia concéntrica del ventrículo izquierdo, con hipocinesia de la pared cardiaca posterior en sus tres segmentos y de la pared inferior en sus segmentos medio y basal. FEVI= 55 %. Un ECG de aquella fecha (Figura 3) proporcionó signos de lesión subepicárdica posterolateral izquierda baja y alta, que se extendía también a regiones posteriores altas del ventrículo derecho: desnivel positivo convexo del segmento RS–T en DII, DIII, aVF, V5 a V9 y, discreto, de V9R a V7R. Había, a su vez, desnivel negativo cóncavo de RS–T de V2 a V4 y en la unipolar abdominal media epicárdica (ME). La pequeña onda Q empastada, de unos 40 mseg, en DII, DIII, aVF y de V5 a V9, sugería la existencia de miocardio inactivable en el borde posterolateral izquierdo con probable extensión de la zona lesionada hacia regiones posteriores altas de la pared libre del ventrículo derecho. El tiempo de inicio de la deflexión intrinsecoide (TIDI) de 50 mseg en aVF y V6 abogaba a favor de hipertrofia ventricular izquierda. Se trataba, en resumen, de un infarto agudo posterolateral izquierdo extenso, asociado a hipertrofia ventricular homolateral. Según la nomenclatura actual, se trata de un infarto inferolateral extenso.

Una gammagrafía perfusoria miocárdica, realizada el mismo día de la toma del electrocardiograma, demostró la existencia de un infarto transmural inferolateral, i.e. posterolateral izquierdo, que se extendía del tercio basal al apical con acinesia homolateral.
El estudio por resonancia magnética, efectuado el 28 de enero de 2009 (Figura 4), dio imágenes en eje corto en los tercios basal (a), medio (b) y apical (c) del ventrículo izquierdo tras la administración de un medio de contraste (gadolinio). Las flechas señalan un infarto de las paredes inferior e inferolateral con imagen de obstrucción micro–vascular, la que se caracteriza por la presencia de una zona hipointensa (*) rodeada por una zona hiperintensa.
La coronariografía, efectuada a las 6 horas del comienzo del dolor torácico (i. e. el día previo a la realización de la resonancia magnética), mostró oclusión de la arteria circunfleja (flecha), así como una lesión significativa de la coronaria descendente anterior (cabeza de flecha) (Figura 5).
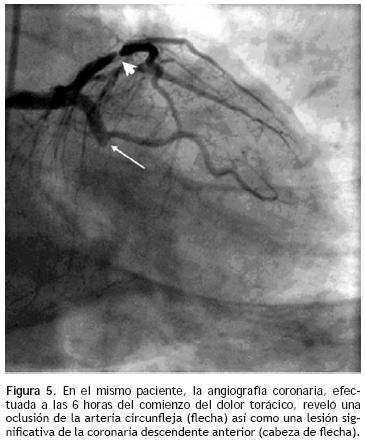
Los hallazgos descritos muestran una buena concordancia de los resultados obtenidos mediante los estudios hemodinámicos, electrocardiográficos mediante el círculo torácico y de la resonancia magnética.
Conclusiones
Los métodos actuales de exploración cardiaca: ecocardiografía, estudios de medicina nuclear, resonancia magnética y tomografía coronaria computarizada, son de gran utilidad para poder establecer diagnósticos anatómicos y funcionales muy aceptables. Pero no permiten rechazar procedimientos de exploración cardiaca más abordables y de menor costo, particularmente útiles en seguimientos prolongados. Más aún, cada uno de ellos no puede ofrecer una información completa acerca de todos los componentes del síndrome de infarto miocárdico. Por ejemplo, la exploración ecocardiográfica revela la existencia de hipo–contractilidad de las fibras miocárdicas dañadas, mas no indica la causa: isquemia o lesión o necrosis.30 Y no debe olvidarse que la isquemia generalmente es transitoria y la lesión puede evolucionar hacia la isquemia y la resolución o hacia la "necrosis" y la pérdida transitoria o definitiva de la función contráctil de las fibras miocárdicas afectadas.
La misma resonancia magnética no da información acerca de cambios en las concentraciones electrolíticas intra y extracelulares, cosas que la electrocardiografía sí puede señalar. Además, debe tenerse presente que las derivaciones unipolares torácicas posteriores V7, V8 y V9 pueden proporcionar directamente los signos de isquemia, lesión y "necrosis" de regiones miocárdicas, que corresponden a la definida como inferolateral, según la nomenclatura actual.5–7
De todos modos, la resonancia magnética indica la presencia y la extensión de edema celular, debido verosímilmente a despolarización diastólica parcial de las células miocárdicas por pérdida de potasio y acumulación de calcio, sodio y cloro intracelulares, lo que acarrea agua.31,32 Así que, en el síndrome de infarto miocárdico agudo, caracterizado por los signos electrocardiográficos de lesión y por los imaginológicos de edema, puede existir una equivalencia entra tales manifestaciones de la despolarización diastólica parcial de las células miocárdicas.
En conclusión, debe hacerse hincapié en el hecho de que tanto la electrocardiografía, con su enfoque esencialmente funcional, como la resonancia magnética, con su enfoque sobre todo estructural, logran explorar las mismas regiones cardiacas y detectar la existencia de miocardio en riesgo. Por lo tanto, estos dos procedimientos diagnósticos no deben contraponerse sino integrarse. Dicha integración puede expresarse con los versos dirigidos a su tiempo por el premio Nobel Max Planck33 al también premio Nobel, Arnold Sommerfeld:
Yo también, como tú, flores arranqué.
¿Por qué no combinar su belleza,
haciendo un intercambio de flores,
que juntas en primorosa guirnalda brillen más?
Referencias
1. Testut L, Latarget A. Angiología, En Tratado de Anatomía Humana. T. II. Libro IV. Novena Edición. Barcelona. Ed. Salvat, 1960, pp. 5–6. [ Links ]
2. Netter Frank H, Yonkman F: Anatomía del corazón. En Colección Ciba de Ilustraciones Médicas. T. V. El corazón. Nueva York. Ed. Salvat, 1969. Barcelona. 1ª Versión española, 1976; Reimpresión, 1988. [ Links ]
3. Anderson RH, Loukas H. The importance of attitudinally appropriate description of cardiac anatomy. Clin Anat 2009;22 (1);47–51. [ Links ]
4. Onciu M, Popescu S. Comprobación de un modelo de segmentación cardiaca en la mitad izqulerda del corazón. Rev Med Chir Med Iasi 2005;109 (4):841–847. [ Links ]
5. Wagner GS, Cowan MJ, Flowers NC, et al. Nomenc1ature of myocardial wall segments. Committee report. Computerized interpretation of the ECG.VIII. Proceeding Engineering Foundation Conference. (Selvester R H, Ed). Nueva York. Engineering Foundation, 1983. [ Links ]
6. Startt Selvester RH. Recommendations for nomenclature of myocardial subdivisions. J Electrocardiol 1986;19(2):III. [ Links ]
7. Cerqueira MD, Weissman NJ, Dilsizian V, et al. Standardized myo–cardial segmentation and nomenclature for tomographic imaging of the heart. Circulation 2002;105:539–542. [ Links ]
8. Contreras R, Costero I. Localización de los infartos del miocardio en cortes topográficos del corazón. En Aterosclerosis y Enfermedad coronaria. (Coord. I. Chávez). México. Ed. Interamericana S.A. 1960, pp. 69–78. [ Links ]
9. Sodi D, Anselmi G, Contreras R, et al. Proceso de activación y correlación anatómica en cortes seriados, como base de una nueva clasificación de los infartos. En Aterosclerosis y enfermedad coronaria. (Coord. I. Chávez). México. Ed. Interamericana S. A., 1960, pp. 189–209. [ Links ]
10. Ortiz PJT, Rodríguez J, Meyers SN, et al. Correspondence between the 17–segment model and coronary arterial anatomy using contrast–enhanced cardiac magnetic resonance imaging. JACC Cardiovasc Imag 2008;1(3);282–293. [ Links ]
11. Sodi D, Bisteni A, Pileggi F, et al. Acerca del tejido eléctricamente muerto. Principia Cardiol 1957;4:163–188. [ Links ]
12. Tranchesi J. Análisis vectorial do electrocardiograma nos en–fartes da pared dorsal do miocardio ventricular. Arq Bras Cardiol 1958; 11(2):77–96. [ Links ]
13. Abams LH. Angiocardiography. The normal angiocardiogram En Cardiovascular Disorders. (N A Brest, H J Moyer, Eds). Part I. Philadelphia Pa. Davis Co, 1965, pp. 298–300. [ Links ]
14. De Micheli A, Aranda A, Medrano Ga. Acerca del valor diagnóstico de los hallazgos ECG indirectos de infarto miocárdico posterolateral basal izquierdo. Arch Cardiol Mex 2007;77(2):150–155. [ Links ]
15. Sodi D, Medrano GA, Bisteni A, et al. Electrocardiography and vectorcardiography. Posterior infarction. En Cardiovascular Disorders. (N A Brest, H J Moyer, Eds). Part II. Philadelphia Pa, Davis Co, 1968, pp. 248–259. [ Links ]
16. Barbato E, Pileggi F, Debes AC, et al. Study of the sequence of ventricular activation and the QRS complex of the normal human heart using direct unipolar leads. Am Heart J 1958;55(6):867–880. [ Links ]
17. De Micheli A, Medrano GA, Iturralde P. El círculo torácico en la exploración eléctrica del corazón. Arch Inst Cardiol Mex 2000;70(2):187–196. [ Links ]
18. Madias JE, Hood W B. Diagnosis of high anterolateral and true posterior myocardial infarction by chest wall ECG mapping. J Electrocardiol 1976;9(4):375–377. [ Links ]
19. Sodi D, Bisteni A, Cisneros F, et al. Reliability of the electrocardiogram in diagnosis of myocardial infarction. En Coronary Heart Disease. (W. Likoff, H. J. Moyer, Eds). Nueva York. Grune & Stratton, 1963, pp. 278–294. [ Links ]
20. Zalenski RJ, Cooke D, Rydman R, et al. Assessing the diagnostic value of an ECG containing leads V4R, V8 and V9 the 15–lead ECG. Ann Emerg Med 1993;22;786– 793. [ Links ]
21. Zalenski RJ, Rydman R, Sloan EP, et al. Value of posterior and right ventricular leads in comparison to the standard 12–lead electrocardiogram in evaluation of ST–segment elevation, in suspected acute myocardial infarction. Am J Cardiol 1997;79:1579–1585. [ Links ]
22. Matetzky S, Freinmark D, Chouraqui P, et al. Significance of ST segment elevation in posterior chest leads (V7 to V9) in patients with acute inferior myocardial infarction, application for throm–bolytic therapy. J Am Coll Cardiol 1998;31:506– 511. [ Links ]
23. Matetsky S, Freinmark D, Feinberg MS, et al. Acute myocardial infarction with isolated ST–segment elevation revealing acute posterior infarction. J Am Coll Cardiol 1999;34:748–753. [ Links ]
24. Aqel RA, Hage FG, Ellipeddi P, et al. Usefulness of three posterior chest leads for the detection of posterior wall acute myocardial infarction Am J Cardiol 2009;103 (2):159–164. [ Links ]
25. De Micheli A, Aranda A, Medrano GA. Fibrosis miocárdica septal. Un cotejo electro–anatómico. Arch Cardiol Mex 2002;72(1):45–48. [ Links ]
26. De Micheli A, Aranda A, Medrano GA. Infartos miocárdicos con onda Q y sin onda Q. Arch Cardiol Mex 2005;75(Supl 3):S30–S37. [ Links ]
27. De Micheli A, Aranda A, Medrano GA. Infartos posterolaterales biventriculares. Un cotejo electro–anatómico. Arch Cardiol Mex 2005;75(Supl 3) :S140–S142. [ Links ]
28. De Micheli A, Aranda A, Medrano GA. Aspectos eléctricos de la asociación de miocardio inactivable y bloqueos tronculares de grado intermedio. Arch Cardiol Mex 2007;77(1):67–73. [ Links ]
29. Lomelí EC, Aranda A, Lorenzo NJA, et al. Infarto posterolateral izquierdo extenso. Cotejo electro–anatómico, Arch Cardiol Mex 2008;78(3):338–343. [ Links ]
30. De Micheli A, Medrano GA. En torno al concepto electrofisiopatológico y las manifestaciones electrocardiográficas de isquemia, lesión y necrosis. Arch Cardiol Mex 2009;79(1):2–4. [ Links ]
31. Iseri LT, Alexander LC, McCaughy RS, et al. Water and electrolyte content of cardiac and skeletal muscle in heart failure and myo–cardial infarction. Am Heart J 1952;43:215–227. [ Links ]
32. De Micheli A, Aranda A, Chávez E. Sustratos celulares del síndrome de infarto miocárdico agudo. Arch Inst Cardiol Mex 1995;65(1):79–88. [ Links ]
33. Planck M. Autobiografía científica. México. Ed. UNAM, 1987. Seminario de Problemas Científicos y Filosóficos. Supl. 10, pp. 245–247. [ Links ]














