1. Introducción
El cáncer de piel es una enfermedad que ha venido manifestándose de manera progresiva en la población mundial [1], que aparte de cobrar cientos de miles de vidas por año, ha generado un incremento alarmante en los costos por tratamiento y prevención de la misma [2, 3, 4]. De hecho, es una de las enfermedades cancerígenas más comunes y de mayor impacto en la sociedad contemporánea. Es por ello, que la medicina preventiva busca permanentemente implementar nuevas técnicas y/o tecnologías que permita realizar un diagnóstico temprano de esta enfermedad [5], donde los costos operativos sean reducidos sin sacrificar la eficiencia y calidad en el servicio, los cuales son fundamentales para un sistema de salud al que se le exige mayor atención y prontitud en el o los diagnósticos por parte sus pacientes. Con base en esta problemática y requerimientos que exigen los centros hospitalarios especializados en tratar el cáncer no melanoma y la queratosis actínica, se plantea el desarrollo de un programa informático que permita realizar un análisis en el contexto de la imagenología clínica, mediante la implementación de diversos algoritmos matemáticos integrados a través de métodos de procesamiento y análisis de imágenes propios de la visión e inteligencia artificial.
Para ello, se parte del hecho que las imágenes de estudio son manchas o lunares en la piel, cuya pigmentación y morfología se caracterizan por su tonalidad y estructura diferenciada con respecto a las manchas comunes de la piel.
El estudio parte del hecho de transformar una imagen compuesta por tres canales (RGB) a uno de dos y un canal, debido a que con esta trasformación permite aplicar algoritmos que facilitan discriminar parámetros propios en las vecindades de la muestra de estudio que aportan información relevante sobre la forma y estructura de los objetos que las conforman, con la particularidad de ampliar o minimizar la escala de observación con el correspondiente número de objetos a analizar.
Entiéndase por objetos, los pixeles que forman parte de la imagen. En cuanto al tratamiento de la imagen (reconocimiento, descripción, interpretación y comprensión) se recurre a una serie de fases propias de la visión artificial [6] que se combina con el aprendizaje profundo (inteligencia artificial), donde cada una de ellas implica el uso de un conjunto de algoritmos que permiten el registro y detección en primera instancia de los objetos que poseen ciertas irregularidades dentro o en la frontera de la mancha o lunar, que son clave para determinar sin son malignas o benignas. Las fases se resumen en la figura 1.
La primera fase consiste en la adquisición o captura de una imagen por medio de un dispositivo como una cámara digital o dermatoscopio. La siguiente fase consiste en realizar un tratamiento del color, pasando de tres a dos y un canal. En esta fase se puede aplicar otras instrucciones como la de seleccionar la región de la imagen a evaluar para centralizar el estudio sobre la misma. Luego, la imagen se segmenta [7] bien basado en sus características (niveles de gris, histograma, umbralización, texturas), transiciones (operadores gradiente, compás y Laplace) y modelos como la transformada de Hough [8]. Con estos métodos de segmentación se obtienen patrones específicos que resaltan detalles relevantes de la muestra de estudio. En cuanto al etiquetado, corresponde a parámetros como a la selección de regiones de interés en la que se determinan los pixeles asociados a las mismas.
De igual manera, a estos pixeles se les etiqueta y determina la vecindad a la que pertenecen, que puede ser de grado 4 u 8. Si es 4, indica puntos conectados en direcciones perpendiculares (arriba, abajo, izquierda, derecha). Si es 8, toma las direcciones perpendiculares y diagonales. Cabe señalar, que la adquisición digital de las imágenes corre por parte del médico especialista, previo registro de los datos del paciente en una ficha clínica, que luego será cargada a la carpeta repositorio del sistema, para luego iniciar la aplicación conforme a las fases expuestas.
El registro de la imagen es fundamental a la hora de realizar el análisis para la extracción de características de los objetos de estudio, puesto que la clave radica en la calidad o resolución que posee la imagen, ya que esta se almacena normalmente como mapa de bits, por lo que si el registro es deficiente va a requerir emplear de manera complementaria técnicas de restauración que implica un gasto en recursos computacionales y tiempo adicional que muchas veces el especialista no tiene.
2. Metodología
Antes de explicar los algoritmos más representativos empleados en el proyecto, es pertinente explicar las características del cáncer de piel con la que se trabajó y el porqué de ello.
La razón radica en poder establecer una vez realizado el estudio, qué algoritmos son los más apropiados, sumado a los requerimientos de análisis y estudio que debe realizar el especialista debido a que el diagnóstico es de carácter específico.
La piel tiene la función de proteger al cuerpo del calor, la luz solar, de lesiones e infecciones, al igual que ayuda a controlar la temperatura corporal mediante el almacenamiento de agua y grasa. Está compuesta por tres capas: epidermis, dermis y tejido subcutáneo, en la que cada una de ellas tiene una función específica, que para el caso del cáncer de piel comienza en la epidermis (capa externa), que se compone de células escamosas, células basales y melanocitos.
En cuanto a los tipos de cáncer de piel se tiene los de células escamosas y de células basales o no melanomatosos [9, 10]. Este último tipo responde a los tratamientos bastante bien en contraposición al primero; el cual es más agresivo que la mayoría de los otros tipos de cáncer de piel.
El cáncer denominado melanoma [11, 12] si no es diagnosticado a tiempo la probabilidad que invada otros tejidos y otras partes del cuerpo es muy alta, proceso conocido como apoptosis [13]. El 95 % de los melanomas se presentan en la piel, aunque también, puede presentarse en las superficies mucosas o en sitios a los que migran las células como la úvea, la capa vascular del ojo o inclusive, las meninges [14].
Cuando se ha llegado a este nivel o estado de evolución de esta enfermedad, el tiempo de vida del paciente se reduce, puesto que, aunque existen tratamientos agresivos los resultados en la mayoría de los casos no son prometedores.
Como dato adicional, el número de casos de melanoma aumenta cada año, sólo el 2% de todos los cánceres de piel son melanomas, que se le atribuye la mayoría de las muertes por este tipo de enfermedad. [15] Como caso particular, para Colombia se presentan 1488 casos nuevos cada año de melanoma, de los cuales 328 mueren por esta causa [16], en la que se proyecta que se presente un aumento significativo para los próximos años [17]. Este panorama es equivalente para otros países tropicales y subtropicales del mundo debido a la propia etiología del melanoma, ya que esta es de tipo multifactorial, que como señala [14], presenta tasas de incidencia que varían según el género, edad, grupos étnicos y región.
Información general sobre el cáncer de piel
Según los estudios pormenorizados del Instituto Nacional del Cáncer de los EE. UU [18] sobre el cáncer de piel, se resume en los siguientes puntos:
− El cáncer de piel es una afección por la que se forman células malignas (cancerosas) en los tejidos de la piel.
− Hay diferentes tipos de cáncer que empiezan en la piel.
− El color de la piel al estar expuesto a la luz solar, puede aumentar el riesgo de presentar cáncer tipo no melanoma y queratosis actínica.
− El cáncer de piel no melanoma y la queratosis actínica suelen aparecer a menudo como un cambio de tonalidad.
− Para detectar y diagnosticar el cáncer de piel no melanoma y la queratosis actínica, se utilizan pruebas o procedimientos que examinan la piel.
− Ciertos factores influyen en el pronóstico (probabilidad de recuperación) y las opciones de tratamiento.
Cáncer de piel no melanoma y queratosis actínica
El no melanoma [19] y la queratosis actínica [20] son los tipos de cáncer que suelen aparecer como un cambio anormal en la pigmentación de la piel en ciertos puntos localizados. Para el caso del no melanoma, los signos más comunes son una herida que no cicatriza, zonas elevadas de la piel o lisas, brillantes y con aspecto perlado [21]. También, suelen manifestarse como manchas blancas, amarillas o marrones que presentan aspecto de cicatriz. Otra forma de manifestarse, son elevaciones de piel cuya tonalidad es de color rojo o marrón rojizo. En casos extremos, puede presentarse como piel escamosa [22], sangrante o con costras.
Con la queratosis actínica [23] en contraposición al no melanoma, se manifiesta por un área levantada, plana y/o escamosa áspera de la piel, en forma de parche rojizo, de color rosado o marrón.
Detección y diagnóstico de no melanoma y queratosis actínica
Existen diversos procedimientos para la detección de estos dos tipos de cáncer de piel:
− Examen directo de la piel: Se examina in situ la piel, con miras a detectar la presencia de bultos o manchas anormales, bien sea por su color, tamaño, forma o textura. Este examen depende de la experticia por parte del especialista, ya que es de tipo observacional.
− Biopsia de piel: Se realiza una toma de tejido total o parcial de la región comprometida, para su posterior análisis patológico en busca de células cancerosas. Este estudio tarda varios días en emitir un diagnóstico. [24]
− Dermatoscopia o epiluminiscencia: Es una técnica que emplea un dispositivo óptico convencional o con luz polarizada, que amplifica la imagen de la región cutánea, eliminando en el proceso la refracción y reflexión de la luz sobre la piel. [25] Con ello el médico especialista, observa en detalle la estructura y morfología del área de estudio.
Como se aprecia, en general los procedimientos de detección son analógicos, no suelen emplear tecnologías informáticas directas para un estudio preliminar de estos tipos de cáncer, incluso para realizar un estudio de trazabilidad del comportamiento del tejido una vez efectuado cualquiera de los procedimientos citados.
Por consiguiente, observando esta necesidad en el entorno clínico en Colombia, se procedió a realizar un estudio y posterior desarrollo de un programa informático basado en visión e inteligencia artificial, que permitiera realizar un análisis de imágenes de cáncer de tipo no melanoma y queratosis actínica, con miras a ayudar al médico especialista a examinar sus características estructurales y morfológicas, de tal manera que le facilite determinar rápidamente el tipo de cáncer, estado y/o evolución del mismo.
Como factor crítico del proyecto, fue tomar como referente la identificación estándar de los tipos de melanoma enunciados por medio del autoexamen; en la que se emplea el método estándar ABCDE del melanoma [26], en la que se registran patrones como la asimetría, el borde, el color, el diámetro y evolución de la mancha o lunar, tal y como se muestra en la figura 2.
Estos parámetros le indican al médico especialista el tipo de análisis clínico a realizar y posterior tratamiento a efectuar.
Se evalúa la asimetría de la mancha, forma de los bordes, tonalidad, diámetro y etapa de evolución a la que se encuentra. Fuente imagen: Catálogo maestro de guías de práctica clínica: IMSS-547-12. Este método es requerido, puesto que el tipo de morfología y pigmentación juegan un papel fundamental a la hora de trabajar con cambios en el color de la muestra de estudio.
Otro aspecto a considerar son las variables externas que pueden hacer que la imagen presente falsos positivos, entendido en el contexto que, si el entorno en el cual se hizo su captura no cuenta con buena iluminación o la piel está sucia o cubierta por algún tipo de crema, es factible que aparezca una imagen con brillos y cambios de tonalidad que conlleven a un análisis e interpretación errónea del método ABCDE.
Debe tomarse en cuenta que pueden presentarse causas de degradación de la imagen asociados con la cámara o dispositivo de captura, tales como: calibración o enfoque defectuosos, ruido producido por los sensores, movimiento involuntario del dispositivo o del paciente, transmisión defectuosa de la señal capturada (P. ej. cable de datos o conexiones entrada/salida dañados), perturbaciones aleatorias relacionadas con el medio de captura (generalmente el aire).
Según el modelo ABCDE, la Asimetría permite establecer si el lunar es benigno o maligno trazando una línea por la mitad. El Borde, indica si el lunar los presenta de manera desigual e irregular, en este caso se considera maligno. El Color, caracteriza el lunar en el sentido que si es único se considera benigno. Para el caso que presente distintas tonalidades se considera maligno.
El Diámetro, establece la dimensión del lunar, si es benigno, deberá tener un tamaño menor a los 6 mm. [27] La Evolución, mide los cambios que puede presentar el lunar en un determinado tiempo, lo que denota que es maligno. Esta información es fundamental a la hora de llevar acabo cualquier tipo de análisis sistemático sobre una imagen.
Por consiguiente, la clasificación ABCDE se registra como plantilla de referencia en el software y como variables para realizar el estudio, tanto para el especialista como para el personal clínico de apoyo. En consecuencia, la imagen al ser considerada como variable de carácter observacional, está supeditada a parámetros que el software no puede controlar asociados al factor humano, tales como: el cansancio, enfermedad incapacitante, medicación, etc., que puede influir de una u otra manera en la toma y análisis, de ahí la importancia de mantener la plantilla como referencia en el software.
En términos técnicos, las variables a controlar son la variación de la luz del entorno y forma de registro de la imagen de estudio, que debe estar enfocada específicamente en el área afectada, ya que con base en este parámetro se determina la calidad de la misma.
Otro aspecto a tomar en cuenta en la captura de la imagen, es que la piel del paciente no debe tener ningún tipo de crema o suciedad, que a nivel óptico genera patrones de refracción y/o reflexiones irregulares sobre la zona de estudio, lo que conlleva a un análisis erróneo de la muestra.
Este último caso es más de control y asepsia antes de la prueba y registro de la imagen, que no puede omitirse porque un error de captura bajo este supuesto conlleva a una mala interpretación de la información.
3. Análisis y procesamiento de imágenes
El desarrollo del proyecto de investigación se enfocó en realizar un estudio acerca de las características morfológicas y físicas de las manchas de la piel según la metodología ABCDE, esto permitió establecer qué algoritmos serían los ideales para efectuar un análisis de las muestras a estudiar, manteniendo en el proceso un patrón comparativo con la imagen original, todo ello gestionando a través de una aplicación desarrollada en el software de Matlab®.
El procesamiento de imágenes tiene como objetivo mejorar el aspecto y/o buscar detalles que no se perciben a simple vista de los objetos que conforman la imagen de estudio. Este procedimiento se realiza con el fin de hacer más evidentes los detalles de una imagen y permitir con ello realizar una inspección precisa sobre las características más relevantes de la misma.
Segmentación y binarización
Uno de los primeros pasos en el procesamiento de imágenes, aparte de la captura digitalizada, es segmentar los objetos que conforman la imagen con el fin de diferenciar la región de estudio de la que no lo es, a través del aislamiento de los objetos de interés.
Para poder aplicar los algoritmos de segmentación, como el de discontinuidad o el de similitud, la condición es que la imagen debe estar en escala de grises, con el fin de determinar los límites de las regiones de estudio mediante la creación de umbrales, contornos activos y análisis de color e intensidad.
Con la discontinuidad se aplica un modelo laplaciano que divide la imagen con base en los cambios bruscos que se presenta a nivel de las tonalidades de gris, para luego, aplicar los algoritmos de detección de puntos aislados, de líneas y de bordes. Estos algoritmos están relacionados con el concepto de umbralización, que implica métodos como la entropía, histograma, clustering, espacialidad local y similitud. Para el caso de este último método, se encarga de dividir la imagen buscando regiones que tengan valores parecidos, conforme a unos criterios prefijados, tales como el crecimiento de las regiones y el de umbralización.
Un proceso paralelo a la segmentación, es obtener la máscara binaria [28, 29], que consiste básicamente en realizar un barrido matricial de la imagen por medio de bucles o recursividad, con el fin de reducir la escala de grises a valores de 0 y 1 (imagen lógica), donde cero indica pixeles de color negro, y uno, pixeles de color blanco. En este mismo contexto de análisis, se habla del preprocesado de la imagen, que consiste en transformarla a nivel de grises, que es fundamental para el posterior estudio algorítmico, para luego umbralizarla, pues lo que se persigue es la separación de los objetos del fondo de la imagen I, por lo que se selecciona un umbral U para cualquier punto de coordenadas (x,y), que cumpla con la siguiente condición:
donde el umbral U es un número que está entre 0 y 255. Bajo este rango de valores se puede ajustar la imagen con miras a establecer aspectos puntuales relacionados con la resolución de los objetos de interés perteneciente a la imagen de estudio.
Umbralización de contornos
Con la umbralización de contornos se buscan cambios bruscos en los niveles de gris presentes en los objetos de la imagen, lo que resulta ser un indicativo de la presencia de bordes en la misma. En términos generales se puede ver el método de la umbralización como una operación en la que se evalúa cada pixel con respecto a una función U de la forma:
donde I(x,y) representa el nivel de gris de un pixel de coordenadas (x,y) y p(x,y) que describe la propiedad local del pixel con respecto a sus vecinos o vecindad, en la que se toma la imagen en su totalidad como una matriz de tamaño MxN. Por consiguiente, la umbralización da como resultado otra imagen Im definida bajo las siguientes condiciones:
De estas condiciones se infiere de Im lo siguiente: en primer lugar representa un pixel de coordenadas (x,y) de la imagen, donde la etiqueta 1 corresponde a los objetos; y en segundo lugar, la etiqueta 0 que corresponde al fondo.
En la fase de umbralización, se consideran algunos aspectos en cuanto al tratamiento de la imagen, tales como: pérdidas de conectividad entre los pixeles que forman parte del borde de la imagen por el ruido inherente a la misma, también, por la existencia de bordes poco o demasiado definidos y por filtrado de ruido mediante el uso de algoritmos exigentes.
Cada uno de estos elementos es relevante para un análisis pormenorizado de la imagen, ya que el nivel de detalle al cual se realiza el estudio, solo puede hacerse por medio del uso de un software especializado y un sistema de cómputo dispuesto para tal fin.
Algoritmos para detección de bordes
La detección de bordes es una técnica de procesamiento de imágenes que permite la búsqueda de límites que demarcan los objetos dentro de la imagen. Esto se logra a través del uso de aproximaciones mediante derivadas de primer y segundo orden, que detectan discontinuidades en el brillo de los objetos.
Para ello se procedió a emplear técnicas de detección de bordes, que se fundamentan en los siguientes algoritmos: Roberts, Prewitt, Sobel y Canny. [30] Estas técnicas combinadas con otros algoritmos de conteo de objetos [31], dan cierto grado de confiabilidad a la hora de efectuar un estudio minucioso de la imagen a través de máscaras, que permiten calcular el gradiente.
Las máscaras de los primeros algoritmos están representadas de la siguiente manera:
− Roberts: solo emplea dos puntos para cada máscara tal como se indica en la matriz, por lo que lo torna ideal cuando se trabaja con imágenes binarias:
− Sobel: se caracteriza porque permite eliminar parte del ruido que porta la imagen suavizándola y con ello los falsos bordes:
Uno de los algoritmos más relevantes de este estudio fue el de Canny [32], desarrollado por fases para detectar bordes empleando filtros en las direcciones horizontal, vertical y diagonal. La primera fase, es la obtención del gradiente previo proceso de suavizado de la imagen para evitar la sobredetección de los bordes. Este suavizado es mediante una función filtro gaussiano representado matemáticamente como:
donde σ es la desviación estándar calculada en el pixel (x,y).
El gradiente de la imagen I(x,y) en un punto (x,y), se describe por un vector bidimensional G que tiene la forma de:
El vector gradiente se representa por el laplaciano:
La dirección entre
La siguiente fase de análisis, consiste en la supresión no máxima a los gradientes, en la que se busca obtener bordes de un pixel de dimensión. Por lo tanto, se toma un conjunto discreto de direcciones para el análisis de 0, 45, 90 y 135 grados. Luego, se procede a calcular la histéresis del umbral a la fase anterior, eliminando máximos del ruido entre otros detalles no esenciales para el estudio de la imagen. Finalmente, se aplica la fase de cierre de los contornos abiertos de la imagen.
En cuanto a los algoritmos de Roberts, Prewitt y Sobel, se diferencian unos de otros por las máscaras utilizadas sobre los bordes de la imagen, por su sensibilidad al ruido y direcciones verticales, horizontales y diagonales [28]. Con la implementación de estos algoritmos, implica para el especialista poder determinar cuáles son los más idóneos para el estudio, brindado una amplia gama de presentación de los objetos en cuanto a tonalidades, morfología y expresión más relevantes.
Con estas opciones dadas en el programa, se pueden seleccionar los algoritmos que más convenga según el tipo de estudio que se desee efectuar sobre la muestra, bien en color original, en escala de grises o binarizado. Este último proceso se realiza con el fin de establecer la uniformidad de los pixeles en los objetos relevantes de la imagen de estudio y establecer si es o no pertinente un nuevo registro de los mismos.
4. Presentación del sistema
Antes de iniciar el proceso de análisis, el médico especialista debe registrarse en el sistema informático, -con el fin que a posteriori pueda crear la ficha clínica del paciente- ingresando la información personal para quedar registrado en la base de datos desarrollada en este caso en MySQL. El sistema confirma el usuario y contraseña en la base de datos para el posterior ingreso de este al programa.
Una vez realizado este paso, el médico estará listo para registrar los datos personales del paciente en consultas posteriores.
El siguiente paso, consiste en la toma y almacenamiento de las imágenes de la piel afectada del paciente en el repositorio de la base de datos.
Para ello, se carga la imagen original desde una cámara digital o de un dermatoscopio, conectados directamente al computador, o realizar la captura aparte y luego transferirla al repositorio de trabajo del programa. Una vez hecho este paso, se procede a transformar la imagen a escala de grises, para luego aplicar los algoritmos de binarización o umbralización según se desee.
Otra opción a emplear es calcular el complemento de la imagen, sea esta en RGB, en escala de grises o binaria, en la que se conserva el mismo tamaño y clase de la imagen de entrada. Ahora, el complemento de la imagen puede obtenerse mediante el uso de las unidades de procesamiento gráfico (GPU), que devuelve en este caso la imagen original según el formato de entrada (RGB, grises o binaria).
Puede ocurrir que la mancha en la piel no necesariamente sea plana, por lo que el uso del algoritmo del complemento invierte la imagen permitiendo observar áreas con poca luz, incluso realzar detalles que a simple vista pasan inadvertidos. Aunque la captura de la imagen está en un entorno controlado, el uso del complemento puede ser útil para mejorar la luminosidad en determinadas regiones, en particular cuando se presentan rangos dinámicos bajos con niveles de ruido altos, que afectan el rendimiento de los algoritmos empleados en visión artificial.
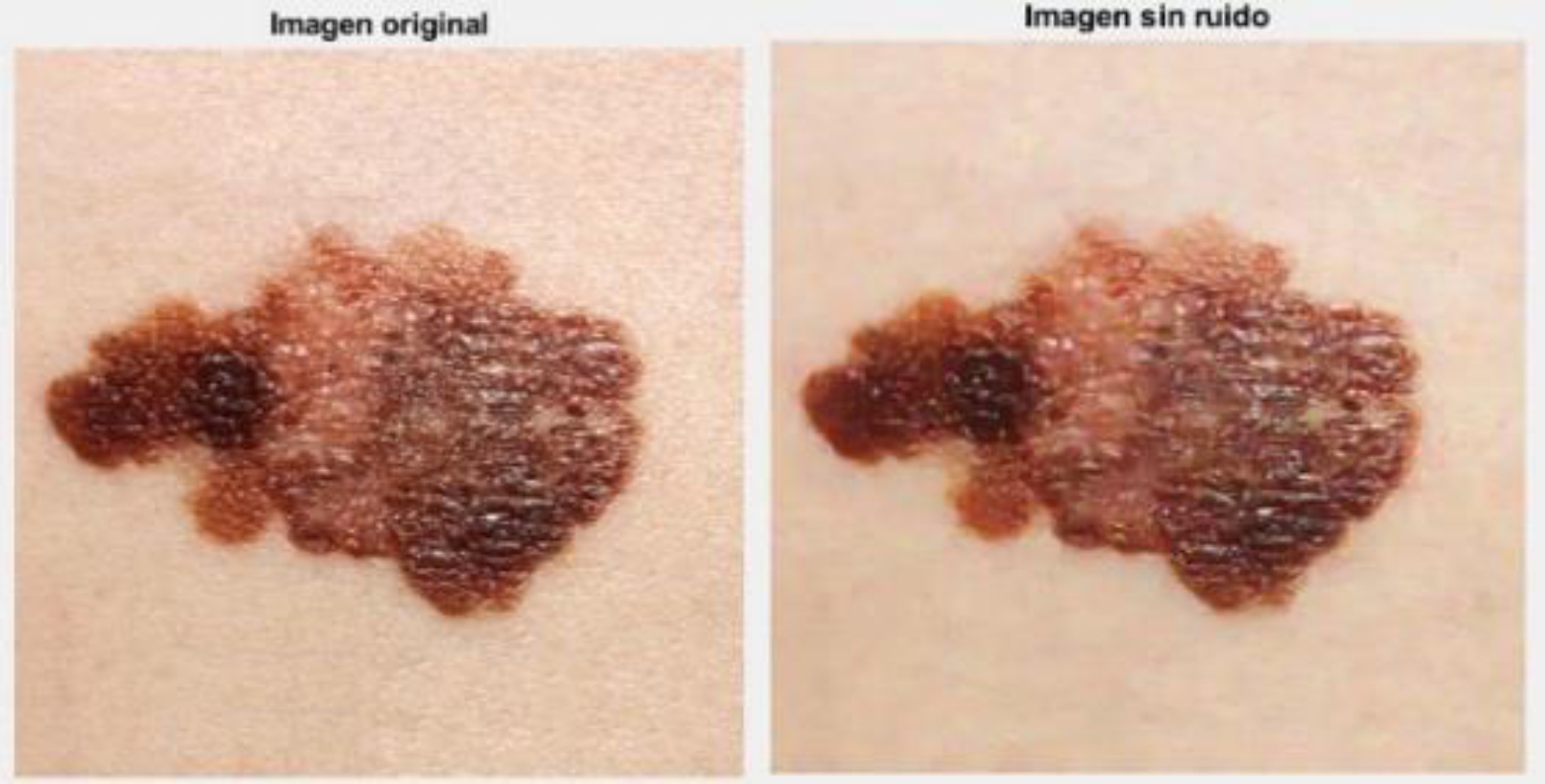
En la figura 3, se muestra la imagen original sobre la cual se han empleado algoritmos de Dehazing [33] en el que se realiza un realce de contraste de la imagen, manteniendo un rango dinámico medio, que facilita aplicar el modelo ABCDE en cuanto a su interpretación. El siguiente paso se enfocó a eliminar pixeles del contorno de la mancha o lunar y objetos que difieren en la toma de la muestra.
En este proceso se presentó la opción de aplicar algoritmos morfológicos [34] como la dilatación, erosión, apertura y cierre, sobre la imagen binarizada [35], que permitieron limpiar y/o eliminar el contorno y vecindades de la imagen I(x,y) de objetos poco relevantes para el estudio.
Cabe señalar, que el orden de los algoritmos morfológicos se debe respetar para obtener mejores resultados. Cada morfología genera un elemento estructural que es una subimagen I’(i,j). Matemáticamente las estructuras morfológicas E de I’ se designan por los operadores ⨁ y ⊗, que definen un conjunto de datos según el algoritmo aplicado. Para el caso del proceso de la dilatación, este cumple con la propiedad conmutativa y asociativa, al igual que es invariante a la transformación que además es creciente, es decir, el número de filas de la matriz I’ es igual o mayor que la matriz I. Entonces, la dilatación se define como el conjunto:
Este conjunto está sujeto a la siguiente condición:
Es decir, permite adicionar pixeles en las fronteras de la imagen de estudio con el fin de mejorar variaciones en las vecindades de los objetos que la componen.
En cuanto al proceso de la erosión, esta cumple con las propiedades de no ser conmutativa e invariante a las transformaciones, es invertible (una vez aplicada no se puede devolver), es dual y es una transformación creciente:
Este conjunto está sujeto a la siguiente condición:
Es decir, permite remover pixeles de las fronteras de la imagen de estudio, con el fin de suavizar las vecindades de los objetos que la componen. Estos modelos toman valores que están fuera de la imagen binarizada, lo que supone que su nivel de gris es igual a cero, I(x,y) = 0. Además, si se aplica una función XOR a cualquiera de las dos morfologías se obtienen los contornos de la imagen que ha quedado como opción de uso para el especialista.
Para el caso de la apertura y cierre, estas son combinaciones de la erosión y la dilatación, que permiten eliminar detalles de la imagen más pequeños que los del elemento estructural. Las operaciones respectivas son:
Tanto las operaciones de apertura y cierre son idempotentes, es decir, que se pueden ejecutar las veces que se desee y se obtiene el mismo resultado.
Con el uso de los algoritmos morfológicos permite eliminar todo objeto no conexo a la imagen de estudio, lo que disminuye en cierto porcentaje los falsos positivos, tales como: lunares, manchas y/o pecas cerca al área de estudio, incluso imperfecciones de la piel como cicatrices o vellosidades.
Para minimizar este problema, es conveniente adicionar pixeles al contorno de los objetos presentes en la imagen de estudio, con el fin de mejorar su frontera tal como se observa en la figura 4, en la que una vez establecido el histograma permite observar el nivel de pixeles de grises y su distribución en la imagen, que para este caso muestra sombras pálidas en algunas regiones, por lo que se define su viabilidad de estudio o no.
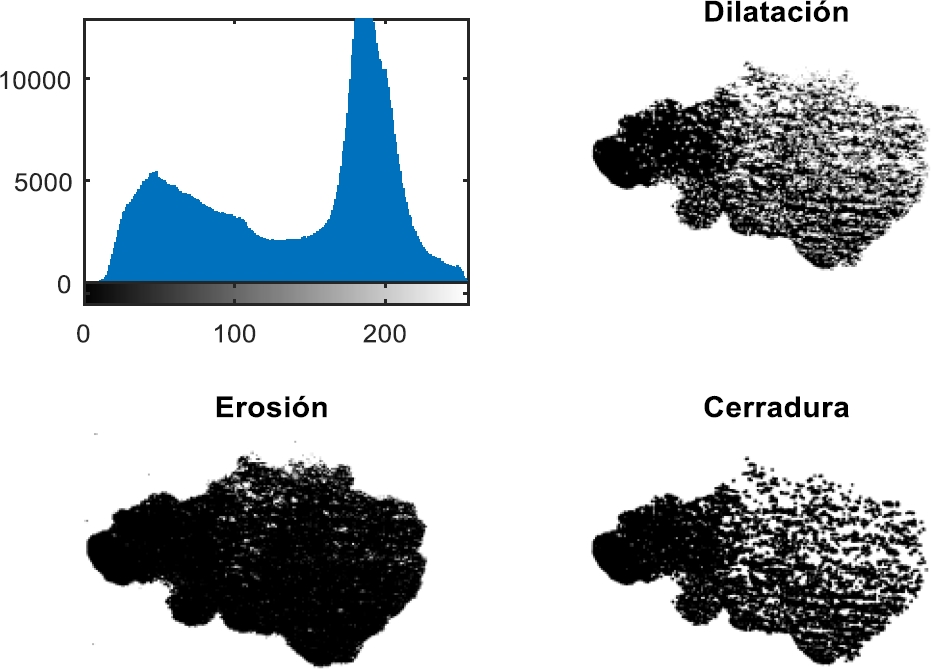
Fig. 4 Aplicación de los algoritmos de dilatación para establecer su morfología y erosión para eliminar detalles irrelevantes de la imagen, reduciendo o afinando la misma. Luego, se aplica el algoritmo de cerradura que suaviza el contorno de la imagen por el exterior. Otro algoritmo que eventualmente se emplea, es el de apertura que suaviza la imagen por el interior
Como el histograma es una representación gráfica de las frecuencias relativas según los colores que componen la escena de una imagen, se puede determinar si la imagen es oscura (tonos apagados), posee muchas regiones oscuras o fondo negro (sombras), regiones muy claras (sobreexposición) o no posee regiones oscuras (sombras pálidas). En este sentido, [36] se define el histograma como una función discreta que representa el número de pixeles en la imagen en función de los niveles de intensidad (g), donde la probabilidad de ocurrencia P(g) de un determinado nivel g se define como:
P(g) se evalúa en el intervalo [0,1], N(g) representa el número de píxeles que se encuentra a un nivel de intensidad g y M representa el número de píxeles de la imagen.
Dentro de las propiedades estadísticas características de un histograma que se evalúa en una imagen a escala de grises son: la media, varianza, asimetría, energía y entropía. A este proceso se le puede adicionar el algoritmo de ecualización, que permite mejorar la resolución de la imagen repartiendo de manera cuasi uniforme los niveles de intensidad de gris en un rango [0, L- 1].
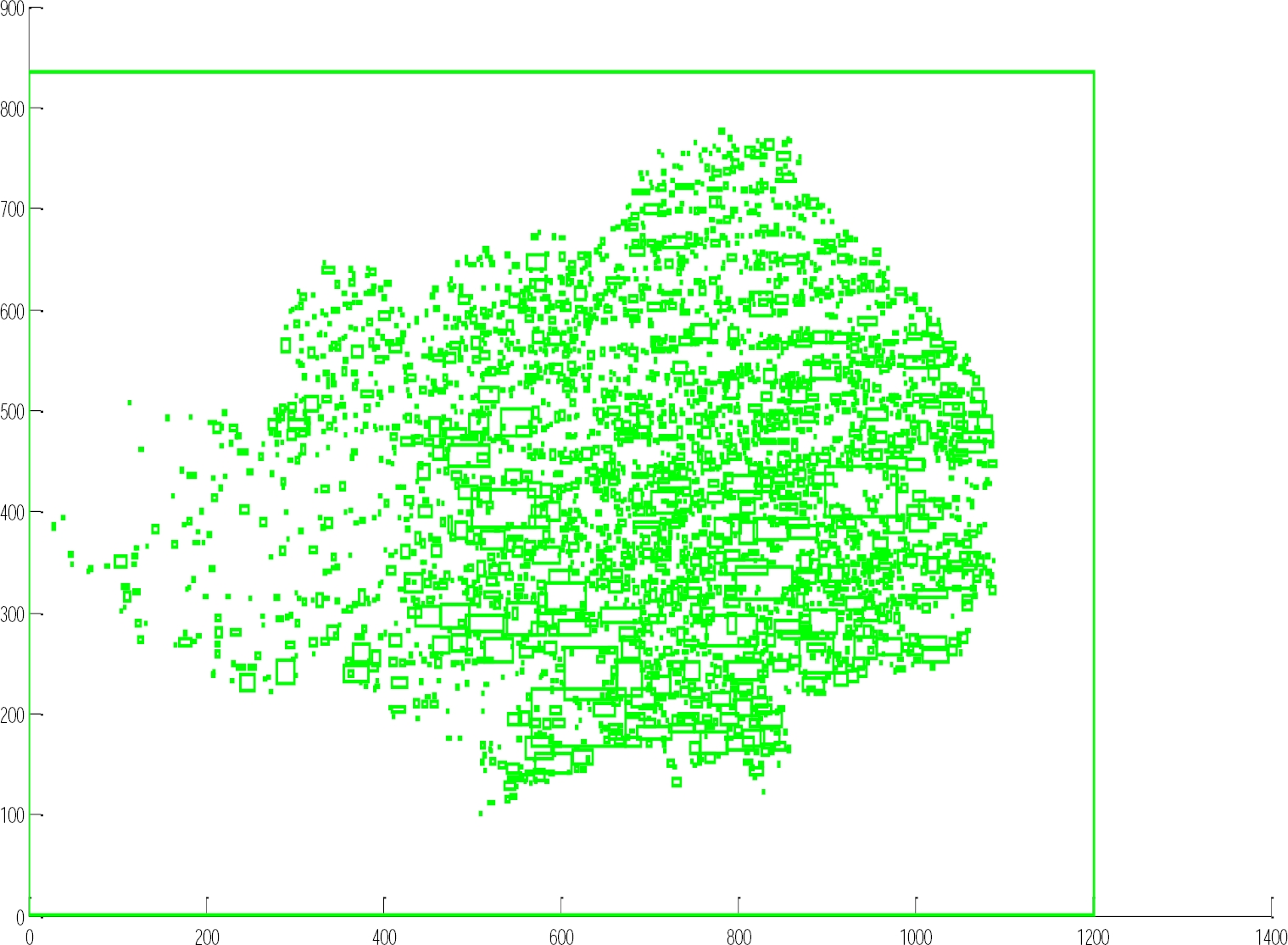
Prosiguiendo con el análisis, se definió el grado de reflexión y refracción de la zona de estudio, en la que se somete la imagen a máscaras de tipo RGB, con el fin de observar diferencias y coherencias según el modelo ABCDE. De igual manera, se procede a realizar el conteo de objetos relevantes de la imagen, tal como se aprecia en la figura 5, en la que se define el área y geometría que se desea estudiar en el interior de la muestra.
El proceso de conteo es importante a la hora de comparar las imágenes en el tiempo, debido a que, si hay cambios mínimos en la estructura del lunar o mancha, con el conteo se sabrá de inmediato si ha evolucionado o involucionado.
No sobra mencionar, que este conteo se realiza de forma automática. Una opción complementaria a las máscaras, es emplear el algoritmo de Mahalanobis [37], que permite determinar la similitud entre dos variables aleatorias multidimensionales a través de la medida de la distancia entre distribuciones:
donde
La distancia euclídea (d) a diferencia de la de Mahalanobis, toma en cuenta la correlación entre las variables aleatorias (xi, yi). Para el caso de imágenes en 2D, la distancia se calcula de la siguiente manera:
Es decir, la distancia de Mahalanobis se calcula entre dos variables aleatorias que tienen la misma distribución de probabilidad, que se relacionan con una matriz de covarianza [38], por lo cual los resultados en cuanto a la distribución de pixeles bien sean en color o escala de grises de la imagen resulta ser mejor que la euclidiana, tal como se observa en la figura 6. Esto no implica que se descarta la métrica euclidiana, puesto que el filtro puede arrojar datos relevantes de determinados objetos, adicional a que se emplea para medir el diámetro de los objetos, aumentar o reducir el tamaño de la imagen y recortar una parte de ella dado el caso, entre otras opciones, todas ellas conducentes a extraer los patrones más representativos, con el fin de facilitar al especialista inferir sobre las características morfológicas y aspecto de las manchas para su posterior comparación con el modelo ABCDE.
Una ayuda que se incorporó al sistema, es el uso de la diferenciación como método para calcular el grado de separación entre niveles de grises vecinos, detección de bordes y distribución de probabilidad de pixeles (objetos). Para ello, se aplican los algoritmos de filtrado [39], tales como: Roberts, log, Poisson y Speckle. Cada uno de estos algoritmos presenta cambios en la imagen de estudio, que eventualmente se combinan con otros que el especialista estime necesario en pro de clarificar detalles y descartar falsos positivos.
Como complemento a lo desarrollado anteriormente, se emplea una serie de algoritmos de correlación característicos de la imagen, que permiten establecer propiedades de ciertos objetos de estudio que pueden ser relevantes para el análisis clínico, en cuanto a crecimiento y patrones asociados al modelo ABCDE, por lo que puede tomarse como herramienta de apoyo al mismo. También, con el método de correlación se establece un patrón de comparación entre la imagen original y una imagen que se ha registrado a posteriori o una sección de ella, con el fin de establecer si hay variaciones en una determinada región de la mancha, tal como se observa en la figura 7.
El método de correlación es ideal cuando se requiere establecer variaciones en cuanto a saturación, tono y brillo de los objetos de una imagen, siempre y cuando se respete las condiciones de luminosidad a la hora de su captura para poderla comparar con las que se encuentran en el repositorio de la base de datos. Lo más recomendable es trabajar la muestra e imagen original a escalas de grises, o en su defecto a color si se dispone de buenos recursos computacionales.
5. Discusión y análisis de resultados
Con los procedimientos actuales para la detección temprana de cáncer de piel, en particular el de no melanoma y el de queratosis actínica, adolecen de un sistema informático complementario que actúe como soporte al diagnóstico de este tipo de enfermedades, máxime cuando se requiere que el médico especialista efectúe una detección en sus primeros estados. En la revisión bibliográfica obligatoria para el desarrollo de proyecto, se observa que hay poco material enfocado directamente a la temática tratada.
Existen investigaciones para el procesamiento de imágenes de cáncer de piel en la que se toma las imágenes dermatoscópicas [40], aplicando técnicas de análisis morfológico, manipulación de color, segmentación de imágenes y caracterización [41, 42], incluso empleando redes neuronales, que han demostrado ser buenas acerca de seleccionar regiones de estudio específicas, más no para el no melanoma y la queratosis como casos particulares.
En contraposición a las técnicas mencionadas, el sistema propuesto combina diversos algoritmos de análisis de bordes, filtrado, color y adaptación lumínica según el caso, entre otros; que permite un estudio pormenorizado sobre la morfología y estructura de la mancha o lunar bajo diferentes condiciones de registro imagenológico o de cambios de pigmentación según la trazabilidad que se realice a la muestra de estudio.
Se prestó especial atención a la detección de discontinuidades, tales como bordes, líneas y esquinas, donde el algoritmo de canny fue de particular interés, al igual que el de sobel, roberts y prewit. El por qué tomar estos cuatro algoritmos, radica principalmente tal como expone [43] en aplicar la reconstrucción de imágenes considerando combinaciones de fase y magnitud de fuentes diversas muestran, además, que la fase es la portadora de esta información, que con únicamente las discontinuidades es posible reconocer el contenido de la imagen. El combinar diversos algoritmos en conjunto, permite efectuar un estudio pormenorizado de regiones específicas de la imagen, lo cual es muy importante para un posterior estudio histológico.
También, dentro del análisis de las características de la imagen, se ha dispuesto un combo de filtros estándar, bien para trabajar con morfologías de tipo top-hat y bottom-hat, como para mejorar la calidad de realce de la muestra, tales como los filtros: gaussiano, salt & pepper [44] y multiplicativo, con diversas configuraciones para aumentar o disminuir el nivel de ruido.
Según las pruebas realizadas en un entorno controlado, un elemento importante es la calidad de la imagen, por lo que se recomienda el uso del dermatoscopio. Aunque se realizó una serie de registros fotográficos con cámara digital convencional, incluso con imágenes capturadas desde un dispositivo móvil, el sistema demostró ser flexible y funcional a la hora de efectuar el procesamiento de las imágenes.
Sin embargo, se implementó una red neuronal preentrenada (DnCNN) [45] basada en aprendizaje profundo (Deep learning) para mejorar el realce de la imagen reduciendo el ruido Gaussiano [46], tal como se observa en la figura 8, y sobre ella emplear los algoritmos mencionados anteriormente. Aunque la red neuronal preentrenada (DnCNN) ayuda a mejorar la calidad de la imagen, no es muy flexible sobre tratar ruidos desconocidos, por lo que es preciso entrenarla según necesidades propias del problema.
Por lo tanto, este tipo de red presenta ciertas limitaciones tales como: solo funciona con ruido gaussiano y con una desviación estándar limitada. Solo trabaja con imágenes de un solo canal en 2D. Si la imagen es en 3D o tiene varios canales de color, debe eliminarse el plano o ruido por canal por separado respectivamente. Sin embargo, a pesar de estas limitaciones la red demostró ser ideal para imágenes cuya captura se hizo en un entorno no controlado.
La experiencia adquirida supone que, si dado el caso el paciente por factores de acceso y ubicación no puede trasladarse a un centro de salud, sólo con la captura de una buena imagen por medio de un Smartphone, Tablet o cámara digital, puede trasmitirla directamente al celular del médico especialista, permitiendo de esta manera llevar a cabo el análisis que a posteriori discriminaría si lo que se observa es o no un melanoma.
De hecho, con el avance que existe actualmente en cuanto a plataformas de desarrollo para aplicaciones móviles, se puede extrapolar parte del código desarrollado para el programa de escritorio e implementarlo en un Smartphone, bien sea en código de Matlab (empleando el paquete de Matlab Mobile) o bajo otros lenguajes como OpenCV [47], Java [48] o Python [49], entre otros. El sistema desarrollado está pensado como un complemento a los procedimientos de diagnóstico citados, que permite al médico especialista y/o patólogo, realizar un estudio pormenorizado y personalizado de la evolución del melanoma.
Cabe señalar que, al efectuar el estudio visual no automatizado, se está sujeto a cometer errores de tipo humano, por ejemplo, cansancio y observación prolongada, entre otros, en la que se pueden omitir detalles clave del lunar o mancha sospechosa. Por lo tanto, este es un aspecto a tomar en consideración en cuanto a funcionalidad del sistema, sumado a su escalabilidad a la hora de implementar nuevos algoritmos de análisis y procesamiento, dado el caso de requerirse para nuevos estudios.
A futuro se pretende que al sistema desarrollado se integren algoritmos avanzados de visión artificial, combinados con algoritmos inteligentes basados en aprendizaje profundo [50, 51] como las redes neuronales convolucionales [52] (profundas) y/o máquinas de aprendizaje (machine learning) [51], lo que sin duda va a mejorar su desempeño, ya que estos algoritmos permiten realizar comparaciones y/o correlaciones entre objetos bajo parámetros de un dataset creado para tal fin, lo que permitirá establecer si los tratamientos clínicos realizados están funcionando como se espera o no.
Las correlaciones han probado su valía en otros contextos de la imagenología clínica e ingeniería en general, por lo que su aplicación en el proyecto en mención para una posterior fase ha sido considerada.
6. Conclusiones
El estudio de imágenes clínicas ha tomado gran relevancia en los últimos años, debido en parte al crecimiento exponencial de la potencia computacional, al igual que el desarrollo de nuevas aplicaciones que permiten simular algoritmos matemáticos de alta complejidad de manera rápida y eficiente.
Es así que, al emplear la visión artificial para la identificación temprana de cáncer, el médico especialista puede efectuar un análisis pormenorizado de las anomalías cutáneas como el no melanoma y la queratosis actínica en sus primeras etapas de evolución.
Un aspecto a tomar en cuenta del programa, es que este puede aplicarse a otro tipo de anomalías de la piel, sabiendo combinar los diversos algoritmos para el procesamiento de imágenes, cuya manifestación visual puede ser identificada de forma rápida, basado en la clasificación ABCDE del melanoma. Al combinar algoritmos de realce de contorno de imágenes, segmentación, binarización, umbralización, métricas euclidianas y de mahalanobis, entre otros, se obtienen resultados ideales para un estudio visual de los melanomas citados, sumado a que facilita el campo de investigación observacional de este tipo de enfermedad.
Aunque se han realizado pruebas preliminares con redes neuronales estándar, se requiere investigar más afondo sobre la potencial fusión de las redes neuronales convolucionales con el sistema desarrollado, al igual que la incorporación de otros algoritmos de visión artificial, tales como: Viola Jones [53, 54] que, aunque en principio se emplea para la detección de rostros, puede emplearse para la detección de patrones específicos asociados a factores de iluminación [55], AdaBoost [56], segmentación de texturas mediante filtros de Gabor [57, 58] y meta-algoritmos adaptativos de machine learning [59, 60], entre otros, con el fin que el programa sea más dinámico y asertivo a la hora de identificar patrones anormales en los lunares y/o manchas de la piel, por lo que se espera una identificación rápida y temprana del melanoma.
Para que esto sea posible, se requiere que estos algoritmos estén acompañados del uso de GPU Nvidia locales o en la nube, que reducen el tiempo de entrenamiento de una red neuronal, donde la programación al respecto es mínima con pocos cambios de configuración para el caso de Matlab.
Para finalizar, un aspecto a mencionar del programa desarrollado es que permite ser instalado en un computador portátil, lo que facilita su movilidad para el médico especialista que deba desplazarse a zonas de difícil acceso y realizar su estudio in situ. En este sentido, las potencialidades del sistema son bastante amplios, esto en parte, porque con el avance progresivo de la tecnología móvil, en cuanto a capacidad de almacenamiento y procesamiento, la incorporación de nuevos algoritmos al sistema expuesto, puede ser progresivo y escalable, por ende, con unas ligeras modificaciones se puede instalar en un dispositivo móvil como una aplicación (App) o navegar como una versión de página web optimizada y adaptable (WebApp).











 text new page (beta)
text new page (beta)