Introducción
Los analgésicos antiinflamatorios no esteroideos (AINE) son uno de los grupos farmacológicos que más se consumen con o sin prescripción médica a nivel mundial para el tratamiento sintomático de diversos padecimientos dolorosos agudos y crónicos.1,2 En una revisión sistemática en donde se comparó la eficacia analgésica de los AINE contra opioides de baja y alta potencia en la osteoartritis de rodilla se encontró que los puntajes de reducción de dolor por WOMAC (Western Ontario and McMaster Universities Osteoarthritis Index) no eran diferentes ni clínica ni estadísticamente entre los diversos fármacos,3 lo cual explica, en parte, la razón por la que los pacientes buscan y encuentran alivio con la toma de algún AINE-que, además, pueden obtener sin necesidad de una prescripción-.
La libre venta de AINE y la escasa conciencia que existe entre la población general -e incluso, el personal médico- sobre los riesgos que entraña ser usuario de AINE, sobre todo en ausencia de indicación, ha generado un uso indebido y, con mucha frecuencia, excesivo.4 En los Estados Unidos, hasta 44% de los consumidores regulares de AINE llegan a tomar dosis diarias mayores que las recomendadas,5 o bien realizan combinaciones con más de un medicamento del mismo grupo, lo cual incrementa en forma sustancial el riesgo de sobredosificación, toxicidad y efectos adversos.
El Colegio Americano de Reumatología, la Sociedad Española de Dolor, la Liga Europea contra el Reumatismo, la Sociedad Internacional para la Investigación en Osteoartritis y el Colegio Americano de Gastroenterología han publicado guías de tratamiento, intentando orientar a los clínicos en el uso de medicamentos analgésicos a largo plazo;5 para ello, han evaluado no sólo la eficacia en el alivio sintomático y el impacto en la calidad de vida y funcionalidad de los pacientes;6 también se han preocupado por los riesgos derivados de los efectos colaterales sobre el aparato gastrointestinal, cardiovascular, renal, hematológico y hepático, así como las reacciones alérgicas que pueden presentar los usuarios de AINEs.2,7
Así, dichas sociedades han establecido que en aquellos pacientes cuyo dolor no sea aliviado con dosis adecuadas de paracetamol,5,8 o bien en quienes la terapia antiinflamatoria mediante AINE sea estrictamente necesaria, entonces se deberá usar la dosis mínima efectiva de un AINE por el menor tiempo posible, con el propósito de limitar la frecuencia de estos efectos secundarios.5,9,10
El objetivo de este trabajo es hacer una revisión sobre los factores que determinan los diferentes riesgos en los enfermos, así como la relevancia que juega la selección del AINE, la dosis, la frecuencia y su uso concomitante con otras terapias en la presentación de desenlaces adversos.
Generalidades sobre aspectos cinéticos y dinámicos de los AINE
Históricamente, los AINE se han ganado su lugar en el arsenal terapéutico por sus propiedades analgésicas, antiinflamatorias y antipiréticas, ya que inhiben la producción de prostanoides proinflamatorios1 (papel en la hiperalgesia periférica y central) mediante el bloqueo competitivo y reversible o no, por acetilación del sitio de unión de ciclooxigenasa (COX) 1 y 2 al ácido araquidónico, impidiendo así la conversión oxidativa en prostaglandina G2 y H2 y toda la cascada subsecuente9 (Figura 1).
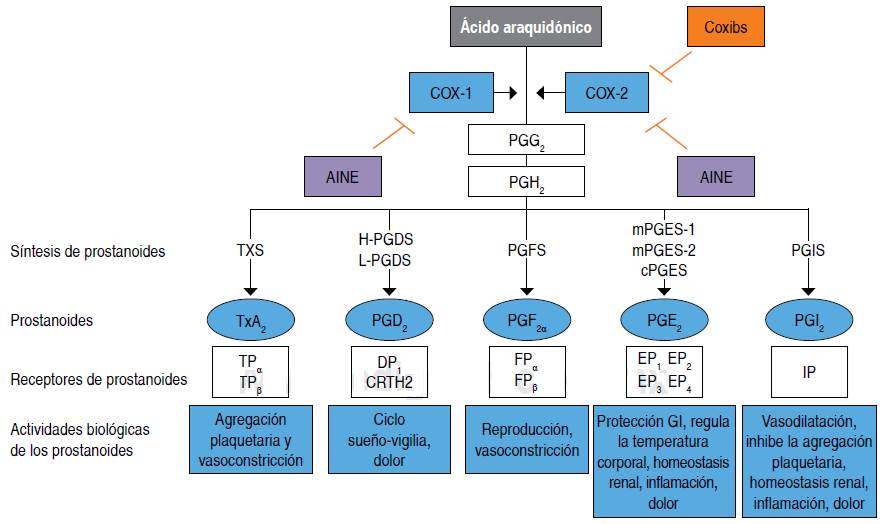
Traducido de: Brune K, Patrignani P. New insights into the use of currently available non-steroidal anti-inflammatory drugs. J Pain Res. 2015; 8: 105-118.
Figura 1 Ácido araquidónico como precursor de los prostanoides proinflamatorios.
Los AINE están disponibles para su administración por diversas vías: oral, intravenosa, rectal, sublingual, intramuscular o tópica. Por vía oral, los AINE tienen buena biodisponibilidad, sufren un importante metabolismo de primer paso en los citocromos hepáticos (CYP) y se unen extensamente a proteínas del plasma.11 Se metabolizan mediante reacciones de fase I y II (CYP3A4, CYP2C19, CYP2C9), o bien por glucuronidación; su excreción es sobre todo renal y, en su mayoría, en forma de metabolitos.1,9
Según su estructura química, se pueden clasificar en ácidos o no ácidos, lo cual determinará su distribución. Así, los AINE no ácidos como celecoxib se distribuyen en todos los tejidos corporales; por el contrario, aquéllos con grupos ácidos como diclofenaco, ketoprofeno e ibuprofeno tienden a distribuirse y permanecer en los sitios de inflamación, a pesar de que sus concentraciones en plasma decaen con rapidez, lo cual podría implicar un efecto terapéutico a nivel local más sostenido.9,12
La COX-1 se expresa de manera constitutiva en la mayoría de las células y los tejidos, incluyendo el endotelio vascular, los monocitos, epitelio gastrointestinal y plaquetas.12 La COX-2, por el contrario, se expresa constitutivamente en pocos tejidos y durante la inflamación sufre una regulación a la alta en el endotelio vascular, la membrana sinovial, monocitos y macrófagos.1,4,9
El efecto analgésico pleno y antiinflamatorio se obtiene cuando se alcanzan concentraciones plasmáticas que inhiben la actividad de COX-2 al 80% en sangre total (IC80).12 Entonces, debemos entender que para que cualquier AINE tenga el efecto deseado debe ser inhibidor de la COX-2, con diferentes grados de inhibición de COX-1 como «efecto colateral»9 (Cuadro 1 y Figura 2).
Cuadro 1 Selectividad relativa de los AINE por COX-1 y COX-2.
| AINE no selectivos | Inhibidores COX-2 |
| Diclofenaco | Celecoxib |
| Diflunisal | Etoricoxib |
| Etodolaco | Lumiracoxib |
| Fenoprofeno | Rofecoxib |
| Flurbiprofeno | Valdecoxib |
| Ibuprofeno | Parecoxib |
| Indometacina | |
| Ketoprofeno | |
| Ketorolaco | |
| Meloxicam | |
| Naproxeno | |
| Piroxicam | |
| Tolmetin |
Modificado de: Danelich IM, Wright SS, Lose JM, Tefft BJ, Cicci JD, Reed BN. Safety of nonsteroidal antiinflammatory drugs in patients with cardiovascular disease. Pharmacotherapy. 2015; 35 (5): 520-535.
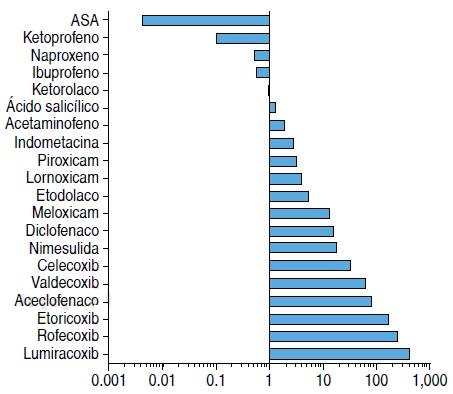
Tomado de: Brune K, Patrignani P. New insights into the use of currently available non-steroidal anti-inflammatory drugs. J Pain Res. 2015; 8: 105-118.
Figura 2 Radio de selectividad COX-1/COX-2 de AINEs usados comúnmente basados en los valores de IC50.
Es importante tomar en cuenta que la frecuencia y gravedad de los efectos secundarios no dependen solo del AINE seleccionado, también tiene que ver con la dosis empleada, los intervalos de administración, la forma de liberación (inmediata o retardada, esta última con mayor riesgo) y las condiciones basales del paciente, así como la coexistencia de otros factores que lo pongan en riesgo2 (Figura 3).
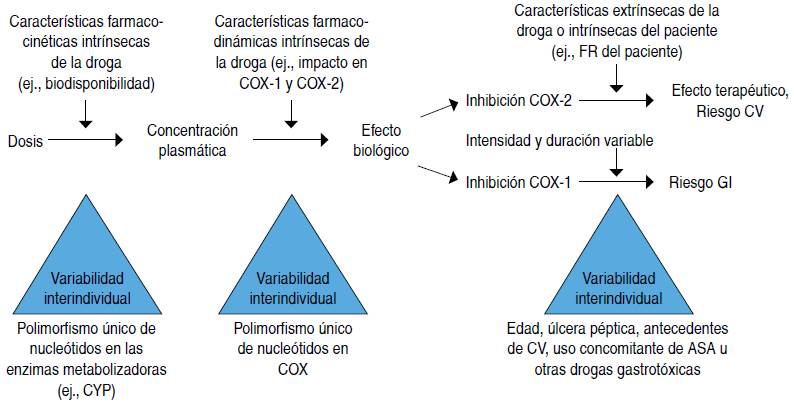
Traducido de: Brune K, Patrignani P. New insights into the use of currently available non-steroidal anti-inflammatory drugs. J Pain Res. 2015; 8: 105-118.
Figura 3 Factores determinantes de la presentación de efectos secundarios durante la terapia con AINE.
Los AINE que presentan vidas medias plasmáticas cortas se asocian con una mayor tolerabilidad, ya que el aclaramiento del plasma permite que el fármaco permanezca una menor cantidad de tiempo en contacto con los tejidos no objetivo (mucosa gastrointestinal, riñón, pared vascular) y, así, favorezca la recuperación de dichas células de los efectos deletéreos derivados de la inhibición de COX-2. Sin embargo, el uso de estos mismos fármacos en dosis altas puede eliminar estos beneficios.9
Elección de una alternativa analgésica eficaz y segura
El Colegio Americano de Reumatología, la Sociedad Española de Dolor, la Liga Europea contra el Reumatismo, la Sociedad Internacional para la Investigación en Osteoartritis y el Colegio Americano de Gastroenterología han publicado guías de tratamiento, intentando orientar a los clínicos en el uso de medicamentos analgésicos a largo plazo; para ello, han evaluado no sólo la eficacia en el alivio sintomático y el impacto en la calidad de vida y funcionalidad de los pacientes, también se han preocupado por los riesgos derivados de los efectos colaterales que presentan los consumidores de dichas terapias.2,3,7
La recomendación que estas sociedades hacen al ponderar el riesgo/beneficio es que, en caso de que la terapia antiinflamatoria mediante AINE sea en verdad necesaria o en los casos en que el dolor no ceda apropiadamente con dosis adecuadas de paracetamol,8 se deberá usar la dosis mínima efectiva de un AINE por el menor tiempo posible, con el propósito de limitar la frecuencia de efectos secundarios.2,3,9,10
De este modo, el riesgo de presentar efectos adversos relacionados a la terapia se vuelve una de las consideraciones con mayor relevancia e impacto clínico, por lo que no deberá tomarse a la ligera.
Repercusiones deletéreas de los AINE en el aparato gastrointestinal
Por mucho, los efectos gastrointestinales son los más frecuentes y se pueden presentar en un amplio espectro que va desde la dispepsia, malestar abdominal y pirosis, pasando por las erosiones de la mucosa gastrointestinal, úlceras, sangrado y obstrucción hasta la perforación;1 las cuales pueden ser causa o contribuir a la muerte de los pacientes.5
La razón de riesgo para eventos gastrointestinales con la toma de al menos cuatro días de AINEs, incluidas dosis bajas de ácido acetilsalicílico (ASA), va de 2.7-5.3 en los diferentes estudios,5 lo cual demuestra que no es sólo el tratamiento a largo plazo el que constituye riesgo de complicaciones, también ciclos cortos podrían ser nocivos en determinados pacientes vulnerables.12
De manera tradicional, se pensaba que las lesiones por AINE se presentaban sólo en el tubo digestivo alto (principalmente, estómago y duodeno);10 sin embargo, con el advenimiento de la tecnología con cápsulas videoendoscópicas se evidenció que los estragos se extendían mucho más allá del ligamento de Treitz. Estos hallazgos alentaron el desarrollo de nuevas drogas y estrategias que disminuyeran el riesgo gastrointestinal de los pacientes; aparecieron entonces los inhibidores selectivos de la COX-29 (coxib) y se adicionaron fármacos con efecto protector a la mucosa (inhibidores de la bomba de protones o IBP, antagonistas H2 y misoprostol) a la terapia analgésica convencional.2,13 El resultado fue una disminución significativa del número de eventos gastrointestinales en el tubo digestivo alto, pero que se acompañó de un despunte en la frecuencia de eventos en el tubo digestivo bajo (intestino delgado y colon), ya que el efecto antisecretor de los IBP no se extiende más allá del duodeno. El estudio VIGOR demostró que hasta 40% de los eventos gastrointestinal suceden en el tracto inferior.5
La enteropatía inducida por AINE no es un fenómeno pH-dependiente, sino que se debe a la supresión de la síntesis de prostaglandinas con efectos gastroprotectores (producción de moco y bicarbonato, favorecen la microcirculación entérica) en toda la extensión del tubo digestivo.5 A diferencia de las lesiones en el tubo digestivo alto, en la parte baja, los daños en la mucosa parecen estar influenciados por la ausencia de acidez y la presencia de bilis y bacterias gastrointestinales. Se ha propuesto que los IBP favorecen el daño a este nivel por propiciar la presencia de disbiosis.5
En distintas series se ha observado que independientemente del riesgo gastrointestinal que tengan los pacientes, sólo 30-60% se encuentran recibiendo gastroprotección; de éstos, un buen porcentaje tiene mal apego,2,5 por lo que sus posibilidades de presentar sangrado gastrointestinal casi se duplican en comparación con las de los pacientes que toman la medicación como se indica.5
Aquí radica la importancia de aprender a estratificar el riesgo en el que se encuentra cada paciente. Para ello es necesario identificar los factores de riesgo que se han asociado a un incremento del riesgo de complicaciones a nivel gastrointestinal; a partir de ello, se considerará que un paciente es de bajo riesgo cuando no cuente con ningún factor de riesgo, de riesgo intermedio cuando tenga uno o dos factores, y de riesgo alto cuando reúna tres o más y/o tenga historia previa de complicaciones por úlcera y/o tratamiento simultáneo con anticoagulantes2(Cuadro 2).
Cuadro 2 Factores de riesgo a considerar en el uso de anticoagulantes para la presentación de complicaciones.
Modificado de: Scheiman JM, Hindley CE. Strategies to optimize treatment with NSAIDs in patients at risk for gastrointestinal and cardiovascular adverse events. Clin Ther. 2010; 32 (4): 667-677.
Papel de los coxib en la reducción del riesgo gastrointestinal
En los estudios CONDOR y VIGOR se demostró que celecoxib también se asocia con un incremento del riesgo gastrointestinal en todo el tubo digestivo; sin embargo, éste es menos frecuente (RR 0.26-0.39) y de menor intensidad que con AINEns (antiinflamatorios no esteroideos no selectivos). El coxib es mejor tolerado aun cuando el AINEns se combine con IBP.2,5,11
Cabe señalar que la actividad de COX-2 promueve la curación de lesiones de la mucosa; por lo tanto, en pacientes que ya las presentan, el uso de un coxib podría retrasar su cura.9 A pesar de que la administración conjunta de un coxib con ASA atenúa su seguridad gastrointestinal,2 se sabe que la combinación de celecoxib con una dosis baja de ASA se asocia con un menor riesgo de eventos adversos en el tracto gastrointestinal superior, en comparación con AINEns más ASA a dosis bajas.5
Consideraciones adicionales
En pacientes con alto riesgo gastrointestinal, se recomienda otorgar protección adicional con IBP2(Figura 4).
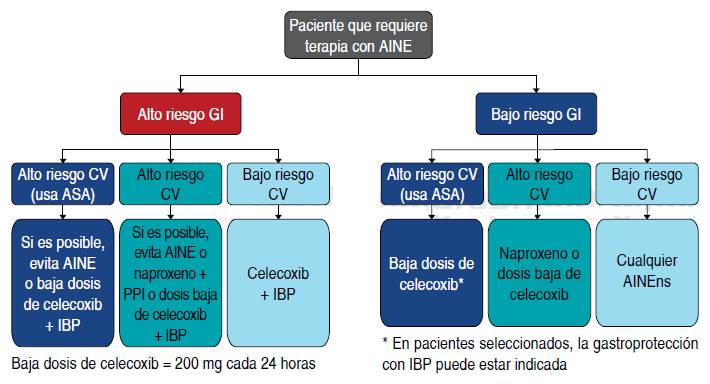
Se debe buscar, y de encontrarse presente, tratar la infección por H. pylori en pacientes con historia de úlcera péptica.
Traducido de: Scarpignato C, Lanas A, Blandizzi C, Lems WF, Hermann M, Hunt RH. Safe prescribing of non-steroidal anti-inflammatory drugs in patients with osteoarthritis- an expert consensus addressing benefits as well as gastrointestinal and cardiovascular risks for the International NSAID Consensus Group. BMC Med. 2015; 13: 55.
Figura 4 Algoritmo para el tratamiento con AINE de acuerdo con los factores de riesgo cardiovascular y gastrointestinal de los pacientes.
También es aconsejable tamizar y erradicar la infección por Helicobacter pylori en todos aquellos pacientes en quienes se planee iniciar un tratamiento con AINE y cuenten con riesgo gastrointestinal.2,5
Una vez que el paciente ha suspendido la terapia con AINE, deben pasar dos meses para que su riesgo retorne al basal.1
Efectos cardiovasculares de los AINE
La inhibición de COX-2 bloquea la producción de PGI2, la cual tiene efectos protectores cardiacos y del aparato circulatorio.12 Adicionalmente, se genera un desbalance en la relación tromboxano/prostaciclina, lo que disminuye los efectos benéficos derivados de la medicación cardiovascular (ASA, IECA y antagonistas de receptores de angiotensina II) y favorece la retención de agua y sodio, que puede contribuir al deterioro sintomático de pacientes con insuficiencia cardiaca.4
En lo que se refiere al riesgo de eventos cardiovasculares mayores (infarto al miocardio, angina, accidente vascular isquémico, trombosis venosa y/o arterial periférica), múltiples ensayos clínicos han documentado un incremento en el riesgo de hasta tres veces en aquellos pacientes bajo tratamiento con inhibidores selectivos de COX-2 en comparación con personas que no consumen AINEs.2,4,12
Sin embargo, cabe aclarar que no son sólo los coxib los que tienen este potencial proagregante y vasoconstrictor, se ha demostrado que en realidad es el radio de inhibición IC50 (concentración inhibitoria de COX al 50%) entre COX1/COX2, dado por las propiedades químicas del fármaco y la dosis empleada, el que determina el riesgo para cada fármaco; cuanto más cercana sea esta relación a 1.0, el fármaco tendrá una inhibición predominantemente sobre COX-1, y cuanto menor sea, la potencia inhibitoria por la isoforma 2 será mayor.9,12
En un metaanálisis se encontró que el riesgo cardiovascular de celecoxib era similar al de los AINEns, con excepción de naproxeno,5 que parece tener una mayor selectividad in vitro e in vivo por la isoenzima COX-1, por lo que podría ofrecer un efecto cardioprotector2 (potencia de inhibición similar al ASA a dosis de 1000 mg/día). El diclofenaco, a dosis mayores de la necesaria para alcanzar IC80:150 mg/día (el riesgo aumenta de manera lineal conforme se incrementa la dosis), parece poseer el perfil de mayor riesgo, con una frecuencia de eventos cardiovasculares asociados similar a la de etoricoxib, esto debido a su radio de selectividad, que se inclina en forma notoria hacia COX-2.9
En el estudio precisión, se aleatorizaron sujetos con osteoartritis o artritis reumatoide y factores de riesgo cardiovascular subyacentes para recibir tratamiento con celecoxib, ibuprofeno o naproxeno. Los resultados revelaron tasas similares de eventos cardiovasculares (muerte por causas cardiovasculares, que incluyen muerte hemorrágica, infarto de miocardio no mortal o accidente cerebrovascular no mortal) entre los tres grupos de tratamiento.14
Interacción con ASA
A pesar de que el consumo de dosis bajas de ASA se ha asociado claramente con riesgo de sangrado gastrointestinal, su uso como prevención secundaria (se requiere una inhibición de más del 95% de la producción de tromboxano dependiente de COX-1 para producir los efectos cardioprotectores) sobrepasa los riesgos, al reducir la frecuencia de eventos cardiovasculares y cerebrales en más de tres veces; no es así cuando se usa como prevención primaria.5
En estudios experimentales y clínicos se ha demostrado que el consumo intercurrente de dosis bajas de ASA (75 a 100 mg/día) y AINEns (excepto diclofenaco)5 podría interferir con el efecto antiagregante de ASA por una interacción competitiva a nivel farmacodinámico, en donde el otro AINE ocupa de manera temporal el sitio de unión para ASA en la COX-1, lo que impide la acción inhibitoria irreversible de ASA.2 Esto es muy importante, pues, contrario a lo que se pudiera pensar, el uso concurrente aumenta el riesgo de recurrencia de infarto, incluso durante tratamientos cortos. La interacción con naproxeno es más marcada cuando éste se toma antes de ASA que cuando se toma dos horas después (Figura 4).
Los AINE con vidas medias de más de 12 horas (ej., piroxicam, naproxeno y meloxicam) se han asociado con un riesgo cardiovascular mayor en comparación con los que duran menos de 12 horas, lo cual desalienta el uso de presentaciones de liberación prolongada y resalta la importancia de que los periodos entre las administraciones permitan que la concentración plasmática decaiga lo suficiente para permitir la recuperación del efecto protector de los derivados de COX-2.12
Se debe recordar que cuando el ASA se usa a dosis mayores que las recomendadas para profilaxis, tiene un comportamiento muy similar al resto de los AINEns.4
A diferencia de los AINEns, los coxib no interfieren con el efecto antiplaquetario de las dosis bajas de ASA5 ni prolongan el tiempo de sangrado, lo que los convierte en los analgésicos de elección (celecoxib 200 o 400 mg una vez al día, HR 1.1) en pacientes que se encuentran antiagregados con ASA como prevención de eventos cardiovasculares y cerebrales, en quienes la terapia antiinflamatoria es imprescindible y no se dispone de otra alternativa.5
Efectos renovasculares de los AINE
El riesgo de lesión renal no depende de si el paciente es usuario de AINEns o coxib, ya que la frecuencia de complicaciones a este nivel es similar entre ambos.7 En el Reino Unido se llevó a cabo un estudio de casos y controles que incluyó 386,916 individuos entre los 50 y 84 años, y se encontró que los principales determinantes para desarrollar falla renal asociada a AINE eran la preexistencia de hipertensión, falla cardiaca y diabetes, así como la dosis (riesgo relativo para lesión renal de 3.3 para las dosis altas, en comparación con 2.5 para las dosis menores) y la duración de uso;10 sin embargo, los estudios observacionales demuestran que incluso una terapia con duración menor de 14 días puede alterar la función renal y el daño se mantiene en el tiempo.12 De nuevo, se atribuye un papel importante a la vida media plasmática del fármaco, con una proporción de probabilidades (OR) de 1.1 para vidas medias menores de cuatro horas y de 2.6 para mayores de cuatro horas.12
Una interacción que resulta clínicamente relevante porque favorece la falla renal, sobre todo al inicio de la terapia, es el uso concomitante de AINE e inhibidores de la enzima convertidora de angiotensina (IECA). Esto ocurre como resultado de la sumación de los efectos vasoconstrictores de la arteriola aferente y vasodilatación de la eferente, que culmina en una reducción drástica del filtrado glomerular.4
En general, la combinación de AINE con diuréticos puede alterar el efecto en la excreción de agua y electrolitos, y de esa manera, interferir con su eficacia. Este mecanismo, aunado a un desbalance en la síntesis de prostaglandinas vasodilatadoras y vasoconstrictoras y al aumento de la endotelina-1, se ha propuesto como la explicación para los incrementos moderados de las cifras de presión arterial (sistólica y media) que se observan en algunos sujetos hipertensos y no hipertensos que se encuentran bajo tratamiento con AINE, en especial con coxib (excepto celecoxib). Se deberá tener precaución al iniciar un AINE en pacientes que tomen medicación antihipertensiva, ya que la interacción tiende a disminuir el efecto de estos últimos.4
Efectos de los AINE en la coagulación
El consumo de AINE únicamente no basta para alterar los tiempos de coagulación. Para que haya una prolongación en el tiempo de sangrado es necesaria la presencia de algún factor concomitante, como el uso crónico de alcohol, anticoagulantes/coagulopatías por otras causas, pacientes ancianos o enfermedad hepática.1,9
Conclusiones
Los profesionales de la salud -y sobre todo, los que nos dedicamos al tratamiento del dolor- tenemos la obligación de buscar que nuestros abordajes sean no sólo eficaces, sino seguros para los pacientes. Así, durante nuestra práctica cotidiana deberemos evaluar a todos aquellos pacientes que requieran terapia analgésica; en primer lugar, se debe determinar la necesidad de que el fármaco empleado posea propiedades antiinflamatorias que justifique el inicio de AINE; si es así, se deberá, entonces, evaluar cuidadosamente los factores de riesgo para eventos cardiovasculares y gastrointestinales de cada caso. Una vez hecho esto, se deberá considerar otras propiedades diversas, como la potencia del fármaco, radio COX-1/COX-2 IC50, propiedades farmacocinéticas y dinámicas, interacciones con otras drogas, consideraciones farmacoeconómicas y el impacto global que todas estas puedan tener en la tolerabilidad y seguridad del tratamiento. Una vez hecho este ejercicio, podremos hacer una elección dirigida a obtener el mayor beneficio para el enfermo.











 text new page (beta)
text new page (beta)


