Introducción
El tejido óseo es un tejido del cuerpo que asemeja un material compósito ya que contiene una fase inorgánica que combina componentes minerales que contienen fosfato, calcio y grupos hidroxilos (hidroxiapatita) y una fase orgánica compuesta principalmente de colágeno. Esta útil combinación de materiales permite que el hueso tenga, al mismo tiempo, resistencia y flexibilidad [1] [2].
La regeneración del tejido óseo se da de manera natural durante toda la vida, sin embargo, cuando existe una afección como fracturas, pérdida de masa ósea derivado de alguna enfermedad como tumores, degeneraciones o infecciones, donde el tejido ha sido destruido o removido lo cual llevan a que el hueso, en este caso, deje que cumplir la función vital de dar soporte y de permitir la comunicación bien protegida de la red nerviosa y la red sanguínea. Es necesario inducir o crear un tejido sustituto a través de la ingeniería de tejidos que cumpla las funciones vitales del tejido, esto es posible gracias a la compleja estructura a micro y nanoescala que presenta el hueso como material compósito bioactivo, mezcla de hidroxiapatita y colágeno [2] [3].
Un biomaterial para regeneración ósea debe cumplir la función de reemplazar al hueso dañado al tiempo que permita que continúe la funcionalidad de los tejidos que forman parte de él, como vasos sanguíneos y nervios. Más aún, es deseable que sea bioactivo, es decir que induzca la reparación natural del tejido óseo conocida como osteogénesis. Los compósitos basados en hidroxiapatita (HAp) son muy utilizados, combinados con un polímero que les aporte flexibilidad y resistencia mecánica [1].
La hidroxiapatita presente en los huesos tiene una composición similar a la HAp sintética, aunque se ha encontrado que esta última suele ser más frágil. Es un material cerámico que presenta una composición de Ca10(PO4)6(OH)2 y mantiene una relación molar de calcio a fósforo (Ca/P) de 1.67, En el tejido óseo, la HAp está presente en un 60% en forma de nanocristales [3]. Para que la HAp sintética pueda ser empleada en aplicaciones médicas es necesario que cumpla con algunas normas, por ejemplo, debe cumplir un grado mínimo de cristalinidad del 45% según la ISO 137779-2:2000, también debe ser ostoconductor, osteoinductivo y bioactivo [2], [4].
El colágeno (Col) es una de las principales proteínas estructurales del tejido conectivo de los vertebrados, constituye alrededor del 30% de sus proteínas totales ya que es el principal componente de tendones, piel, huesos, tejidos del sistema vascular entre otros tejidos [5].
Existen 29 variantes reportadas de colágeno [6], sin embargo, el colágeno tipo I es el componente principal de la matriz extracelular de mamíferos, contribuye a funciones fisiológicas únicas como la protección de tejidos y órganos, así como la regulación fisiológica del entorno celular para muchas especies animales [7]. Como característica principal del colágeno que está compuesto de una cadena de tres hélices, como unidad básica presenta las tres cadenas α que contienen una o más secuencias de polipéptidos (Gly-X-Y) y estas a su vez presentan entre 600 a 3,000 aminoácidos [1].
El colágeno es ampliamente usado en las industrias cosmetológicas, biomédicas, farmacéutica por su excelente biocompatibilidad, biodegradabilidad y baja antigenicidad [8], actualmente se ha extraído de piel y huesos de animales bovinos y porcinos. Sin embargo, ambos han presentado brotes de encefalopatía espongiforme bovina y encefalopatía espongiforme transmisible, es por ello que se pretende extraer el colágeno de animales que no tengan la capacidad de transmitir alguna enfermedad, por lo tanto, se ha optado por la obtención del colágeno a partir de animales marinos, ya que el colágeno tipo I es más común en piel, escamas, huesos y aletas de peces [9].
El presente artículo de revisión tiene como propósito mostrar los trabajos que se han reportado respecto a la extracción de HAp y de colágeno a partir de desechos de pescado, ya que esta recuperación puede ser una alternativa prometedora y amigable con el ambiente para obtener precursores de biomateriales compósitos para regeneración ósea.
Cronología
Colágeno
En los años noventas Kimura y colaboradores aislaron colágeno equinodermos indicando la presencia de colágeno fibrilar en la pared del cuerpo [10]. Unos años después Nomura y colaboradores extrajeron colágeno de escamas de sardina, obteniendo un rendimiento del 5%. En este estudio se propone que la etapa de desmineralización de las escamas es un paso importante para la recuperación del colágeno [7].
En el año 2000, Nagai y colaboradores [11] aislaron colágeno a partir de la piel, las aletas y los huesos del pescado. En su trabajo hacen mención de la escasa información disponible sobre la presencia de colágeno en tejidos calcificados de peces. Determinan que la temperatura de desnaturalización del colágeno obtenido de la piel de las diferentes especies de peces es de alrededor de 25°C, 10°C menos que el colágeno porcino, mientras que para el colágeno extraído de hueso de pescados es de 29°C. Más tarde, varios trabajos siguen la metodología de Nagai para extraer colágeno soluble en ácido y en pepsina a partir de escamas [5], [12], de entre los cuales destaca Jongjareonrak y colaboradores porque reporta rendimientos del 9 y 4.7% para colágenos solubles en ácido y en pepsina, respectivamente [5]. Posteriormente Dasong y colaboradores en 2012 extrajeron y caracterizaron colágeno soluble en pepsina obtenido de escamas, aletas, huesos y piel. Su trabajo es relevante porque describe detalladamente la metodología que siguieron, mencionando las diferencias de solubilidad en las reacciones de extracción del colágeno obtenido de escama y hueso contra el obtenido de piel. Dos años después Dasong compara el colágeno soluble en ácido obtenido de la piel y escamas de cuatro tipos de carpas, observando diferencias en la presencia y concentración de las cadenas α, mostrando tres cadenas α1, α2 y α3, y no solo dos como se había reportado anteriormente [8].
Más recientemente Chuaychan y colaboradores aislaron colágeno soluble en pepsina (PSC) y colágeno soluble en ácido (ASC) a partir de escamas y siguiendo la metodología establecida por Nagai; sin embargo, reportan rendimientos mucho menores (0.38% ASC, 1.06% PSC) [9]. Wang y colaboradores logran extraer colágeno tipo I soluble en ácido y en pepsina con rendimientos de alrededor del 20% de piel de lochas nativas de Asia, postulando a este procedimiento como una buena alternativa al colágeno extraído de mamíferos. Finalmente Bhuimbar y colaboradores reportaron la extracción de colágeno soluble en ácido láctico proveniente de la piel de la medusa y muestran su potencial, junto con quitosano, como antibacterial [13].
Hidroxiapatita
Wen-Kuang Liu et al. extrajeron hidroxiapatita a partir de escamas para emplearla en la remoción de iones de plomo en aguas residuales.[14] Ulfyana y su equipo aislaron hidroxiapatita de las escamas de pescado reportando un rendimiento de la obtención de calcio de 83.62% y 12.7% de fosfato. Contemplaron que la HAp debía cumplir un grado de cristalinidad mínimo del 45% para poder ser un material empleado en el área de los biomateriales, realmente de la escama sólo obtuvieron el precursor de HAp que es el óxido de calcio (CaO), para obtener la hidroxiapatita se añadieron ácido fosfórico e hidróxido de amonio.[4] Más recientemente, Wibison y colaboradores describen la obtención de precursores de un material con fases secundarias de β-TCP para la HAp de las escamas, éste estudio lo realizaron a partir de escamas de nemátodos y conchas de cangrejo por métodos húmedos [15].
Compósitos HAp/colágeno
Sasmal y Begam sintetizaron un material compósito de hidroxiapatita/colágeno, extrajeron el colágeno a partir de piel de un pescado y posteriormente elaboraron el compósito por método químico húmedo.[16] Yoruc y colaboradores sintetizaron el compósito de HAp/col, utilizando colágeno tipo I de origen bovino y los precursores de HAp a través del método de precipitación.[17] Posteriormente Yoruc y colaboradores sintetizaron un compósito de HAp/β-fosfato tricalcio/colágeno (HAp/ β-TCP/Col), ellos aislaron el fosfato de calcio y el colágeno de escamas obteniendo una concentración en porcentaje de peso para el calcio igual a 31.8% y 20% en peso del fosfato [18]. Recientemente Chai y colaboradores reportaron la comparativa de dos procesos de elaboración de estructuras híbridas de colágeno/hidroxiapatita, en uno de los experimentos colocaron moléculas de colágeno (Col-M/HAp) y en el otro colocaron fibras de colágeno (Col-F/HAp), con el objetivo de conocer los procesos de auto organización de las estructuras híbridas con la finalidad de comprender mejor el mecanismo de formación de los tejidos óseos [19].
Métodos
Extracción de colágeno a partir de piel de pescado
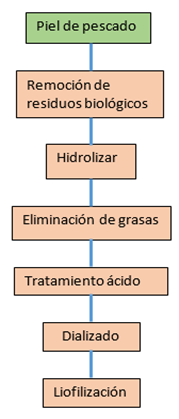
Para la obtención de colágeno soluble en ácido y soluble en pepsina, Nagai y colaboradores han establecido las bases de la metodología que se continúa empleando en estudios recientes (Figura 1). Hacen énfasis en mantener la piel a 4°C durante la extracción para evitar desnaturalizar el colágeno. Proponen un tratamiento previo de cortado de la piel y lavado, a continuación la hidrólisis o remoción de proteínas no colagenosas y la eliminación de grasas suspendiendo los residuos anteriores en una solución de alcohol butílico. Posteriormente proceden con el tratamiento ácido para obtener colágeno soluble en ácido, o en una solución de ácido más pepsina para obtener colágeno soluble en pepsina. Después de precipitar, realizan la diálisis y la liofilización del colágeno [11].
Extracción de colágeno a partir de escamas
La extracción de colágeno a partir de las escamas de pescado ha sido reportada por Dasong et al., cuya metodología ha sido citada por trabajos más recientes (Figura 2).
Este grupo propone seguir los mismos pasos reportados por Nagai[11] para la extracción de colágeno a partir de piel, añadiendo algunas modificaciones en la concentración de las soluciones y sustituyen la eliminación de grasa en piel por la descalcificación de escamas [20].
Extracción de HAp a partir de escamas
Ulfyana y colaboradores han descrito recientemente una metodología para extraer precursores de HAp de las escamas del pescado (Figura 3). En ella incluyen como primer paso la remoción de todo residuo biológico no deseado, para posteriormente ser sometidas a hidrólisis, esterilización, secado y calcinación.
Con ello se obtiene el óxido de calcio como precursor de la HAp. Posteriormente vierten un una solución el óxido de calcio con el precursor de fosfato (ácido fosfórico), una vez mezclados estos componentes, se continúa con los tratamientos mecánico y térmico que permiten obtener la HAp [4].
Síntesis de compósito HAp/Col
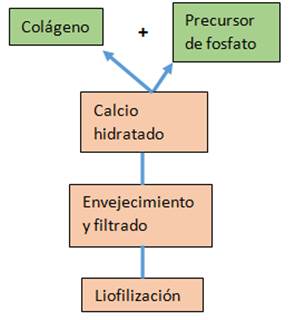
En cuanto a la síntesis del material compósito (Figura 4), Sasmal y Begam propusieron la obtención del mismo a través del método de precipitación que consiste en mezclar el colágeno con el precursor de fosfato y por adición incorporar el calcio hidratado, posteriormente dejar envejecer el material, filtrar y liofiizarlo [16].
Caracterización y cuantificación de colágeno extraído
Para confirmar la presencia de colágeno tipo I en el material extraído de piel o escamas, como se describió en las Figuras 1 y 2, se suelen utilizar técnicas de caracterización fisicoquímica tales como Electroforesis de Gel (para determinar qué tipo de colágeno se tiene), espectroscopía infrarroja con transformada de Fourier (FT-IR) (para ver los enlaces característicos del material en cuestión), espectrofotometría UV-visible (verificar la presencia del compuesto/material) y BET (determinación de área superficial, porosidad del material). Todas estas técnicas detectan la presencia de las cadenas α1 y α2, y de las bandas amida que son características del colágeno tipo I [6] [8].
En cuanto a la caracterización de la HAp se emplean técnicas fisicoquímicas como difracción de rayos-x (XRD) para determinar la estructura cristalina y con ello el grado de cristalinidad, FT-IR para identificar los grupos funcionales característicos de la HAp, microscopía electrónica de barrido (SEM) para analizar la morfología del material, espectrometría de energía dispersiva (EDS) para cuantificar la presencia de los elementos presentes en la muestra, entre otras técnicas [21].
Discusión
Como se muestra en la Tabla 1, los diferentes autores que han extraído colágeno a partir de residuos de pescado han encontrado diferencias en los rendimientos de colágeno obtenido, esto podría deberse, en parte, a las diferentes especies de pescado utilizadas así como a la metodología y cuidado de la temperatura durante la extracción. Se debe tener en cuenta la observación que realiza Nagai [11] respecto a la temperatura de desnaturalización del colágeno respecto al lugar de origen de los peces ya que él hace referencia sobre que el colágeno obtenido de los peces que viven en aguas más frías tiene una temperatura de desnaturalización menor que los que viven en aguas más cálidas. Además como lo comenta Jongjareonrak [5], la cantidad de colágeno aislada también varía con la edad y temporada en la cual se adquirió el pez.
Tabla 1 Rendimiento de la extracción de colágeno.
| REG. | PESCADO | REND. % | REF | ||
| ASC | PSC | ||||
| Asia | Sardina | Escama | -- | -- | [7] |
| Asia | Lateolabrax japonicus (Lubina japonesa) | Piel Huesos Aletas |
51.4 40.7 5.2 |
-- -- -- |
[11] |
| Asia | Scomber japonicus (estornino) | Piel | 49.8 | -- | |
| Asia | Heterodontus (tiburón toro o bullhead shark) | Piel | 50.1 | -- | |
| Asia | Katsuwonus pelamis (listado) | Hueso | 42.3 | [11] | |
| Asia | Pagrus major (pargo japonés) | Escama | -- | 2 | [12] |
| Asia | Oreochromis niloticus (tilapia del nilo) | Escama | -- | ||
| Asia | Sardina | Escama | -- | 50.9 | [22] |
| Asia | Lateolabrax japonicus (Lubina japonesa) | Escama | -- | 41 | |
| Asia | Pagellus bogaraveo | Escama | -- | 37.5 | |
| Asia | Lutjanus vitta (pargo) | Piel | 9 | 4.7 | [5] |
| Asia | Siganus fuscescens (pez conejo) | Piel | 3.6 | -- | [23] |
| Asia | Kyphosus bigibbus (carpa marrón) | Piel | 3.6 | -- | |
| Asia | Myliobatis tobijei | Piel | 3.5 5.7 |
--- | |
| Asia | Dasyatis akajei | Piel | |||
| Asia | Dasyatis laevigata | Piel | |||
| Europa | Cyprinus carpio (carpa) | Piel Escama Hueso |
41.3 1.35 1.06 |
-- -- -- |
[24] |
| Asia | Parupeneus heptacanthus | Escama | 0.46 | 1.2 | [25] |
| Asia | Pangasianodon hypophthalmus (pez gato) | Piel | 5.1 | 7.7 | [26] |
| Asia | Istiophorus platypterus (pez vela) | Piel | 5.7 | 2.1 | [27] |
| Asia | Lates calcifer (barramundi) | Escama | 0.38 | 1.06 | [9] |
| Asia | Ctenopharyngodon idella (carpa herbívora) | Piel Escama Aleta |
-- -- -- |
-- -- -- |
[28] |
| Asia | Oreochromis niloticus (tilapia del nilo) | Escama Piel |
3.2 27.2 |
-- -- |
[29] |
| América del sur | Oreochromis ssp (tilapia roja) | Escama
Piel Hueso |
6.5 15.5 5.6 |
-- -- -- |
[30] |
| Asia | Dover sole | Piel | 19.2 | -- | [31] |
REG: Región de origen del pescado.
REND: Rendimiento de la extracción de colágeno.
REF: Referencia.
ASC: Colágeno soluble en ácido.
PSC: Colágeno soluble en pepsina.
Aún con algunas de las observaciones realizadas por los grupos de investigación sobre los rendimientos obtenidos de colágeno es importante destacar que la variabilidad del rendimiento es grande con respecto a los datos reportados por Nagai. Para poder obtener rendimientos con una variabilidad mínima es necesario establecer una metodología que sea aplicada para la mayor parte de los peces o incluso hacerlas para aquellos que cumplan la mayor cantidad de características de una población, lo que ayudaría a conocer con mayor exactitud el rendimiento promedio de la extracción de colágeno a partir de los residuos de pescado y de esta manera poder equipararlo e incluso competir con el colágeno obtenido de animales bovinos y porcinos y con ello poder incrementar su aplicación en el área médica y evitando la potencial transmisión de enfermedades que conlleva la utilización de colágeno bovino y porcino.
Debido a la literatura consultada referente al material compósito HAp/colágeno a partir de desechos de pescado, se ha observado que existe información limitada sobre este tema, lo cual indica que es un área con gran potencial de investigación para la obtención de materiales que son recuperados de residuos.
Conclusiones
La recuperación de materiales, tales como el colágeno y la HAp, a partir de desechos de pescado, es una alternativa importante con impacto positivo para el medio ambiente y para la fabricación de biomateriales de baja toxicidad y mayor biocompatibilidad, con potencial uso médico, en particular para la regeneración ósea.











 text new page (beta)
text new page (beta)