Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista internacional de contaminación ambiental
Print version ISSN 0188-4999
Rev. Int. Contam. Ambient vol.31 n.2 Ciudad de México Aug. 2015
Concentración total y geodisponible de elementos potencialmente tóxicos en suelos volcánicos con uso agrícola del Nevado de Toluca, México
Total concentration and geoavailability of potentially toxic elements in volcanic soils with agricultural use in the Nevado de Toluca, Mexico
Germán Martínez-Alva1, Margarita Eugenia Gutiérrez-Ruiz2, Ángel Roberto Martínez-Campos1, Rafael Villalobos-Pietrini3 y Tizbe T. Arteaga-Reyes1*
1 Instituto de Ciencias Agropecuarias y Rurales, Universidad Autónoma del Estado de México, El Cerrillo Piedras Blancas, Toluca, Estado de México, CP 50090, México*Autor de correspondencia: tizbe@hotmail.com
2 Facultad de Química, Universidad Nacional Autónoma de México, Ciudad Universitaria, México DF 04510, México
3 Centro de Ciencias de la Atmósfera, Universidad Nacional Autónoma de México, Ciudad Universitaria, México DF 04510, México
Recibido junio 2014;
aceptado enero 2015
RESUMEN
En el Nevado de Toluca, México el uso indiscriminado de agroquímicos para la producción de alimentos ha generado impactos negativos en el suelo, como cambios en sus propiedades físicas, químicas y bioquímicas, lo que representa un riesgo potencial para la salud humana y el ambiente. El objetivo del presente estudio fue evaluar la concentración total y geodisponible de los elementos potencialmente tóxicos (As, Pb, Cd, Zn, Cu y Fe) en suelos agrícolas del Nevado de Toluca en los que se practica agricultura intensiva, semi-intensiva y tradicional. La evaluación de la concentración de los elementos potencialmente tóxicos se realizó por espectroscopia de emisión atómica por plasma de acoplamiento inductivo. En el caso del As, por espectroscopia de absorción atómica con generación de hidruros. Los resultados indican que en los suelos en los que se practica agricultura intensiva y semi-intensiva existe una mayor concentración total (mg/kg) de elementos potencialmente tóxicos que en los suelos en los que se practica agricultura tradicional. En algunos elementos potencialmente tóxicos se observó un aumento evidente en su geodisponibilidad (mg/L), no obstante que las concentraciones en términos absolutos son bajas. El uso no controlado de agroquímicos es un factor de degradación de los suelos agrícolas del Nevado de Toluca ya que modifica sus propiedades físicas y químicas, principalmente en los que se practica la agricultura intensiva y semi-intensiva para el cultivo de papa. La adición de agroquímicos ha causado una fuerte acidificación (pH = 2.8 - 4.2) y consecuente intemperismo acelerado de las arcillas, que ha favorecido la reducción de la capacidad de intercambio catiónico, la disminución de la materia orgánica y el aumento de la conductividad eléctrica. Por tanto, los resultados de este estudio evidencian el riesgo ambiental (calidad de suelos) y a la salud humana en el largo plazo por el abuso de agroquímicos.
Palabras clave: agroquímicos, contaminantes, estrategias agrícolas.
ABSTRACT
The indiscriminate use of agrochemicals for food production in the Nevado de Toluca, Mexico, has caused negative impacts on the soil, including changes in its physical, chemical and biochemical properties, which implies a potential risk to human health and the environment. Therefore, the objective of the current study was to evaluate the total and geoavailable concentrations of potentially toxic elements (As, Pb, Cd, Zn, Cu and Fe) in agricultural soils of Nevado de Toluca where intensive, semi-intensive and traditional agriculture are practised. Inductively coupled plasma atomic emission spectroscopy was applied to the determination of concentrations of potentially toxic elements. Determination of total arsenic levels was carried out by hydride generation atomic absorption spectrometry. Results show that soils where intensive agriculture and semi-intensive agriculture are practised, total concentration (mg/kg) of potentially toxic elements is greater than in those soils of traditional agriculture. In some of the potentially toxic elements it was observed an evident increase of their geoavailability (mg/L), even though such concentrations are low in absolute terms. The uncontrolled use of agrochemicals is a factor of degradation in agricultural soils of Nevado de Toluca since it modifies their physical and chemical properties, mainly in soils where intensive agriculture and semi-intensive agriculture are practised to cultivate potatoes. The addition of agrochemicals has caused a severe acidification (pH = 2.8 - 4.2) and consequently an accelerated weathering of clay, which has favoured the reduction of the cationic exchange capacity, the decreased organic matter content and the increase of electrical conductivity. Hence, the results of this study demonstrate environmental (soil quality) and human health risks in the long run due to the abuse of agrochemicals.
Key words: agrochemicals, contaminants, agricultural strategies.
INTRODUCCIÓN
El manejo irracional de los recursos naturales y el manejo inadecuado de los residuos generados por los diferentes procesos antrópicos están condicionando el estado de conservación de recursos como el agua y el suelo (Tchobanoglous et al. 1998, Doménech 2000). Esta problemática se ha observado en el Nevado de Toluca (NT), el cual forma parte del Sistema Nacional de Áreas Naturales Protegidas de México (CONANP 2008). El NT se localiza en el centro de México y forma parte del sistema montañoso suroccidental del Valle de Toluca (CONAGUA 2008). Esta zona se caracteriza por presentar bosques de alta montaña y en ellos se ha observado la degradación de la calidad del aire, de los cuerpos de agua y del suelo, así como una disminución en la densidad del arbolado, pérdida de la biodiversidad genética y ecosistémica y proliferación de plagas y enfermedades (CONANP 2008).
Las principales causas que se asocian al deterioro del NT son: el crecimiento de la población del Valle de Toluca, los cambios de uso del suelo, la extracción de recursos forestales maderables y no maderables, el sobrepastoreo y la agricultura (Franco et al. 2006). Sin duda alguna, la agricultura ha generado un mayor impacto en el agua, el suelo y la atmósfera debido al uso intensivo de agroquímicos, en especial plaguicidas y fertilizantes que contienen elementos potencialmente tóxicos (EPT). No obstante los agroquímicos proporcionan algunos elementos que son esenciales para las plantas, en exceso resultan tóxicos. Por ejemplo, los plaguicidas contienen oxicloruro e hidróxido de cobre y los fertilizantes proporcionan sulfatos y quelatos de zinc, hierro, aluminio, manganeso y cobre (Cheng 1990, Benítez y Bárcenas 1996, Hernández et al. 2006).
Los plaguicidas son "sustancias o mezclas de sustancias que tienen la finalidad de prevenir, destruir, controlar o repeler plagas, incluidos los vectores de enfermedades humanas y de animales, así como las especies no deseadas que dañan o interfieren con la producción agropecuaria y forestal" (USEPA 2010). Los fertilizantes son sustancias que incrementan el potencial productivo de los cultivos debido a la incorporación de nutrimentos para la plantas (Ferrer 2003). La aplicación controlada de agroquímicos (plaguicidas y fertilizantes) es una medida muy aceptada ya que permite aumentar el potencial productivo de los cultivos (Mansour 2004), razón por la que esta industria se ha desarrollado vertiginosamente. Sin embargo, en la búsqueda de nuevos productos de este tipo se han desarrollado compuestos tóxicos persistentes que están comprometiendo la salud de las personas expuestas durante la producción y aplicación de agroquímicos e inclusive de las que consumen los productos alimenticios obtenidos (Haro et al. 2002, Bolognesi 2003, Garry 2004, Waliszewski et al. 2004, Bull et al. 2006, Cavallo et al. 2006, Ismail et al. 2008). Dichos compuestos al transportarse en el ambiente pueden convertirse en un factor de contaminación del suelo, de cuerpos de agua superficial y profunda, de sedimentos y de la atmósfera (Cheng 1990, Bain et al. 2000, Armienta et al. 2001, Jung 2001, Moral et al. 2002, Albert 2005, Wong et al. 2008). El transporte de los elementos que constituyen a los agroquímicos se debe principalmente a la infiltración o erosión de los suelos, aunque también pueden movilizarse por transporte atmosférico o por escurrimiento durante lluvias o riego agrícola (On-gley 1996, Kishida et al. 2007, Wong et al. 2008).
La contaminación de los recursos primarios (agua, suelo, atmósfera) con agroquímicos (plaguicidas) que contienen EPT está ampliamente documentada a nivel internacional. En aguas superficiales destacan los trabajos de Caldas et al. 1999, Thurman et al. 2000, Golfinopoulos et al. 2003, Fytianos et al. 2006, Gilliom 2007, Malla et al. 2007, Chen et al. 2008 y Prieto et al. 2009. En agua de lluvia los de Coupe et al. 2000 y Dubus et al. 2000. En sedimentos los de Daniels et al. 2000, Barakat et al. 2002, Hong et al. 2008 y Hoai et al. 2010. En suelos agrícolas los de Jung 2001, Fytianos et al. 2001, Ho y Egashira 2001, Moor et al. 2001, Ramos-Bello et al. 2001 y Davor 2005. Sin embargo, en México son relativamente escasos los estudios sobre la contaminación de estos recursos por el uso de plaguicidas y prevalecen los estudios que se refieren a la contaminación de los recursos por organoclorados (Rueda et al. 1997, Gutiérrez et al. 1998, Hernández-Romero et al. 2004, Alegría et al. 2006, Ramírez et al. 2008).
La problemática más evidente de los agroquímicos a base de metales como As, Pb, Cu, Cd, Zn, Fe, Mg y Mn radica principalmente en que pueden ser acumulados en los suelos, especialmente en los agrícolas que son acondicionados con material orgánico de diferente origen (Corinne et al. 2006). Algunos de estos metales, por ejemplo el Cu, pueden formar complejos relativamente solubles con ligantes orgánicos aumentando su geodisponibilidad. En casos de largos periodos de aplicación en suelos con bajos contenidos de fosfatos y arcillas se han contaminado e inclusive han afectado los cultivos (Cordero y Ramírez 1979). Cuando se supera la capacidad de retención de un suelo y pierde su capacidad de inmovilizar los contaminantes mediante procesos de adsorción y precipitación, se puede convertir en un factor de riesgo potencial para cuerpos de agua y en consecuencia, para la salud humana y la biota (Li y Shuman 1996, Virkutyte et al. 2002, Mahler 2003, García y Dorronsoro 2005, Corinne et al. 2006).
Al tomar en cuenta los posibles impactos negativos reportados en estudios previos por el uso inadecuado o excesivo de plaguicidas y de los fertilizantes en suelos agrícolas, se realizó el presente estudio en el NT donde destaca la aplicación de agroquímicos que contienen EPT para el cultivo de la papa (Solanum tuberosum). El objetivo consistió en evaluar la concentración total y geodisponible de los EPT en tres tipos de prácticas agrícolas de la zona (agricultura intensiva, semi-intensiva y tradicional). Según Davor (2005) las propiedades de cada una son: i) agricultura intensiva (A-I), se caracteriza por el abuso del uso de los agroquímicos (generalmente se incorpora más del doble de la dosis señalada en la etiqueta), por los altos rendimientos productivos, por la nula incorporación de materia orgánica (MO), por la nula rotación del cultivo y por el alto laboreo mecanizado, ii) agricultura semi-intensiva (AS-I), se caracteriza por el uso de agroquímicos (generalmente se respeta la dosis señalada en la etiqueta), por los rendimientos moderados en la producción, por el aporte ocasional de MO, por la ocasional rotación del cultivo y por el moderado laboreo mecanizado, iii) agricultura tradicional (A-T), se caracteriza por la nula o casi nula incorporación de agroquímicos, por los rendimientos moderados de la producción (generalmente menores a los de la AS-I), por el aporte frecuente de MO, por la rotación de cultivos y por el moderado laboreo con herramientas de tracción animal o manual.
MATERIALES Y MÉTODOS
Descripción del área de estudio
La extensión del NT es de 46 784 ha, está ubicado en el sureste del Valle de Toluca, Estado de México, México dentro de la provincia fisiográfica denominada Sistema Neovolcánico Transversal entre las coordenadas geográficas 18°51'31'' y 19°19'03': de latitud Norte y 99°38'54'' y 100°09'58'' de longitud Oeste (CONANP 2008). Esta zona incluye los municipios mexiquenses de Almoloya de Juárez, Amanalco de Becerra, Calimaya, Coatepec Harinas, Temascaltepec, Tenango del Valle, Texcaltitlán, Toluca, Villa Guerrero, Villa Victoria y Zinacantepec (GEM 2011; Fig. 1).
El rasgo geográfico más representativo es el volcán NT o Xinantécatl, que alcanza una altura máxima de 4680 msnm. Debido a su geomorfología y a su rango altitudinal (mayor a 3000 msnm), descienden numerosos arroyos que contribuyen al origen de las cuencas del río Lerma-Chapala-Santiago al norte y al oriente, y del río Balsas al sur y al occidente (CONAGUA 2008). Cerca de 50 arroyos permanentes descienden del NT en sus cuatro direcciones. Estos cuerpos de agua albergan una alta biodiversidad debido a factores como la humedad, la conformación topográfica del área y el tipo de vegetación que se establece a las orillas de los cauces (CONABIO 2004).
De acuerdo con su formación geológica (roca encajonante "caolinita-pirita") y a los criterios de clasificación FAO-UNESCO, el NT se caracteriza por tener suelos de tipo Andosol Úmbricos, Rego-sol Eútricos y Feozem. El clima predominante es frío en la cima del volcán, semifrío en las laderas con régimen de lluvias en verano y subhúmedo y templado con lluvias en verano en los límites inferiores. La temperatura media anual oscila entre 2 y 7 °C y registra precipitaciones entre los 700 y 1000 mm anuales aproximadamente (CONANP 2008). El principal cultivo en el NT es la papa, cultivo que en general requiere el uso de agroquímicos de una amplia naturaleza química (Franco et al. 2006).
Los valores de fondo que se consideraron en la discusión son los propuestos por Gutiérrez-Ruiz et al. (2009) que se establecieron para la elaboración de un Mapa Regional de Valores de Fondo de EPT en Suelos de México (Cuadro I y II).


Muestras y análisis de laboratorio
Los sitios de muestreo se ubicaron por medio de un GPS conforme al sistema que utiliza actualmente el Instituto Nacional de Estadística, Geografía e Informática (INEGI) de México, en coordenadas UTM - WGS84. Dichos sitios se seleccionaron de acuerdo con la dirección del viento y del agua, que fluyen del norte al sur y son las vías de dispersión de los suelos.
Se muestrearon en total 30 parcelas que se usan para el cultivo de papa según los criterios propuestos por Davor (2005) para la identificación de la estrategia agrícola de las parcelas muestreadas.
En cada una de las 30 parcelas, se tomaron 10 muestras simples que se mezclaron para formar una única muestra compuesta por parcela. De esta manera fueron analizadas 30 muestras compuestas, 10 por cada estrategia agrícola (A-I, AS-I y A-T). Las muestras de suelo se tomaron en agosto de 2011 siguiendo los criterios que establece la Norma Mexicana NMX-AA-132-SCFI-2006 en el horizonte Ap (0-25 cm), con una pala de punta hecha de aluminio (la cual era lavada con agua corriente y secada con papel secante después de la toma de cada muestra para evitar la contaminación cruzada) en una distribución de tresbolillo (500 g de muestra aproximadamente).
Las muestras se embalaron en bolsas de plástico herméticas, se etiquetaron y se transportaron al laboratorio donde se secaron en horno a 90 °C durante 48 h. Se retiraron piedras, hojas y otros materiales que no eran suelo. Se cuartearon y se dividieron en dos partes iguales: una se resguardó como "retenido original" y el resto del suelo se utilizó para las evaluaciones. El suelo a evaluar se molió con un mazo de madera cubierto con plástico y posteriormente se tamizó a través de una malla del número 10 (2000 pm) para los análisis físicos y químicos.
En todas las muestras se determinaron las siguientes propiedades edáficas: textura (Bouyoucos 1963), pH en agua en relación suelo-solución 1:2.5 y pH en KCl (Mc Lean 1982), conductividad eléctrica (CE) en relación sólido-agua de 1:5, porcentaje de MO (Walkey y Black 1947) y capacidad de intercambio catiónico (CIC) por el método de acetato de amonio (Chapman 1965).
Los análisis de las concentraciones totales y geodisponibles de los EPT de interés (As, Pb, Cd, Zn, Cu y Fe, por ser los elementos indicados con alta frecuencia en las etiquetas de los agroquímicos empleados en la producción de papa) se realizaron en el caso del As, por espectroscopia de absorción atómica con generación de hidruros (AA-GH) y para los otros elementos (Pb, Cd, Cu, Zn y Fe) por espectroscopia de emisión atómica por plasma de acoplamiento inductivo (ICP-AES).
Las concentraciones de referencia que se consideraron para definir la situación de los EPT en este estudio son las que establece la Norma Oficial Mexicana NOM-147-SEMARNAT/SSA1-2007.
El procedimiento de digestión ácida se realizó de acuerdo con lo indicado en la Norma Oficial Mexicana NOM-147-SEMARNAT/SSA1-2007 para la extracción del elemento total. Se tomaron por cuarteo aproximadamente 5 g de muestra y se trituraron en un sistema de molino de bolas de óxido de zirconio. La muestra molida se pasó por malla 100 (tamaño de partícula <149 (μm). De esta muestra se pesaron aproximadamente 0.5 g por triplicado dentro de vasijas de teflón para microondas. Se preparó un blanco y un blanco adicionado, también por triplicado. Al blanco adicionado se le añadieron 0.5 mL de una disolución estándar de 100 ppm de Ag, Al, As, B, Ba, Be, Bi, Ca, Cd, Co, Cr, Cu, Fe, Ga, In, K, Li, Mg, Mn, Na, Ni, Pb, Se, Tl, V y Zn. Posteriormente se adicionaron a cada muestra 10 mL de HNO3 concentrado. El sistema se dejó abierto durante una hora para permitir que las reacciones entre el ácido nítrico y los carbonatos de la muestra concluyeran. De ese modo se evitó la formación de CO2 durante la digestión. Se cerraron las vasijas y se colocaron en un soporte estilo carrusel. En la primera etapa de la digestión se elevó la temperatura hasta 175 ºC durante 20 min a una potencia de 400 W. La segunda etapa consistió en mantener la misma temperatura durante 15 min adicionales. Finalmente se dejaron enfriar las vasijas por 24 h. Una vez terminada la digestión, las muestras se filtraron con papel Whatman No. 42 y se aforaron a 100 mL con agua desionizada.
Para la extracción del elemento geodisponible, las muestras se dejaron a saturación durante 24 h con agua desionizada, posteriormente se filtraron y aforaron a 25 mL y se tomó una alícuota de esta disolución para su análisis espectroscópico.
Los valores de las muestras duplicadas indicaron que la repetibilidad varía entre 3 y 9 %.
Adicionalmente, se realizó un análisis de varianza y una prueba de Tukey (P < 0.05) de los EPT por tipo de agricultura con el paquete estadístico SAS (SAS, Institute, Inc. 1988), de acuerdo con el diseño experimental.
RESULTADOS Y DISCUSIÓN
Propiedades físicas y químicas
Los resultados de las propiedades físicas (textura) y químicas que se determinaron en los suelos agrícolas del NT se presentan en el cuadro III y IV respectivamente, considerando las tres estrategias de producción que se practican en la zona de estudio: A-I, AS-I y A-T.


Los suelos estudiados se clasifican texturalmente como francos por su contenido semiequilibrado de arena, limo y arcilla (FAO 1990). Sin embargo, debido a la intemperización de las arcillas, específicamente resultan franco-arenosos (Cuadro III).
Los suelos son eminentemente ácidos (Cuadro IV). Sin embargo, en los que se practica A-I y AS-I (pH= 3.1 en ambos casos) fueron aún más ácidos respecto a los suelos en los que se practica A-T (pH= 4.0). Estos valores de acidez son menores que el valor mínimo reportado como valor de fondo para los suelos de México que es de pH = 4.3 (Cuadro I).
Es importante resaltar que los suelos en los que se practica A-T presentan un valor de pH de 4.0, el cual es similar al pH de 4.3 de los suelos más ácidos no afectados por actividades antrópicas (Cuadro I) y al de otros suelos agrícolas ácidos de zonas volcánicas (Ramos-Hernández y Flores-Román 2008). Esto podría indicar que el uso de agroquímicos es el factor determinante que está acidificando los suelos en los que se practica A-I y AS-I, ya que los sulfatos de metales que contienen los agroquímicos se hidrolizan al liberar protones. Asimismo, cuando la acidez aumenta, elementos como el Al quedan disponibles lo cual provoca que este metal forme junto con el agua (presente en los horizontes superficiales) un complejo de esfera interna muy estable y el producto de su hidrólisis es un ácido moderadamente fuerte con pKa de 4, lo que aumenta claramente la acidez. También se podría deducir que esta acidez está relacionada con el origen volcánico de los suelos (andosoles) o a que esporádicamente reciben agroquímicos que contienen sulfatos ácidos.
La acidificación (como en el caso de los suelos en los que se practica A-I y AS-I), provoca la intemperización acelerada de la arcilla (por la sustitución de los cationes básicos por protones) y la disminución de la MO, lo que genera la disminución de la CIC del recurso, la pérdida de su capacidad de adsorción y el aumento de la CE, ya que se solubilizan cationes. Esto sucede especialmente en los suelos en los que se practica A-I que presentan una triple carga derivada del aporte consistente de cloruros y sulfatos de amonio y potasio, entre otros. Los valores de CE en los suelos en los que se practica A-I (399 pS/cm) y AS-I (367 pS/ cm) fueron significativamente más altos que los valores de los suelos de vocación tradicional (250 pS/cm), los cuales estuvieron alrededor del valor promedio de fondo de 255 pS/cm para suelos de México (Cuadro I). Se asume que dicha diferencia se debe a que en los suelos en los que se practica A-T no se incorporan agroquímicos que modifiquen su CE.
El porcentaje de MO en los suelos varía significativamente dependiendo del tipo de agricultura que se practica (Cuadro IV). Los valores más altos corresponden a los suelos con prácticas de A-T (MO = 9.33 %), que se caracterizan por colindar con las zonas boscosas. Los valores intermedios corresponden a los suelos en los que se practica AS-I (MO = 7.21 %) y finalmente los valores notablemente menores son los de los suelos que se usan para la A-I (MO = 1.79 %). La carencia de buenas cantidades de MO en los suelos en los que se practica AS-I y A-I evita que los oxianiones de metales pesados sean reducidos a la forma trivalente, ya que al carecer de este donador de electrones (MO) u otros compuestos reductores inorgánicos asociados, la dinámica global del suelo es impactada negativamente, sobre todo a nivel de la movilidad de los micronutrimentos y a la vida microbiana (Bain 2000).
La arcilla y la MO son las propiedades que más influyen en el valor de la CIC del suelo, de tal forma que en los suelos más ácidos la degradación de la arcilla ha provocado una clara disminución de la CIC (Cuadro IV). Se encontraron diferencias significativas de la CIC entre las estrategias de producción (A-I, AS-I y A-T); las menores fueron en los suelos que se usan para la A-T. Dichas diferencias se pueden deber a la cantidad de agroquímico depositado, a la condición prevalente de degradación de la arcilla y al valor de pH asociado. Por otra parte, en todos los suelos muestreados se identificaron pequeñas concentraciones de esmectita cristalizada e illita como filosilicato predominante en la fracción arcilla, lo que se traduce también en una menor CIC.
Concentración total y geodisponible de EPT
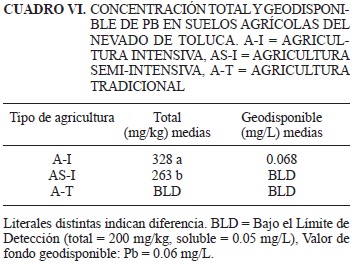
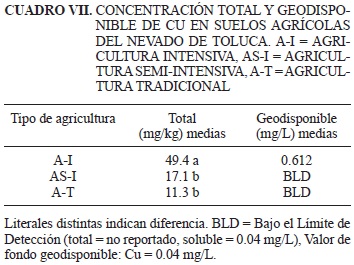
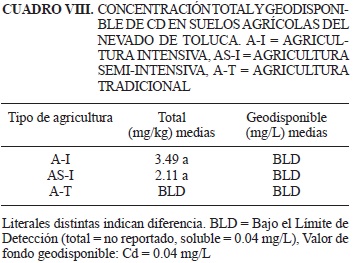
En los cuadros V-X se presenta la concentración total y geodisponible de los EPT (As, Pb, Cu, Cd, Zn y Fe) en los suelos agrícolas del NT de acuerdo con cada estrategia agrícola que se practica para la producción de papa (A-I, AS-I o A-T).
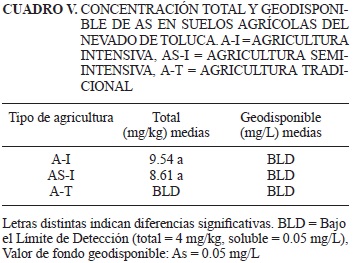
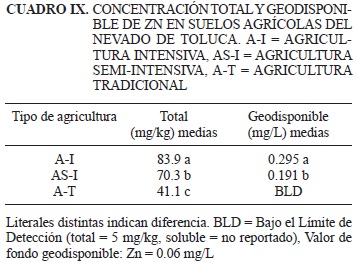

Los suelos en los que se practica A-I se caracterizan por presentar las mayores concentraciones totales de todos los EPT considerados en el estudio respecto a los suelos que se usan para la AS-I y A-T. Las concentraciones totales de los EPT en los suelos en los que se practica A-I se encuentran dentro de los valores de fondo (Cuadro I).
Las concentraciones geodisponibles en los suelos en los que se practica A-I y AS-I son más altas que en los que se practica A-T. En los suelos en los que se practica AS-I, la mayoría de los EPT estuvieron por debajo del límite de detección de las técnicas analíticas empleadas (AA-GH e ICP-AES). En los suelos que se usan para la A-T todas las concentraciones de estos elementos estuvieron por debajo del límite de detección. Finalmente, en los suelos en los que se practica A-I, los EPT en su mayoría presentaron concentraciones geodisponibles que no representan un riesgo para el ambiente por el momento.
La concentración total de As (Cuadro V) que se encontró en las parcelas que se utilizan para la A-I y AS-I no es significativamente diferente (9.54 y 8.61 mg/kg, respectivamente) y está dentro de los valores de fondo. La NOM-147-SEMARNAT/SSA1-2007, considera como peligrosa una concentración total de As mayor o igual a 22 mg/kg (valores de referencia; Cuadro II), por lo tanto las concentraciones encontradas no representan un problema en este momento. No obstante, el As es considerado un elemento susceptible de acumularse y solubilizarse si se forman complejos con elementos de intercambio pasivo como el Al, Se, Mn y Mg (característico de los andosoles), factor que puede propiciar su acumulación y potencial disponibilidad (Davor 2005). Lo anterior podría explicar que la concentración geodisponible de As en las parcelas de A-I, AS-I y A-T estuviera por debajo del límite de detección, ya que pudo haber sido captado por las plantas de papa o estar en los horizontes edáficos profundos (o en la atmósfera) debido a su solubilidad característica.
Las concentraciones totales de Pb (cercanas a los valores de fondo; Cuadro VI), sólo se detectaron en los suelos que se usan para la A-I y AS-I, como en el caso del As. No obstante, la concentración total de Pb fue significativamente diferente entre la práctica A-I (328 mg/kg) y la AS-I (263 mg/kg), lo cual seguramente está provocado por la cantidad de agroquímicos que se depositan. En los suelos en los que se practica A-T las concentraciones estuvieron por debajo del límite de detección.
De acuerdo con la NOM-147-SEMARNAT/SSA1-2007 (uso agrícola, comercial e industrial; Cuadro II) las concentraciones totales de Pb que se detectaron en los suelos que se usan para A-I y AS-I no representan un riesgo a la salud humana o al ecosistema (valor de referencia 400 mg/kg) ni tampoco en términos de concentraciones geodisponibles (A-I = 0.068 mg/L; valor de referencia 0.50 mg/L). Sin embargo, se tiene que considerar que el efecto acumulativo a largo plazo de los EPT sí podría generar un impacto negativo. Se infiere que estos elementos podrían estar formando compuestos de baja solubilidad o estar adsorbidos en partículas coloidales. Por ejemplo, el As se adsorbe en oxihidróxidos de Fe y forma complejos de esfera interna. Los cationes se unen a las arcillas y a la MO o pueden estar como sulfatos insolubles como es el caso del Pb.
Es importante resaltar que las concentraciones totales de Pb detectadas en los suelos evaluados pueden ser objeto de discusión técnica, debido a que en los valores de referencia que reporta la Secretaría del Medio Ambiente y Recursos Naturales (SEMARNAT) se asume que el suelo presenta características similares en el país (entidad cerrada). No obstante, el estudio de Gutiérrez-Ruiz et al. (2009) que reporta los valores de fondo para los suelos de México, considera la diversidad de las características particulares del suelo (entidad dinámica natural). También es importante resaltar que los valores de referencia que emite dicha Secretaría se han modificado con el tiempo. Por ejemplo, según la SEMARNAT (2002), 200 mg/kg de Pb representaban un riesgo para la salud humana (RSH) y 100 mg/kg representaban un riesgo ecológico (RE), en el caso de otros EPT como el As y el Cd, 20 mg/kg en ambos casos representaban RSH y RE. La tendencia ha sido ampliar la concentración de EPT permisible.
Las concentraciones geodisponibles de Cd (Cuadro VIII) detectadas en los suelos en los que se practica A-I y AS-I no representan un problema para la salud humana o el ambiente ya que se observan por debajo del límite de detección en todas las parcelas analizadas. Es común encontrar depósitos encajonados y encriptados de Cd en suelos de origen volcánico que difícilmente interactúan con compuestos reductores (orgánicos o inorgánicos), lo cual limita su dinámica de interacción y de disponibilidad (Alloway 1995).
A pesar de que las fracciones totales de EPT en general son bajas, posiblemente dado el alto nivel de precipitación de la zona (valor promedio anual de 700-1000 mm en el NT), no implica que no representan un riesgo potencial para la salud humana o el ambiente. La constante incorporación de agroquímicos que se observa en la zona, seguramente aumentará la concentración total de EPT y su disponibilidad potencial.
Es importante destacar que en el NT, el régimen de evaporación es 3.9 veces mayor que el de las precipitaciones. Esto indica que la escorrentía superficial que se forma en época lluviosa puede ser más importante que la infiltración, por lo que el mayor riesgo ambiental potencial es la dispersión del drenaje ácido cargado de EPT hacia los arroyos de la zona (50 aproximadamente). Sin embargo, se asume que el drenaje ácido (cargado de EPT) es amortiguado por los efectos de dilución y por el contacto con sedimentos que contienen arcillas y rocas con cierto carácter básico. Los estudios realizados por Ávila-Pérez et al. (2007) y Zarazúa (2008) en algunos cuerpos de agua al interior del NT y en la cuenca alta del Río Lerma, indican que la calidad del agua superficial no ha sido afectada por el drenaje ácido o metales pesados presentes en los suelos agrícolas.
Las consecuencias esperadas del flujo del drenaje ácido (cargado de EPT) en el recurso son: (a) disminución de la disponibilidad de nutrimentos (P, Mg2+, Ca2+) por haber sido intercambiados por otros cationes como H+ o Al3+, b) oxidación de la MO, (c) intemperismo acelerado de las arcillas y liberación de Al3+, el cual es muy tóxico para las plantas, (d) riesgo de toxicidad por los EPT acumulados que en condiciones ácidas pueden llegar a ser muy móviles, (e) agotamiento de la capacidad de amortiguamiento del suelo, (f) condiciones perjudiciales para la puesta en marcha de cultivos y (g) disminución del crecimiento de plantas y de los procesos microbiológicos que ocurren en el suelo. Con esta última consecuencia se perdería el aporte de nueva MO y del proceso de humificación, se limitarían los procesos de nitrificación que realizan las bacterias generando a su vez el debilitamiento de la estructura de los agregados del suelo que favorece la aireación y el movimiento de agua y se formarían costras superficiales que aumentan la escorrentía y disminuyen la lixiviación (Gutiérrez-Ruiz et al. 2007, 2009).
Los resultados obtenidos en los suelos agrícolas del NT en los que se practica A-I, AS-I y A-T aportan evidencias sobre la relación entre la intensidad del uso de agroquímicos y la acumulación de EPT en el suelo. La similitud en el comportamiento de los EPT en los suelos en los que se practica A-I y AS-I se puede deber a que en ambos casos se abusa del uso de agroquímicos (particularmente en la A-I). En los suelos en los que se practica A-I se incorpora la mayor cantidad de agroquímicos (endosulfan, dimetomorf y etilén-bis-ditiocarbamato de manganeso y plomo) por unidad de área (Gutiérrez-Ruiz et al. 2009). En los suelos en los que se practica A-T, los valores son significativamente menores. En estos suelos los EPT también se encuentran en bajas concentraciones (Cu = 11.3 mg/kg, Cd = debajo del límite de detección, Zn = 41.1 mg/kg y Fe = 2.3 %; Cuadro VII-X). La presencia de Cu y Fe puede estar relacionada a que esporádicamente los agricultores incorporan agroquímicos a base de sulfatos de NH4, Cu y Fe con la expectativa de que incrementen el potencial productivo de sus cultivos. En el caso del Fe no hay reportes de fitotoxicidad o problemas de salud.
A pesar de que en los suelos en los que se practica AS-I y A-T las concentraciones de EPT son menores respecto a los suelos que se usan para la A-I, un incremento en el ingreso o en el poder adquisitivo de los agricultores podría provocar un cambio (probablemente negativo) en las prácticas de manejo agrícola. Lo anterior se vería reflejado en un mayor uso de agroquímicos que incrementarían las concentraciones de EPT y la superficie agrícola en el NT con mayor probabilidad de riesgo de contaminación de suelos junto con los efectos secundarios asociados a dichas prácticas.
CONCLUSIONES
Los agroquímicos son un factor de degradación de los suelos agrícolas del NT ya que modifican sus propiedades físicas y químicas, principalmente en los suelos en que se practica la A-I y AS-I para el cultivo de papa.
En los suelos en donde se practica la A-I y AS-I, la acidificación del recurso genera la disminución de la MO y la CIC, así como el aumento de la CE, lo que propicia a su vez que se incremente la geodisponibilidad de algunos EPT.
La acidificación es un proceso que está causando la inmovilización de nutrimentos esenciales para los cultivos, especialmente para la papa que requiere de un pH más alto y de la disponibilidad de P. Por tanto es urgente encalar los suelos del NT en los que se practica A-I y AS-I para lograr aumentar el pH a 4, con lo que se podrá precipitar el Al y evitar el intemperismo de las arcillas.
Los valores de los EPT obtenidos en los suelos agrícolas del NT en los que se practica A-I y AS-I no representan un riesgo ambiental de acuerdo con los valores de la NOM-147-SEMARNAT/SSA1-2007. Sin embargo, podrían ser un problema a largo plazo debido a la acumulación y a la geodisponibilidad de estos elementos.
AGRADECIMIENTOS
Al Dr. Francisco Martín Romero y la Dra. Águeda Elena Ceniceros Gómez, investigadores de los Institutos de Geología y Geografía de la Universidad Nacional Autónoma de México (UNAM), respectivamente. Al Laboratorio de Análisis Físicos y Químicos del Ambiente (Q.F.B. Reyna Roldán Armas y Q. Raquel Domínguez Martínez). Al Laboratorio de Geoquímica Ambiental (Instituto de Geología-UNAM) por su colaboración en el procesamiento de las muestras. A los estudiantes de Ingeniería en Biotecnología de la Universidad Politécnica del Valle de Toluca: Gloria Itzel Vigueras Romero, José Adrián Silis Cano, Mario Alberto Rico Rodríguez, Omar Avilés Mercado y Joel Bravo Arizmendi. Al CONA-CyT y a la UAEMéx por las becas otorgadas en los estudios de doctorado del M. en C. Germán Martínez Alva. Al Instituto de Ciencias Agropecuarias y Rurales de la UAEMéx y al proyecto "Caracterización de los residuos sólidos y líquidos derivados de las actividades agroforestales en el NT", financiamiento PIFI, clave 3077/2011E.
REFERENCIAS
Albert L. (2005). Panorama de los plaguicidas en México. Rev. Toxicol. 44, 145-155. [ Links ]
Alegría H.A., Bidleman T.F. y Salvador-Figueroa M. (2006). Organochlorine pesticides in the ambient air of Chiapas, Mexico. Environ. Pollut. 140, 483-491. [ Links ]
Alloway B.J. (1995). Heavy metals in soils. Blackie Academic and Profesional. Nueva York, EUA, 386 pp. [ Links ]
Armienta M.A., Villaseñor G., Rodríguez R., Ongley L.K. y Mango H. (2001). The role of arsenic-bearing rocks in groundwater pollution at Zimapan Valley, Mexico. Environ Geol. 40, 571-581. [ Links ]
Ávila-Pérez P., Zarazúa G., Carapia-Morales L., Tejeda S., Díaz-Delgado C. y Barceló-Quintal I. (2007). Evaluation of heavy metals and elemental composition of particles in suspended matter of the Upper Course of the Lerma River. J. Radioanal. Nucl. Chem. 273, 625-633. [ Links ]
Bain J.G., Blowes D.W., Robertson W.D. y Frind E.O. (2000). Modelling of sulfi oxidation with reactive transport at a mine drainage site. J. Contam. Hydrol. 41, 23-47. [ Links ]
Barakat A.O., Kim M., Qian Y. y Wade T.L. (2002). Organochlorine pesticides and PCBs residues in sediments of Alexandria Harbour. Egypt. Mar. Pollut. Bull. 44, 1421-1434. [ Links ]
Benítez J.A. y Bárcenas C. (1996). Patrones de uso de los plaguicidas en la zona costera del Golfo de México. En: Golfo de México contaminación e impacto ambiental: diagnóstico y tendencias. (A.V. Botello, G. J. L. Rojas, J. Benítez. y L. D. Zarate, Eds.). EPOMEX, Campeche, México, pp. 155-167. [ Links ]
Bolognesi C. (2003). Genotoxicity of pesticides: a review of human biomonitoring studies. Mutat. Res. 543, 251-272. [ Links ]
Bouyoucos J. (1963). A rapid determination of soil textury. J. Agric. Sci. 23, 456-459. [ Links ]
Bull S., Fletcher K., Boobis A.R. y Battershill J.M. (2006). Evidence for genotoxicity of pesticides in pesticide applicators: a review. Mutag. 21, 93-103. [ Links ]
Caldas E.D., Coelho R.L.C., Souza K.R. y Siba S.C. (1999). Organochlorine pesticides in water, sediment, and fish of Paranoá Lake of Brasilia, Brazil. Bull. Environ. Contam. Toxicol. 62, 199-206. [ Links ]
Cavallo D., Cinzia L.U., Carelli G., Iavicoli I., Ciervo A., Perniconi B., Rondinone B., Gismondi M. e IavicoLi S. (2006). Occupational exposure in airport personnel characterization and evaluation of genotoxic and oxidative effects. Toxicol. 223, 26-35. [ Links ]
Chapman H.D. (1965). Diagnostic criteria for plants and soils. En: Diagnostic criteria for plants and soils. Agronomy 9 (C.A. Black, Ed.). Am. Soc. Agronomy. Riverside, California, EUA, pp. 902-904. [ Links ]
Chen J., Liu C., Yang Z. y Wang J. (2008). Residues and characteristics of organochlorine pesticides in the surface water in the suburb of Beijing. Earth Sci. Front. 15, 242-247. [ Links ]
Cheng H.H. (1990). Pesticides in the soil environments -An overview. En: Pesticides in the soil environment: processes, impacts, and modelling. (H. Cheng, Ed.). Soil Science Society of America, Madison, EUA, pp. 1-5. [ Links ]
CONABIO (2004). Comisión Nacional para el Conocimiento de la Biodiversidad. Regiones Terrestres Prioritarias de México [en línea]. http://www.conabio.gob.mx/informacion/metadata/gis/rtp1mgw.xml?_httpcache=yes&_xsl=/db/metadata/xsl/fgdc_html.xsl&_indent=no. 06/05/2014. [ Links ]
CONAGUA (2008). Comisión Nacional del Agua. Estadísticas del agua en México [en línea]. http://www.conagua.gob.mx/CONAGUA07/Publicaciones/Publicaciones/EAM_2008.pdf. 06/05/2014. [ Links ]
CONANP (2008). Comisión Nacional de Áreas Naturales Protegidas. Parques Nacionales [en línea]. http://nevadodetoluca.conanp.gob.mx. 06/05/2014 [ Links ]
Cordero A. y Ramírez G.F. (1979). Acumulamiento de cobre en los suelos del Pacífico Sur de Costa Rica y sus efectos detrimentales en la Agricultura. Agron. Costarr. 3, 63-78. [ Links ]
Corinne P.R., Fang-Jie Z. y Steve McGrath P. (2006). Phytotoxicity of nickel in a range of European soils: Influence of soil properties, Ni solubility and speciation. Environ. Pollut. 145, 596-605. [ Links ]
Coupe R.H., Manning M.A., Foreman W.T., Goolsby D.A. y Majewski M.S. (2000). Occurrence of pesticides in rain and air in urban and agricultural areas of Mississippi, Sci. Total Environ. 248, 227-240. [ Links ]
Daniels W. M., House W. A., Rae J. E. y Parker A. (2000). The distribution of micro-organic contaminants in river bed sediment cores. Sci. Total Environ. 253, 81-92. [ Links ]
Davor R. (2005). Heavy metals distribution in agricultural top soils in urban area. Environ. Geol. 43, 795-805. [ Links ]
Doménech X. (2000). Química ambiental. El impacto ambiental de los residuos. Miraguano, Madrid, España, 254 pp. [ Links ]
Dubus I.G., Hollis J.M. y Brown C.D. (2000). Pesticides in rainfall in Europe. Environ. Pollut. 110, 331-344. [ Links ]
FAO (1990). Soil map of the world (Revised Legend). Food and Agriculture Organization of the United Nations. Roma, Italia. 23 pp. [ Links ]
Ferrer A. (2003). Intoxicación por plaguicidas. Toxicol. Clín. 26, 1-5. [ Links ]
Franco S., Regil H. y Ordoñez J. (2006). Dinámica de perturbación de las zonas forestales en el Parque Nacional Nevado de Toluca. Madera y Bosque 12, 17-28. [ Links ]
Fytianos K., Katsianis G., Triantafyllou P. y Zachariadis G. (2001). Accumulation of heavy metals in vegetables grown in an industrial area in relation to soil. Bull. Env. Contam. Toxicol. 67, 423-427. [ Links ]
Fytianos K., Meesters R. J. W., Schroder H. Fr., Gouliar-mou B. y Gantidis N. (2006). Concentration and distribution of organochlorine pesticides in surface water and sediments in Lake Volvi (northern Greece). Int. J. Environ. Anal. Chem. 86, 109-118. [ Links ]
García I. y Dorronsoro C. (2005). Contaminación por metales pesados. En: Tecnología de Suelos. Universidad de Granada. Departamento de Edafología y Química Agrícola, Madrid, España, pp. 145-148. [en línea]. http://edafologia.ugr.es. [ Links ]
Garry V. F. (2004). Pesticides and children. Toxicol. Appl. Pharmacol. 198, 152-163. [ Links ]
GEM (2011). Gobierno del Estado de México. Secretaría de Medio Ambiente. Comisión Estatal de Parques Naturales y de la Fauna. Áreas Naturales Protegidas en el Estado de México. Categorías de las áreas protegidas [en línea]. http://portal2.edomex.gob.mx/cepanaf/areas_naturales_protegidas/categorias_areas_protegidas/index.htm. 06/05/2014. [ Links ]
Gilliom R.J. (2007). Pesticides in U.S. streams and groundwater. Environ. Sci. Technol. 41, 3409-3414. [ Links ]
Golfinopoulos S. K., Nikolaou A. D., Kostopoulou M. N., Xilourgidis N. K., Vagi M. C. y Lekkas D. T. (2003). Organochlorine pesticides in the surface waters of Northern Greece. Chemosphere 50, 507-516. [ Links ]
Gutiérrez G.E., Ríos L. M., Muñoz G.F. y Villaescusa J.C. (1998). Chlorinated hydrocarbons in marine sediments of the Baja California (Mexico) - California (USA) border zone. Mar. Pollut. Bull. 36, 27-31. [ Links ]
Gutiérrez-Ruiz M.E., Ceniceros-Gómez A.E., Luna-González L., Morales-Manilla L.M., Romero F., Martínez-Jardines L.G., Rosas H. y López-Blanco J. (2009). Elaboración de un Mapa Regional de Valores de Fondo de EPT's en Suelos de México. CONABIO. FB1283/65002/08. [ Links ]
Gutiérrez-Ruiz M.E., Romero F.M. y González-Hernández G. (2007). Suelos y sedimentos afectados por la dispersión de jales inactivos de sulfuros metálicos en la zona minera de Santa Bárbara, Chihuahua, México. Re. Mex. Cien. Geol. 24, 170-184. [ Links ]
Haro G.L., Chaín C.T., Barrón A.R. y Bohórquez L.A. (2002). Efectos de plaguicidas agroquímicos: Perfil epidemiológico-ocupacional de trabajadores expuestos. Rev. Med. IMSS. 40, 19-24. [ Links ]
Hernández A., Hernández P. y Gordillo A. (2006). Manual para la evaluación de impactos ambientales. INNCIVE, Madrid, España, 770 pp. [ Links ]
Hernández-Romero A.H., Tovilla-Hernández C., Malo E.A. y Bello-Mendoza R. (2004). Water quality and presence of pesticides in a tropical coastal wetland in southern Mexico. Mar. Pollut. Bull. 48, 1130-1141. [ Links ]
Ho T.L. y Egashira K. (2001). Solid-solution ratio on extraction of heavy metals by dilute acids from agricultural soils and river-sediments in Hanoi, Vietnam. Com. Soil Sci. Plant Anal. 32, 643-660. [ Links ]
Hoai P.M., Ngoc N.T., Minh N.H., Viet P.H., Berg M., Alder A.C. y Giger W. (2010). Recent levels of or-ganochlorine pesticides and polychlorinated biphenyls in sediments of the sewer system in Hanoi, Vietnam. Environ. Pollut. 158, 913-920. [ Links ]
Hong S.H., Kim U.H., Shim W.J., Oh J.R., Viet P.H. y Park P.S. (2008). Persistent organochlorine residues in estuarine and marine sediments from Ha Long Bay, Hai Phong Bay, and Ba Lat Estuary, Vietnam. Chemosphere 72, 1193-1202. [ Links ]
Ismail I.B.S., Farihah K. y Khairiah J. (2008). Bioaccumulation of heavy metals in vegetables from selected agricultural areas. Bull. Environ. Contam. Toxicol. 74, 320-327. [ Links ]
Jung M.C. (2001). Heavy metal contamination of soils and waters in and around the Imcheon Au-Ag mine, Korea. Applied Geochem. 16, 1369-1375. [ Links ]
Kishida M., Imamura K., Maeda Y., Lan T.T.N., Thao N.T.P. y Viet P.H. (2007). Distribution of persistent organic pollutants and polycyclic aromatic hydrocarbons in sediment samples from Vietnam. J. Health Sci. 53, 291-301. [ Links ]
Li Z. y Shuman L.M. (1996). Heavy metal movement in metal contaminated soil profiles. Soil Sci.161, 656-666. [ Links ]
Mahler R.L. (2003). General overview of nutrition for field and container crops. En: National proceeding: forest and conservation nursery associations. (L. E. Riley, R. K. Dumroese, T. D. Landis. Eds.). Springfield, IL. Proc. RMRS, Nueva York, EUA, pp. 33-39. [ Links ]
Malla R., Tanaka Y. y Mori K.L. (2007). Short term effect of sewage irrigation on chemical build up in soils and vegetables. Toxicol. 5, 67-72. [ Links ]
Mansour S. (2004). Pesticide exposu re-Egyptian scene. Toxicol. 198, 91-115. [ Links ]
Mc Lean E.O. (1982). Soil pH and lime requirements. En: Methods of soil analysis. Part 2. Agronomy 9 (A.L. Page, R.H. Miller, D.R. Keeney, Eds.). Am. Soc. Agronomy, Madison, EUA, pp. 199-224. [ Links ]
Moor C., Lymberopoulou T. y Dietrich V.J. (2001). Determination of heavy metals in soils, sediments and geological materials by ICP-AES and ICP-MS. Microchim. Acta. 136, 123-128. [ Links ]
Moral R., Gilkes R.J. y Moreno-Caselles J. (2002). A comparison of extractants for heavy metals in contaminated soils from Spain. Commun. Soil Sci. Plant An. 33, 2781-2791. [ Links ]
Norma Mexicana NMX-AA-132-SCFI-2006. Que establece el procedimiento para el muestreo de suelos, para la identificación y la cuantificación de metales y metaloides, y manejo de la muestra. Diario Oficial de la Federación. 14 de enero de 2006. [ Links ]
Norma Oficial Mexicana NOM-147-SEMARNAT/SSA1-2007. Que establece los criterios para determinar las concentraciones de remediación de suelos contaminados por arsénico, bario, berilio, cadmio, cromo (vi), mercurio, níquel, plata, plomo, selenio, talio y/o vanadio y otros. Diario Oficial de la Federación. 2 de marzo de 2007. [ Links ]
Ongley E.D. (1996). Control of water pollution from agriculture. FAO Irrigation and drainage paper 55. Roma, Italia, 111 pp. [ Links ]
Prieto M.J., González R.C.A., Román G.A.D. y Prieto G.F. (2009). Contaminación y fitotoxicidad en plantas por metales pesados provenientes de suelos y agua. Tropic. Subtropic. Agroecos. 10, 29-44. [ Links ]
Ramírez Q.Y., López G.E., Barceló Q.I.D. y Domínguez E.Z.J. (2008). Caracterización de triazinas en la cuenca alta del Río Lerma en Estado de México, México. Memorias. XXXI Congreso Interamericano de Ingeniería Sanitaria y Ambiental. Santiago de Chile. Chile. 15 al 19 de mayo, 2008. CD-ROM. [ Links ]
Ramos-Bello R., Cajuste L.J., Flores-Román D. y García-Calderón N.E. (2001). Heavy metals, salts and sodium in Chinampa soils in Mexico. Agrociencia 35, 385-395. [ Links ]
Ramos-Hernández S. y Flores-Román D. (2008). Comparación de dos fuentes fosfatadas en suelos volcánicos cultivados con café del soconusco, Chiapas, México. Agrociencia 42, 391-398. [ Links ]
Rueda L.Q., Botello A.V. y Díaz G.G. (1997). Presencia de plaguicidas organoclorados en dos sistemas lagunares del estado de Chiapas, México. Rev. Int. Contam. Ambie. 13, 55-61. [ Links ]
SAS, INSTITUTE, INC. (1988). SAS user's guide: Statistics. Release 6.03. (SAS Institute Incorporation Ed.). Cary, Carolina del Norte, EUA, 1028 pp. [ Links ]
SEMARNAT (2002). Secretaría de Medio Ambiente y Recursos Naturales. Límite permisible de metales pesados en México. Diario Oficial de la Federación. 7 de noviembre de 2002. [ Links ]
Tchobanoglous G., Theisen H. y Vigil S. A. (1998). Gestión integral de residuos sólidos. McGraw-Hill, Madrid, España, 1107 pp. [ Links ]
Thurman E.M., Bastian K.C. y Mollhagen T. (2000). Occurrence of cotton herbicides and insecticides in playa lakes of high plains of West Texas. Sci. Total Environ. 248, 189-200. [ Links ]
USEPA (2010). United States Environmental Protection Agency. Types of Pesticides. United States Environmental Protection Agency [en línea]. http://www.epa.gov/pesticides/about/types.htm. 17/10/2013 [ Links ]
Virkutyte J., Sillanpää M. y Latostenmaa P. (2002). Electrokinetic soil remediation- Critical overview. The Sci. Tot. Environ. 289, 97-121. [ Links ]
Waliszewski S.M., Gómez-Arroyo S., Infanzón R.M., Carvajal O., Villalobos-Pietrini R., Trujillo P. y Maxwell Hart M. (2004). Persistent organochlorine pesticide levels in bovine fat from México. Food Addit. Contam. 21, 774-780. [ Links ]
Walkey A.L. y Black A. (1947). A rapid determination of soil organic matter. J. Agric. Sci. 25, 563-568. [ Links ]
Wong F., Alegria H.A., Jantunen L.M., Bidleman T.F., Salvador-Figueroa M., Gold-Bouchot G., Ceja-Moreno V., Waliszewski S.M. e Infanzon R. (2008). Organochlorine pesticides in soils and air of Southern Mexico: Chemical profiles and potential for soil emissions. Atmos. Environ. 42, 7737-7745. [ Links ]
Zarazúa G. (2008) Evaluación de las contribuciones naturales y antropogénicas de los metales pesados Cr, Mn, Fe, Cu, Zn y Pb y su distribución en el agua y sedimento en el Curso Alto del Río Lerma. Tesis de Doctorado. Centro Interamericano de Recursos del Agua-Facultad de Ingeniería. Universidad Autónoma del Estado de México. Toluca, Estado de México, México, 159 pp. [ Links ]














