Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista internacional de contaminación ambiental
Print version ISSN 0188-4999
Rev. Int. Contam. Ambient vol.27 n.4 Ciudad de México Nov. 2011
Revisión
Hongos micorrízicos arbusculares y la fitorremediación de plomo
Arbuscular mycorrhizal fungi and the phytoremediation of lead
Carlos J. ALVARADO1, Nabanita DASGUPTA–SCHUBERT1, Enrique AMBRIZ2, Juan M. SÁNCHEZ–YAÑEZ1 y Javier VILLEGAS1
1 Instituto de Investigaciones Químico Biológicas, Universidad Michoacana de San Nicolás de Hidalgo, Cd. Universitaria, Morelia, C.P. 58060, Michoacán, México. Tel: +52 443 326 5788 ext. 128; Fax: +52 443 326 5790; Email: charliealvarado@gmail.com
2 Facultad de Ingeniería en Tecnología de la Madera, Universidad Michoacana de San Nicolás de Hidalgo, Cd. Universitaria, Morelia, C.P. 58060, Michoacán, México. Tel: +52 443 326 0379
Recibido agosto 2010
Aceptado agosto 2011
RESUMEN
Entre los metales pesados, el plomo (Pb) es un contaminante potencial y real en algunos lugares en el mundo ya que se acumula con facilidad en suelos y sedimentos. La presencia de Pb en el ambiente se debe principalmente a las actividades antrópicas. El Pb no es un elemento esencial para las plantas, los animales o para los seres humanos, por lo que concentraciones elevadas de este metal pesado en los humanos causan diferentes síntomas de toxicidad tales como: retraso del crecimiento, impacto al sistema nervioso, entre otros. La fitorremediación es una tecnología alternativa de bajo costo que consiste en la utilización de plantas para descontaminar los suelos. Los hongos micorrizicos arbusculares (HMA) ofrecen un atractivo mecanismo de fitorremediación, debido a que durante la interacción simbiótica, el sistema radical de las plantas micorrizadas se incrementa y con esto se aumenta el potencial para tomar Pb. Algunos reportes muestran que la mayor concentración de Pb en plantas micorrizadas que crecen en suelos contaminados se encuentra en las raíces, funcionando la micorriza como un sistema fitoestabilizador. También se ha observado que la inoculación de plantas con HMA permite la acumulación de Pb en tallos y hojas. Los mecanismos por los cuales se logra almacenar el Pb en la raíz y en la parte aérea de la planta son desconocidos. Por lo que en este trabajo se hace una revisión breve del uso de HMA en la fitorremediación de suelos contaminados por Pb y se comentan los posibles mecanismos relacionados con la remediación de suelos contaminados con Pb mediante la utilización de HMA.
Palabras clave: metales pesados, micorrizas, fitoacumulación, biorremediación.
ABSTRACT
Amongst the heavy metals, lead (Pb) is a potential and in many cases an actual contaminant in several areas of the world as it accumulates easily in soil and sediment. Its presence in the environment is mainly due to anthropogenic activities. Pb is not an essential element for plants, animals and humans. High concentrations of Pb in humans causes different symptoms of toxicity such as the lack of growth and an impact on the nervous system, amongst others. Phytoremediation is an alternative environmental technology that is low in cost and environmentally sustainable. Arbuscular mycorrhizal fungi (AMF) offer an attractive system to assist in phytoremediation because the symbiotic interaction increases the root system of plants and thereby the potential of the bioavailability of Pb in soil is increased. AMF also confer high resistance to drought, salinity and others stresses. When the highest concentration of Pb in plants grown in contaminated soil is found in the roots, the fungus–plant interaction is considered as a phytostabilization system. Some studies have shown that mycorrhizal plants accumulate high amounts of Pb in their above–ground parts. According to these reports the plant–fungus interaction could also be suitable for phytoextraction. The mechanisms involved in the remediation of Pb contaminated soils are unknown. Therefore in this paper an overview of the use of arbuscular mycorrhizal fungi and the mechanism involved in phytoremediation of soils contaminated by Pb is presented.
Key words: heavy metals, mycorrhyza, phytoaccumulation, bioremediation.
INTRODUCCIÓN
El plomo (Pb) es un metal gris azulino que se presenta en forma natural en la corteza terrestre. El Pb es tóxico para el sistema nervioso y se asocia con la depresión de muchas funciones endócrinas. El uso más amplio de este es para la fabricación de acumuladores; aunque también es empleado para la fabricación de tetraetilo de plomo, pinturas, cerámicas, forros para cables, elementos de construcción, vidrios especiales, pigmentos, soldadura suave y municiones. El Pb se encuentra naturalmente en tres estados de oxidación, Pb0, Pb2+ y Pb4+.
El Pb al ser ingerido, inhalado o absorbido por la piel a niveles entre 10 y 100 µg/dL, resulta ser muy tóxico para los seres vivos en general y para los humanos en particular. Se sospecha que este metal pesado es tóxico para los sistemas endócrino, cardiovascular, respiratorio, inmunológico, neurológico y gastrointestinal además de poder afectar la piel y los riñones (Cuadro I).

Cuando el plomo se encuentra presente en el suelo puede entrar en la raíz a través de la difusión pasiva. Estudios de absorción de Pb en plantas han demostrado que la mayor parte de éste se queda en las raíces (Kumar et al. 1995). La retención de Pb en las raíces se basa en la unión de Pb a los sitios de intercambio iónico en la pared celular (Gaur y Andholeya 2004).
Los síntomas específicos de toxicidad por Pb en las plantas son la inhibición del crecimiento de la raíz, retraso en el crecimiento de la planta y clorosis (Burton et al. 1984). Cuando el Pb entra en las células de la planta, produce varios efectos adversos en los procesos fisiológicos, entre los que se encuentra la inhibición de la actividad enzimática, alteración de la nutrición mineral, desequilibrio hídrico, cambios en el estado hormonal y alteración en la permeabilidad de la membrana celular. Estos trastornos fisiológicos por las altas concentraciones de Pb pueden llevar a la planta a la muerte (Ernst 1998, Seregin e Ivanov 2001). Sin embargo, existen plantas que tienen resistencia a la toxicidad del Pb y no muestran gran disminución de sus propiedades fisiológicas en la presencia de altos niveles. Este hecho forma la base de la biotecnología ambiental de fitorremediación.
Al no ser un elemento biodegradable el Pb se convierte en una amenaza para el ambiente. Las técnicas de remediación convencionales se basan principalmente en la excavación del suelo contaminado y posterior procesamiento fisicoquímico del mismo. Sin embargo, estos procesos son costosos, poco prácticos y causan daños secundarios al ambiente. En contraste el uso de plantas como estrategia de remediación (fitorremediación), es una alternativa económica y sustentable (Salt et al. 1995, Kramer 2005, Peuke y Rennenberg 2005). Existen dos mecanismos principales mediante los cuales puede llevarse a cabo la fitorremediación de suelos contaminados con Pb. La fitoestabilización, en la cual el Pb es inmovilizado en el suelo por las raíces de la planta y la fitoextracción, en la que el Pb es tomado por la raíz y transportado a la parte aérea (Mucciarelli et al. 1998, Khan et al. 2000, Lavania y Lavania 2000, Shu et al. 2002). Las plantas con alta capacidad de tolerar y absorber metales pesados como Pb, se dividen en tres tipos: los hiperacumuladores (HA) de metales pesados, los acumuladores ó indicadores (A) y los exclusores (E) (Baker 1981). Los A absorben y almacenan menos que los HA y sirven como indicadores de la presencia de metales pesados en el suelo. Los E son plantas que absorben y almacenan los metales pesados casi exclusivamente en sus raíces. Hasta ahora no se ha descubierto ningún HA de Pb. La mayoría de las plantas que absorben el Pb (sin intervención humana) son los E. Por esta razón los procesos en la rizosfera contribuyen de manera importante en la fitorremediación del Pb. Un proceso que probablemente puede servir a este fin es la simbiosis con microorganismos del suelo tales como los hongos micorrízicos.
HONGOS MICORRIZICOS ARBUSCULARES EN SUELOS CONTAMINADOS CON PLOMO
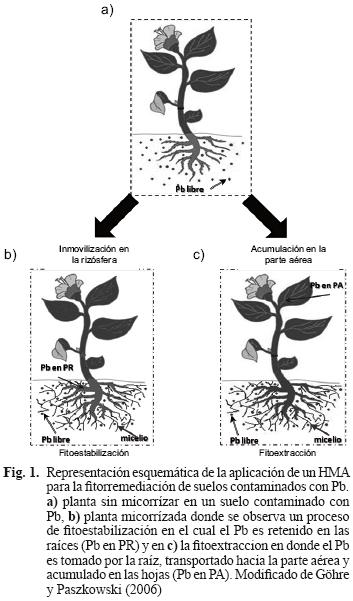
Los HMA son un componente natural de los suelos en la mayoría de los ecosistemas terrestres. Se sabe que más del 80 % de las plantas terrestres son capaces de presentar una asociación simbiótica con ellos y pueden ser considerados como una extensión de las raíces de las plantas ya que amplían considerablemente el volumen de suelo que puede ser explorado y por ende se incrementa la cantidad de nutrientes que pueden ser obtenidos por la planta (Harrison 1999). El incremento de nutrimentos es más evidente cuando las plantas micorrizadas se encuentran en condiciones adversas para su crecimiento, como es el caso de suelos contaminados con plomo. Bajo esta condición, se ha reportado que en algunos casos las plantas micorrizadas pueden mostrar mayor captación de metales pesados por la raíz y aumentar el transporte de estos a la parte aérea de la planta (fitoextracción) (Rabie 2005), mientras que en otros casos el uso de HMA contribuye a la inmovilización del metal en las raíces de las plantas (Gaur y Andholeya 2004) o en el suelo (González–Chávez et al. 2004) (fitoestabilización) (Fig. 1). Esto muestra que el resultado de la micorrización de plantas con fines de fitorremediación de suelos contaminados depende de la combinación planta–hongo–metal y está influenciado por las condiciones del suelo.
Las esporas de los HMA normalmente tienen diferente nivel de sensibilidad a la presencia de metales pesados en ausencia de las plantas dependiendo de la especie del hongo. En la fase presimbiótica, Glomus intrarradices es uno de los hongos micorrízicos que ha mostrado mayor tolerancia a metales como Cd y Pb (Pawlowska y Charvat 2004). En fase simbiótica, este hongo también ha mostrado tolerancia a metales pesados; un ejemplo de ello es la mayor acumulación de Pb en las raíces micorrizadas de Vetiveria zizanioides con dicho hongo (Wong et al. 2007).
Los mecanismos de transporte de Pb en el micelio externo de los HMA han sido poco estudiados. Sin embargo, existen datos que sugieren que el movimiento del Pb hacia el micelio interno podría ser a través del fósforo. El fósforo en HMA es transportado del micelio externo al interno principalmente en forma de polifosfato (Harrison y Van Buuren 1995, Maldonado–Mendoza et al. 2001). La unión del Pb y polifosfato ha sido observada como un mecanismo de estabilización de Pb en suelo (Gaur y Adholeya 2004). El complejo Pb–polifosfato también ha sido observado en el micelio interno de HMA (Turnau et al. 1993). Por lo tanto, existe la posibilidad de que el Pb sea transportado a la raíz micorrizada vía el micelio externo. Sin embargo, se requiere profundizar aun más en el estudio de los mecanismos del transporte de Pb a través del micelio de HMA.
HONGOS MICORRIZICOS ARBUSCULARES EN LA FITOESTABILIZACIÓN DE PLOMO
La fitoestabilización consiste en inmovilizar metales pesados mediante el uso de especies de plantas tolerantes, con un sistema radicular que provea una buena cobertura de suelo. Las plantas con este tipo de sistemas radiculares pueden acumular una gran cantidad de Pb en las raíces. Además la presencia de HMA puede contribuir a una mayor inmovilización del metal. Entre las posibles estrategias de inmovilización de Pb por el hongo se encuentran: la inmovilización del Pb soluble mediante glicoproteínas secretadas por el hongo, la adsorción del Pb en las paredes celulares y la quelación de metales al interior de la hifa, siendo estas estrategias similares a las utilizadas por las plantas (Gaur y Andholeya 2004).
La glomalina es una glicoproteína insoluble secretada por el hongo que se ha encontrado en el suelo ligada a metales pesados. Para el caso específico de suelos contaminados con Pb se ha logrado extraer hasta 1.12 mg de Pb por gramo de glomalina (González–Chávez et al. 2004) y recientemente se ha observado que la concentración de Pb en la glomalina puede variar entre 0.8 y 15.5 % del total de Pb en el suelo (Vodnik et al. 2008).
Por otro lado, es ampliamente conocido que los HMA pueden producir una gran cantidad de micelio externo. También es conocido que la pared celular de este micelio está compuesta mayormente por quitina y que este compuesto estructural provee una eficiente superficie para la adsorción de los metales pesados del suelo (Galli et al. 1994, González–Chávez et al. 2004). Este potencial de adsorción se debe a que las hifas del hongo presentan una mayor afinidad (2 a 4 veces más) que las raíces (Joner et al. 2000), por lo que la inoculación de plantas tolerantes con HMA podrían incrementar significativamente la estabilización de metales pesados contenidos en el suelo.
Otros agentes potenciales de retención del Pb en el micelio de los HMA son las metalotioneinas. En plantas acumuladoras de metales (Clemens 2001) y en hongos ectomicorrízicos (Morselt et al. 1986, Galli et al. 1994) se ha observado la presencia de estos polipéptidos capaces de adsorber metales pesados. Aunque estos compuestos no han sido aún observados en unión con Pb, se ha detectado en el micelio de HMA una alta expresión de un gen que codifica para la síntesis de este tipo de polipéptido en presencia de metales pesados (Lanfranco et al. 2002).
La absorción e inmovilización del Pb es mayor por las raíces que se encuentran micorrizadas en comparación con las raíces no micorrizadas (Gaur y Andholeya 2004, Chen et al. 2005). La forma en que el metal se incorpora al interior de la raíz micorrizada es desconocida. Sin embargo, el hecho de que se ha observado un aumento en el número de vesículas con el incremento de concentración de Pb en el suelo (Joner et al. 2000) sugiere que el Pb en las raíces micorrizadas podría ser inmovilizado en las vesículas o en el interior del micelio interno.
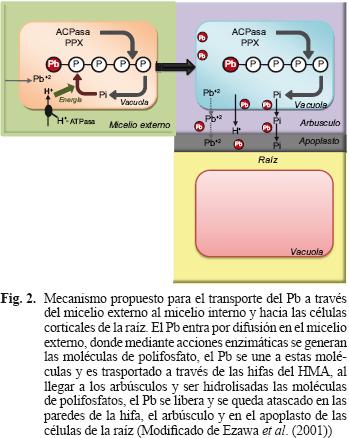
Se ha documentado la acumulación de metales pesados, tales como Cd, Zn y Cu, en el interior del micelio interno de HMA especialmente en gránulos de polifosfato en el interior de la vacuola (Turnau et al. 1993). En el caso de hongos micorrízicos arbusculares no se ha observado la acumulación de Pb en gránulos de polifosfato. Sin embargo los HMA se caracterizan por adquirir una gran cantidad de fósforo y transportarlo de la solución del suelo al interior de la raíz en forma de polifosfato. Una vez que el polifosfato llega a los arbúsculos, es liberado en la reacción de hidrólisis del polifosfato en las vacuolas de las células (Capaccio y Callow 1982, Saito 1995, Kojima et al. 1998, Ezawa et al. 2001). Lo anterior refleja el gran potencial de los HMA con fines de fitoestabilización. Sin embargo, se desconoce si la mayor estabilización de Pb en las raíces micorrizadas se realiza mediante: a) acumulación de Pb en vesículas, b) absorción en pared celular y en vacuolas en micelio interno, y c) absorción en pared celular y en polipéptidos en micelio externo. Probablemente la estabilización podría darse a través de un mecanismo como el propuesto por Ezawa et al. (2001) para el fósforo, donde el metal pesado podría quedarse en la vacuola o incorporarse a la pared celular del micelio (Fig. 2).
También se debe tener en cuenta que el sistema es muy complejo y que el mecanismo no puede ser predicho de antemano, ya que cada sitio contaminado tiene sus características específicas, por lo que la elección de los genotipos de la planta y el hongo podrían determinar el comportamiento del sistema como fitoestabilizador o como fitoextractor. Ejemplo de todo lo anterior es la inoculación de Vetiveria zizanioides con Glomus intrarradices creciendo en suelo contaminado con concentraciones crecientes de Pb, donde se observó que a baja concentración de Pb (10 a 100 mg Pb kg–1 suelo) está funcionando esta relación simbiótica como fitoestabilizador, mientras que a elevada concentración de Pb (1000 mg Pb kg–1 suelo) se obtuvo un aumento en la concentración de Pb en las partes aéreas (Wong 2007), lo cual indica que también esta relación simbiótica puede posiblemente ayudar en el proceso de fitoextracción.
HONGOS MICORRÍZICOS Y FITOEXTRACCIÓN DE PLOMO
La fitoextracción es la tecnología más atractiva para limpiar suelos contaminados con metales pesados (Kramer 2005). Mediante esta tecnología los metales son adquiridos por las raíces de las plantas y transportados a las partes aéreas (hojas y tallos), posteriormente hojas y tallos conteniendo los metales pesados pueden ser cosechadas, logrando así la remoción del contaminante e incluso su posterior recuperación (fitominería). Para esto se busca emplear plantas con características específicas, como son las hiperacumuladoras de metales pesados que que son muy tolerantes a los metales pesados y también gran capacidad para acumularlas. La desventaja encontrada en plantas con dichas características es que no tienen una buena generación de biomasa en un tiempo corto (Ernst 1998). Una de las principales limitaciones que encuentra la fitoextracción es la biodisponibilidad de los metales pesados para ser obtenidos por la planta. Una de las formas más comunes de mejorar esta deficiencia es la adición de quelantes sintéticos para aumentar la biodisponibiladad de los metales (Salt et al. 1995). Blaylock et al. (1997) demostraron la alta capacidad del quelante sintético EDTA (acido etilendiamino tetraacético) para aumentar la fitoextracción de Pb usando la planta Brassicajúncea, esto debido a que el EDTA presenta una afinidad por el Pb y contribuye a ponerlo en forma biodisponible para la planta. Sin embargo, se considera que este método causa un daño secundario en el ambiente por la lixiviación del Pb hacia los mantos acuíferos (Chaney 2008), ya que los metales no pueden ser absorbidos por la planta a la misma velocidad en que son quelados.
Con la finalidad de volver estos procesos más amigables con el ambiente, se está buscado utilizar nuevas estrategias para mejorar la fitoextracción, como puede ser la utilización de HMA. Estos hongos podrían ayudar a incrementar la tolerancia de las plantas al Pb, el transporte de éste a la parte aérea debido a una mejor adquisición de nutrientes del suelo y contribuir en general al mejor desarrollo de la planta (Göhre y Paszkowski 2006).
La cantidad de Pb transportado a la parte aérea podría depender de factores como la combinación de planta y hongo, así como de la cantidad de Pb en el suelo. En este sentido se observó que la simbiosis Glomus deserticola – Eucalyptus globulus incrementó significativamente la concentración de Pb en hojas y tallo en comparación con la simbiosis G. mosseae – E. globulus. Esta tolerancia a metales pesados por parte de las plantas micorrizadas podría estar relacionada con la acumulación en zonas metabólicamente menos activas como lo es el tallo (Arriagada et al. 2005). Con relación a la especie de planta, se observó que en suelos con una concentración de Pb de 1500 mg Pb Kg–1 suelo (Rabie 2005), las platas de frijol inoculadas con G. mosseae acumulan mayor cantidad de Pb en la parte aérea con relación a su raíz, mientras que las plantas de trigo tratadas con la misma concentración de Pb e inoculadas con el hongo acumulan menor cantidad de Pb en la parte aérea en relación a la raíz (Rabie 2005). Esta mayor acumulación de Pb en la parte aérea de las plantas de frijol podría estar relacionada con la mayor absorción de fósforo, mejorando con ello la síntesis de proteínas y de enzimas antioxidantes.
También se ha observado el incremento del transporte de Pb hacia la parte aérea en suelos con valores inferiores a 1500 mg Pb kg–1 (Arriagada et al. 2005, Nowak 2007). Este comportamiento en el transporte de Pb coincide con la absorción de nutrientes como nitrógeno y fósforo, lo cual sugiere que la fitoextracción podría depender en gran medida de una mayor toma de nutrientes por parte de la planta micorrizada.
PERSPECTIVAS DE LA APLICACIÓN DE HONGOS MICORRÍZICOS ARBUSCULARES EN LA FITORREMEDIACIÓN DE PLOMO
La presencia de metales pesados en la solución del suelo altera la disponibilidad de nutrimentos para las plantas. La baja disponibilidad de fósforo provoca una reducción del crecimiento y por ende un menor potencial de fitorremediación. La utilización de hongos micorrízicos arbusculares en procesos de fitorremediación ha sido propuesta debido a que mejora la adquisición de fósforo vía el micelio externo.
Hasta el momento se pueden encontrar observaciones contradictorias, con una amplia variación en los resultados, como lo muestran las revisiones recientes (Gaur y Adholeya 2004, Khan 2005). Sin embargo, es importante llevar a cabo más estudios en torno a la interacción HMA–planta en suelos contaminados, con el objeto de aumentar la eficacia de la fitorremediación (Göhre y Paszkowski 2006). Los HMA podrían además tener un impacto a nivel de fitoestabilización debido a la aparente incapacidad de los hongos para transportar el Pb a la interfase hongo–planta, quedando la mayoría del Pb unido al micelio interno del hongo.
Al respecto, en nuestro grupo de trabajo se está estudiando la interacción simbiótica entre Tagetes erecta y el HMA Glomus intrarradices utilizando una forma insoluble de Pb. Los resultados hasta ahora obtenidos muestran una buena tolerancia de T. erecta en presencia de altas concentraciones de Pb, así como un aumento en la concentración de Pb en las raíces micorrizadas con relación a las raíces no micorrizadas (datos no publicados).
Aunque la mayoría de los resultados indican que los hongos promueven la fitoestabilización, existen algunos indicios de que también podrían participar activamente en la fitoextracción. En este contexto se ha observado que la obtención de hierro en suelos contaminados con Pb disminuye significativamente a 1500 mg Pb Kg–1 de suelo, mientras que otros elementos como el fósforo no reducen su acumulación (Arriagada et al. 2005). Dicha disminución altera directamente la asimilación de carbono, puesto que el hierro es parte importante de la clorofila, lo cual podría dar lugar a una disminución en el transporte de Pb a la parte aérea. Con relación en esto, Punamiya et al. (2008) observaron que la inoculación de pasto con hongos micorrízicos facilita el transporte de Pb a la parte aérea y que esto tal vez fue producto de la elevada actividad de la clorofila. La fitoextracción con hongos micorrízicos arbusculares podría darse también en combinación con otros organismos reductores de hierro, sin embargo, hay que realizar más estudios para confirmar esta hipótesis.
La utilización de hongos micorrízicos asociados a plantas leñosas con fines de fitorremediación es un campo que ha sido poco explorado. No obstante, existen trabajos (Arriagada et al. 2005) en los que se ha observado que dicha combinación cuenta con un futuro promisorio para fines de fitoextracción. Por lo que también es necesario evaluar en trabajos futuros el efecto de estas asociaciones en la fitorremediación.
REFERENCIAS
Arriagada M.A., Herrera M.A. y Ocampo J.A. (2005). Contribution of arbuscular mycorrhizal and saprobe fungi to the tolerance of Eucalyptus globulus to Pb. Water Air Soil Poll. 166, 31–47. [ Links ]
Baker A.J.M. (1981). Accumulators and excluders–strategies in the response of plants to heavy metals. J. Plant Nutr. 3, 643–654. [ Links ]
Blaylock M.J., Salt D.E., Dushenkov S., Zakharova O., Gussman C., Kapulnik Y., Ensley B.D. y Raskin I. (1997). Enhanced accumulation of Pb in Indian mustard by soil–applied chelating agents. Environ. Sci. Technol. 31, 860–865. [ Links ]
Burton K.W., Morgan E. y Roig A. (1984). The influence of heavy metals on the growth of sitkaspruce in South Wales forests in greenhouse experiments. Plant Soil. 78, 271–282. [ Links ]
Capaccio L.V.M. y Callow J.A. (1982). The enzymes of polyphosphate metabolism in vesicular–arbuscular mycorrhizas. New Phytol. 91, 81–91. [ Links ]
Chaney R.L. (2008). Anthropogenic contamination of urban soils: sources, risks, remediation. Joint Meeting of the Geological Society of America, Soil Science Society etc., Hoston, Texas, USA. 7 de Octubre de 2008. http://gsa.confex.com/gsa/2008AM/finalprogram/abstract_149953.htm (ultimo acceso 19 de Oct. de 2011). [ Links ]
Chen X., Wu C., Tang J. y Hu S. (2005). Arbuscular mycorrhizae enhance metal lead uptake and growth of host plants under a sand culture experiment. Chemosphere 60, 665–671. [ Links ]
Clemens S. (2001). Molecular mechanisms of plant metal tolerance and homeostasis. Planta 212, 475–486. [ Links ]
Ernst W.H.O. (1998). Effects of heavy metals in plants at the cellular and organismic levels. En: Ecotoxicology: Ecological Fundamentals, Chemical Exposure and Biological Effects (G. Schuurmann y B. Markert, Eds.). Wiley, Heidelberg, pp. 587–620. [ Links ]
Ezawa T., Smith S.E. y Smith F.A. (2001). Differentiation of polyphosphate metabolism between the extra– and intraradical hyphae of arbuscular mycorrhizal fungi. New Phytol. 149, 555–563. [ Links ]
Galli U., Schüepp H. y Brunold C. (1994). Heavy metal binding by mycorrhizal fungi. Physiol. Plantarum. 926, 364–368. [ Links ]
Gaur A. y Adholeya A. (2004). Prospects of arbuscular mycorrhizal fungi in phytoremediation of heavy metal contaminated soils. Current Sci. 86, 528–534. [ Links ]
Göhre V. y Paszkowski U. (2006). Contribution of the arbuscular mycorrhizal symbiosis to heavy metal phytoremediation. Planta 223, 1115–1122. [ Links ]
González–Chávez M.C., Carrillo–González R., Wright S.F. y Nichols K.A. (2004). The role of glomalin, a protein produced by arbuscular mycorrhizal fungi, in sequestering potentially toxic elements. Environ. Pollut. 130, 317–323. [ Links ]
Harrison M.J. y Van Buuren M.L. (1995). A phosphate transporter from the mycorrhizal fungus Glomus versiforme. Nature 378, 626–629. [ Links ]
Harrison M.J. (1999). Molecular and cellular aspects of the arbuscular mycorrhizal symbiosis. Annu. Rev. Plant Physiol. Plant Mol. Biol. 50, 361–389. [ Links ]
Joner E.J., Briones R. y Leyval C. (2000). Metal–binding capacity of arbuscular mycorrhizal mycelium. Plant Soil. 226, 227–234. [ Links ]
Khan A.G., Kuek C., Chaudhry T.M., Khoo C.S. y Hayes W.J. (2000). Role of plants, mycorrhizae and phytochelators in heavy metal contaminated land remediation. Chemosphere 41, 197–207. [ Links ]
Khan A.G. (2005). Role of soil microbes in the rhizospheres of plants growing on trace metal contaminated soils in phytoremediation. J. Trace Elem. Med. Biol. 18, 355–364. [ Links ]
Kojima T., Hayatsu M. y Saito M. (1998). Intraradical hyphae phosphatase of the arbuscular mycorrhizal fungus, Gigaspora margarita. Biol. Fert. Soils. 26, 331–335. [ Links ]
Kramer U. (2005). Phytoremediation: novel approaches to cleaning up polluted soils. Curr. Opin. Biotechnol. 16, 133–141. [ Links ]
Kumar N.P.B.A., Dushenkov V., Motto H., Raskin I. (1995). Phytoextraction: the use of plants to remove heavy metals from soils. Environ. Sci. Technol. 29, 1232–1238. [ Links ]
Lanfranco L., Bolchi A., Ros E.C., Ottonello S. y Bonfante P. (2002). Differential expression of a metallothionein gene during the presymbiotic versus the symbiotic phase of an arbuscular mycorrhizal fungus. Plant Physiol. 130, 58–67. [ Links ]
Lavania U.C. y Lavania S. (2000). Vetiver grass technology for environmental technology and sustainable development. Current Sci. 78, 944–946. [ Links ]
Maldonado–Mendoza I.E., Dewbre G.R. y Harrison M.J. (2001). A phosphate transporter gene from the extraradical mycelium of an arbuscular mycorrhizal fungus Glomus intraradices is regulated in response to phosphate in the environment. Mol. Plant Microbe In. 14, 1140–1148. [ Links ]
Morselt A.F.W., Smits W.T.M. y Limonard T. (1986). Histochemical demonstration of heavy metal tolerance in ectomycorrhizal fungi. Plant Soil. 96, 417–420. [ Links ]
Mucciarelli M., Bertea C.M., Scannerini S. y Gallino M. (1998). Vetiveria zizanioides as a tool for environmental engineering. Acta Hortic. 457, 261–269. [ Links ]
Nowak J. (2007). Effects of cadmium and lead concentrations and arbuscular mycorrhizal on growth, flowering and heavy metal accumulation in scarlet sage (Salvia splendens sello 'torreador'). Acta Agrobot. 60, 79–83. [ Links ]
Pawlowska T.E. y Charvat I. (2004). Heavy–metal stress and developmental patterns of arbuscular mycorrhizal fungi. Appl. Environ. Microbiol. 70, 6643–6649. [ Links ]
Peuke A.D. y Rennenberg H. (2005). Phytoremediation. EMBO Rep. 6, 497–501. [ Links ]
Punamiya P., Datta R., Sarkar D., Barber S., Patel M. y Das P. (2010). Symbiotic role of Glomus mosseae in lead phytoextraction using vetiver grass [Chrysopogon zizanioides (L.)]. J. Hazard. Mat., 177, 465–474. [ Links ]
Rabie G.H. (2005). Contribution of arbuscular mycorrhizal fungus to red kidney and wheat plants tolerance grown in heavy metal–polluted soil. African J. Biotechnol. 4, 332–345. [ Links ]
Saito M. (1995). Enzyme activities of the internal hyphae and germinated spores of an arbuscular mycorrhizal fungus, Gigaspora margarita Becker & Hall. New Phytol. 129, 425–431. [ Links ]
Salt D.E., Blaylock M., Kumar P.B.A.N., Dushenkov V., Ensley B.D., Chet I. y Raskin I. (1995). Phytoremediation: a novel strategy for the removal of toxic metals from the environment using plants. Nat. Biotechnol. 13, 468–175. [ Links ]
Seregin I.V. e Ivanov VB. (2001). Physiological aspects of cadmium and lead toxic effects on higher plants. Russian J. Plant Physiol. 48, 523–544. [ Links ]
Shu W.S., Xia H.P., Zhang Z.Q., Lan C.Y. y Wong M.H. (2002). Use of vetiver and three other grasses for revegetation of Pb/Zn mine tailings: field experiment. Inter. J. Phyto. 4, 47–57. [ Links ]
Turnau K., Kottke I. y Oberwinkler F. (1993). Elemental localization in mycorrhizal roots of Pteridium aquilinum (L.) Kuhn collected to experimental plots treated with cadmium dust. New Phytol. 123, 313–324. [ Links ]
Vodnik D., Grcman H., Macek I., Van Elteren J.T. y Kovacevic M. (2008). The contribution of glomalinrelated soil protein to Pb and Zn sequestration in pol–luted soil. Sci. Total Environ. 392, 130–136. [ Links ]
Wong C.C., Wu S.C., Kuek C., Khan A.G. y Wong M.H. (2007). The role of mycorrhizae associated with vetiver grown in Pb–/Zn–contaminated soils: Greenhouse study. Restor. Ecol. 15, 60–67. [ Links ]














