Introducción
La docencia de cualquier disciplina debe atender las diversas formas de aprendizaje para lograr atender a los estudiantes con distintas formas de aprender. Una de esas formas es la kinestésica, el aprendizaje del tacto. El uso de laboratorios para que los estudiantes se apropien de conceptos científicos es imprescindible, tal y como lo demuestra Amaya Franky (2009) y Kirchhoff (2007) en sus estudios. La Escuela de Ciencias Ambientales de la Universidad Nacional en Costa Rica cuenta con un laboratorio destinado a la docencia en Química Ambiental y Tecnologías Ambientales. Durante años el laboratorio ha funcionado bajo el esquema de prácticas demostrativas, donde el estudiante observa, pero no ejecuta. Posteriormente en su ejercicio profesional se detecta esta carencia (Valerio Hernández et al., 2011). Es de suma importancia fomentar el desarrollo de habilidades de ejecución en el estudio de las ciencias ambientales. Ahora bien, una Escuela de Ciencias Ambientales debe ser pionera en lograr que la educación se logre con una menor contaminación.
Lorandi Medina, Hermida Saba, Hernández Silva y Ladrón de Guevara Durán (2011) proponen laboratorios virtuales, sin embargo, la tecnología actual aún no permite desarrollar muchos conceptos con esta herramienta, pero tanto Lorandi Medina et al. (2011) como Monge Najera y Méndez Estrada (2007) coinciden en las ventajas de los laboratorios virtuales. La herramienta de laboratorios virtuales puede ser un medio que llene un vacío en una amplia gama de tecnologías y ha sido una estrategia parcialmente utilizada en la Escuela de Ciencias Ambientales. Propiamente, la herramienta ha consistido en videos o bien en charlas magistrales de cómo se hace un laboratorio, no en simuladores, que ya son un poco más difíciles de generar. Sin embargo, considerando el tipo de carrera que se desarrolla en la Escuela de Ciencias Ambientales, a saber, la Ingeniería en Gestión Ambiental, ya que en principio se espera de los ingenieros un mayor conocimiento tecnológico que el de otros profesionales, por ende, la preparación virtual no es apropiada en este caso.
Asimismo, se espera que los ingenieros ambientales trabajen no solo de la mano de la tecnología, sino también de una forma amigable con el ambiente. Experiencias previas en la Escuela de Química (Vargas González et al., 2015) indican que se pueden desarrollar prácticas de laboratorio más amigables con el ambiente; la Escuela de Ciencias Ambientales debe ser ejemplo en esta materia y no lo ha logrado aún. Es por ello que se propone buscar herramientas para reducir los desechos generados en el laboratorio de docencia como parte de la educación transversal que los estudiantes deben adquirir en razón de su carrera.
Los egresados de la carrera de Gestión Ambiental insisten en la necesidad de un laboratorio más tecnológico, (Valerio Hernández et al., 2011), sin embargo, el camino a ello es la organización; la primera tarea es diseñar qué tipo de prácticas de laboratorio se espera seguir realizando con los muchachos, de forma tal que logren ellos descifrar la componente tecnológica de su carrera a través de estas prácticas. En razón de ello se propone el proyecto para fortalecer la situación actual del laboratorio de docencia en Química y Tecnologías Ambientales con miras a ofrecer a los estudiantes de la Escuela de Ciencias Ambientales medios para el desarrollo de sus habilidades profesionales.
Metodología
Con el objetivo de trabajar en los laboratorios de docencia de una forma menos contaminante, se evaluó para un curso las prácticas de laboratorio que se desarrollaban para buscar opciones que generaran menor cantidad de residuos y fueran más verdes, o tuvieran un mayor enfoque a química verde. Para ello se estudió primero, para cada práctica, las técnicas a aprender. Se valoró cada práctica según el uso de energía y el volumen de residuos generados. Luego se valoró qué tan verde era esa práctica y una propuesta que tuviese las mismas técnicas a evaluar incorporadas. Posteriormente, se determinó la cantidad de moles de residuos y se comparó en grupos de estudiantes la adquisición de conocimientos en cada práctica: la usual y la propuesta verde.
El alcance de la investigación fue una práctica del curso Medición de Agentes Contaminantes impartido en la Escuela de Ciencias Ambientales de la Universidad Nacional de Costa Rica. Propiamente la retrovaloración o valoración por retroceso en muestras sólidas. Para evaluar el uso de energía se establecieron criterios de uso de energía según se detalla a continuación:
Nulo cuando el procedimiento no requería el uso de ningún
Muy bajo cuando se requería utilizar un equipo una vez, pero que no fuera ese equipo un calentador.
Bajo cuando se requería del uso de equipos varias veces, pero ningún calentador.
Medio cuando se requería usar un equipo de bajo consumo de forma casi permanente.
Alto cuando el uso del equipo era por varias horas y era algún tipo de calentador o resistencia y la temperatura era menor a 100°C.
Muy alto cuando el uso del equipo era por varias horas y era algún tipo de calentador o resistencia y la temperatura era mayor a 100°C.
Para evaluar la generación de residuos peligrosos se estableció una escala en función de la cantidad y la peligrosidad:
Nulo cuando el procedimiento no generaba residuos peligrosos.
Muy bajo cuando se generaban menor de 10 ml de residuos por estudiante catalogados como de contaminación incipiente a baja; peligrosidad incipiente a baja.
Bajo cuando la generación era de 11 a 50 ml por estudiante de residuos peligrosidad incipiente a baja, o 10 ml de residuos de peligrosidad media a alta.
Medio cuando la generación era de 51 a 500 ml por estudiante de residuos peligrosidad incipiente a baja, o de 11 a 25 ml de residuos de peligrosidad media a alta.
Alto cuando la generación era de 501 a 1,000 ml por estudiante de residuos peligrosidad incipiente a baja, o de 26 a 50 ml de residuos de peligrosidad media a alta.
Muy alto cuando la generación era de más de 1,000 ml por estudiante de residuos peligrosidad incipiente a baja, más de 50 ml de residuos de peligrosidad media a alta.
La práctica que generó más residuos peligrosos fue seleccionada para sustituirla. Una vez seleccionada la práctica a sustituir se realizó una valoración según los principios de la química verde, mediante una adaptación (Tabla 1) de la metodología propuesta por Morales Galicia et al. (2011) y por Fernández Sánchez, Soto-Téllez y Hernández-Martínez (2013); la evaluación se realizó sobre la práctica de retrovaloración desarrollada en el curso Medición de Agentes Contaminantes del año 2015 I Ciclo y II Ciclo. Esta metodología consiste en una serie de pasos a desarrollar para generar un valor de 1 a 10 (Tabla 2), el cual cuanto más cercano a 10, más verde será el experimento.
Tabla 1 Metodología para realizar la evaluación verde de las prácticas evaluadas
| Paso | Procedimiento |
|---|---|
| 1 | Hacer un resumen del procedimiento a analizar que explique los pasos clave del proceso |
| 2 | Elaborar un diagrama de flujo del método experimental asignando a cada etapa una letra en minúscula y un orden alfabético consecutivo |
| 3 | Colocar para cada etapa experimental un cuadro conteniendo un número que indique el principio de la química verde que se aplica y evaluar asignando de1a 10 un valor según la Tabla 2, ese valor se anota entre paréntesis |
| 4 | Incluir a la par de cada etapa los pictogramas de toxicidad, inflamabilidad, corrosión y daño al medio ambiente, de reactivos, disolventes, productos y residuos |
| 5 | Anotar en una tabla los pasos experimentales del diagrama de flujo en el orden asignado y justificar la evaluación de los principios de la química verde realizada en el paso 3 |
| 6 | Sumar las puntuaciones asignadas para todas las veces que se evaluó un principio verde y dividir entre ese número de veces que se evaluó un principio verde |
| 7 | Presentar la evaluación en un diagrama mostrando la escala de colores y la ubicación en esa escala del experimento evaluado |
Fuente: adaptado de Morales Galicia et al. (2011)
Tabla 2 Escala de análisis y evaluación
Fuente: adaptado de Morales Galicia et al. (2011)
Además de la evaluación verde se realizó una medición de residuos. Para determinar la cantidad de residuos se realizó una cuantificación de moles partiendo de la estequiometría de reacción y asumiendo que las reacciones sucedían en un 100%.
A partir de los reportes de laboratorio se valoró la adquisición de los conocimientos que se consideraban importantes en la práctica a sustituir. Se analizaron las conclusiones del estudiantado con respecto al proceso de la retrovaloración, así como el desarrollo de los cálculos y el trabajo con muestras sólidas. Si se denotaba la adquisición del conocimiento se marcaba como A (adquirido), y si este no era explicito se marcaba como EP (en proceso). La importancia de esta valoración radicaba en que el estudiantado tuviera observaciones y conclusiones similares en ambos casos, de forma tal que la sustitució de la práctica no tuviera impacto en su formación.
Resultados y discusión
En primera instancia se valoró la técnica a aprender en esa práctica, el uso de energía y la cantidad de residuos generados asignando valores cualitativos. Se buscó sustituir la práctica que presentaba mayor impacto ambiental. Las prácticas desarrolladas en el curso se presentan en la Tabla 3.
Tabla 3 Prácticas de laboratorio desarrolladas en el curso Medición de Agentes Contaminantes 2013-2015
| Número de práctica | Nombre de la práctica |
|---|---|
| 1 | Técnicas básicas de laboratorio |
| 2 | Concepto de incertidumbre, incertidumbre equipo analítico y propagación de error |
| 3 | Calibración de equipo volumétrico |
| 4 | Preparación de una disolución patrón por el método directo y preparación de una disolución patrón por el método indirecto para análisis ambiental |
| 5 | Indicadores ácido base y volumetría: determinación de ácido acético con NaOH |
| 6 | Volumetría potenciométrica: determinación de mezcla de HCl y H3PO4 con NaOH |
| 7 | Volumetría de formación de complejos: dureza cálcica, magnésica y total del agua |
| 8 | Retrovaloración |
| 9 | Gravimetría de pérdida de masa |
| 10 | Gravimetría de precipitación |
| 11 | Determinación del espectro ultravioleta visible, el máximo de absorción y el coeficiente de absortividad. |
| 12 | Muestreo de aguas y determinación de hierro por espectrofotometría |
| 13 | Muestreo de aire y determinación de NO2 en aire método pasivo |
| 14 | Muestreo de suelos, pH y acidez en suelos |
Cada práctica de laboratorio busca no solo ejemplificar un concepto teórico, sino también permitir que el estudiantado adquiera una destreza de laboratorio importante. La valoración de las destrezas a adquirir fue determinada según el criterio técnico de más de 5 años de experiencia impartiendo el curso.
La Tabla 4 refleja la evaluación con respecto a la destreza a adquirir, el uso de energía y la generación de residuos peligrosos realizada. La valoración se realizó sobre prácticas desarrolladas en el laboratorio del curso Medición de Agentes Contaminantes, que implica una química analítica con aplicación ambiental y de las diversas prácticas trabajadas entre el 2013 y el 2015 (I ciclo). Se valoró cada práctica estudiando las técnicas de laboratorio que implicaban, así la práctica 1 de la Tabla 3 llamada «Técnicas básicas de laboratorio» estudiaba las técnicas de pipeteo, trasvase cuantitativo y lavado de cristalería; el uso de energía para esa práctica se consideró negativo y la generación de residuos peligrosos muy baja porque solo fue jabón.
Tabla 4 Estudio de las técnicas trabajadas en el curso Medición de Agentes Contaminantes
| Práctica y técnica a estudiar | Uso de energía | Generación de residuos peligrosos | |
|---|---|---|---|
| 1 | Pipeteo, trasvase cuantitativo, lavado de cristalería | Negativo | Muy bajo |
| 2 | Incertidumbre, factores de conversión | Muy bajo | Negativo |
| 3 | Calibración de balones y pipetas, cuidados en calibración | Muy bajo | Negativo |
| 4 | Preparación de disoluciones estándar de diferentes formas | Muy bajo | Bajo |
| 5 | Familiarizarse con indicadores y volumetría directa | Muy bajo | Bajo |
| 6 | Volumetría potenciométrica para ácido con más de un protón | Bajo | Medio |
| 7 | Volumetría por diferencia: total, cálcica y magnésica | Bajo | Medio |
| 8 | Valoración de muestras sólidas y retrovaloración | Muy bajo | Muy Alto |
| 9 | Gravimetría de pérdida de masa y uso del embudo separador | Medio | Alto |
| 10 | Gravimetría de precipitación y filtración al vacío | Muy alto | Bajo |
| 11 | Determinación del espectro ultravioleta y longitud de medición | Medio | Bajo |
| 12 | Determinación espectrofotométrica | Medio | Bajo |
| 13 | Muestreo de aire y determinación en aire | Bajo | Alto |
| 14 | Determinación en suelos y muestreo de suelos | Bajo | Bajo |
La práctica 8 tocaba el tema de retrovaloración; al analizarla se vio que las técnicas involucradas no eran solo la retrovaloración, sino también la valoración de muestras sólidas. El uso de energía fue muy bajo (Tabla 4). También fue la que se valoró como la mayor generadora de residuos peligrosos como muy alto, esto se debe a que se genera casi 150 ml de disolución de cromo con concentración cercana a 1 mol/l por estudiante, ya que era una determinación de la materia orgánica en suelos mediante la degradación de la materia orgánica con dicromato de potasio en medio ácido y su posterior retrovaloración con sal de Mohr (Tabla 5). Por esta razón se buscó sustituir la práctica para el II Ciclo del 2015 con una que reflejara el principio y la técnica de la retrovaloración, pero con mayor acercamiento a los principios de la química verde.
Tabla 5 Procedimiento de la práctica de retrovaloración del I Ciclo 2015
| Procedimiento |
|---|
| A 0.5 g de suelo en un balón de 50 ml se adicionan 10 ml de K2Cr2O7 y luego 10 ml de H2SO4. Se agita y se deja enfriar, se lleva a 50 ml con agua destilada. 10 ml de esa disolución se trasvasan a un erlenmeyer, se le adicionan 5 gotas de H3PO4 y se valoran el K2Cr2O7 sobrante con sal de Mohr (sulfato de hierro II y amonio) usando difenilguanidina como indicador. Este proceso se repite 3 veces |
Así, es entonces posible hacer la sustitución de prácticas de laboratorio manteniendo la misma calidad en la educación, pero con una contaminación ambiental prácticamente nula.
La Tabla 6 y la Figura 1 muestran la evaluación según los principios de la química verde para la práctica clásica realizada de retrovaloración con dicromato de potasio y sal de Mohr.
Tabla 6 Evaluación verde de la práctica de retrovaloración utilizada del 2013 al 2015.
| Paso | Evaluación |
|---|---|
| a | Se emplean reactivos bastante tóxicos y peligrosos en altas concentraciones, por lo cual se evalúan los principios 1, 10 y 12 como totalmente cafés, con una puntuación de 1 |
| b | Se usa un disolvente inocuo, por lo cual se evalúa el principio 5 como un buen acercamiento verde con una puntuación de 7; no se le da un valor mayor porque no se da el proceso en ausencia de disolvente |
| c | De nuevo se utilizan reactivos peligrosos, pero al ser poca cantidad se evalúan los principios 1 y 12 como ligeramente café, con una puntuación de 4 |
| d | Se valora los principios 1 y 12 como totalmente cafés porque se usan reactivos nocivos e irritantes en altas concentraciones y debe repetirse el proceso 3 veces |
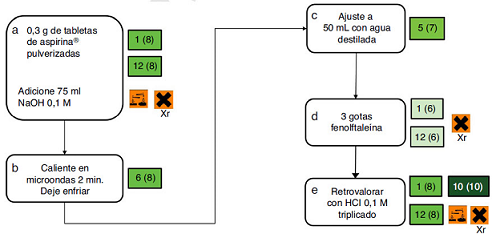
La práctica alternativa de retrovaloración propuesta implicó un tratamiento de neutralización del ácido acetilsalicílico presente en una tableta de Aspirina con hidróxido de sodio y la retrovaloración con ácido clorhídrico (Tabla 7).
Tabla 7 Procedimiento de la práctica de retrovaloración utilizada en el I Ciclo 2015.
| Procedimiento |
|---|
| A 0.3 g de Aspirina® en un erlenmeyer de 50 ml se adicionan 75 ml de NaOH y luego se coloca en un microondas por 3 min. Se calienta varias veces hasta que el volumen baje a la mitad. Se agita y se deja enfriar, se trasvasa a un balón de 50 ml y se afora con agua destilada; 10 ml de esa disolución se trasvasan a un erlenmeyer, y se valora el NaOH sobrante con HCl usando fenolftaleína como indicador. Este proceso se repite 3 veces |
Se realizó también la evaluación verde de esta práctica. La Tabla 8 y la Figura 2 muestran la evaluación según los principios de la química verde para la práctica propuesta con HCl y NaOH. De la observación de las figuras se desprende que la práctica propuesta de retrovaloración del ácido acetilsalicílico es una práctica que tiene un mayor acercamiento verde. Los reactivos utilizados en la práctica alternativa, como se observa en la Figura 2, presentan mucha menor toxicidad que los que se utilizaban tradicionalmente, pasando de reactivos altamente reconocidos por su toxicidad como el Cromo VI del dicromato de potasio a reactivos apenas corrosivos, y que en las concentraciones utilizadas en realidad son de peligrosidad incipiente. Aunado a ello, en ambos casos se mantiene el trabajo con muestra sólida, así como el proceso de retrovaloración, que eran las técnicas que se quería trabajar en esta práctica. En las Figuras 1 y 2 se aprecia además que se pasa de reacciones con poco volumen y concentraciones elevadas a reacciones con volumen similar, pero concentraciones 10 veces menores.
Tabla 8 Evaluación verde de la práctica de retrovaloración utilizada en el II Ciclo del 2015
| Paso | Evaluación |
|---|---|
| a | Se utilizan reactivos corrosivos y nocivos, pero en muy baja concentración. Además, se utiliza un reactivo prácticamente inocuo como lo es la Aspirina®, por ello se evalúan los principios 1 y 12 con un muy buen acercamiento verde, que le da un valor de 8 |
| b | Se evalúa el principio 6 debido al uso de energía. Se le asigna un valor de 8 porque, si bien se usa una fuente de energía verde, el hecho de requerir energía hace que se valore como con un muy buen acercamiento verde |
| c | Se usa un disolvente inocuo, por lo cual se evalúa el principio 5 como un buen acercamiento verde con una puntuación de 7; no se le da un valor mayor porque no se da el proceso en ausencia de disolvente |
| d | De nuevo se utilizan reactivos nocivos, pero al ser poca cantidad se evalúan los principios 1 y 12 como ligero acercamiento verde, con una puntuación de 6 |
| e | Se valora los principios 1 y 12 con un muy buen acercamiento verde porque se usan reactivos nocivos e irritantes en muy bajas concentraciones y debe repetirse el proceso 3 veces. Se valora el principio 10 como totalmente verde, ya que el producto del proceso es una sal biodegradable |
La Figura 3 muestra la evaluación final de ambas prácticas. La práctica tradicional tuvo una evaluación 3 que, según señalan Morales Galicia et al. (2011), es una práctica «medianamente café». Se puede apreciar que el cambiar la práctica de retrovaloración a una práctica con reactivos menos contaminantes permite una práctica más verde y por ende menor contaminación. La práctica propuesta tuvo una evaluación de 8, que se señala como «muy buen acercamiento verde» según la metodología de evaluación trabajada.

Figura 3 Resultado de la evaluación según los principios de la química verde para las prácticas de retrovaloración de dicromato con sal de Mohr para determinar materia orgánica (A) y de NaOH con HCl para determinar Aspirina
Mediante los reportes de laboratorio se hizo una evaluación de la adquisición de los conocimientos clave de la práctica utilizada en el I Ciclo del 2015 versus la utilizada en el II Ciclo del 2015. Los conocimientos valorados fueron: ¿qué es una retrovaloración? (R); ¿cómo hacer los cálculos en una retrovaloración? (C), y ¿cómo trabajar con una muestra sólida? (MS). La valoración se hizo sobre cada concepto asignando una A (adquirido) si se evidenciaba la adquisición del conocimiento y EP (en proceso) si no se evidenciaba, y tal y como se observa en la Figura 4 para los dos casos el aprovechamiento se mantiene similar. Por ejemplo, el caso del concepto de retrovaloración, tanto en el I Ciclo (sal de Mohr) como en el II Ciclo (Aspirina), se mantiene una proporción parecida de tamaño. Y el mismo caso se presenta con los demás conceptos MS y C, en la Figura 4 se observa presentan relaciones análogas, las diferencias radican en la cantidad de estudiantes de cada ciclo.

Figura 4 Evaluación de la adquisición de conocimientos en los puntos de la práctica para el año 2015 con práctica normal (I Ciclo) y práctica verde (II Ciclo). C: cálculos; MS: muestra sólida; R: retrovaloración.
Con el fin de evaluar la generación de residuos se determinó por balance de masa según la estequiometria de las reacciones la cantidad de moles que se generaban de residuos según los procedimientos realizados. La Figura 5 representa los resultados de esa cuantificación. Se observa claramente como la generación de residuos en la práctica de retrovaloración de dicromato con sal de Mohr, es considerablemente mayor 3.3003 mol en relación con la retrovaloración de hidróxido de sodio con ácido clorhídrico, que fue 0.2003 mol. Así la práctica genera también un menor impacto ambiental en cuanto a cantidad de residuos.
Asimismo, para el caso en estudio cuyos grupos rondaban en cada ciclo los 40 estudiantes, si se multiplica la por cada práctica, la reducción por ciclo será de 132 moles de residuos de cromo y ácido fuete a 8 mol de residuos de salicilato de sodio.
Conclusiones
La determinación de materia orgánica en suelos con un exceso de dicromato y retrovalorando con sal de Mohr presenta un acertamiento a café más que a verde, con una calificación de 3 “medianamente café”. Mientras que la determinación de Aspirina® con exceso de hidróxido de sodio y retrovalorando con ácido clorhídrico presenta un acercamiento verde de 8, que es un “muy buen acercamiento verde”.
Es posible cambiar las prácticas de laboratorio logrando el mismo resultado en la población estudiantil, pero con reactivos que tengan menor toxicidad logrando con ello tanto el aprendizaje de la técnica como una gestión adecuada de residuos, ya que la evidencia demuestra que tanto en la retrovaloración de dicromato con sal de Mohr como en la de hidróxido de sodio con ácido clorhídrico se logra la misma adquisición de conocimientos.
La generación de residuos es sustancialmente menor pasando de 3.3 mol de residuos de peligrosidad alta a 0.2 mol de residuos de peligrosidad incipiente. Se concluye que la química verde permite trabajar una educación con generación de residuos mínima.











 text new page (beta)
text new page (beta)