Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Educación química
Print version ISSN 0187-893X
Educ. quím vol.20 n.2 Ciudad de México Apr. 2009
Doble vía
Precisiones sobre la geometría de la molécula de la portada de enero 2008
Aarón Pérez-Benítez
Facultad de Ciencias Químicas de la Benemérita Universidad Autónoma de Puebla. 14 sur y av. San Claudio, colonia San Manuel, 72570 Puebla, Pue. Correo electrónico: aronper@siu.buap.mx
Nuestro querido amigo Aarón Pérez Benítez nos entregó esta carta sobre la geometría de la molécula del fullerano Ih-C180H180 que apareció en nuestra portada del número de enero-marzo de 2008, gracias a la gentileza de la revista ChemPhysChem y del autor, el profesor Linnolahti. Además del análisis de la estereoquímica de esa molécula, Aarón nos proporciona una plantilla para modelarla, por lo que esta carta podría considerarse como artículo de la sección CÓMO SE MODELA. Gracias Aarón.
Acerca de la estereoquímica del fullerano Ih-C180H180
Estimado Andoni:
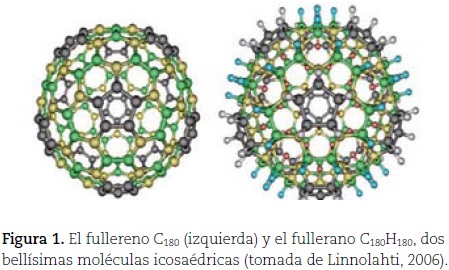
En la portada de la revista número 1 (enero de 2008), volumen 19 de Educación Química apareció publicada la imagen de una molécula bellísima y aparentemente complicada de visualizar: el fullerano Ih-C180H180, el pariente totalmente hidrogenado del fullereno Ih-C180 (figura 1).
Con el fin de apoyar a nuestros lectores a conceptualizar la estructura del Ih-C180H180, hasta ahora sólo probablemente existente en el polvo interestelar, me permito hacer los siguientes comentarios:
1. Nótese que las terminaciones "ano" y "eno" indican que estas moléculas están totalmente hidrogenadas y deshidrogenadas, respectivamente, según las reglas de nomenclatura propuestas por la IUPAC (Moss, 2008).
2. El hecho de agregar un hidrógeno a cada uno de los carbonos del C180 para obtener el C180H180 implica un cambio en la geometría de estos carbonos (ahora muy cercana a la tetraédrica), pero eso no conlleva una pérdida de la simetría molecular icosaédrica, Ih, de acuerdo con los estudios teóricos reportados por Linnolahti y sus colaboradores (Linnolahti, 2006). Por lo tanto, su estereoquímica puede ser estudiada de la misma manera en la que se hizo para el Ih-C500 (Pérez-Benítez, 2000); es decir, considerando solamente una de las 20 secciones triangulares del icosaedro imaginario en el que pueden inscribirse este tipo de moléculas. Estas secciones triangulares se señalan con líneas punteadas en las figuras 2-4, (3).
3. Desde un punto vista exterior a la molécula y perpendicular al plano formado por los tres átomos de carbono marcados con la letra "a" de esa sección, se puede realizar un dibujo en proyección de cuña (figura 2i), en el que tres de los sustituyentes de cada Ca (los dos Cb y el Cc) se encuentran cercanos al observador y el cuarto sustituyente (Ha) se encuentra alejado del observador; es decir, hacia el exterior y el interior del plano del papel (figuras 2ii y 3). Así que en un cuarto plano, todavía más cercano al observador que el formado por los Q/s y Cb's, se encuentran los hidrógenos Hb y Hc (figura 2ii).
4. La equivalencia entre los carbonos de esa sección —y de ahí sus etiquetas— se determinó en función de su conectividad: los vértices "c" forman parte de un pentágono y dos hexágonos, es decir son vértices 5:6:6. A un enlace de distancia de ellos se encuentran los vértices "a" y a dos enlaces los "b"; por lo tanto, aunque ambos son 6:6:6, son diferentes entre sí.
5. La desigualdad que hay entre los carbonos determina automáticamente la desigualdad que hay entre los hidrógenos unidos a ellos, por lo que en la figura 2ii se etiquetan como Ha, Hb y Hc y en 2iii se modelan con esferas rojas, azules y blancas, respectivamente.
6. Para obtener esa disposición de los hidrógenos del hexágono central de dicha sección se requiere una conformación de silla con seis hidrógenos axiales: tres apuntando al observador (los azules) y tres alejándose de él (los rojos). Los tres blancos pertenecen a los ciclos de cinco carbonos y también apuntan hacia el observador (figura 2iii).
7. Multiplicando los tres H's interiores (Ha) y los seis exteriores (Hb y Hc) que hay en cada sección de la molécula, por las 20 caras que constituyen un icosaedro, se obtienen los 60 hidrógenos interiores y los 120 hidrógenos exteriores del C180H180 que se comentaron en la página 1 de la revista Educación Química mencionada. Sin embargo, ahora podemos puntualizar que la relación entre elloses: 60Hb: 60Hb:60Hc.
8. La estereoquímica de esta molécula puede ser analizada objetivamente si se elabora un modelo molecular recortando la plantilla de la figura 3. Al eliminar las puntas y pegar las pestañas se forman pentágonos huecos a través de los cuales se pueden observar a los pentágonos alternados de los vértices opuestos. Este hecho permite ubicar en esos sitios a los 12 ejes impropios de rotación-reflexión de orden diez, S10, que caracterizan al grupo puntua Ih l (Dresselhaus, 2007). El modelo terminado se presenta en la figura 4.
9. Este estudio no tendría mucho sentido sino es porque se puede predecir el aspecto que tendrían los espectros de resonancia magnética nuclear de 13C y 1H. Dado que la relación de carbonos es 1:1:1, el espectro de RMN13C presentaría tres señales de igual intensidad, muy probablemente con desplazamiento químico Cc>Cb>Ca. Del mismo modo, el espectro de RMN1H presentarían tres multipletes con integrales 1:1:1 y desplazamiento químico Hc>Hb>Ha, pues los Ha se encuentran muy protegidos al estar dentro de la molécula y, por lo tanto, requerirían mayor intensidad del campo magnético aplicado para resonar. En contraste, los Hc están geométricamente más expuestos en los vértices del icosaedro que los Hb en las caras y requerirían menor intensidad del campo aplicado. Dejo como ejercicio para los estudiantes de una clase de espectroscopía de RMN la determinación de la multiplicidad de las señales de los espectros mencionados.
Referencias
Dresselhaus, M.S., Dresselhaus, G., Jorio, A., Group theory: Application to the physics of condensed matter (p. 485), Berlin: Springer-Verlag, 2007. [ Links ]
Linnolahti, M., Karttunen, A.J., Pakkanen, T.A., ChemPhys-Chem., 7(8), 1661-1663, 2006. [ Links ]
Moss, G.P., Powell, W.H., Nomenclature for the C60-Ih and C70-D5h(6) Fullerenes (IUPAC Recommendations 2002), consultada por última vez el 23 de diciembre de 2008, de la URL http://www.chem.qmul.ac.uk/iupac/fullerene/ [ Links ]
Pérez-Benítez, A. y Santiesteban, F., Acerca de la estereoquímica del fullereno gigante Ih-C500: Un modelo tridimensional y cálculo de las líneas de su espectro de RMN13C, Educ. quím., 11(2), 284, 2000. [ Links ]