Introducción
Lisianthus (Eustoma grandiflorum (Raf.) Shinn) es una especie ornamental que se cultiva para producir flor de corte o plantas en maceta y que tiene potencial de comercialización por su belleza, su variedad de colores y larga vida en florero (Castillo et al., 2018), esta especie se ha posicionado en el gusto de los consumidores a nivel mundial (Kiamohammadi y Hashemaabadi, 2011), su hábitat natural es en zonas áridas y semiáridas del sur de Estados Unidos de América y Norte de México (de la Riva et al., 2013).
El cultivo se adapta a condiciones extremas en comparación con la mayoría de las especies florícolas, debido a su tolerancia a una conductividad eléctrica elevada (López et al., 2014). Tradicionalmente el cultivo se siembra en suelo y existe poca información acerca del comportamiento de esta planta en hidroponía, de acuerdo a de la Riva et al. (2013), el cultivo sin suelo constituye una alternativa moderna de producción aplicable a zonas áridas y semiáridas. Además de ser una técnica muy adecuada para producirse en lugares en que la calidad del suelo limita la producción, ya sea por excesiva salinidad, iones tóxicos específicos, alta pedregosidad o elevada infestación de agentes patógenos, como Fusarium spp.
La experimentación en sistemas hidropónicos contempla la medición de variables destructivas, sin embargo, existen avances tecnológicos en el desarrollo de hardware y software que han permitido implementar un procedimiento no destructivo para obtener y procesar imágenes (Padrón-Pereira y Arapa-Carcasi, 2016).
En este sentido algunos autores Dutta-Gupta e Ibaraki (2015) han desarrollado algoritmos y procedimientos que ha sido una herramienta utilizada en la investigación botánica y en la agricultura, una de las herramientas utilizadas es el color en las hojas y flores que podrían ser analizados con los valores de (análisis de imágenes basadas en la intensidad de los tres colores primarios rojo (R), verde (G) y azul (B), RGB siendo que las células vegetales tienen varios tipos de pigmentos, que son la fuente de su color, como las hojas de las plantas, entre los cuales la clorofila es la más importante, el verde de una hoja depende del contenido de clorofila y proporciona información clave para el diagnóstico del estado fisiológico de la planta, incluido el estado del nitrógeno o del agua. Yadav et al. (2010) estimaron el contenido de clorofila en las hojas de las plántulas de papa micropropagadas utilizando los valores de RGB.
La información obtenida mediante análisis de imágenes puede ser utilizada para el ajuste de las soluciones nutritivas, lo cual es útil en procesos de automatización.
Considerando lo anterior el objetivo del presente trabajo fue evaluar por medio de imágenes digitales el cambio en el color de las hojas y de las flores en el cultivo de lisianthus en hidroponía con diferentes soluciones nutritivas.
Materiales y Métodos
Material vegetal
El experimento fue realizado dentro de un invernadero en la Universidad Politécnica de Francisco I. Madero, en el estado de Hidalgo, que mantuvo una temperatura media de 24.61 (C y una humedad relativa promedio de 69.29%. Las plántulas de lisianthus utilizadas para el experimento fueron de la variedad mariachi blanco, con una altura promedio de 4 cm y con tres pares de hojas verdaderas, que fueron trasplantadas el día 22 de marzo del 2018, las plántulas fueron colocadas en bolsas de polietileno de 15 × 20 cm utilizando tezontle como sustrato, previamente humedecido con agua potable. Se colocaron dos plántulas por bolsa y en cada una de ellas fueron colocadas en hilera en un sistema hidropónico.
Soluciones nutritivas
Las soluciones nutritivas (SN) evaluadas fueron preparadas con agua potable, a la cual se le realizó previamente un análisis químico para formular los tratamientos (Cuadro 1).
Cuadro 1 Análisis químico del agua utilizada para la preparación de soluciones nutritivas evaluadas en plantas de lisianthus.
Table 1. Chemical analysis of the water used for preparation of the nutritional solutions evaluated in lisianthus plants.
F.Q. = fórmula química; mg L-1 = miligramos por litro; mEq L-1 = miliequivalentes por litro.
F.Q. = chemical formula; mg L-1 = milligrams per liter; mEq L-1 = milliequivalents per liter.
Las soluciones nutritivas ensayadas fueron cuatro, como testigo se utilizó la solución Steiner (SN1), y el resto de los tratamientos fueron soluciones modificadas a partir de esta (Cuadro 2). En la solución nutritiva dos, se utilizó el doble de la concentración de la solución Steiner, lo cual generó una conductividad eléctrica elevada (6 dS m-1 en promedio). Por otro lado, la SN3, fue adicionada con una cantidad elevada de K (14 mEq L‑1), mientras que la solución nutritiva 4 con una mayor cantidad de Ca (18 mEq L-1) en relación con el testigo.
Cuadro 2: Tratamientos para evaluar el crecimiento y desarrollo en plantas de lisianthus cv. mariachi blanco
Table 2: Treatments to evaluate growth and development in lisianthus cv. white mariachi plants.
|
Fertilizantes |
||||
|
- - - - - - - - mEq L-1 - - - - - - - - |
||||
|
Ca(NO3) 4H2O |
0.5 |
9.5 |
2.5 |
9.5 |
|
KNO3 |
7.5 |
10.47 |
10.96 |
1.96 |
|
Mg(NO3)2 |
2.49 |
|||
|
KH2PO4 |
0.8 |
1.51 |
||
|
MGSO4H2O |
2.5 |
|||
|
K2SO4 |
0.42 |
2.5 |
2.53 |
4.53 |
SN = solución nutritiva; mEq L-1 = miliequivalentes por litro.
SN = nutrient solution; mEq L-1 = milliequivalents per liter.
Una vez formuladas las soluciones nutritivas se instaló un sistema de riego con cuatro tanques con diferentes capacidades, se diseñó un sistema automático para que cada uno de los tanques por separado pudiera realizar los riegos conforme a las diferentes soluciones nutritivas. Todas las plantas se regaron durante un minuto cada hora desde la 9:30 am hasta las 5:40 pm.
Desde el trasplante hasta el día 27 todas las plantas se regaron con la solución nutritiva 1, para efectos de aclimatación, posteriormente se hicieron cuatro grupos de 50 macetas (100 plantas), cada grupo fue regado con una solución nutritiva diferente, después de 72 días se aumentó el tiempo de riego a 1.5 minutos.
Variables evaluadas
Altura de la planta y número de hojas. Estas dos variables fueron evaluadas cada semana a partir del día 27 después del trasplante (DDT), se realizaron 19 repeticiones por cada tratamiento, se dejó de tomar datos a los 85 días (DDT).
Número de botones florales. Se contó el número de botones florales por repetición a los 64 DDT, cuando en la mayoría de ellas se observó el botón floral.
Diámetro de la flor. Esta variable se midió con un vernier digital, en una muestra de seis plantas (repeticiones) por tratamiento, flores totalmente abiertas.
Captura y análisis de imágenes. Para la captura de las imágenes se utilizó una cámara digital de marca Samsung de ocho megapíxeles, configurada en modo automático de enfoque. Las imágenes se tomaron a los 61, 74 y 85 días después del trasplante. Se capturó una imagen de cada una de las plantas del experimento a una distancia constante (50 cm). Posteriormente las imágenes fueron cargadas en el programa R Statistics (R Core Team, 2018), por medio de la paquetería reportada por Ma et al. (2010). Primero las imágenes fueron descompuestas en canales RGB, pertenecientes a los espacios del color del mismo nombre y se descartaron los pixeles que no correspondían a la planta, posteriormente se obtuvieron los promedios RGB. Además, se generaron variables a partir de los datos de RGB obtenidos de la imagen de acuerdo a las siguientes ecuaciones:
donde:
Fo = distancia euclidiana de R a G.
Fk = distancia euclidiana de B a G.
Fv = distancia euclidiana de B a R.
Área RGB (×) = área del triángulo generado por los vértices RGB.
Resultados y Discusión
Altura de la planta
Durante el ciclo de Lisianthus, se observó una diferencia significativa en la SN1 (Steiner) con respecto a la SN4 con mayor cantidad de Ca, el comportamiento de SN1 fue constante durante el desarrollo y crecimiento de lisianthus, mientras que la solución nutritiva donde se incrementó el doble de calcio no tuvo efecto en la altura de la planta (Cuadro 3).
Cuadro 3 Altura promedio (cm) en plantas de lisianthus cv. mariachi blanco, cultivadas con diferentes soluciones nutritivas.
Table 3. Average height (cm) in lisianthus cv white mariachi plants grown with different nutritional solutions.
|
- - - - - - - - - - - - - - - - - - - - cm - - - - - - - - - - - - - - - - - - - - |
||||
|
27 |
8.6920 a† |
8.6640 a |
7.7440 ab |
6.8480 b |
|
37 |
13.7526 ab |
14.0789 a |
12.9368 ab |
12.1500 b |
|
43 |
18.6842 a |
16.5368 ab |
15.4579 bc |
13.9947 c |
|
50 |
22.468 a |
21.063 ab |
19.474 bc |
17.763 c |
|
57 |
27.911 a |
27.468 a |
25.363 ab |
23.353 b |
|
64 |
34.300 a |
32.700 ab |
30.358 ab |
29.200 b |
|
71 |
37.905 a |
37.000 a |
34.268 a |
33.789 a |
|
78 |
41.984 a |
40.268 a |
37.705 a |
39.376 a |
|
85 |
45.632 a |
43.332 a |
40.368 a |
42.916 a |
DDT = días después del trasplante; SN = solución nutritiva; † Medias con letras iguales entre filas no indican diferencia estadística significativa (Tukey, P ≤ 0.05).
DDT = days after transplant; SN = nutrient solution; † Means with equal letters between rows do not indicate significant statistical difference (Tukey’s, P ≤ 0.05).
La altura obtenida a partir del día 78 DDT en el presente estudio coincide con (Melgares de Aguilar, 1996), quien indica que llegan alcanzar una altura entre 40 y 50 cm dependiendo de la variedad.
Número de hojas
Se encontró una diferencia significativa en el día 27 en la solución nutritiva 1 (Steiner) con respecto a la SN4 con una mayor cantidad de Ca, mientras que para el día 37 la diferencia significativa se encontró entre la SN2 con respecto a la SN4, este comportamiento se mantuvo en el resto de los días (Cuadro 4).
Cuadro 4: Número de hojas promedio en plantas de lisianthus cv. mariachi blanco, cultivadas con diferentes soluciones nutritivas.
Table 4: Average number of leaves in lisianthus cv white mariachi plants grown with different nutritional solutions.
|
- - - - - - - - - - - - - - - - - - Número de hojas - - - - - - - - - - - - - - - - - - |
||||
|
27 |
15.8400 a† |
15.9200 a |
14.0800 b |
13.4400 b |
|
37 |
17.7895 ab |
19.5263 a |
17.8421 ab |
16.9474 b |
|
43 |
21.2105 ab |
22.2105 a |
20.4211 ab |
19.2632 b |
|
50 |
24.7368 a |
24.0000 a |
22.4211 ab |
20.3684 b |
|
57 |
27.474 ab |
29.842 a |
28.368 a |
23.316 b |
|
64 |
28.947 a |
31.000 a |
31.368 a |
26.737 a |
|
71 |
30.947 ab |
33.211 a |
32.684 a |
26.737 b |
|
78 |
31.368 ab |
34.526 a |
34.842 a |
27.579 b |
|
85 |
31.526 ab |
34.526 a |
34.842 a |
27.579 b |
DDT = días después del trasplante; SN = solución nutritiva; † Medias con letras iguales entre filas no indican diferencia estadística significativa (Tukey, P ≤ 0.05).
DDT = days after transplant; SN = nutrient solution; † Means with equal letters between rows do not indicate significant statistical difference (Tukey’s, P ≤ 0.05).
Resultados similares se encontraron con Miranda-Villagómez et al. (2014) en el cultivo de freesia × hybrida en hidroponía, donde evaluaron diferentes concentraciones de la solución Steiner y no encontraron diferencias significativas entre tratamientos, mencionando también que se detectó una notable disminución en altura de planta, longitud del tallo floral, área foliar, menor concentración de clorofila, longitud de espiga y grosor de tallo con la solución Steiner a 100%.
Número de botones y diámetro de la flor
No hubo diferencia significativa en ninguno de los tratamientos para la variable de número de botones, mientras que, para la variable de diámetro de la flor, se encontró una diferencia significativa en la solución nutritiva Steiner con respecto a la solución nutritiva cuatro con una mayor concentración de Ca (Cuadro 5).
Cuadro 5: Número de botones a los 64 DDT y diámetro de flor en el día 85 DDT en plantas de lisianthus cv. mariachi blanco, cultivadas con diferentes soluciones nutritivas.
Table 5: Number of buds at 64 days after transplant (DAT) and flower diameter on day 85 DAT in lisianthus cv white mariachi plants, grown with different nutritional.
|
Solución nutritiva |
Número de botones |
Diámetro de la flor |
|
mm |
||
|
64 DDT |
85 DDT |
|
|
1 |
3.8947 a† |
72.253 a |
|
2 |
3.4211 a |
62.245 ab |
|
3 |
3.0000 a |
59.833 bc |
|
4 |
2.0000 a |
49.612 c |
DDT = días después del trasplante; † Medias con letras iguales entre filas no indican diferencia estadística significativa (Tukey, P ≤ 0.05).
DDT = days after transplant; † Means with equal letters between rows do not indicate significant statistical difference (Tukey’s, P ≤ 0.05).
Resultados similares fueron encontrados por Halevy y Kofranek (1984) quienes encontraron un diámetro de flor de 6 a 9 cm en cuatro variedades de lisianthus cultivada en hidroponía en un invernadero.
Cambios en el color de las hojas
Durante el desarrollo y crecimiento de lisianthus el color de la hoja no se vio afectada por los tratamientos a partir de las modificaciones que se le realizaron a la solución Steiner. La variable R solo presentó diferencia significativa en el tratamiento uno (Steiner) con respecto al tratamiento cuatro con mayor cantidad de calcio (18 mEq L-1), sin embargo, no ocurrió lo mismo para las demás variables y solo este fenómeno se presentó en el día 61 DDT.
El color de las hojas de lisianthus en los días 74 y 85 no mostraron diferencias en aquellos tratamientos donde se aumentó las dosis de potasio y calcio, aparentemente las funciones fisiológicas de estos nutrimentos no están relacionadas de manera directa con el color de las hojas (Azcón y Talón, 2013) (Cuadro 6).
Cuadro 6: Resultados obtenidos en los valores rojo, verde, azul (RGB) y variables artifíciales en el color de la hoja.
Table 6: Results obtained in red, green, and blue (RGB) color model intensity values and artificial variables in leaf color.
|
Variables | |||||||||
|
|
R |
G |
B |
Y |
|||||
|
61 DDT | |||||||||
|
110 a |
137 a |
121 a |
98 a |
214 a |
220 a |
204 a |
319 a |
69 a |
|
|
104 ab |
132 a |
118 a |
96 b |
204 a |
210 a |
194 a |
304 a |
64 a |
|
|
104 ab |
135 a |
119 a |
96 ab |
208 a |
216 a |
198 a |
311 a |
66 a |
|
|
P |
0.044 |
0.648 |
0.707 |
0.003 |
0.328 |
0.577 |
0.347 |
0.418 |
0.393 |
|
74 DDT | |||||||||
|
133 a |
151 a |
130 a |
95 a |
247 a |
244 a |
233 a |
362 a |
83 a |
|
|
132 a |
151 a |
129 a |
94 a |
246 a |
244 a |
233 a |
361 a |
83 a |
|
|
125 a |
145 a |
125 a |
94 a |
234 a |
234 a |
222 a |
346 a |
77 a |
|
|
124 a |
145 a |
123 a |
94 a |
233 a |
232 a |
220 a |
343 a |
76 a |
|
|
P |
0.262 |
0.296 |
0.251 |
0.286 |
0.281 |
0.278 |
0.266 |
0.275 |
0.256 |
|
85 DDT | |||||||||
|
159 a |
172 a |
144 a |
94 a |
286 a |
279 a |
271 a |
418 a |
103 a |
|
|
148 a |
164 a |
139 a |
94 a |
271 a |
266 a |
256 a |
396 a |
95 a |
|
|
140 a |
153 a |
128 a |
93 a |
254 a |
248 a |
239 a |
371 a |
86 a |
|
|
145 a |
162 a |
134 a |
93 a |
266 a |
260 a |
250 a |
388 a |
92 a |
|
|
P |
0.425 |
0.306 |
0.412 |
0.738 |
0.369 |
0.350 |
0.391 |
0.370 |
0.381 |
SN = solución nutritiva; Fo = distancia euclidiana de R a G; Fk = distancia euclidiana de B a G; Fv = distancia euclidiana de B a R; S = semiperimetro; A = área. † Medias con letras iguales entre filas no indican diferencia estadística significativa (Tukey, P ≤ 0.05).
SN = nutrient solution; Fo = euclidean distance from R to G; Fk = euclidean distance from B to G; Fv = euclidean distance from B to R; S = semi-perimeter; A = area. † Means with equal letters between rows do not indicate significant statistical difference (Tukey’s, P ≤ 0.05).
Resultados similares fueron encontrados por Riccardi et al. (2014), quienes compararon el color (RGB) de imágenes fotográficas y el contenido relativo de clorofila, con la concentración de clorofila foliar, obtenida por extracción de pigmentos de hojas de amaranto (Amaranthus sp.) y quinua (Chenopodium quinoa Willd) por otro lado, se observaron cambios en el color de las hojas a través del tiempo, a los 62 DDT con respecto a los días 74 y 84 encontrando valores de RGB ligeramente más elevados en comparación con la fecha anterior, lo cual indicaría una coloración más clara en las hojas, lo que a la vista humana implicaría un color verde de menor intensidad (Figura 1).
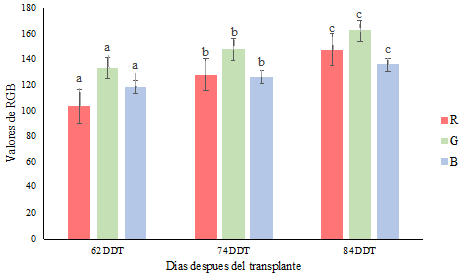
Resultados similares se encontraron en el índice SPAD en plantas de lisianthus en función de diferentes dosis de nitrógeno en un ambiente protegido (Ribeiro et al., 2015), dicho índice disminuyó con el aumento de la dosis de nitrógeno a partir del día 63 y 105 DDT, momento en el que las plantas iniciaron el proceso reproductivo y la hoja se tornaban menos verdes debido a una disminución en la concentración de nitrógeno foliar, esto puede ser debido a que el movimiento del nitrógeno de las hoja se fue hacia los demás órganos de las plantas, principalmente para la formación de los botones florales, por otro lado (Rojas et al., 2017) menciona que uno de los síntomas más visibles en el cambio de color es a consecuencia de la degradación de las clorofilas.
Efecto de la SN sobre el color de las flores
Los datos mostraron diferencias estadísticamente significativas en las flores que crecieron en la solución nutritiva tres, dicha solución contenía una concentración de potasio elevada en comparación con los demás tratamientos ensayados. En estas flores los parámetros RGB obtenidos de las imágenes, así como las variables Fo, Fv y Fk, resultaron con valores bajos en relación con los demás tratamientos (Cuadro 7), lo cual indica valores de color más lejanos al blanco absoluto. En contraste el resto de los tratamientos mostraron valores de RGB cercanos a la unidad, indicando colores cercanos al blanco absoluto.
Table 7: Result of means from the analysis of visible images in flower color.
|
Solución nutritiva |
Medias R |
Medias G |
Medias |
Medias |
Medias |
Medias |
Medias |
Medias area |
|
1 |
0.9924 a† |
0.9939 a |
0.9930092 a |
1.7202 a |
1.7206 a |
1.7197 a |
2.5803 a |
0.7976 a |
|
2 |
0.9880 ab |
0.9927 a |
0.9928762 a |
1.7153 a |
1.7181 a |
1.7154 a |
2.5745 ab |
0.7949 ab |
|
3 |
0.9816 b |
0.9871 b |
0.987102 b |
1.7050 b |
1.7081 b |
1.7050 b |
2.5590 b |
0.7878 b |
|
4 |
0.9930 a |
0.9931 a |
0.99112 ab |
1.7200 a |
1.7189 a |
1.7189 a |
2.5789 a |
0.7970 a |
|
PROB |
0.0378 |
0.00208 |
0.0086 |
0.0079 |
0.0014 |
0.0064 |
0.0039 |
0.0039 |
Fo = distancia euclidiana de R a G; Fk = distancia euclidiana de B a G; Fv = distancia euclidiana de B a R; S = semiperimetro, A = área. † Medias con letras iguales entre filas no indican diferencia estadística significativa (Tukey, P = 0.05).
Fo = euclidean distance from R to G; Fk = euclidean distance from B to G; Fv = euclidean distance from B to R; S = semi-perimeter, A = area. † Means with equal letters between rows do not indicate significant statistical difference (Tukey’s, P = 0.05).
Dicho comportamiento implica que las elevadas concentraciones de potasio tienen un efecto adverso en la coloración de las flores de lisianthus, posiblemente debido a un desbalance en la concentración de dos o más nutrientes derivada de la alta concentración de potasio en la solución nutritiva (Beltrano y Giménez, 2015).
Conclusiones
- El uso de nuevas tecnologías implementadas en la agricultura moderna nos permite hacer uso de imágenes y obtener resultados de manera simple y económica de manera no destructiva, un parámetro de interés fueron los resultados obtenidos en los valores de RGB en el color de las flores, que a una concentración elevada de potasio las variables de Fo, Fv y Fk , resultaron valores bajos con respecto a las demás soluciones lo cual está más lejano al blanco absoluto algo difícil de observar con el ojo humano.
- En cuanto al desarrollo y crecimiento del cultivo de lisianthus el comportamiento de la solución nutritiva 1(Steiner) fue constante.











 text new page (beta)
text new page (beta)



