ANTECEDENTES
La sepsis se define como la existencia de una infección junto con manifestaciones sistémicas de infección.1 El grupo de trabajo formado por expertos en sepsis de la Sociedad Europea de Medicina de Cuidados Intensivos y de la Sociedad de Medicina de Cuidados Críticos de Estados Unidos definen a la sepsis como “la disfunción orgánica causada por una respuesta anómala del huésped a la infección que supone una amenaza para la supervivencia”.
La disfunción de órganos puede identificarse como un cambio agudo en la escala SOFA, la puntuación total mayor a 2 puntos, como consecuencia de la infección, refleja un riesgo de mortalidad global de aproximadamente 10% en la población general.1-3
A finales del decenio de 1970, se estimaron 164,000 casos de sepsis en Estados Unidos cada año.2 Para el año 2000 la incidencia aumentó a más de 650,000 casos, quizá como consecuencia de la edad avanzada, inmunosupresión e infecciones por microorganismos resistentes a múltiples fármacos.
Entre un tercio y la mitad de los pacientes con sepsis mueren, ésta continúa siendo causa frecuente de muerte en países de altos ingresos como en los de medianos y bajos ingresos. Cada año de 20 a 30 millones de personas en todo el mundo enferman de sepsis. En Estados Unidos la incidencia de sepsis posquirúrgica se ha triplicado en los últimos años, lo que representa un gasto de 1460 millones de dólares, con incremento anual al costo ajustado a la inflación de 11.9%. Se estima que en todo el mundo cada tres segundos alguien muere por sepsis. La sepsis causa la muerte cada año de 6 millones de niños y por lo menos de 100 mil mujeres en el periodo posparto.
El estudio de su fisiopatología representa uno de los campos médicos de mayor investigación, debido a que su incidencia continúa incrementándose a pesar de contar con tratamientos específicos. En 1972, Lewis Thomas refirió que la respuesta del sistema inmunitario puede ser nociva al estar en contacto con los microorganismos durante la infección. Posteriormente, Roger Bone acuñó el término síndrome de respuesta inflamatoria sistémica (SIRS) para describir a los pacientes que tenían evidencia clínica de este fenómeno proinflamatorio.4
La eosinopenia es un marcador de infección, la describió Zapperten en 1893 y posteriormente Shilling a principios del siglo XX.
En 20025 Gil y su grupo mostraron diferencia significativa entre la tasa de eosinófilos en los pacientes infectados en comparación con los pacientes con enfermedades inflamatorias sistémicas o neoplásicas. Los autores encontraron buena especificidad para el diagnóstico de sepsis y buen valor predictivo positivo de la asociación entre eosinopenia y leucocitosis. Concluyeron que la sepsis se asocia estrechamente con hiperleucocitosis por encima de 10,000 células/mm3 y recuentos de eosinófilos bajos de 40 células/mm3. En otro trabajo publicado en 2002,6,7 la eosinopenia mostró buena sensibilidad para el diagnóstico de las infecciones, pero sólo en bilis y en orina. Abidi y su grupo destacaron el valor de este marcador en el diagnóstico de las infecciones bacterianas como indicador de sepsis en los pacientes de la unidad de cuidados intensivos, en comparación con la PCR o procalcitonina.8
En 20109 se analizó el recuento de eosinófilos en 66 pacientes con diagnóstico de enfermedad pulmonar obstructiva crónica exacerbada y se encontró que la mortalidad fue significativamente mayor en los pacientes con eosinopenia al inicio del estudio que en los que tenían valores normales de eosinófilos (17 vs 2%, respectivamente). Estos autores sugirieron que el recuento de eosinófilos podría ser un marcador útil de la gravedad y el pronóstico de manera independiente de otros indicadores que se utilizan de rutina.
Los eosinófilos son células que normalmente representan sólo 1 a 3% de los leucocitos totales, con un máximo de 350 células/mm3. Su capacidad de marcador en sepsis se relaciona con su papel en la respuesta inmunitaria.9 La reducción en el número de eosinófilos sigue siendo un fenómeno inexplicado, pero puede estar vinculado con la acción de las citocinas inflamatorias, como el factor de necrosis tumoral, reactantes de fase aguda, glucocorticoides y epinefrina.10La reducción de los eosinófilos, acompañada de la disminución concomitante de CRTH2 (molécula homóloga del receptor expresada en los linfocitos Th2) y CCR3 (receptor de quimiocinas CC tipo 3) se ha observado durante la aparición y mantenimiento del choque séptico.11
Abidi y colaboradores12-14 demostraron que el recuento de eosinófilos durante los primeros siete días puede utilizarse como marcador pronóstico de mortalidad en los pacientes en estado crítico, por lo que puede ser una herramienta clínica útil en la unidad de cuidados intensivos. En el análisis multivariado, la eosinopenia fue predictor de mortalidad a 28 días con riesgo relativo de 1.8.15 Por último, se ha demostrado que los pacientes con bacteriemia persistente y eosinopenia tienen un riesgo significativamente mayor de mortalidad.16,17Asimismo, los que tienen una relación de recuento de neutrófilos-linfocitos mayor de 7 también están en mayor riesgo de mortalidad. Por tanto, el recuento de eosinófilos y la relación del recuento de neutrófilos-linfocitos podrían considerarse marcadores independientes de los resultados en los pacientes con bacteriemia.18-20El uso de algunos recuentos de leucocitos como marcador de la evolución del paciente es fácil, rápido y barato y, por tanto, podría ser de utilidad en la práctica clínica diaria, sobre todo en los países en desarrollo.
MATERIAL Y MÉTODO
Estudio observacional, descriptivo, longitudinal y prospectivo, en el que se incluyeron pacientes con diagnóstico de sepsis ingresados en el Hospital General Xoco, de la Secretaría de Salud de la Ciudad de México, en el periodo comprendido de marzo de 2015 a noviembre de 2016. Asimismo, fue aprobado por el Comité de Ética Institucional y está apegado a la normatividad vigente de investigación en salud.
Se incluyeron 60 pacientes, hombres y mujeres de 18 a 70 años de edad, con diagnóstico de sepsis. Se colectó el recuento relativamente bajo de eosinófilos y se estimó la puntuación de las diferentes escalas de severidad, así como su modificación después de 72 horas de tratamiento. De manera concomitante, se registraron variables de mortalidad y requerimiento de apoyo multiorgánico como parte de la evaluación de la severidad de la sepsis.
Se registró la edad, sexo, antecedentes crónico-degenerativos, diagnóstico, foco infeccioso y gravedad clínica del paciente por escala SOFA, con seguimiento a 72 horas. Se midió la presión arterial media, frecuencia cardiaca, frecuencia respiratoria, temperatura y la escala de Glasgow.
Se solicitaron estudios de laboratorio al ingreso y a las 72 horas para seguimiento del paciente crítico, como biometría hemática completa, pruebas de función hepática, gasometría arterial, química sanguínea y electrólitos séricos.
Con los datos de laboratorio, se realizó el recuento de eosinófilos y se obtuvo la media aritmética. Se consideró eosinopenia relativa con valores por debajo de la media de eosinófilos. Posteriormente se realizó la asignación a grupos de acuerdo con la elevación del recuento de eosinófilos después de 72 horas de tratamiento en comparación con su valor inicial.
La sepsis se caracterizó y evaluó en función de la escala de severidad SOFA, como se describe a continuación. Las puntuaciones se calcularon 24 horas después del ingreso en la unidad de cuidados intensivos y posteriormente cada 48 horas. Además, se evaluó la reducción de puntos porcentuales de la escala predictora del paciente crítico (SOFA) después de 72 horas de tratamiento.
Análisis estadístico
En cuanto a la estadística descriptiva se utilizaron medidas de resumen, como porcentajes, medidas de tendencia central y de dispersión, de acuerdo con la naturaleza de cada variable.
En relación con la estadística inferencial, se formaron grupos de acuerdo con el recuento de eosinófilos y la respuesta después de 72 horas de tratamiento. En estos grupos se comparó la puntuación de la escala de severidad SOFA mediante comparación de medias con la prueba t para muestras independientes. Se determinó la asociación de variables cualitativas (independiente vs dependiente) por medio de la prueba c2. Se consideró estadísticamente significativo un valor de p menor de 0.05. Los datos se registraron en una hoja de cálculo en formato Excel para su posterior importación al paquete estadístico SPSS edición 20 para su análisis estadístico final.
RESULTADOS
Se incluyeron 60 pacientes con estado crítico que requirieron apoyo multiorgánico. La mayoría eran hombres y el promedio de edad fue de 51 años. Sus características clínico-demográficas se muestran en el Cuadro 1.
Cuadro 1 Características clínico-demográficas (n = 60)
* = p < 0.05, de medición basal (T0) vs seguimiento 72 horas, prueba T no pareada.
Debido a la forma de comparación planteada en la metodología, la muestra se dividió con base en la media de cuenta de eosinófilos (la cuenta de eosinófilos por debajo de la media se consideró “eosinopenia relativa”). Las características se muestran en el Cuadro 2.
Cuadro 2 Comparación en grupos divididos por eosinopenia
* = p < 0.05, medición basal (T0) vs seguimiento (T72 horas); ** = p < 0.05, medición entre grupos sin eosinopenia vs con eosinopenia. Los análisis se realizaron mediante prueba t no pareada.
De acuerdo con las observaciones en el comportamiento de las variables, la muestra se volvió a dividir con base en la respuesta de eosinopenia (aumento significativo de eosinófilos) después de 72 horas. Las características se muestran en el Cuadro 3.
Cuadro 3 Comparación en grupos divididos por aumento de eosinófilos en 72 horas
* = p < 0.05, medición basal (T0) vs seguimiento (72 horas); ** = p < 0.05, medición entre grupos sin eosinopenia vs con eosinopenia. Los análisis se realizaron mediante prueba t no pareada.
Por último, para evidenciar más la diferencia del puntaje SOFA en el grupo con aumento de eosinófilos después de 72 horas, se elaboró la Figura 1.
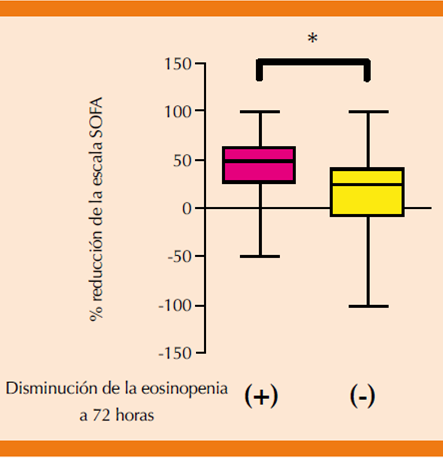
* p < 0.05, comparación de valores de grupos con vs sin disminución de la eosinopenia. Los análisis se realizaron mediante prueba t no pareada.
Figura 1 Reducción de la escala SOFA en función del aumento de eosinófilos. Se muestra el porcentaje de reducción del puntaje SOFA en el grupo con disminución de la eosinopenia (caja izquierda) y sin disminución de la eosinopenia (caja derecha).
DISCUSIÓN
Nuestra población de estudio se caracterizó por ser principalmente diabética y la hipertensión arterial estuvo presente en la menor parte de los pacientes con prevalencia de 27%. Predominaron las edades alrededor de 51 años, leucocitosis y recuento de eosinófilos menor a 1% al ingreso al estudio, que después de 72 horas del tratamiento se elevaron al menos hasta 1%.
El tratamiento que recibieron los pacientes también indujo alivio significativo del curso clínico en la mayoría de los pacientes, reflejado en la mejoría de la calificación SOFA a las 72 horas de la evaluación. Esto se explica, en gran parte, por el manejo y soporte del proceso infeccioso que contrarrestó el proceso inflamatorio y la hipoperfusión tisular asociados con la sepsis. Esto indica la importancia de la detección oportuna de sepsis, así como del inicio temprano del tratamiento médico.
Al comparar el puntaje SOFA del grupo con eosinopenia vs sin eosinopenia se encontraron diferencias significativas, lo que pareciera indicar que la eosinopenia tiene un efecto clínico directo en el estado del paciente; es decir, el grupo con eosinopenia tuvo mayor hipoperfusión tisular o insuficiencia orgánica en comparación con el grupo sin eosinopenia. Se encontró elevación significativa de eosinófilos a las 72 horas.
La variable de aumento de eosinófilos después de 72 horas se relacionó más estrechamente con la mejoría en la escala SOFA, probablemente debido a que refleja un comportamiento dinámico de respuesta a tratamiento.
Se ha demostrado que el recuento de eosinófilos durante los primeros siete días puede utilizarse como marcador pronóstico de mortalidad en los pacientes en estado crítico y puede ser una herramienta clínica útil en la unidad de cuidados intensivos.16
Entre las limitaciones de este estudio destaca el hecho de haberse realizado en una sola unidad hospitalaria y el tamaño de la muestra. Al considerar esto, nos planteamos como perspectiva el desarrollo de nuevos estudios idealmente multicéntricos y con mayor tamaño de muestra para determinar con mayor precisión el papel que juega la eosinopenia y otros biomarcadores en el contexto de la sepsis y sepsis severa.











 text new page (beta)
text new page (beta)


