ANTECEDENTES
La cardiomiopatía de takotsubo, también conocida como cardiomiopatía de estrés o síndrome de balonamiento apical ventricular izquierdo, se distingue por disfunción transitoria y regional del ventrículo izquierdo durante la sístole que involucra la punta y los segmentos medios del ventrículo izquierdo, con hipercinesia del segmento basal. El síndrome se describió inicialmente en la población japonesa y una vez identificado se ha descrito en todos los grupos raciales. El término takotsubo se acuñó debido a la semejanza de la morfología ventricular con una red para atrapar pulpos utilizada en Japón (Figura 1). El diagnóstico se establece cuando se cumplen los criterios de la Clínica Mayo: 1) disfunción transitoria del ventrículo izquierdo que involucra al segmento apical o medio, con afectación que no correlaciona con la distribución del flujo coronario epicárdico, 2) coronarias permeables, 3) cambios electrocardiográficos caracterizados por alteraciones del segmento ST y de la onda T, vinculados con incremento en la troponina, 4) ausencia de alguna otra enfermedad cardiaca. En casos graves puede haber coágulos intracavitarios, insuficiencia cardiaca aguda y excepcionalmente rotura ventricular.1

Figura 1 Trampa utilizada en Japón para atrapar pulpos llamada takotsubo, de donde se tomó el nombre del síndrome por la semejanza morfológica que adopta el ventrículo izquierdo con la vasija.
El origen de este padecimiento frecuentemente se asocia con exposición masiva a catecolaminas, como la que ocurre en situaciones de estrés emocional o físico extremo, traumatismo craneoencefálico, hemorragia subaracnoidea, administración exógena o tumores secretores de catecolaminas. Los casos de cardiomiopatía de takotsubo secundaria a sepsis están bien identificados, pero los reportes son escasos. Se describe el caso de una paciente con cardiomiopatía de takotsubo secundaria a sepsis a fin de destacar esta asociación que, aunque poco frecuente, es de gran relevancia por su significado clínico.
CASO CLÍNICO
Paciente femenina de 80 años de edad que inició su padecimiento 10 días previos a su ingreso, con fiebre y tos productiva. Recibió tratamiento ambulatorio con antiinflamatorios no esteroides y levofloxacino que no indujeron mejoría. Persistió con fiebre, además de disnea y datos de insuficiencia respiratoria, motivo por el cual acudió al servicio de urgencias. A su ingreso tenía taquicardia, taquipnea y fiebre de 39oC. A la exploración, se registró presión arterial de 90/50 mmHg, frecuencia cardiaca de 110 lpm, frecuencia respiratoria de 22 rpm y saturación al aire ambiente de 80%. En los exámenes para-clínicos se reportaron leucocitos de 5,400/mcL con desviación a la izquierda y procalcitonina en 13 ng/dL. La prueba rápida de influenza fue negativa. Los resultados gasométricos fueron: pH de 7.35, PaCO2 de 47 mmHg y PaO2 de 55 mmHg. En la radiografía simple de tórax se corroboró condensación basal derecha; el electrocardiograma inicial indicó ritmo sinusal sin alteraciones en la conducción y repolarización normal. Se integró el diagnóstico de neumonía grave adquirida en la comunidad, por lo que se decidió su hospitalización. Durante ese periodo se agravó la insuficiencia respiratoria y la hipoxemia, además sufrió hipotensión resistente a manejo con líquidos. Se integró el diagnóstico de choque séptico y se le ingresó al servicio de terapia intensiva, en donde se le realizó estudio ecocardiográfico que reveló hipertrofia ventricular izquierda con adecuada contractilidad global y segmentaria, y fracción de eyección de 65%, con función ventricular derecha normal. El manejo consistió en ventilación mecánica invasiva, nutrición enteral, vancomicina y fluconazol con base en los resultados de cultivos de secreción bronquial, que fueron Candida albicans y Staphylococcus aureus, así como apoyo vasopresor con norepinefrina. De esta manera se logró estabilidad hemodinámica y mejoría progresiva de la función pulmonar. Durante la evolución sufrió de manera súbita hipotensión y cambios electrocardiográficos caracterizados por bradicardia sinusal, inversión de la onda T en DI y aVL y desnivel negativo del ST de V2 a V6 e inversión de la onda T (Figura 2). Las enzimas cardiacas durante el evento fueron CPK-MB de 10.40 U/L y troponina T de 121.7 pg/mL. Ante la sospecha de síndrome coronario agudo se realizó nuevo ecocardiograma, que evidenció hipocinesia ventricular izquierda del segmento medial y acinesia apical con contractilidad basal conservada, además de insuficiencia mitral moderada con fracción de eyección del ventrículo izquierdo de 30%. La función ventricular derecha se reportó normal, sin evidencia de dilatación ni trombos intracavitarios (Figura 3). Posteriormente se le realizó cateterismo cardiaco y coronariografía, que mostró arterias coronarias sin obstrucción, flujo TIMI III, con pequeñas placas de ateroma sin obstruir más de 10% de su luz, con lechos y flujo distal normal en todos los territorios evaluados. En la ventriculografía se observó acinesia anterolateral, inferolateral y apical con movimiento normal de los segmentos basales, anterior y posterior, y se corroboró fracción de expulsión de 30% e insuficiencia mitral leve. De esta manera se integró el diagnóstico de síndrome de takotsubo secundario a sepsis. Se inició tratamiento con levosimendán y betabloqueadores que produjeron mejoría significativa del estado hemodinámico y de la función cardiaca. En el ecocardiograma de control se apreció mejoría significativa de la contractilidad e involución del balonamiento apical.
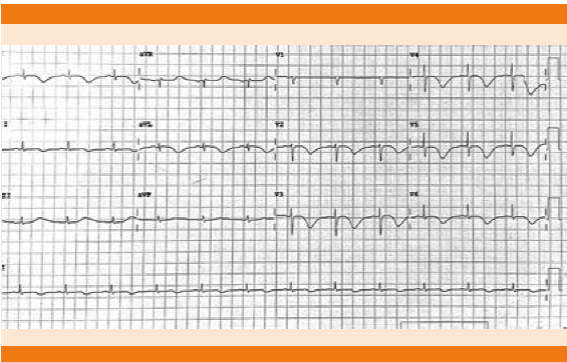
Figura 2 Electrocardiograma en el que se observa inversión de la onda T en DI y aVL, desnivel negativo del segmento ST e inversión de la onda T en las derivaciones V2 a V6.
DISCUSIÓN
La sepsis continúa siendo la principal causa de ingreso a las unidades de cuidados intensivos (UCI) en todo el mundo. Estadísticas recientes estiman que es la responsable de más de 60% de todas las admisiones a las UCI, y que aumentó de 7 a 11% en un periodo de 12 años debido a la aplicación de criterios más objetivos para su diagnóstico y al crecimiento de la población añosa e inmunodeprimida. Se estima que de 0.4 a 1 de cada 1,000 habitantes ingresan a un hospital con diagnóstico de sepsis en Estados Unidos, Europa y el Reino Unido, y que de forma paralela la mortalidad ha disminuido de 35 a 18%.2-6 El principal sitio de infección en general son los pulmones (64%), seguido del abdominal (20%), hematógeno (15%) y genitourinario (14%). El 47% de los patógenos responsables son grampositivos y Staphylococcus aureus es el agente aislado con más frecuencia, 62% son gramnegativos (Pseudomonas spp) y 19% son hongos.7 Cuando el germen responsable es resistente a meticilina o alguna especie de Candida, la mortalidad aumenta considerablemente (43 y 50%, respectivamente).8
La fisiopatología de la sepsis involucra interacciones complejas entre el organismo patógeno y el sistema inmunitario del huésped, el cual inicia una respuesta inflamatoria en contra del agente invasor y regula la respuesta a los componentes moleculares asociados con los patógenos (PMAPs).9-11 Normalmente esta respuesta inflamatoria es de alivio espontáneo y regulada por citocinas antiinflamatorias; sin embargo, en la sepsis existe una respuesta inflamatoria exagerada por un desequilibrio entre citocinas proinflamatorias y antiinflamatorias. La producción excesiva de mediadores proinflamatorios promueve la formación de especies reactantes de oxígeno y nitrógeno que causan mayor daño tisular y liberación de patrones moleculares asociados con daño (PMADs), como las proteínas de choque de calor, proteínas de alta movilidad del grupo 1 (HMGB1), histonas y lipoproteínas oxidadas, las cuales pueden ampliar la cascada inflamatoria creando un círculo vicioso que finalmente contribuye a la disfunción cardiaca, insuficiencia orgánica múltiple y muerte.12,13
La cardiopatía inducida por sepsis es una complicación frecuente que fue descrita hace más de 30 años y actualmente nuevas estrategias para su tratamiento y prevención están en investigación.13-17 Se sabe que incluso 60% de los pacientes con choque séptico padecen miocardiopatía, la cual tiene tres características esenciales: dilatación del ventrículo izquierdo de inicio súbito, fracción de eyección disminuida y recuperación en 7 a 10 días en los pacientes que logran sobrevivir.18 Mediadores químicos como endotoxinas, citocinas y óxido nítrico tienen un papel importante en la fisiopatología de la miocardiopatía séptica al reducir la respuesta miofibrilar al calcio,19 induciendo disfunción mitocondrial20 y generando alteraciones en la regulación de los receptores β-adrenérgicos.21,22
El síndrome de takotsubo (también conocido como cardiomiopatía por estrés o síndrome del balonamiento apical izquierdo) fue descrito por primera vez en 1990 en Japón y rápidamente reconocido en todo el mundo.23 Es un síndrome que se distingue por disfunción sistólica apical transitoria del ventrículo izquierdo con hipercontractilidad de la base, que hacen que éste adquiera una forma redondeada similar a una trampa utilizada en Japón para cazar pulpos llamada takotsubo (Figura 1). En términos electrocardiográficos simula un infarto de miocardio, pero no hay evidencia angiográfica de obstrucción coronaria o rotura aguda de placa, y puede haber elevación leve de troponinas.24,25 La cardiomiopatía de takotsubo es más frecuente en mujeres,26 y se estima que actualmente tiene una prevalencia de 1 a 3% de la población en general y de 6 a 9% de las mujeres con síndromes coronarios agudos.27 La edad media de aparición varía de 60 a 75 años, con un pronóstico generalmente favorable, aunque la mortalidad es de 0 a 8%, y es menor en los hombres.28 Los mecanismos fisiopatológicos que se han propuesto tienen que ver con situaciones de estrés emocional o físico vinculadas con periodos de hiperactividad del sistema nervioso simpático durante los cuales se han demostrado cifras suprafisiológicas de catecolaminas plasmáticas y neuropéptidos relacionados con el estrés que una vez que alcanzan los adrenorreceptores cardiacos inducen toxicidad en los cardiomiocitos, provocando cambios en la microvasculatura y metabolismo celular.29-33 Aunque no existe evidencia a favor de ello, un mecanismo descrito es el de espasmo de la microvasculatura epicárdica que condiciona alteraciones en el flujo sanguíneo a este nivel,34-36 y otro, el más aceptado, está vinculado con toxicidad directa de las catecolaminas, las cuales disminuyen la disponibilidad de AMP secundaria a la sobrecarga de calcio y radicales libres de oxígeno,36 mecanismo favorecido por la distribución de los receptores catecolaminérgicos en la región apical del ventrículo, en donde la relación de receptores B2-B1 induce mayor respuesta y vulnerabilidad a la estimulación simpática.37,38 El diagnóstico del síndrome de takotsubo se realiza de acuerdo con los criterios de la Clínica Mayo basados en los siguientes puntos: 1) disfunción sistólica transitoria en los segmentos apicales o medios del ventrículo izquierdo con anormalidades en el movimiento de la pared que se extienden más allá de la distribución vascular epicárdica, 2) ausencia de enfermedad coronaria obstructiva o rotura de placa, 3) elevación del segmento ST o inversión de la onda T con elevación leve de troponinas cardiacas y 4) ausencia de otras causas por enfermedad torácica.39 El manejo debe orientarse primero a descartar isquemia cardiaca y posteriormente iniciar medidas de soporte como α-β-bloqueadores, IECA y diuréticos si hay datos de congestión. Se recomienda la anticoagulación durante la fase aguda, especialmente si la disfunción del ventrículo izquierdo es severa.37,40 En caso de insuficiencia cardiaca, los agentes inotrópicos estarían contraindicados, ya que se argumenta que los betaagonistas podrían empeorar el cuadro o prolongar la recuperación.41 El levosimendán ha producido resultados exitosos y actualmente se recomienda como el agente inotrópico de elección, a pesar de la ausencia de ensayos clínicos aleatorizados.42
Las infecciones bacterianas son la causa más frecuente de síndrome de takotsubo en sepsis, debido a que hacen más vulnerable al miocardio a los efectos tóxicos de las catecolaminas,70 aunque también se ha reportado que agentes virales como enterovirus, adenovirus, parvovirus B19, herpes, Epstein-Barr y citomegalovirus pueden causar cardiomiopatía por un mecanismo fisiopatológico totalmente diferente, más relacionado con efectos citotóxicos directos del virus que aunado a la cardiotoxicidad de las catecolaminas desencadenan insuficiencia ventricular izquierda durante la sístole.71,72 En el Cuadro 1 se resumen los casos descritos de síndrome de takotsubo secundario a sepsis recopilados de la bibliografía. Como se anota, todos son casos aislados, lo que está en relación con lo poco frecuente de esta asociación.
Cuadro 1 Casos reportados de síndrome de takotsubo secundario a sepsis de diferente causa
| Autor | Año | Género | Desenlace |
| Chidiac y col.43 | 1995 | Mujer | Defunción |
| Kusaba y col.44 | 2004 | Mujer | Sobrevivió |
| Greco y col.45 | 2006 | Mujer | Sobrevivió |
| Ohigashi-Suzuki y col.46 | 2007 | Hombre | Sobrevivió |
| Singh y col.47 | 2007 | Mujer | Sobrevivió |
| Cattaneo y col.48 | 2007 | Mujer | Sobrevivió |
| Bigalke y col.49 | 2007 | Mujer | Sobrevivió |
| Geng y col.50 | 2008 | Mujer | Sobrevivió |
| Palacio y col.51 | 2009 | Mujer | Sobrevivió |
| Sarullo y col.52 | 2010 | Mujer | Sobrevivió |
| Li y col.53 | 2010 | Mujer | Sobrevivió |
| Lee y col.54 | 2010 | Mujer | Sobrevivió |
| Tanriver y col.55 | 2010 | Mujer | Sobrevivió |
| Gariboldi y col.56 | 2011 | Mujer | Sobrevivió |
| Okumura y col.57 | 2011 | Mujer | Sobrevivió |
| Yonekawa y col.58 | 2011 | Mujer | Sobrevivió |
| Odigie-Okon y col.59 | 2011 | Mujer | Sobrevivió |
| Hassan y col.60 | 2011 | Mujer | Sobrevivió |
| Van Beek y Knockaert61 | 2011 | Mujer | Sobrevivió |
| Jung y col.62 | 2012 | Mujer | Sobrevivió |
| Brunetti y col.63 | 2012 | Hombre | Sobrevivió |
| Karvouniaris y col.64 | 2012 | Hombre | Sobrevivió |
| Santoro y col.65 | 2013 | Hombre | Sobrevivió |
| Galea y col.66 | 2013 | Mujer | Sobrevivió |
| Contreras y col.67 | 2013 | Mujer | Sobrevivió |
| Piccirillo y col.68 | 2013 | Hombre | Sobrevivió |
| Núñez y col.69 | 2013 | Mujer | Sobrevivió |
La fisiopatología del síndrome de takotsubo inducido por sepsis es compleja. Se han descrito los siguientes mecanismos en su génesis:73
Inflamación inducida por sepsis y liberación de citocinas. Hay evidencia de que el factor de necrosis tumoral y la interleucina 1B inducen, además de depresión en la contractilidad miocárdica, activación del sistema nervioso simpático local y la vía de la mitógeno p38 proteincinasa, que ocasiona cardiodepresión.
Toxicidad por catecolaminas endógenas, potenciada por inflamación, estrés oxidativo y acumulación de calcio intracelular.
Toxicidad por administración de catecolaminas, en especial norepinefrina, en pacientes en estado de choque.
Isquemia miocárdica secundaria a inadecuada perfusión microcirculatoria.
El tratamiento del síndrome de takotsubo secundario a sepsis no difiere de lo ya conocido, como en el caso que describimos, se recomienda implantar medidas de sostén, control del proceso infeccioso, disminuir en lo posible la dosis de norepinefrina y si es pertinente suspenderla e iniciar manejo farmacológico con betabloqueadores. En casos en que la disfunción contráctil sea significativa y altere la perfusión sistémica se puede prescribir levosimendán, inotrópico no adrenérgico, que ha mostrado ser útil en este escenario. En casos extremos que no responden a la terapia habitual se ha sugerido el apoyo circulatorio extracorpóreo.74,75
Este caso se agrega a la lista de reportes de una asociación poco frecuente, sepsis con síndrome de takotsubo, evento que deberá estar en la mente del intensivista, destacando la importancia de la ecocardiografía como herramienta diagnóstica en la evaluación integral del deterioro hemodinámico en el paciente con sepsis.











 text new page (beta)
text new page (beta)



